文档内容
第二章 化学物质及其变化
第二节 离子反应
第一课时 电解质的电离
【学习目标】1.通过探究几组物质的导电性实验形成电离的概念,能从宏微结合的角度进一步对物
质进行分类,以探究的方式建构电离模型。
2.通过合作探究对溶液导电性的分析,知道电解质、非电解质的概念,认识常见的电解质,能从微
观的角度(电离)认识酸、碱和盐,并能用电离方程式表示酸、碱、盐的电离过程。
3.通过化学实验认识电解质的电离及电离条件,建立电离方程式的认知模型,激发学习化学的兴
趣,培养严谨求实、勇于探索的科学精神。
【学习重点】电解质及电离的概念、电离方程式的书写。
【学习难点】电解质概念的理解及判断、实验方案的设计。
【课前预习】
旧知回顾:1.请分别举例说明你所知道的有哪些能导电和不能导电的化学物质?
2.你能依据初中物质导电性实验猜测湿手容易触电的原因吗?说出你的理由。
新知预习:酸、碱、盐的水溶液能够导电,是因为它们在水溶液中发生了 ,解离
出 。现有下列物质:①硫酸 ②食盐水 ③氯气 ④碳酸钙 ⑤乙醇
⑥Al(OH) ⑦醋酸 ⑧铜 ⑨NaO ⑩氨气 ⑪CO ⑫NaHCO ⑬CHCOONH ⑭HO其中属于电解质的是
3 2 2 3 3 4 2
__________________,属于非电解质的是___________,既不是电解质,也不是非电解质的是
______________。
【课中探究】
情景导入:观看生活中用电的图片和视频,思考在日常生活中,给电气设备通电时,为什么湿手操作
易发生触电事故呢?(见PPT图片、视频)
一、电解质和非电解质
活动一、认识电解质和非电解质
任务一、实验探究:阅读教材P14页内容,根据实验1-2,完成下列实验,并填写表格内容。
实验步骤 实验内容 实验现象 实验结论
步骤一 向三个烧杯中分别加入硝酸钾固体、氯化钠固
体和蒸馏水。按照课本中的图示连接装置,将石墨电极伸入到烧杯中,观察小灯泡是否发
光。
步骤二 将少量硝酸钾固体和氯化钠固体加入盛有水的
烧杯中,搅拌使其完全溶解转化为相应的溶
液,重复上述的导电性实验,观察小灯泡是否
发光。
任务二、结合教材P14页最后自然段,讨论交流下列物质哪些能导电,哪些本身不能导电,但在一定
条件下可以导电?
硫酸溶液、Cu、熔融NaOH、MgCl 、KOH固体、HSO 、Fe (SO ) 、NaCO 、硫酸钡、蔗糖、酒
2 2 4 2 4 3 2 3
精。
任务三、讨论交流:根据物质的导电性规律,思考如何对化合物进行再分类?电解质和非电解质的概
念是什么?
【对应练习】1.下列物质不能导电的是( )
A.KNO 固体 B.NaCl溶液 C.铜丝 D.熔融MgCl
3 2
2.下列说法中不正确的是( )
①将硫酸钡放入水中不能导电,硫酸钡是非电解质;
②氨溶于水得到氨水溶液能导电,氨水是电解质;
③固态氯化氢不导电,液态氯化氢可以导电;
④硫酸氢钠电离出的阳离子有H+,硫酸氢钠是酸;
⑤电解质放在水中一定能导电,非电解质放在水中一定不导电。
A.仅①④ B.仅①④⑤ C.仅②③ D.①②③④⑤
活动二、探究化合物与电解质和非电解质的关系
任务一、思考交流:结合NaCl固体与NaCl溶液、HCl与盐酸、金属铜等物质的导电性,谈谈你对电
解质和非电解质有哪些更深入的理解。
任务二、问题探究:已知NaO、SO 水溶液、盐酸、氯化钠溶液能导电, BaSO 、AgCl难溶于水,
2 3 4
它们都是电解质吗?【对应练习】1.下列说法中,正确的是( )
A.液态HCl、固态NaCl均不导电,所以HCl、NaCl均是非电解质
B.NH 、CO 的水溶液均能导电,所以NH 、CO 均是电解质
3 2 3 2
C.蔗糖、酒精在水溶液里或熔融状态时均不导电,所以它们是非电解质
D.铜、石墨均导电,所以它们是电解质
2.下列说法正确的是( )
A.铜、石墨均能导电,所以它们都是电解质
B.氨、二氧化碳的水溶液都能导电,所以它们都是电解质
C.液态氯化氢、固体氯化钠都不能导电,所以它们都是非电解质
D.蔗糖、酒精在水溶液里和熔融状态下都不能导电,所以它们都是非电解质
二、电离及电离方程式
活动一、认识电解质的电离
任务一、阅读教材P15页第3、4、5自然段,观察图1-10、1-11,探究固体NaCl的溶解及熔化的微观
过程,回答NaCl固体溶于水能导电的原因是什么?
任务二、阅读教材P16页第一自然段,观察图1-12,思考NaCl固体等加热至熔化为什么能导电,而蔗
糖等固体加热至熔化却不能导电?
任务三、根据上面电解质导电的微观探析,思考电解质导电与离子有何关系,什么是电解质的电离?【对应练习】1.下列物质中,含有自由移动的Cl-的是( )
A.KClO 溶液 B.CaCl 溶液
3 2
C.KCl晶体 D.液态氯化氢
2.下列说法中正确的是( )
A.金属铜、石墨碳棒、氯化钠晶体都能导电
B.电解质溶液和金属在外电场作用下,定向移动的粒子不同
C.电解质在水溶液中通电后才能发生电离,产生移动的离子
D.硫酸钡沉淀不能导电,所以它是非电解质
活动二、电解质的电离方程式及书写
任务一、阅读教材P16页第二自然段,什么叫电离方程式?如何从电离的角度理解酸、碱、盐的本
质?
①定义:
②书写:
③酸、碱、盐的本质如下表:
电离特征(本质) 实例
酸
碱
盐
任务二、讨论交流:联系酸、碱、盐的本质,请尝试写出 HNO 、HPO 、Ba(OH) 、NH ‧H O、
3 3 4 2 3 2
NaSO 、Fe (SO )、(NH )SO 的电离方程式。
2 4 2 4 3 4 2 4
任务三、归纳总结:书写电离方程式应注意哪些问题?
【对应练习】1.下列在水溶液中的电离方程式,错误的是( )
A.NaCO===2Na++CO B.HSO ===2H++SO
2 3 2 4C.NaHCO ===Na++H++CO D.NaHSO===Na++H++SO
3 4
2.下列物质在指定条件下电离方程式正确的是( )
A.NaCO 溶于水:NaCO===Na+CO
2 3 2 3
B.Fe(OH) 部分溶与水电离:Fe(OH) ===Fe3++3OH-
3 3
C.NaHS溶于水HS-的电离:HS-+HO HS+OH-
2 2
D.NaHSO 加热熔化:NaHSO===Na++HSO
4 4
【课后巩固】1.(易)教材作业:P20页练习1、2、5
2.(易)下列各组物质,前者属于电解质,后者属于非电解质的是( )
A.NaCl晶体、BaSO B.铜、二氧化硫
4
C.液态的醋酸、酒精 D.熔融的KNO、硫 酸溶液
3
3.(中)对电解质概念理解正确的是( )
A.在水溶液或熔融状态下能导电的物质
B.凡在水中能生成离子而能导电的物质
C.氧化钠溶于水能生成钠离子和氢氧根离子,尽管氧化钠是化 合 物 , 其
水溶液能导电,但溶液中的氢氧根离子并非氧化钠本身电离,因而氧化钠是非电解质
D.在水溶液里或熔融状态下本身能电离出阳离子和阴离子而能导电的化合物
4.(中)下列关于化合物、单质、混合物、电解质和非电解质的正确组合是( )
化合物 单质 混合物 电解质 非电解质
A 烧碱 液态氧 冰水混合物 醋酸 二氧化硫
B 生石灰 白磷 胆矾 氧化铝 氯气
C 干冰 铁 氨水 石灰石 酒精
D 空气 氮气 小苏打 氯化铜 硫酸钡
5.(中)下列说法正确的一组是( )
①难溶于水的盐(CaCO、BaSO 等)都是非电解质
3 4
②不是电解质的物质一定是非电解质
③强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
④电解质溶液导电的原因是溶液中有自由移动的阴离子和阳离子
⑤熔融的电解质都能导电
A.①③⑤⑥ B.②④⑤
C.只有④ D.只有⑤
6.(难)NaCl是我们生活中必不可少的物质。将NaCl固体溶于水,溶解过程如图所示,下列说法正
确的是( )
A.该过程发生了分解反应
B.离子从固体表面脱离后不会再回到固体表面C.水合Na+的图示不科学
D.NaCl溶于水后发生了电离,是在通电条件下进行的
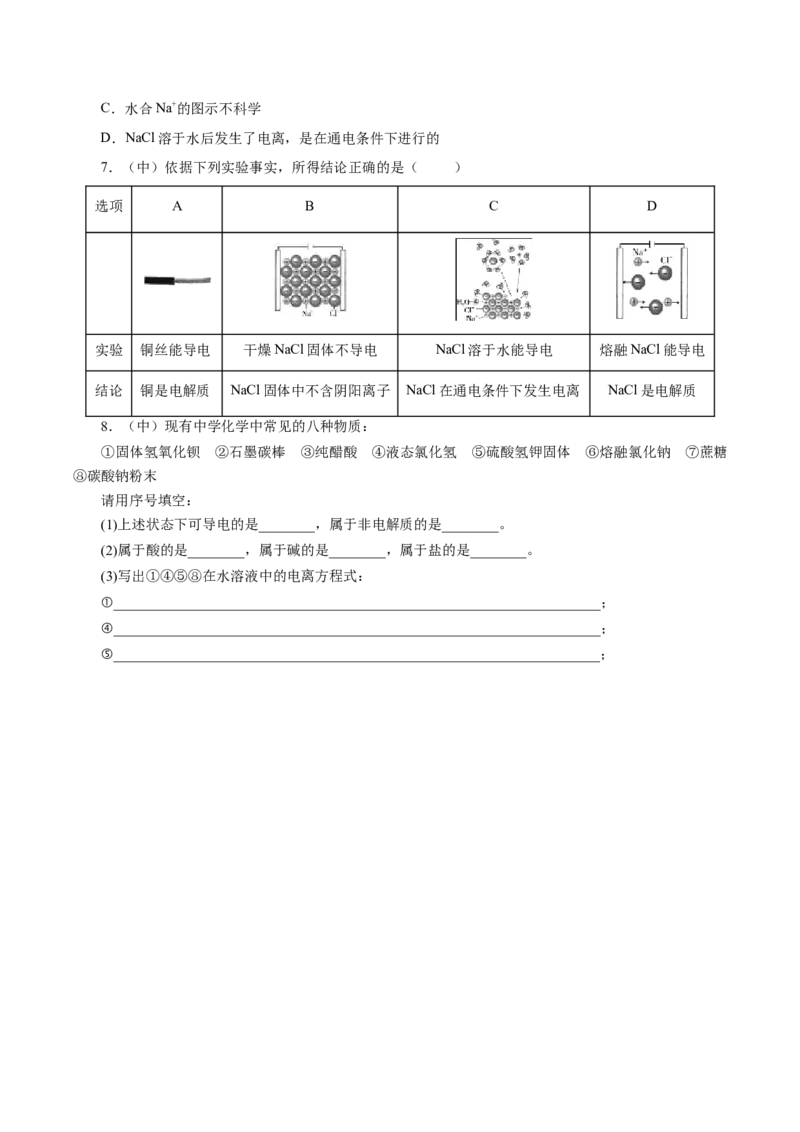
7.(中)依据下列实验事实,所得结论正确的是( )
选项 A B C D
实验 铜丝能导电 干燥NaCl固体不导电 NaCl溶于水能导电 熔融NaCl能导电
结论 铜是电解质 NaCl固体中不含阴阳离子 NaCl在通电条件下发生电离 NaCl是电解质
8.(中)现有中学化学中常见的八种物质:
①固体氢氧化钡 ②石墨碳棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥熔融氯化钠 ⑦蔗糖
⑧碳酸钠粉末
请用序号填空:
(1)上述状态下可导电的是________,属于非电解质的是________。
(2)属于酸的是________,属于碱的是________,属于盐的是________。
(3)写出①④⑤⑧在水溶液中的电离方程式:
①_____________________________________________________________________;
④_____________________________________________________________________;
⑤_____________________________________________________________________;