文档内容
第一章 物质及其变化
第二节 离子反应 课时作业
第一课时 电解质的电离
基础达标
1.在下列试验物质导电性的实验中,接通电源后灯泡不亮的是( )
①盐酸 ②无水酒精 ③氢氧化钠溶液 ④氯化钠溶液 ⑤蔗糖水
A.①② B.③④⑤
C.③④ D.②⑤
【答案】D
【解析】①盐酸中存在自由移动的氢离子和氯离子,能导电,接通电源后灯泡变亮,
①与题意不符;②无水酒精中无自由移动的离子,接通电源后灯泡不亮,②符合题意;③
氢氧化钠溶液中存在自由移动的钠离子和氢氧根离子,能导电,接通电源后灯泡变亮,③
与题意不符;④氯化钠溶液中存在自由移动的钠离子和氯离子,能导电,接通电源后灯泡
变亮,④与题意不符;⑤蔗糖水中无自由移动的离子,接通电源后灯泡不亮,⑤符合题
意;②⑤符合题意,答案为D。
2.下列状态的物质,既能导电又属于电解质的是 ( )
A.氯化镁晶体 B.氯化钠溶液
C.液态氯化氢 D.熔融氢氧化钾
【答案】D
【解析】电解质导电所需的条件是在水溶液里或熔融状态下,氯化镁晶体为固态,不
导电,是电解质;氯化钠溶液导电,为混合物,不是电解质;液态氯化氢不导电,是电解
质,只有溶于水才导电;熔融氢氧化钾导电,是电解质。
3.下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
纯净物 混合物 电解质 非电解质
A 盐酸 冰水混合物 硫酸 干冰
B 纯净水 漂白粉 氧化铝 二氧化硫
C 胆矾 碱石灰 铁 碳酸钙
D 液氯 合金 氯化铜 蔗糖
A.A B.B C.C D.D【答案】D
【解析】A.盐酸是氯化氢的水溶液,属于混合物;冰水混合物是HO,是纯净物;A
2
项错误;B.纯净水不是纯净物,是混合物;漂白粉是氢氧化钙、氯化钙等组成的混合
物,B项错误;C.碱石灰是主要成分为氧化钙、氢氧化钠等组成混合物;铁是单质,既不
是电解质也不是非电解质;碳酸钙是电解质,C项错误;D.液氯是液态的氯气,是纯净
物;合金是混合物;氯化铜是电解质;蔗糖是非电解质,D项正确;答案选D。
4.下列说法不正确的是( )
A.熔融NaCl发生了电离,能导电
B.NaCl晶体不能导电
C.NH NO 电离时产生了NH、NO,无金属离子,所以NH NO 不是盐
4 3 4 3
D.NaHSO 在水溶液中电离出Na+、H+、SO三种离子
4
【答案】C
【解析】明确电解质的导电与电离的关系以及酸、碱、盐的概念是解答本题的前提。
熔融NaCl能电离出Na+和Cl-,故能导电;NaCl晶体中无自由移动的离子,所以不能导
电;NH的性质与金属离子相似,NH NO 是铵盐。
4 3
5.下列叙述正确的是( )
A.氯化钠溶液在电流作用下电离成Na+与Cl-
B.溶于水后能电离出H+的化合物都是酸
C.氯化氢溶于水后能导电,但液态氯化氢不能导电
D.导电性强的溶液中自由移动离子数目一定比导电性弱的溶液中自由移动离子数目
多
【答案】C
【解析】电离不需要通电,A错;NaHSO 溶于水后可以电离出H+,但属于盐,B
4
错;电解质本身不一定导电,液态HCl不导电,但溶于水可电离生成H+和Cl-而导电,C
正确;导电性强弱与带电离子的浓度和所带电荷有关,与离子的个数无确定关系,D错。
6.下列说法正确的是( )
A.将AgCl放入水中不能导电,所以AgCl不是电解质
B.NH 溶于水得到的溶液能导电,所以NH 是电解质
3 3
C.NaHSO 溶于水的电离方程式:NaHSO=Na++H++SO
3 3
D.固态的NaCl不导电,但NaCl是强电解质
【答案】D
【解析】A.AgCl难溶于水,在水溶液中电离产生的自由移动的离子浓度很小,几乎
不导电。但是溶于水的AgCl会完全电离产生自由移动的离子,且在熔融状态可电离产生离子,因此该物质是强电解质,属于电解质,A错误;B.NH 溶于水得到的溶液能导电,
3
是由于发生反应NH +H O=NH ·H O,产生的NH ·H O电离产生了自由移动的NH +、OH-
3 2 3 2 3 2 4
离子,所以NH ·H O是电解质,而NH 是非电解质,B错误;C.NaHSO 是弱酸的酸式
3 2 3 3
盐,溶于水的电离方程式为:NaHSO=Na++HSO -,C错误;D.固态的NaCl不导电,是
3 3
由于在固体中含有的离子不能自由移动,在熔融态或溶于水时会完全电离产生自由移动的
Na+、Cl-,因此NaCl是强电解质,D正确;故合理选项是D。
7.足量NaCl(s)在水中溶解并发生电离,该过程的微观示意图如图。下列相关说法正确
的是 ( )
A. 该过程通常表示为
B. NaCl在水中只部分电离
C. 和 均与水分子中的氧原子结合形成水合离子
D. 离子从固体表面脱离后不会再回到固体表面
【答案】A
【解析】 A.NaCl 在水中完全电离,该过程通常表示为 NaCl==Na++Cl-,A 正确
B.NaCl为强电解质,在水中完全电离,B错误;C.Cl-带负电荷,由图可知,与水分子中的
氢原子结合形成水合离子,C错误D.NaCl溶解时钠离子和氯离子从固体表面脱离进入溶液
中,同时钠离子和氯离子受NaCl表面的氯离子和钠离子的吸引可能再回到固体表面,D错
误;答案选A 。
8.下列电离方程式错误的是 ( )
A.AlCl 在水溶液中的电离方程式为AlCl ===Al3++Cl
3 3
B.Ba(OH) 在水溶液中的电离方程式为Ba(OH) ===Ba2++2OH-
2 2
C.NaHSO 在熔融状态下的电离方程式为NaHSO(熔融)===Na++HSO
4 4
D.CHCOONH 在水溶液中的电离方程式为CHCOONH===NH+CHCOO-
3 4 3 4 3
【答案】A
【解析】AlCl 在水溶液中的电离方程式应为AlCl ===Al3++3Cl-,A错误。
3 39.下列说法正确的是( )
A.NaHCO 的电离方程式是NaHCO ===Na++H++CO
3 3
B.自由移动的离子数目多的溶液一定比自由移动的离子数目少的溶液导电能力强
C.虽然NaO溶于水所得溶液中导电的离子不是它本身产生的,但它却是电解质
2
D.SO 溶于水后所得到的HSO 溶液能导电,故SO 是电解质
3 2 4 3
【答案】C
【解析】A项错选原因在于对酸式盐电离方程式的写法不清楚,NaHCO 是弱酸酸式
3
盐,可以全部电离成Na+和HCO,但HCO不能拆成H+和CO;因此正确写法是
NaHCO ===Na++HCO;错选B的原因在于未明确电解质溶液导电性强弱的本质原因。溶
3
液的导电能力是由溶液中阴、阳离子的浓度所决定的,与离子的个数没有直接的关系。离
子个数少的溶液的导电能力可能会大大强于离子个数多的溶液;D项错选原因在于对概念
的理解很浅,未理解到位。SO 溶于水后发生了反应:SO +HO===H SO ,体系中已经与
3 3 2 2 4
SO 没有任何关系。故溶液能导电只能说明HSO 是电解质。
3 2 4
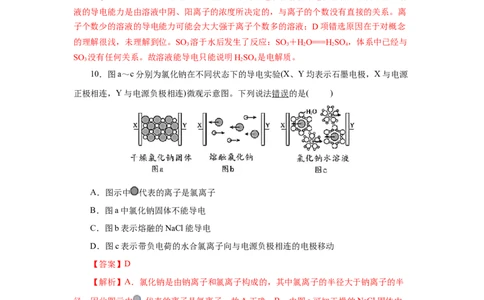
10.图a~c分别为氯化钠在不同状态下的导电实验(X、Y均表示石墨电极,X与电源
正极相连,Y与电源负极相连)微观示意图。下列说法错误的是( )
A.图示中 代表的离子是氯离子
B.图a中氯化钠固体不能导电
C.图b表示熔融的NaCl能导电
D.图c表示带负电荷的水合氯离子向与电源负极相连的电极移动
【答案】D
【解析】A.氯化钠是由钠离子和氯离子构成的,其中氯离子的半径大于钠离子的半
径,因此图示中 代表的离子是氯离子,故A正确;B.由图a可知干燥的NaCl固体中
钠离子和氯离子不能自由移动,因此NaCl固体不能导电,故B正确;C.由图b可知熔融
状态下钠离子和氯离子能自由移动,因此熔融的NaCl能导电,故C正确;D. 表示氯离
子,由图c可知带负电荷的水合氯离子向X电极移动,即向与电源正极相连的电极移动,
故D错误;答案为D。
能力提升11.下列关于电解质电离的叙述中正确的是( )
A.CaCO 在水中溶解度很小,其导电能力很弱,所以CaCO 是弱电解质
3 3
B.水难电离,纯水几乎不导电,水是非电解质
C.氯气和氨气的水溶液导电性都很好,所以它们是强电解质
D.CaCO 在水中溶解度很小,但溶解的CaCO 全部电离,所以CaCO 是强电解质
3 3 3
【答案】D
【解析】CaCO 不是弱电解质,因为溶解的部分全部电离,氯气和氨气在水中均不能
3
电离出离子,它们不是电解质,之所以能够导电是因为生成了电解质 HCl、HClO 和
NH ·H O。水是极弱的电解质。
3 2
12.下列叙述中正确的是 ( )
A.氯化镁晶体不能导电的原因是氯化镁晶体中不含阴、阳离子
B.在电流作用下氯化钠在水溶液中电离成钠离子和氯离子
C.氯化钾晶体不能导电而其水溶液能导电的原因是氯化钾与水发生化学反应产生了
钾离子和氯离子
D.氯化钾晶体不能导电的原因是构成氯化钾晶体的钾离子和氯离子不能自由移动,
而溶于水后在水分子的作用下产生了自由移动的钾离子和氯离子,所以其水溶液能导电
【答案】D
【解析】氯化镁晶体是由镁离子和氯离子构成的,其晶体之所以不导电是因为镁离
子、氯离子被束缚在晶体中不能自由移动,故A项错误;电解质的电离是指电解质溶于水
或者熔融状态下产生能自由移动的离子的过程,电离不需要外加电流就能发生,故B项错
误;氯化钾溶于水并没有发生化学反应,水溶液中的钾离子、氯离子是氯化钾本身含有
的,故C项错误。
13.有以下13种物质,请回答下列问题:
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧
冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
(1)其中能导电的是 ___________; 属于电解质的是 ___________;属于非电解质
的是 ___________。
(2)写出物质⑥溶于水的电离方程式:________________________________。物质⑬
属于___________(填“酸”、“碱”或“盐”)。
(3)写出物质⑦和⑪反应的化学方程式:____________________________________。
(4)写出物质⑥和⑨在水中发生反应的化学方程式:
______________________________。
【答案】(1)①④⑦⑪ ②⑥⑧⑨⑩⑫⑬ ③⑤
(2)NaHCO = Na+ + HCO - 盐
3 3(3)Ba (OH ) + H SO = BaSO ↓+2H O
2 2 4 4 2
(4)NaHCO + HCl=NaCl +H O + CO↑
3 2 2
【解析】(1)①石墨存在自由移动的电子,可以导电;石墨是单质,既不是电解质也
不是非电解质;②氧化钠固体没有自由移动的带电微粒,不可以导电;在熔融状态下可以
导电,属于电解质;③酒精中没有自由移动的带电微粒,不能导电;在水溶液和熔融状态
不能导电属于非电解质;④氨水中含有自由移动的铵根离子和氢氧根离子,可以导电;但
氨水是混合物,既不是电解质也不是非电解质;⑤二氧化碳中没有自由移动的带电微粒,
不能导电;在水溶液中导电是因为生成碳酸的原因,在熔融状态不能导电属于非电解质;
⑥碳酸氢钠固体没有自由移动的带电微粒,不可以导电;在水溶液中可以电离出钠离子和
碳酸氢根离子,可以导电,属于电解质;⑦氢氧化钡溶液中含有自由移动的钡离子和氢氧
根离子,可以导电;氢氧化钡溶液属于混合物,既不是电解质,也不是非电解质;⑧冰醋
酸中没有自由移动的带电微粒,不能导电;冰醋酸的水溶液中含有自由移动的氢离子和醋
酸根离子,可以导电,故冰醋酸属于电解质;⑨氯化氢中没有自由移动的带电微粒,不能
导电;氯化氢的水溶液盐酸中含有自由移动的氢离子和氯离子,可以导电,故氯化氢为电
解质;⑩硫酸铝固体中没有自由移动的带电微粒,不能导电;硫酸铝在水溶液和熔融状态
下有自由移动的铝离子和硫酸根离子,可以导电,故硫酸铝属于电解质;⑪稀硫酸中含有
自由移动的氢离子和硫酸根离子,可以导电;稀硫酸属于混合物,既不是电解质也不是非
电解质;⑫氯化银中没有自由移动的带电微粒,不能导电;氯化银在水溶液和熔融状态下
可以提供自由移动的离子,属于电解质;⑬硫酸氢钠中没有自由移动的带电微粒,不能导
电;在水溶液中可以完全电离出Na+、H+、SO 2-和熔融状态下可以完全电离出Na+和
4
HSO -,可以导电,故硫酸氢钠属于电解质;
4
其中能导电的是 ①④⑦⑪;;属于电解质的是②⑥⑧⑨⑩⑫⑬;属于非电解质的是③⑤;
答案为:①④⑦⑪ ;②⑥⑧⑨⑩⑫⑬ ;③⑤;
(2)碳酸氢钠属于弱酸的酸式盐,溶于水电离出钠离子和碳酸氢离子,电离方程式
为:NaHCO = Na+ + HCO -;属于盐;答案为:NaHCO = Na+ +HCO - ; 盐;
3 3 3 3
(3)氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,反应的化学方程式:Ba (OH ) +
2
HSO = BaSO ↓+2H O;答案为:Ba (OH ) + H SO = BaSO ↓+2H O;
2 4 4 2 2 2 4 4 2
(4)碳酸氢钠和盐酸反应生成氯化钠、水、二氧化碳,化学方程式为: NaHCO +
3
HCl=NaCl +H O + CO↑ 答案为: NaHCO + HCl=NaCl +H O + CO↑
2 2 3 2 2
14.已知:CO +Ca(OH) ===CaCO ↓+HO,CaCO +CO +HO===Ca(HCO ) ,且
2 2 3 2 3 2 2 3 2Ca(HCO ) 易溶于水。试根据如图所示装置回答下列问题:
3 2
(1)通入CO 前,灯泡________(填“亮”或“不亮”)。
2
( 2 ) 开 始 通 入 CO 至 Ca(OH) 恰 好 完 全 反 应 生 成 CaCO , 灯 泡 的 亮 度
2 2 3
________________。
(3)继续通入过量的CO,灯泡的亮度________________。
2
(4)下列四个图中,________(填字母)能比较准确地反映出溶液的导电能力和通入
CO 气体量的关系(x轴表示CO 通入的量,y轴表示导电能力)。
2 2
A B C D
【答案】(1)亮 (2)先变暗后熄灭 (3)又逐渐变亮 (4)D
【解析】(1)灯泡亮,因为Ca(OH) 溶于水后完全电离出离子,溶液中离子的浓度比较
2
大,故灯泡亮。
(2)灯泡先变暗后熄灭,因为发生了CO +Ca(OH) ===CaCO ↓+HO,溶液中自由移动
2 2 3 2
的离子减少。
(3)灯泡熄灭后又逐渐变亮:CaCO +CO +HO===Ca(HCO ) ,Ca(HCO ) 完全电离出
3 2 2 3 2 3 2
自由移动的离子,溶液中离子浓度增大。(4)由于通入CO 后溶液中自由移动的离子的浓度
2
逐渐减小,所以一开始导电能力逐渐下降,随着反应的进行,离子浓度逐渐增大,导电能
力逐渐增大,所以选D。
直击高考
15.下列说法正确的是( )
A.某化合物的水溶液能导电,则该化合物为电解质
B.BaSO 的饱和水溶液导电性很弱,故BaSO 是弱电解质
4 4
C.NaHCO 是强电解质,故NaHCO 的电离方程式为NaHCO ===Na++H++CO
3 3 3
D.等浓度的醋酸溶液的导电能力弱于NaOH溶液
【答案】D
【解析】CO 、SO 的水溶液均能导电,但不是它们本身导电,而是反应生成的HCO
2 2 2 3
和HSO 导电,二者均为非电解质,A项错误;电解质的强弱与溶液的导电性没有必然的
2 3联系,BaSO 是盐,属于强电解质,B 项错误;NaHCO 是强电解质,电离方程式为
4 3
NaHCO ===Na++HCO,C 项错误;等浓度的醋酸溶液中自由移动的离子的浓度小于
3
NaOH溶液,导电能力弱,D项正确。
16.酸、碱、盐溶液是初高中化学中常用试剂。酸、碱、盐溶液之所以能够导电,是因
为它们溶于水时,解离成为自由移动的阴、阳离子。
(1)在酸的溶液里,酸根离子所带________的总数等于酸电离时生成的________的总
数;在碱的溶液里,跟金属离子结合的________的总数等于这种金属离子所带的________
的总数;在盐的溶液中,金属离子所带的________的总数等于酸根离子所带的________的
总数。
(2)下列物质的电离方程式如下:
HClO H++Cl ; Ba(OH) Ba2++2OH-;
4 O− 2
4
Fe (SO ) 2Fe3++3S ; KHSO K++H++S 。
2 4 3 O2− 4 O2−
4 4
属于酸的物质为_______________(写化学式);属于碱的物质为______________;属于
盐的物质为______________。
(3)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧
碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是________________。
② 上 述 物 质 中 既 不 是 电 解 质 也 不 是 非 电 解 质 的 是 ________ 。 依 据 是
__________________。
③写出纯碱的电离方程式: _
。
【答案】:(1)负电荷 H+ OH- 正电荷 正电荷 负电荷
(2)HClO Ba(OH) Fe (SO )、KHSO
4 2 2 4 3 4
(3) ①纯碱 ②盐酸 盐酸是混合物,不是化合物 ③Na
2
CO
3
==2Na++C
O2−
3