文档内容
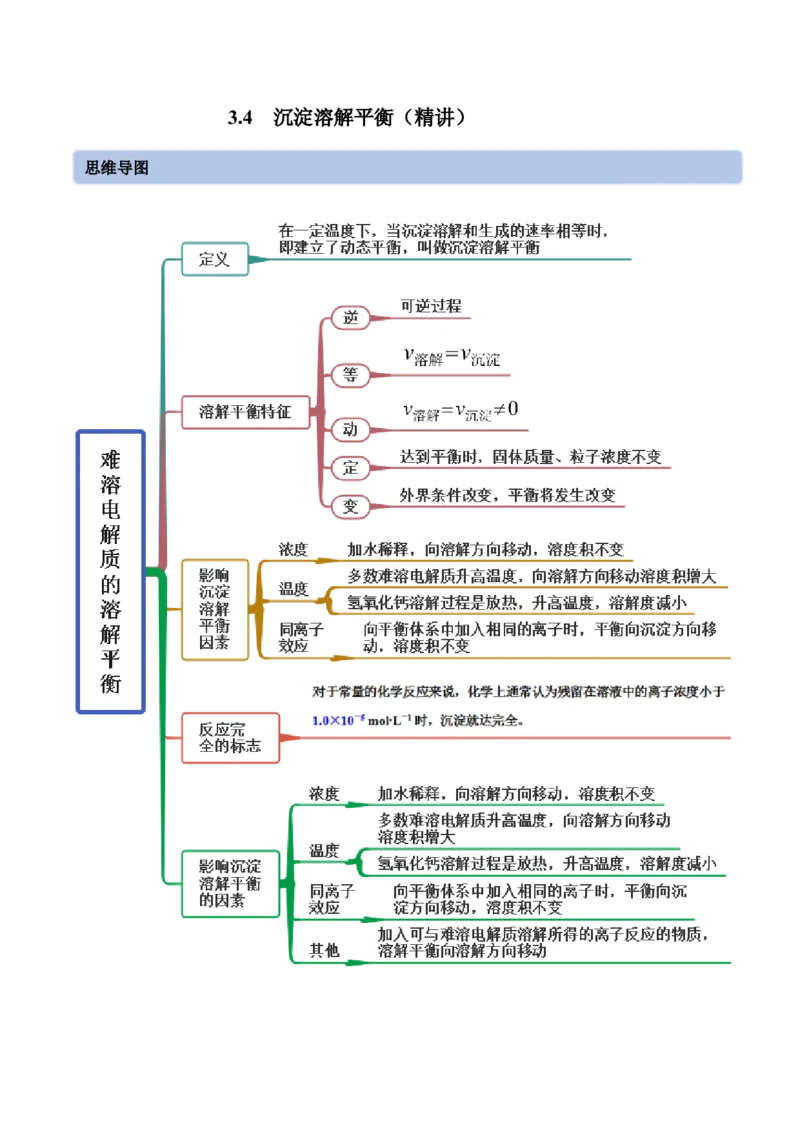
3.4 沉淀溶解平衡(精讲)
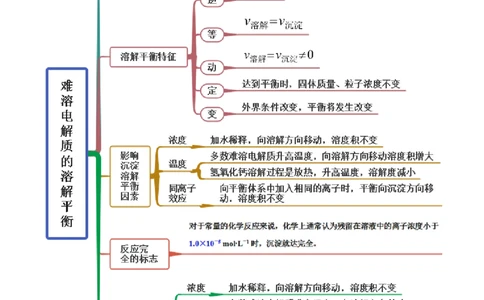
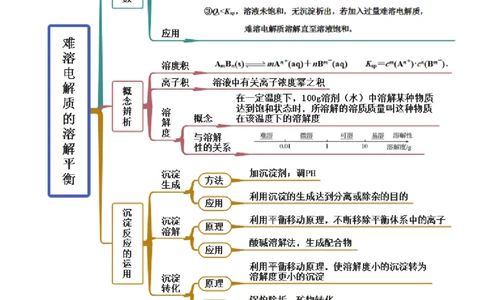
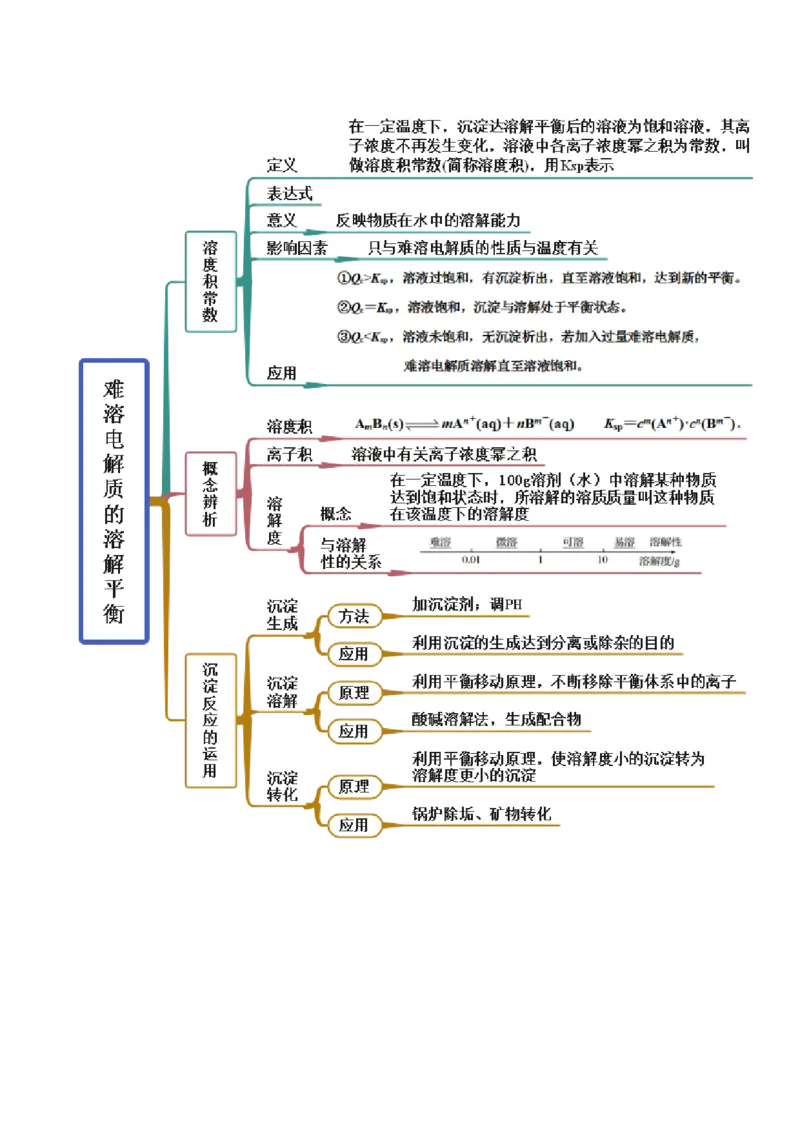
思维导图常见考点
考点一 沉淀溶解平衡
【例1】(2021·全国·高二课时练习)下列说法中正确的是
A.只有易溶电解质在溶液中才存在溶解平衡
B.难溶电解质在溶液中只存在溶解平衡,不存在电离平衡
C.溶解平衡只能通过电解质溶于水时建立
D.溶解平衡时,电解质表面上的离子或分子脱离电解质的速率与溶液中的离子或分子回到电解质表面的
速率相等
【一隅三反】
1.(2022·全国·高二课时练习)有关AgCl沉淀的溶解平衡说法正确的是
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.在AgCl的澄清饱和溶液中,只要向其中加入NaCl溶液,一定会有沉淀生成
D.向含有AgCl沉淀的悬浊液中加入NaCl固体,AgCl的溶解度增大
2.下列关于沉淀溶解平衡的说法正确的是
A.只有难溶电解质才存在沉淀溶解平衡
B.沉淀溶解平衡是可逆的
C.在平衡状态时
D.达到沉淀溶解平衡的溶液不一定是饱和溶液
3.(2021·全国·高二课时练习)对“AgCl(s) Ag+(aq)+Cl-(aq)”的理解正确的是①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底
A.③④ B.②③ C.①③ D.②④
考点二 沉淀溶解平衡的影响因素
【例2】(2022·全国·高二课时练习)在FeS悬浊液中,存在平衡FeS(s) Fe2+(aq)+S2-(aq)。欲使FeS固体
质量减少,Fe2+浓度不变,可向悬浊液中加入的试剂是 ⇌
A.CuSO 溶液 B.盐酸 C.蒸馏水 D.NaS
4 2
【一隅三反】
1.(2022·全国·高二课时练习)25 ℃时,在含有大量PbI 的饱和溶液中存在着平衡PbI (s) Pb2+(aq)+
2 2
2I-(aq),加入KI溶液,下列说法正确的是
A.溶液中Pb2+和I-浓度都增大 B.溶液中Pb2+和I-浓度都减小
C.沉淀溶解平衡向右移动 D.溶液中Pb2+浓度减小
2.(2022·全国·高二课时练习)石灰乳中存在下列平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq);加入下列溶液,
2
可使固体明显减少的是
A.NaCO 溶液 B.KCl溶液
2 3
C.NaOH溶液 D.CaCl 溶液
2
3(2022·浙江丽水·高二开学考试)在平衡体系Ca(OH) (s) Ca2++2OH- H<0中,能使c(Ca2+)减小,
2
而使c(OH-)增大的是 △
A.加入少量CuCl 固体 B.加入少量NaCl固体
2
C.加入少量KCO 固体 D.升高体系温度
2 3
考点三 溶度积常数及其应用
【例3-1】(2022·黑龙江·嫩江市第一中学校高二开学考试)在一定温度下,氯化银在水中存在如下沉淀溶
解平衡:AgCl(s) Ag+(aq)+Cl—(aq),若把AgCl分别放入①100mL0.1mol/LNaNO 溶液中;
3
②100mL0.1mol/LNaCl溶液中;③100mL0.1mol/LAlCl 溶液中;④100mL0.1mol/LMgCl 溶液中,搅拌后
3 2
在相同的温度下Ag+浓度由大到小的顺序是:
A.①>②>④>③ B.②>①>④>③
C.④>③>②>① D.①>④>③>②
【例3-2】(2022·全国·高二课时练习)已知CaCO 的K =2.8×10-9,现将浓度为2×10-4mol•L-1的NaCO 溶
3 sp 2 3液与CaCl 溶液等体积混合,若要产生沉淀,则所用CaCl 溶液的浓度至少应为
2 2
A.2.8×10-2mol•L-1 B.1.4×10-5mol•L-1 C.2.8×10-5mol•L-1 D.5.6×10-5mol•L-1
【例3-3】(2022·云南省通海县第三中学高二期末)已知:某温度时,K (AgCl)=1.8×10-10,K (Ag CrO)
sp sp 2 4
=1.1×10-12。向Cl-和CrO 的浓度都为0.100 mol·L-1的混合溶液中逐滴加入AgNO 溶液(忽略体积的变
3
化)。下列说法中正确的是
A.首先得到的沉淀是Ag CrO
2 4
B.首先得到的沉淀是AgCl
C.同时得到AgCl与Ag CrO 沉淀
2 4
D.将Ag CrO 转化为AgCl比将AgCl转化为Ag CrO 要难
2 4 2 4
【一隅三反】
1.(2022·全国·高二课时练习)已知K (AgCl)=1.8×10-10,K (AgBr)=7.7×10-13,K (Ag CrO)=9.0×10-12.某
sp sp sp 2 4
溶液中含有Cl-、Br-和 的浓度均为0.010mol·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO 溶液时,
3
三种阴离子产生沉淀的先后顺序为
A.Cl-、Br-、 B. 、Br-、Cl-
C.Br-、Cl-、 D.Br-、 、Cl-
2.(2022·内蒙古呼和浩特·高二期末)已知25℃时,AgCl的K =1.56×10-10,AgBr的K =5.0×10-13,将
sp sp
AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银溶液,发生的反应为
A.只有AgBr沉淀生成 B.AgCl和AgBr沉淀等量生成
C.AgCl沉淀少于AgBr沉淀 D.AgCl沉淀多于AgBr沉淀
3.(2021·重庆·巫山县官渡中学高二阶段练习)下表是五种银盐的溶度积常数(25℃),下列有关说法错误
的是
化学式 AgCl Ag SO Ag S AgBr AgI
2 4 2
溶度积 1.8×10-10 1.4×10-5 6.3×10-50 5.0×10-13 8.3×10-17
A.五种物质在常温下溶解度最大的是Ag SO
2 4
B.向AgCl的悬浊液中加入0.1mol/LNa S溶液,则可以生成黑色的Ag S沉淀
2 2
C.外界条件改变时,沉淀溶解平衡也会发生移动
D.常温下,向AgI的悬浊液中加入0.1mol/LNaCl溶液,黄色沉淀变成白色沉淀4.(1)对于Ag S(s) 2Ag+(aq)+S2-(aq),其K 的表达式为_______
2 sp
(2)下列说法不正确⇌的是_______(填序号)。
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH) (s) Al3+(aq)+3OH-(aq)和Al(OH) Al3++3OH-,前者为溶解平衡,后者为电离平衡
3 3
⇌ ⇌
④除去溶液中的Mg2+,用OH-沉淀比用CO 好,说明Mg(OH) 的溶解度比MgCO 大
2 3
⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH) 中混有的Ca(OH) _______
2 2
(4)已知在25 ℃时K [Mg(OH) ]=3.2×10-11,向0.02 mol·L-1的MgCl 溶液中加入NaOH固体,如要生成
sp 2 2
Mg(OH) 沉淀,应使溶液中的c(OH-)最小为_______mol·L-1。
2
考点四 沉淀溶解平衡的应用
【例4】I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg•L-1。处理含镉废水
可采用化学沉淀法。
(1)写出磷酸镉[Cd (PO )]沉淀溶解平衡常数的表达式:K [Cd (PO )]=____。
3 4 2 sp 3 4 2
(2)一定温度下,CdCO 的K =4.0×10-12,Cd(OH) 的K =3.2×10-14,该温度下____[填“CdCO”或
3 sp 2 sp 3
“Cd(OH) ”]的饱和溶液中Cd2+浓度较大。
2
(3)向某含镉废水中加入NaS,当S2-浓度达到7.9×10-8mol•L-1时,废水中Cd2+的浓度为____mol•L-1[已知:
2
K (CdS)=7.9×10-27],此时_____(填“符合”或“不符合”)《生活饮用水卫生标准》。
sp
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,K [Mg(OH) ]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如表:
sp 2
pH <8.0 8.0~9.6 >9.6
颜色 黄色 绿色 蓝色
25℃时,向Mg(OH) 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____。
2
(5)常温下,向50mL0.018mol•L-1的AgNO 溶液中加入50mL0.020mol•L-1的盐酸,生成沉淀。已知该温度下,
3
K (AgCl)=1.8×10-10,忽略溶液体积的变化。
sp
①反应后,溶液的pH=____。
②如果向反应后的溶液中继续加入50mL0.001mol•L-1的盐酸,____(填“有”或“无”)白色沉淀生成。
【一隅三反】1.(2022·福建·莆田第七中学高二期中)某温度时,BaSO 在水中的沉淀溶解平衡曲线如图所示。请回答
4
下列问题:
(1)下列说法正确的是_______。
A.加入NaSO 可以使溶液由a点变到b点
2 4
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO 沉淀生成
4
D.a点对应的K 大于c点对应的K
sp sp
(2)将沉淀用100 mL纯水和100 mL 0.01 mol·L-1的HSO 分别洗涤,两种情况下损失的BaSO 的质量之比为
2 4 4
_______。
(3)工业上用饱和碳酸钠溶液浸泡硫酸钡,将其转化为碳酸钡,发生反应的离子方程式为_______。
2.(2022·陕西宝鸡·高二期末)难溶电解质的沉淀溶解平衡及其溶度积常数在生产、科研等领域有着诸的
应用。25℃时,各物质的溶度积如下表所示:
难溶电解质 AgCl AgBr AgI BaSO
4
Ksp 1.8×10-10 4.9×10-13 8.3×10-17 1×10-10
(1)现将足量AgCl(s)分别加入下列四种溶液:①100mL蒸馏水;②100mL0.1mol·L-1盐酸;
③100mL0.1mol·L-1AlCl 溶液,④100mL0.1mol·L-1MgCl 溶液。充分搅拌后,相同温度下,Ag+浓度由大到
3 2
小的顺序是_______(填序号)。
(2)大量的碘富集在海藻中,用水浸取后浓缩,该浓缩液中主要含有I-、Cl-等离子。取一定量的浓缩液,向
其中滴加AgNO 溶液,当AgCl开始沉淀时,溶液中 为_______。
3
(3)钡餐是医学检查肠胃的常用造影剂。当人体中Ba2+浓度达到2×10-3mol·L-1时会影响健康,若有人误服氯
化钡,请回答能否通过服用5%的硫酸钠溶液有效除去胃中的Ba2+并说明理由。(已知:5%的硫酸钠溶液物
质的量浓度约0.36mol·L-1)_______。
3.(2021·山东·临沂第二中学高二阶段练习)运用化学反应原理,研究硫、磷化合物的反应具有重要意义。(1)已知HPO (次磷酸)的水溶液中存在 HPO 分子。HPO 与足量 NaOH溶液充分反应,消耗的酸和碱的
3 2 3 2 3 2
物质的量相等,则生成盐的化学式为___________,该盐属于___________(填"正盐"或"酸式盐")。HPO 易
3 2
被氧化为 HPO ,已知常温下HPO 的电离常数为 ,请利用以
3 4 3 4
上数据计算推测 NaHPO 溶液的酸碱性___________。(填“酸性”、“碱性”或“中性”)
2 4
(2)常温下,用NaOH溶液吸收 SO 得到 pH=9的NaSO 溶液,吸收过程中水的电离衡___________(填"向
2 2 3
左"、"向右"或"不")移动。试计算该溶液中 ___________。(常温下 HSO 的电离平衡常数
2 3
)
(3)NaHSO 溶液的pH<7,NaHCO 溶液的pH>7,则NaHSO 溶液中c(H SO )___________(填“>”
3 3 3 2 3
“<”或“=”,下同)c( ),NaHCO 溶液中c(H CO)___________c( )。
3 2 3
(4)化工生产中常用 FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(q)+FeS(s) CuS(s)+Fe2+(aq)。
下列有关叙述正确的是___________ 。 ⇌
a.
b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量 NaS固体后,溶液中c(Fe2+)、c(Cu2+)都减小
2
d. 该反应平衡常数倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育