文档内容
3.3.3三大守恒(分层作业)
1.在室温下,下列有关电解质溶液的说法正确的是
A.NaSO 溶液中:c(OH-)=c(HSO- )+c(H SO )+c(H+)
2 3 3 2 3
B.NaHA溶液的pH<7,则溶液中的粒子有:c(HA)>c(A2-)
2
C.向某稀NaHCO 溶液中通入CO 至pH=7:c(Na+)=c(HCO- )+2c(CO2- )
3 2 3 3
D.浓度均为0.1mol·L-1 CHCOOH与NaOH按体积2∶1混合:c(CHCOO-)c(Na+),故D错误;
3 3
故选C 。
2.室温时,用0.1000mol/L的NaOH标准溶液滴定同浓度20mL的NH HSO 溶液(稀溶液中不考虑氨水的
4 4
分解导致氨的逸出)。下列说法错误的是
A.滴定过程中,溶液中c(SO2- )逐渐减小
4
B.V(NaOH)=20mL时:c(NH+ )+c(H+)-c(Na+)=c(OH-)
4
C.V(NaOH)=40mL时:c(Na+)>c(SO2- )>c(NH+ )>c(OH-)
4 4
D.V(NaOH)分别为20mL和40mL时水的电离程度:前者>后者
【答案】C
【解析】A.滴定过程中n(SO2- )不变,但溶液体积变大,故c(SO2- )变小,A正确;
4 4
B.V(NaOH)=20mL时恰好发生反应:2NH HSO +2NaOH=Na SO +(NH)SO +2H O,由电荷守恒,存在:
4 4 2 4 4 2 4 2
c(NH+ )+c(Na+)+c(H+)=2c(SO2- )+c(OH-);由物料守恒,存在:c(Na+)=c(SO2- ),故溶液存在:c(NH+ )+c(H+)-
4 4 4 4
c(Na+)=c(OH-),B正确;
C.V(NaOH)=40mL时:NH HSO +2NaOH=Na SO +NH·H O+HO,溶质为NaSO 和NH ·H O,
4 4 2 4 3 2 2 2 4 3 2
c(Na+)>c(SO2- )>c(OH-)>(NH+ ),C错误;
4 4
D.V(NaOH)=20mL时,溶液中存在等物质的量的NaSO 、(NH )SO ,NH+ 水解,促进水的电离,而
2 4 4 2 4 4V(NaOH)=40mL时一水合氨电离,抑制水的电离,所以前者大于后者,D正确;
故选C。
3.下列有关25℃时1mol/L NaHSO 溶液(H SO 的K =10-2、K =10-8)的说法正确的是
3 2 3 a1 a2
A.NaHSO=Na++H++SO2-
3 3
B.c(HSO- )>c(SO2- )
3 3
C.c(OH-)=c(H+)+c(HSO- )+2c(H SO )
3 2 3
D.n(SO2- )+n(HSO- )+n(HSO )=1mol
3 3 2 3
【答案】B
【解析】A.NaHSO 为弱酸的酸式盐,NaHSO 的电离方程式为NaHSO=Na++HSO- ,故A错误;
3 3 3 3
B.HSO- 的电离平衡常数为1×10-8,所以NaHSO 溶液中c(HSO- )>c(SO2- ),故B正确;
3 3 3 3
C.根据质子守恒,NaHSO 溶液中c(OH-)+c(SO2- )=c(H+)+c(H SO ),故C错误;
3 3 2 3
D.根据物料守恒,c(SO2- )+c(HSO- )+c(H SO )=1mol,没有溶液体积,n(SO2- )+n(HSO- )+n(HSO )不一定为
3 3 2 3 3 3 2 3
1mol,故D错误;
选B。
4.钾的化合物对调节体内循环有重要用途,一定温度下,下列溶液中的离子浓度关系式正确的是
A.0.1 mol·L-1的KHCO 溶液中:c(K+)+c(H+)=c(HCO- )+c(CO2- )+c(OH-)
3 3 3
B.KS溶液中:2c(K+)=c(S2-)+c(HS-)+c(H S)
2 2
C.KCO 溶液中:c(OH-)=c(H+)+c(HCO- )+2c(H CO)
2 3 3 2 3
D.pH相同的①CHCOOK、②KOH、③KClO三种溶液中的c(K+):③>①>②(已知:CHCOOH的
3 3
K=1.75×10-5,HClO的K=4.0×10-8)
a a
【答案】C
【解析】A.根据电荷守恒可得:c(K+)+c(H+)=c(HCO- )+2c(CO2- )+c(OH-),故A错误;
3 3
B.根据物料守恒可得:c(K+)=2c(S2-)+2c(HS-)+2c(H S),故B错误;
2
C.根据质子守恒可得:c(OH-)=c(H+)+c(HCO- )+2c(H CO),故C正确;
3 2 3
D.由K 可知,相同物质的量浓度,三种溶液的pH大小为②>③>①,所以pH相同时,三种溶液的物质的
a
量浓度大小为②<③<①,则c(K+):②<③<①,故D错误;
故选C。
5.常温下,下列说法正确的是
A.pH=8的NaHCO 溶液中,水电离产生的c(OH-)=10-8mol/L
3
B.pH相等的CHCOONa、NaOH和NaCO 三种溶液:c(NaOH)c(SO2- )+c(HSO- ),故D错误;
4 3 3
选B。
7.25℃时HC O 的电离平衡常数为K =5.0×10-2,K =5.4×10-5。常温下,关于1mol·L-1的HC O 溶液的理
2 2 4 a1 a2 2 2 4
解正确的是
A.加水稀释过程中,溶液的pH减小
B.[H C O]+[HC O- ]+[C O2- ]=1mol·L-1
2 2 4 2 4 2 4
C.溶液中,1mol·L-1<[H+]<2mol·L-1
D.溶液中,HC O 电离出的[H+]:[C O2- ]=2:1
2 2 4 2 4
【答案】B
【解析】A.加水稀释促进HC O 电离,但是HC O 电离程度小于溶液体积增大程度,则稀释后c(H+)减
2 2 4 2 2 4
小,溶液的pH增大,故A错误;
B.溶液中存在物料守恒,根据物料守恒得[H C O]+[HC O- ]+[C O2- ]=1mol·L-1,故B正确;
2 2 4 2 4 2 4
C.HC O 是二元弱酸,部分电离且电离程度较小,则溶液中c(H+)<1mol/L,故C错误;
2 2 4
D.HC O 是二元弱酸,部分电离,且第一步电离程度大于第二步电离程度,则溶液中[H+]:[C O2- ]>2:1,故
2 2 4 2 4
D错误;
故选:B。
8.室温下,将两种浓度均为0.10mol·L-1的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各
混合溶液中微粒物质的量浓度关系正确的是
A.NaHCO -Na CO 混合溶液:3c(Na+)=2c(HCO- )+2c(CO2- )+2c(H CO)
3 2 3 3 3 2 3
B.氨水—NH Cl混合溶液(K(NH ·H O)=1.8×10-5) :c(NH+ )>c(Cl-)>c(NH·H O)>c(OH-)>c(H+)
4 b 3 2 4 3 2
C.CHCOOH-CH COONa混合溶液:c(H+)+c(Na+)=c(OH-)+c(CH COOH)
3 3 3
D.HC O-NaHC O 混合溶液:2c(H+)+c(H C O)=c(C O2- )+2c(OH-)
2 2 4 2 4 2 2 4 2 4
【答案】B
【解析】A.根据物料守恒,NaHCO -Na CO 等物质的量的混合溶液中存在:
3 2 3
2c(Na+)=3c(HCO- )+3c(CO2- )+3c(H CO),A错误;
3 3 2 3
1×10−14
B.由K(NH ·H O)=1.8×10-5可知NH+ 水解常数为 <K(NH ·H O),NH+ 水解程度小于NH ·H O的
b 3 2 4 1.8×10−5 b 3 2 4 3 2
电离程度,则氨水—NH Cl混合溶液呈碱性,溶液中c(NH+ )>c(Cl-)>c(NH·H O)>c(OH-)>c(H+),B正确;
4 4 3 2
C.CHCOOH-CH COONa混合溶液中,根据电荷守恒存在:c(H+)+c(Na+)=c(OH-)+c(CH COO-),C错误;
3 3 3
D.HC O-NaHC O 混合溶液,根据电荷守恒:c(H+)+c(Na+)=2c(C O2- )+c(OH-)+c(HC O- ),和物料守恒:
2 2 4 2 4 2 4 2 4c(HC O- )+c(C O2- )+c(H C O)=2C(Na+),可得2c(H+)+c(H C O)=3c(C O2- )+2c(OH-)+c(HC O- ),D错误;
2 4 2 4 2 2 4 2 2 4 2 4 2 4
故选B。
9.磷能形成次磷酸(H PO )、亚磷酸(H PO )等多种含氧酸。
3 2 3 3
(1)次磷酸(H PO )是一种精细化工产品,已知10 mL 1 mol·L-1HPO 与20 mL 1 mol·L-1NaOH溶液充分反应
3 2 3 2
后生成组成为NaH PO 的盐,回答下列问题:
2 2
①NaHPO 属于 (填“正盐”“酸式盐”或“无法确定”)。
2 2
②若25 ℃时,K(H PO )=1×10-2,则0.02 mol·L-1的HPO 溶液的pH= 。
a 3 2 3 2
③设计两种实验方案,证明次磷酸是弱酸: 、 。
(2)亚磷酸(H PO )是二元中强酸,某温度下,0.11 mol·L-1的HPO 溶液的pH为2,该温度下HPO 的电离
3 3 3 3 3 3
平衡常数K 约为 (K =2×10-7,HPO 的二级电离和水的电离忽略不计)。
a1 a2 3 3
(3)向HPO 溶液中滴加NaOH溶液:
3 3
①当恰好中和生成NaHPO 时,所得溶液的pH (填“>”“<”或“=”,下同)7。
2 3
②当溶液呈中性时,所得溶液中c(Na+) c(HPO )+2c(HPO )。
2
③若用甲基橙作为指示剂,用NaOH溶液滴定,达到滴定终点时,所得溶液中c(Na+) c(HPO
2
)+2c(HPO )。
【答案】(1) 正盐 2 测NaH PO 溶液的pH,若pH>7,则证明次磷酸为弱酸 向等物质
2 2
的量浓度的盐酸、次磷酸溶液中各滴入2滴石蕊溶液,若次磷酸溶液中红色浅一些,则说明次磷酸为弱酸
(2)1×10-3
(3) > = <
【解析】(1)①NaOH溶液过量,只生成NaH PO ,说明次磷酸中只有一个可电离的氢原子,因而
2 2
NaH PO 是正盐。②设溶液中的H+浓度为x mol·L-1;
2 2
HPO ⇌ H+ + H2PO- 2
3 2
初始(mol·L-1) 0.02 0 0
平衡(mol·L-1) 0.02-x x x
x2
K(H PO )= =1×10-2,解得x=0.01,故pH=-lg 0.01=2.③可从NaH PO 溶液中存在水解平衡以及
a 3 2 2 2
0.02−x
HPO 存在电离平衡等角度设计实验。
3 2
(2)忽略HPO 的二级电离和水的电离,则c(HPO- )≈c(H+)=1×10-2 mol·L-1,c(HPO )=(0.11-1×10-2)
3 3 2 3 3 3c(H+ )·c(H PO− ) 1×10−2×1×10−2
mol·L-1=0.1 mol·L-1,则该温度下HPO 的电离平衡常数K = 2 3 ≈
3 3 a1
c(H PO ) 0.1
3 3
=1×10-3;
(3)①NaHPO 溶液中,HPO2- 水解,溶液呈碱性。②溶液呈中性时,c(H+)=c(OH-),根据电荷守恒得
2 3 3
c(Na+)=c(HPO- )+2c(HPO2- )。③溶液中存在电荷守恒:c(Na+)+c(H+)=c(HPO- )+2c(HPO2- )+c(OH-),用甲
2 3 3 2 3 3
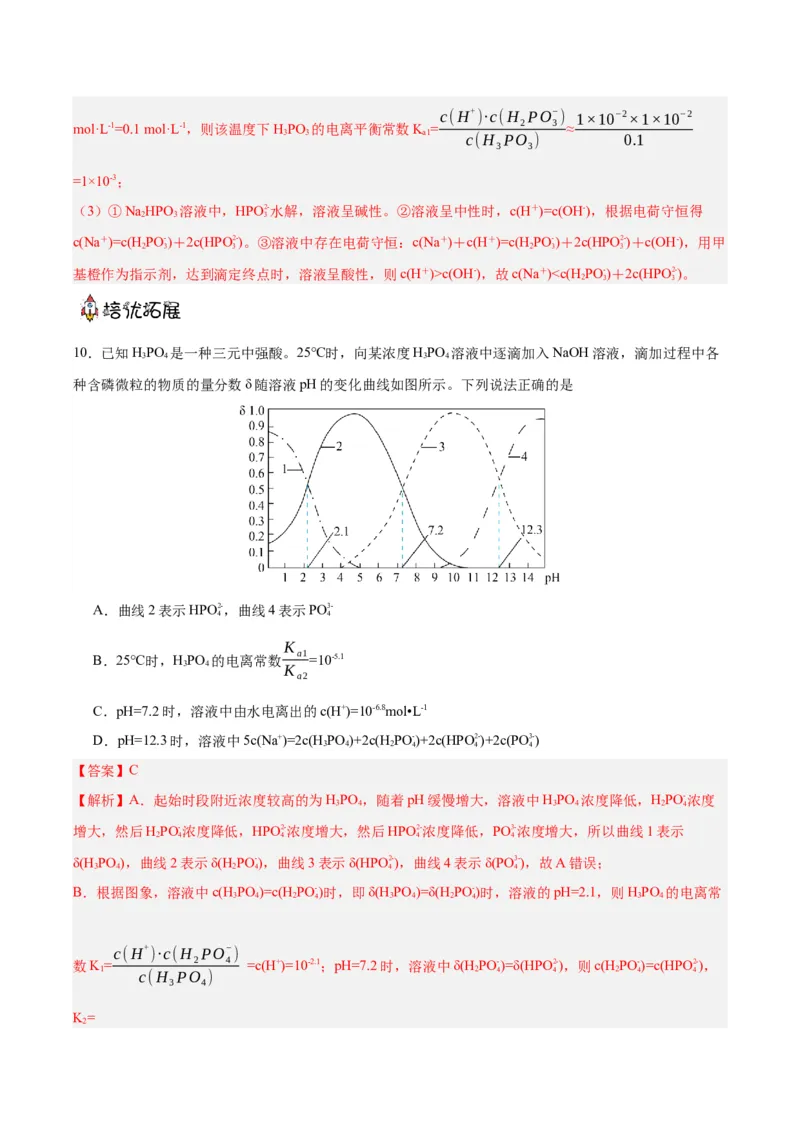
基橙作为指示剂,达到滴定终点时,溶液呈酸性,则c(H+)>c(OH-),故c(Na+)2c(A2-)+c(HA-),D错误;
故答案为:B。
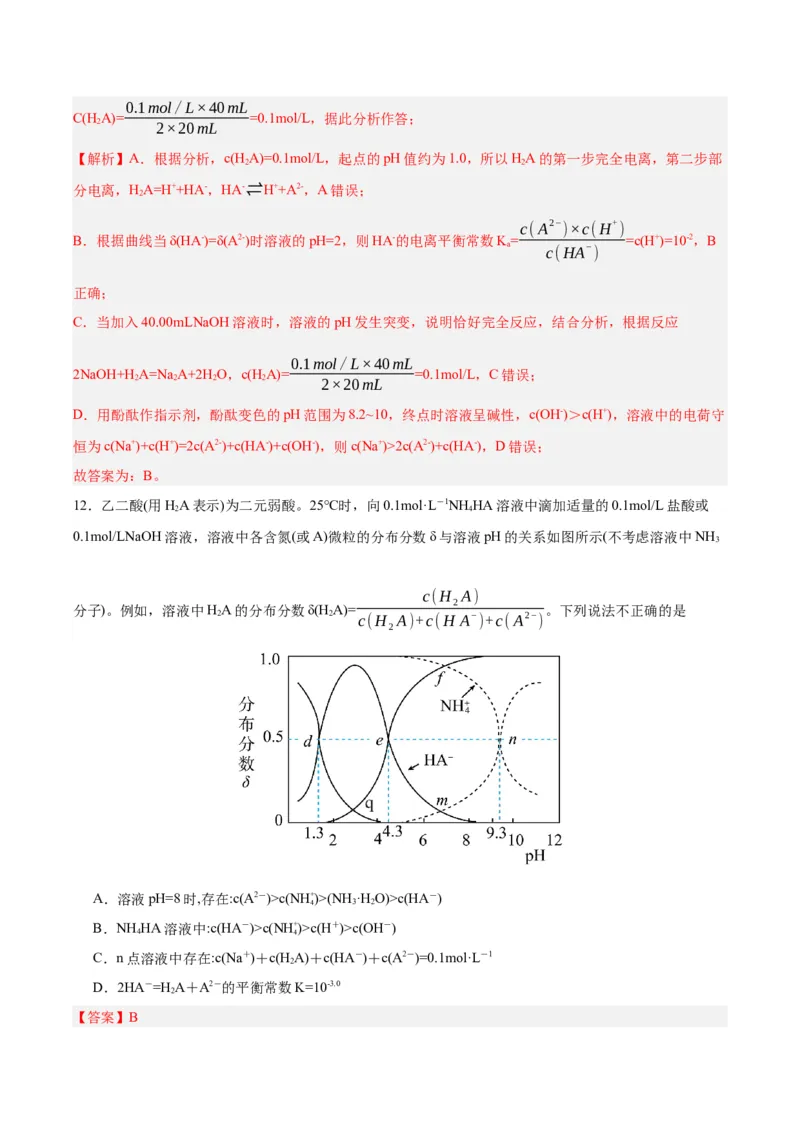
12.乙二酸(用HA表示)为二元弱酸。25℃时,向0.1mol·L-1NH HA溶液中滴加适量的0.1mol/L盐酸或
2 4
0.1mol/LNaOH溶液,溶液中各含氮(或A)微粒的分布分数δ与溶液pH的关系如图所示(不考虑溶液中NH
3
c(H A)
2
分子)。例如,溶液中HA的分布分数δ(H A)= 。下列说法不正确的是
2 2 c(H A)+c(H A− )+c(A2− )
2
A.溶液pH=8时,存在:c(A2-)>c(NH+ )>(NH ·H O)>c(HA-)
4 3 2
B.NH HA溶液中:c(HA-)>c(NH+ )>c(H+)>c(OH-)
4 4
C.n点溶液中存在:c(Na+)+c(HA)+c(HA-)+c(A2-)=0.1mol·L-1
2
D.2HA-=H A+A2-的平衡常数K=10-3.0
2
【答案】B【分析】向NH HA溶液中滴加盐酸,HA-浓度降低,HA浓度增大,向NH HA溶液中滴加NaOH溶液,
4 2 4
HA-浓度降低,A2-浓度增大,NH+ 浓度降低,NH ▪H O浓度增大,所以图像中从左开始曲线依次表示
4 3 2
HA、HA-、A2-、NH+ 和NH ▪H O,从图中可以看出,d点c(HA)=c(HA-),可知HA的K =10-1.3,e点
2 4 3 2 2 2 a1
c(HA-)=c(A2-),可知HA的K =10-4.3,n点c(NH+ )=c(NH▪H O),可知NH ▪H O的K=10-4.7。
2 a2 4 3 2 3 2 b
【解析】A.从图中可以看出,pH=8的溶液中:c(A2-)>c(NH+ )>(NH ·H O)>c(HA-),故A正确;
4 3 2
K 10−14
B.NH HA溶液中,存在着NH+ 的水解、HA-的电离和水解,NH+ 的水解常数K= W = =10-9.3,HA-
4 4 4 h K 10−4.7
ℎ
K 10−14
的电离常数即为HA的K =10-4.3,K= W = =10-12.7,所以以HA-的电离为主,溶液显酸性,所以
2 a2 h K 10−1.3
a1
NH HA溶液中c(NH+ )>c(HA-)>c(H+)>c(OH-),故B错误;
4 4
C.n点时,NH+ 和NH ▪H O的含量相等,说明加入的NaOH溶液的体积与NH HA溶液的体积相等,根据
4 3 2 4
元素守恒有c(Na+)+c(HA)+c(HA-)+c(A2-)=0.1mol·L-1,故C正确;
2
c(A2− )·c(H A) K 10−4.3
D.2HA-=H A+A2-的平衡常数K= 2 = a2 = =10-3.0,故D正确。
2 c2 (H A− ) K 10−1.3
a1
答案选B。
13.常温下,向20mL0.1mol•L-1CHCOOH溶液中逐滴加入等浓度的NaOH溶液或盐酸,CHCOOH和
3 3
c(X)
CHCOO-的分布分数δ与pH的关系如图所示。已知:分布分数δ(X)=
3 c(CH COOH)+c(CH COO− )
3 3
,X为CHCOOH和CHCOO-。
3 3
下列说法错误的是
A.曲线Ⅱ是CHCOO-的分布分数曲线
3B.K(CHCOOH)=10-4.76
a 3
C.将等体积等浓度的CHCOOH与CHCOONa溶液混合后,溶液的pH=4.76
3 3
D.X点溶液中c(CHCOO-)=c(CH COOH)>c(Na+)>c(H+)>c(OH-)
3 3
【答案】C
【解析】A.pH增大的过程中,CHCOOH的分布分数减小,CHCOO-的分布分数增大,因此曲线Ⅰ是
3 3
CHCOOH的分布分数曲线,曲线Ⅱ是CHCOO-的分布分数曲线,A正确;
3 3
c(H+ )c(CH COO− )
B.X点坐标为(4.76,0.5),溶液中c(CHCOO-)=c(CH COOH),则K(CHCOOH)= 3
3 3 a 3
c(CH COOH)
3
=10-4.76,B正确;
10−14
C.由K(CHCOOH)=10-4.76可知,CHCOO-的水解常数K= =10-9.24,即CHCOOH的电离程度大于
a 3 3 h 10−4.76 3
CHCOO-的水解程度,将等体积等浓度的CHCOOH与CHCOONa溶液混合,所得溶液中
3 3 3
c(CHCOO-)>c(CH COOH),则pH>4.76,C错误;
3 3
D.由图可知,X点溶液中c(CHCOO-)>c(CH COOH),则溶液中溶质为CHCOOH和CHCOONa,且
3 3 3 3
c(H+)>c(OH-),结合溶液中的电荷守恒关系c(Na+)+c(H+)=c(CH COO-)+c(OH-),可知c(CHCOO-)>c(Na+),则
3 3
C(CHCOO-)=c(CH COOH)>c(Na+)>c(H+)>c(OH-),D正确;
3 3
故答案为:C。
c(H+
)
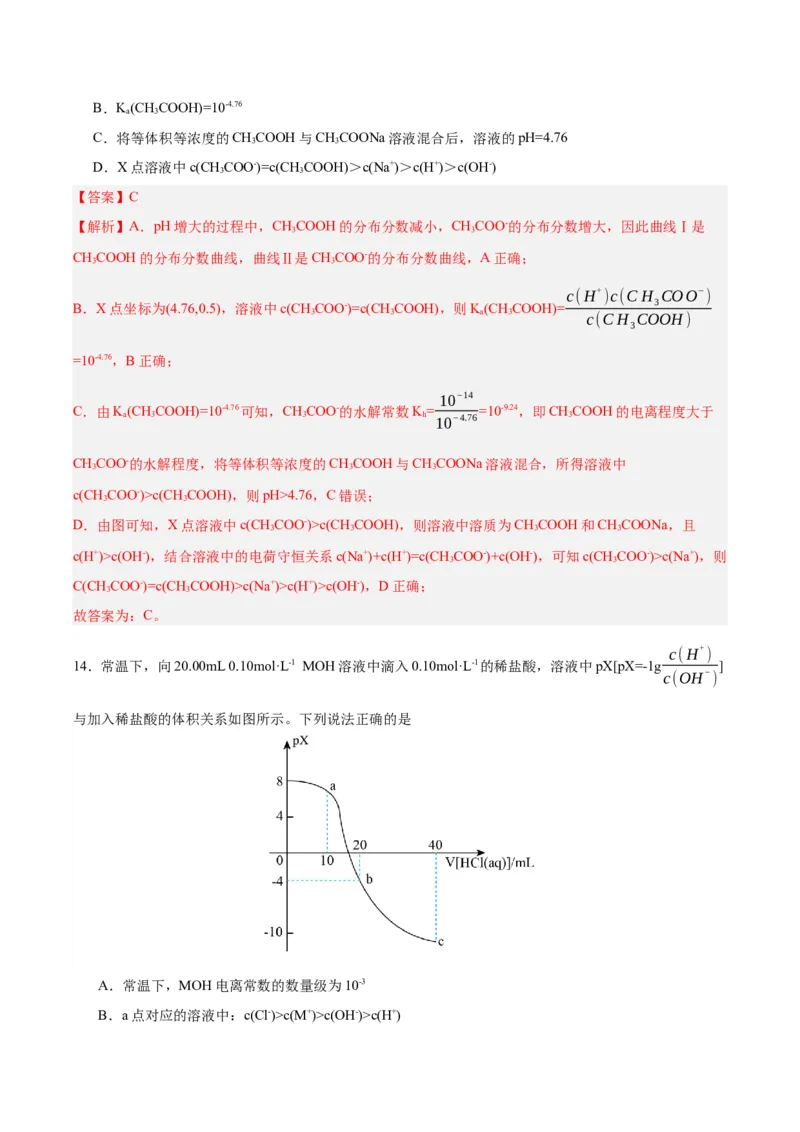
14.常温下,向20.00mL 0.10mol·L-1 MOH溶液中滴入0.10mol·L-1的稀盐酸,溶液中pX[pX=-1g ]
c(OH−
)
与加入稀盐酸的体积关系如图所示。下列说法正确的是
A.常温下,MOH电离常数的数量级为10-3
B.a点对应的溶液中:c(Cl-)>c(M+)>c(OH-)>c(H+)C.b点对应的溶液中水的电离程度最大,且溶液中:c(Cl-)>c(M+)>c(MOH)
D.c点溶液中:c(Cl-)=2c(M+)=2c(MOH)
【答案】D
c(H+ ) c(M+ )·c(OH− )
【解析】A.结合图像,V=0mL时,-1g =8,可知c(OH-)=1×10-3mol·L-1,K= =
c(OH− ) b c(MOH)
10−3×10−3
=10-5
0.1
,A错误;
B.a点对应的溶液中溶质为等物质的量的MOH和MCl,溶液呈碱性,根据电荷守恒:c(M+)+c(H+)=c(Cl-)
+c(OH-),结合c(OH-)>c(H+),得:c(M+)>c(Cl-)>c(OH-)>c(H+),B错误;
C.b点对应酸碱恰好完全中和时,得MCl溶液,此时水的电离程度最大,结合物料守恒,溶液中
c(Cl-)=c(M+)+c(MOH),C错误;
D.c点溶液中溶质为等物质的量的MCl和HCl,根据物料守恒,溶液中c(Cl-)=2c(M+)+2c(MOH),D正确;
答案选D。
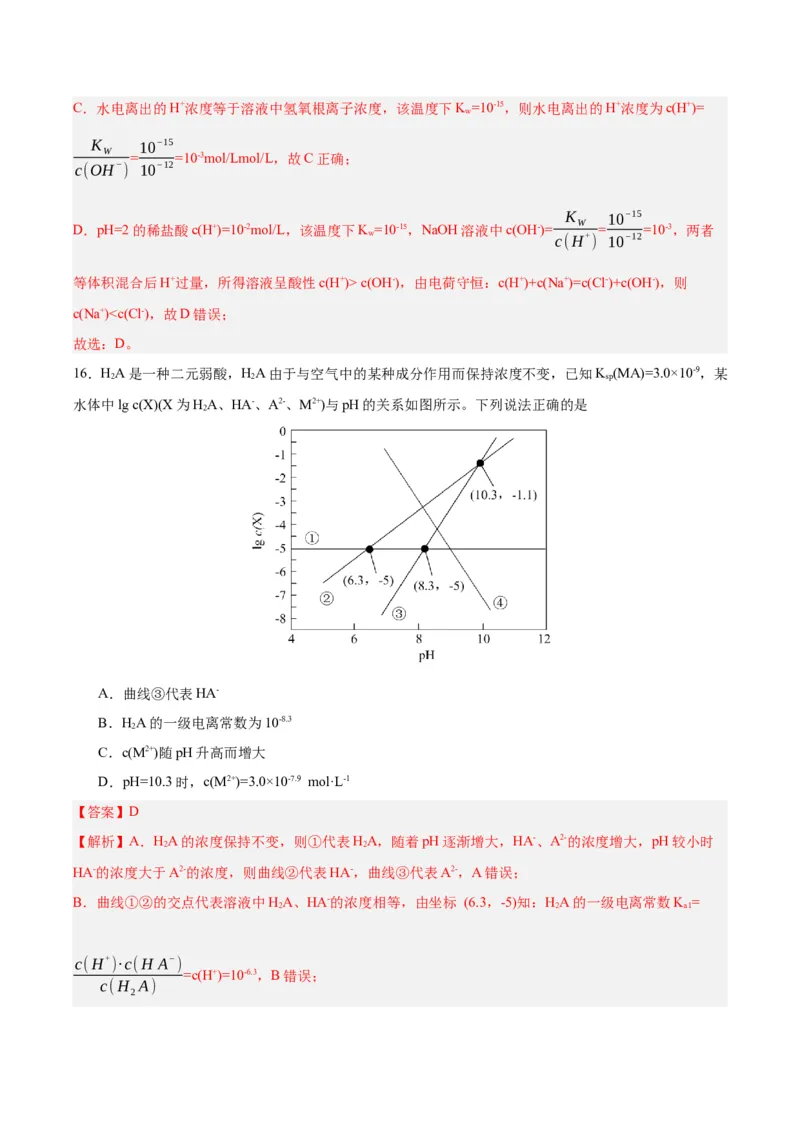
15.已知,某温度下的溶液中c(H+)=10xmol·L-1、c(OH-)=10ymol·L-1,x与y的关系如图所示,下列说法错误
的是
A.该温度低于25℃
B.该温度下,0.1mol·L-1NaSO 溶液中存在:c(HSO- )+2c(SO2- )
2 3 3 3 2 3
c(H+),则c(HSO- )+2c(SO2- ) c(OH-),由电荷守恒:c(H+)+c(Na+)=c(Cl-)+c(OH-),则
c(Na+)c(HB-)>c(H B)>c(B2-)
2
【答案】C
【分析】HB 为二元弱酸,其电离方程式为HB⇌H++HB-、HB-⇌H++B2-,向某浓度的二元弱酸HB溶液
2 2 2
中加NaOH(s),pH 增大促进电离平衡正向移动,所以由图可知:曲线Ⅰ是 c(HB-)的负对数,曲线Ⅱ是
c(HB)的负对数,曲线Ⅲ是 c(B2-)的负对数。
2
【解析】A.由分析知:曲线Ⅰ是 c(HB-)的负对数,曲线Ⅱ是 c(HB)的负对数,曲线Ⅲ是 c(B2-)的负对
2
数,A错误;
B.Z点时,c(HB-)=c(B2-),根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)=c(OH-)+3c(B2-),由于c(H
+)3c(B2-),B错误;
K
C.由Z点可知,c(HB-)=c(B2-),则HB⇌H++HB-,k =1×10-7.1,B2-的水解常数为 W =10-6.9;NH ·H O
2 a2 K 3 2
a2
10−14
的电离常数为 10-4.69,则NH+ 的水解常数为 =10-9.31;故NH+ 水解程度较小,(NH )B溶液呈碱性,C
4 10−4.69 4 4 2正确;
K
D.由X点可知:HB⇌H++HB-,c(HB-)=c(B2-),k =1×10-1.9,HB-的水解常数为K= W =10-12.1,HB-的
2 a1 h K
a1
电离常数k =1×10-7.1,HB-的电离程度大于水解程度,则NaHB溶液中c(Na+)>c(HB-)>c(B2-)>c(H B),D错
a2 2
误;
故选C。
18.25℃时,向弱酸HRO 的溶液中加入NaOH溶液,所有含R微粒的lgc-pOH关系如图所示。下列叙
3 3
述正确的是
已知:①pOH=-lgc(OH-);②a、b、c三点的坐标:a(7.3,-1.3)、b(10.0,-3.6)、c(12.6,-1.3)。
A.HRO 与足量NaOH溶液反应,生成的盐为NaRO
3 3 3 3
B.a点溶液中,c(H+)+c(Na+)=3c(HRO- )+c(OH-)
2 3
C.曲线①表示lgc(H RO)随pOH的变化
3 3
D.反应HRO+HRO2-⇌ 2HRO- 的平衡常数K=104.7
3 3 3 2 3
【答案】B
【分析】由电离常数公式可知,当溶液中R微粒的浓度相等时,电离常数与溶液中的氢离子浓度相等;由
图可知,含R微粒只有3条曲线说明HRO 为二元弱酸,NaHRO 为正盐,由多元弱酸分步电离,以一级
3 3 2 3
电离为主可知,一级电离常数大于二级电离常数,则电离常数越大,溶液中pOH的值越小,则曲线③表示
表示lgc(H RO)随pOH的变化的曲线、曲线②表示lgc(HRO- )随pOH的变化、曲线①表示lgc(HRO2- )随
3 3 2 3 3
pOH的变化;由a点数据可知,a点的pOH=7.3则pH=6.7,c(HRO2- )= c(HRO- ),则K =
3 2 3 a2
c(H+ )c(HRO2−
)
3 =10-6.7,同理,由c点数据可知,HRO 的电离常数K (H RO)= 10—1.4。
H RO− 3 3 a1 3 3
2 3
【解析】A.HRO 是个二元弱酸,所以其与足量NaOH溶液反应,生成的盐为NaHRO ,故A错误;
3 3 2 3B.由图可知,a点溶液中c(HRO2- )= c(HRO- ),由电荷守恒关系c(Na+)+ c(H+)=2c(HRO2- )+ c(HRO- )+ c(OH
3 2 3 3 2 3
—),可得:溶液中c(H+)+c(Na+)=3c(HRO- )+c(OH-),故B正确;
2 3
C.由分析可知,曲线①表示lgc(HRO2- )随pOH的变化,故C错误;
3
c2 (H RO− ) c2 (H RO− )c(H+ ) K
2 3 2 3 a1
D.由方程式可知反应的平衡常数K= = = =
c(H RO )c(HRO2− ) c(H RO )c(HRO2− )c(H+ ) K
3 3 3 3 3 3 a2
10−1.4
=105.3,故D错误;
10−6.7
故选B。
19.研究电解质在水溶液中的平衡能了解它的存在形式。已知25℃时部分弱电解质的电离平衡常数数据如
表所示,回答下列问题:
化学式 CHCOOH HCO HCN NH ·H O
3 2 3 3 2
K =4.3×10−7
电离平衡常 al
K =1.8×10−5 K =6.2×10−10 K =1.8×10−5
数 a K =5.6×10−11 a b
a2
(1)物质的量浓度均为 的下列四种溶液:pH由小到大排列的顺序是 。
A.CHCOONa B.NaCO C.NaCN D.NaHCO
3 2 3 3
(2)常温下,0.1mol/LCH COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填序号)。
3
c(H+ ) c(OH− ) c(CH COO− )c(H+ )
A.c(H+) B. C.c(H+) c(OH—) D. E. 3
c(CH COOH) c(H+ ) c(CH COOH)
3 3
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式: 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸
的电离平衡常数K (用含a、b的代数式表示)。
a
(5)标准状况下将2.24LCO ,通入100mL0.1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
2
c(OH—)= c(H CO)+ 。
2 3
(6)25℃,氨水的浓度为2.0mol/L,溶液中的c(OH—)= mol/L,将CO 通入该氨水中,当溶液中c(OH
2
—)降至1×10—7mol/L时,溶液中c(HCO- ) c(CO2- )。(填“">”或“<”或“=”)
3 3
(7)盐酸肼(N HCl)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH Cl
2 6 2 4
类似。
①写出盐酸肼第一步水解反应的离子方程式 。②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N H2+ )>c(H+)>c(OH-)
2 6
B.c(Cl-)> c[(N H·H O)]+>c(H+)>c(OH-)
2 5 2
C.2 c(N H2+ )+ c[(N H·H O)]++c(H+)= c(Cl-)+c(OH-)
2 6 2 5 2
D.c[(N H·H O)]+>c(Cl-)> c(H+)>c(OH-)
2 5 2
【答案】(1)ADCB
(2)BD
(3)CN—+H O+CO=HCO- +HCN
2 2 3
10−7b
(4)
a−b
(5)c(H+)—c(CO2- )
3
(6)6.0×10—3 >
(7)N H2+ +H O⇌(N H·H O)++H+ AC
2 6 2 2 5 2
【解析】(1)由电离常数可知,酸和酸式根离子在溶液中的电离程度的大小顺序为
CHCOOH>H CO>HCN> HCO- ,由盐类水解规律可知,酸和酸式根离子的电离程度越弱,对应离子在溶
3 2 3 3
液中的水解程度越大,等浓度的盐溶液的pH越大,则四种盐溶液的pH大小顺序为CHCOONa<NaHCO
3 3
<NaCN<NaCO,故答案为:ADCB;
2 3
(2)醋酸溶液稀释时,溶液温度不变,溶液中醋酸、醋酸根离子、氢离子浓度减小,水的离子积常数、
电离常数不变;
A.由分析可知,醋酸溶液稀释时,溶液中氢离子浓度减小,故错误;
c(H+
)
K
a
B.由电离常数公式可知,溶液中 = ,醋酸溶液稀释时,溶液温度不变,
c(cH COOH) c(cH COO− )
3 3
K c(H+
)
a
醋酸根离子浓度减小,电离常数不变,则 和 的值增大,故正确;
c(cH COO− ) c(cH COOH)
3 3
C.水的离子积常数K = c(H+) c(OH—),醋酸溶液稀释时,溶液温度不变,水的离子积常数不变,故错误;
w
D.水的离子积常数K = c(H+) c(OH—),醋酸溶液稀释时,溶液温度不变,溶液中氢离子浓度减小,水的
w
c(OH−
)
离子积常数不变,则溶液中氢氧根离子浓度增大,则 的值增大,故正确;
c(H+
)c(CH COO− )c(H+ )
E.醋酸的电离出K = 3 醋酸溶液稀释时,溶液温度不变,醋酸的电离常数不变,故
a
c(CH COOH)
3
错误;
故选BD;
(3)由电离常数可知,酸和酸式根离子在溶液中的电离程度的大小顺序为HCO>HCN> HCO- ,由强酸制
2 3 3
弱酸的反应原理可知,氰化钠溶液与少量二氧化碳反应生成氢氰酸和碳酸氢钠,反应的离子方程式为CN—
+H O+CO=HCO- +HCN,故答案为:CN—+H O+CO=HCO- +HCN;
2 2 3 2 2 3
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,溶液中
氢离子浓度和氢氧根离子浓度相等,都为10—7mol/L,由电荷守恒c(Na+)+c(H+)=c(CHCOO—)+ c(OH—)可知,
3
b a−b
溶液中c(Na+)=c(CHCOO—)= mol/L,由物料守恒可知溶液中醋酸的浓度为 mol/L,则醋酸的电离出
3 2 2
Ka=
b
×10−7
2 10−7b 10−7b
= ,故答案为: ;
a−b a−b a−b
2
2.24L
(5)由题意可知,二氧化碳与氢氧化钠的物质的量比为 :(0.1mol/L×0.1L)=1:1,则二氧化
22.4L/mol
碳与氢氧化钠溶液恰好反应生成碳酸氢钠溶液,溶液中存在质子守恒关系c(H CO)+c(H+)=c(CO2- )+ c(OH
2 3 3
—),则溶液中c(OH—)= c(H CO)+c(H+)—c(CO2- ),故答案为:c(H+)—c(CO2- );
2 3 3 3
(6)由电离常数可知,2mol/L氨水中氢氧根离子浓度约为❑√1.8×10−5×2mol/L=6.0×10-3mol/L;由碳酸
的电离常数K 可知,当溶液中氢氧根离子浓度为1×10—7mol/L时,氢离子浓度为1×10—7mol/L,则溶液中
a2
c(CO2− ) K 5.6×10−11
3 = a2 = =5.6×10—4,所以溶液中碳酸氢根离子浓度大于碳酸根离子,故答案为:
c(HCO− ) c(H+ ) 1.0×10−7
3
6.0×10—3;>;
(7)①由题意可知,NH2+ 离子在溶液中分步水解,第一步水解生成(N H·H O)+和氢离子,水解的离子方
2 6 2 5 2
程式为NH+ +H O⇌(N H·H O)++H+,故答案为:NH+ +H O⇌(N H·H O)++H+;
2 6 2 2 5 2 2 6 2 2 5 2
②由题意可知,NH+ 离子在溶液中分步水解使溶液呈酸性,一级水解生成的氢离子抑制二级水解,则溶液
2 6
中离子浓度大小顺序为c(Cl—)>c(N H+ )>c(H+)>c(OH—),溶液中存在的电荷守恒关系为2 c(N H+ )+
2 6 2 6
c[(N H·H O)]++c(H+)= c(Cl—)+c(OH—),故选AC。
2 5 2