文档内容
第 14 讲 弱电解质与电离平衡
知识导航
小杨老师 15521324728 侵权必究
课前引入
当你走进便利店,走到琳琅满目的饮料区
时,可曾注意过一类饮料——“电解质饮料”?
所谓电解质饮料,是用水将一组化合物溶解
制成的饮料,可补充人体新陈代谢的消耗。
水和电解质是维持生命基本物质的组成部
分。人体进行新陈代谢的过程实质上是一种复杂
的、相互关联的生物物理和物质化学反应的过
程,而且主要是在细胞内进行的。
杨sir化学,侵权必究
日常生活中,特别是炎热的夏天以及大量的
体力活动过后,人体的水分及电解质会随汗液排
出体外,造成人体缺水与电解质不平衡。如果单
纯摄入大量的水分而没有补充电解质的话,那么
电解质的浓度就会低于身体的正常水平,可能影
响到中枢神经系统的功能,引起水中毒。许多运
动饮料通过补充与人体相当的电解液来避免水中
毒。
那么,什么是电解质呢?知识精讲
小杨老师 15521324728 侵权必究
一、电解质与非电解质
定义 物质类别
电解质 在水溶液或熔融状态下能够导电的化合物 酸、碱、盐、金属氧化物、水
非电解质 在水溶液里和熔融状态下都不导电的化合物 大部分有机化合物、非金属氧化物
二、强电解质与弱电解质
1. 实验探究——盐酸和醋酸的区别
取相同体积、0.1mol/L的盐酸和醋酸, 比较它们pH的大小,试验其导电能力,并分别与等量镁条反应。
观察、比较并记录现象。
杨sir化学,侵权必究
酸 1.0 mol·L-1盐酸 1.0 mol·L-1醋酸
pH _____ _____
导电能力 _____ _____
现象 反应_______,产生气体 反应_______,产生气体
与镁
盐酸反应快,表明盐酸中c(H+)较____,说明盐酸的电离程度______醋酸的电离程
反应 结论
度
【答案】小(pH=1) 大(pH≈3)
强 弱
剧烈 缓慢
大 大于
思考与交流:比较盐酸和醋酸在水中电离出的H+ 浓度大小,该实验现象表明什么问题?
杨sir化学,侵权必究
2.强、弱电解质的定义、物质类别与比较
强电解质 弱电解质
定义 在水溶液中能_______电离的电解质 在水溶液中只能_______电离的电解质
电离过程 不可逆,无电离平衡 可逆,存在电离平衡
在溶液中的
只有离子 既有离子,又有电解质分子
存在形式
①强酸,如HCl、HSO ①弱酸,如CHCOOH、HClO
2 4 3
物质类别
②强碱,如KOH、Ba(OH) ②弱碱,如NH·HO、Mg(OH)
及示例 2 3 2 2
③大部分盐,如NaCl、BaSO ③水
4
【答案】完全 部分
三、电离方程式
杨sir化学,侵权必究
强酸 完全电离,如HCl === H+ + Cl-
强
电 强碱 完全电离,如Ba(OH) 2 === Ba2+ + 2OH-
解 盐 正盐 完全电离,如NaCO === 2Na+ + CO2-
2 3 3强酸的酸式盐 完全电离,如NaHSO === Na+ + H+ + SO2-
4 4
第一步完全电离,第二步弱酸酸根部分电离,如
质 弱酸的酸式盐
NaHCO === Na+ + HCO-,HCO - ⇌ H+ + CO2-
3 3 3 3
一元弱酸 部分电离,如CHCOOH ⇌ CHCOO- + H+
3 3
一元弱碱 部分电离,如 NH ·HO ⇌ NH+ + OH-
弱 3 2 4
电 H 2 O 部分电离, H 2 O ⇌ H+ + OH-
解 分步电离,必须分步写出,不可合并(以第一步电离为主)
多元弱酸
质 如HCO ⇌ H+ + HCO-,HCO- ⇌ H+ + CO2-
2 3 3 3 3
多元弱碱 分步电离,中学阶段要求一步写出。如Fe(OH) ⇌ Fe3+ + 3OH-
3
注意
强酸的酸式盐在熔融状态和水溶液中,电离方程式是不同的。
(1)熔融状态时:NaHSO === Na+ + HSO- ;
4 4
(2)溶于水时:NaHSO === Na+ + H+ + SO2-
4 4 杨sir化学,侵权必究
四、弱电解质的电离平衡
1. 含义
一定条件(如温度、浓度)下,当弱电解质分子电离成离子的速率与离子重新结合成弱电解质分子的速率
相等,溶液中各分子和离子的浓度都不再发生变化时,电离过程就达到了平衡状态,如下图所示。
杨sir化学,侵权必究
2. 特征
3.电离平衡的影响因素
(1)温度:弱电解质的电离一般是______过程,升高温度,电离平衡______移动,电离程度______。
(2)浓度:
杨sir化学,侵权必究①稀释电解质溶液,电离平衡__________移动,电离程度__________。
②加入同一电解质,电离平衡__________移动,电离程度__________。
(3)外加电解质:
①同离子效应:加入与弱电解质具有相同离子的电解质,电离平衡______移动,电离程度______。
②化学反应:加入能与弱电解质电离出的离子发生反应的离子时,电离平衡______移动,电离程度______。
【答案】(1)吸热 正向,增大; (2)正向,增大 正向,减小。
(3)逆向 减小 正向 增大
对点训练
小杨老师 15521324728 侵权必究
题型一:强、弱电解质的判断
杨sir化学,侵权必究
【变1】下列有关电解质、强电解质、弱电解质的分类正确的是
A B C D
电解质 Cu CO NaCl NaOH
2
强电解质 HCl Ba(OH) HClO BaSO
2 4 4
弱电解质 CHCOOH HO Fe(SCN) 氨水
3 2 3
A.A B.B C.C D.D
【答案】C
【详解】
A.Cu是金属单质,而不是化合物,因此不属于电解质,A不符合题意;
B.CO 是化合物,但其溶于水或受热熔化时都不能发生电离而导电,因此属于非电解质,B不符合题意;
2
C.物质分类合理,C符合题意;
D.氨水是混合物,而不是化合物,因此不属于弱电解质,D不符合题意;
故合理选项是C。
题型二:强、弱电解质的性质与区别
杨sir化学,侵权必究
【变2-1】下列说法不正确的是
①氨溶于水得到的溶液能导电,所以NH 是电解质;
3
②盐溶于水一定电离出金属阳离子
③液态HCl不导电,所以属于非电解质;
④金属铜能导电,但它不是电解质,是非电解质
⑤强电解质的导电能力比弱电解质强
⑥NaHSO 在熔融状态下电离生成三种离子
4
A.②③⑥ B.①③⑤ C.全部 D.①②③④⑤
【答案】C【详解】
①氨溶于水得到氨水,溶液中一水合氨部分电离出铵根离子和氢氧根离子,导致溶液能导电,但是氨气自
身不能电离出阴阳离子,不导电,所以NH 是非电解质,故错误;
3
②盐溶于水不一定电离出金属阳离子、可能电离出铵离子,故错误;
③液态HCl不导电,但是HCl溶于水,电离出氢离子和氯离子,能够导电,所以液态HCl属于电解质,故
错误;
④金属铜是单质,既不是电解质也不是非电解质,故错误;
⑤电解质溶液的导电能力与离子浓度成正比,与电解质强弱无必然的联系,所以强电解质的导电能力不一
定强于弱电解质,故错误;
⑥NaHSO 在熔融状态下电离生成钠离子和硫酸氢根离子,故错误;
4
答案选C。
【变2-2】现有下列物质 ①熔化的NaCl ②盐酸 ③氯气 ④冰醋酸 ⑤铜⑥酒精(C HOH) ⑦醋酸铵
2 5
⑧液氨 ⑨SO 请用以上物质回答下列问题。(填序号)
2
(1)属于强电解质的是_______;在上述状态下能导电的是_______;
(2)属于弱电解质的是_______;
(3)属于非电解质,但溶于水后的水溶液能导电的是_______。
【答案】①⑦ ①②⑤ ④ ⑧⑨
【详解】
根据电解质是指在水溶液或熔融状态下能够导电的化合物,非电解质则为在水溶液或熔融状态下均不能够
导电的化合物,强电解质则是在水溶液中能够完全电离的电解质,弱电解质则是在水溶液中部分发生电离
的电解质,据此分析解题:
①熔化的NaCl能导电,是强电解质; ②盐酸能导电,但是属于混合物,既不是电解质也不是非电解质;
③氯气不能导电,属于单质,既不是电解质也不是非电解质,但其水溶液由于Cl 和水反应产生了HCl和
2
HClO而能导电;④冰醋酸本身不能导电,是弱酸,属于弱电解质,水溶液中由于CHCOOH部分电离而
3
导电;⑤铜是金属单质,能够导电,既不是电解质也不是非电解质;⑥酒精(C HOH)是非电解质,在水溶
2 5
液或熔融状态下均不能够导电;⑦醋酸铵是盐,本身不能导电,其水溶液能够导电,且在水溶液中完全电
离,故属于强电解质;⑧液氨虽然水溶液可以导电,但是由于不是NH 本身电离,而是NH 和HO生成的
3 3 2
NH ‧H O发生电离,故其是非电解质;⑨SO 虽然水溶液可以导电,但是由于不是SO 本身电离,而是SO
3 2 2 2 2
和HO生成的HSO 发生电离,故其是非电解质,综上所述可知:(1)属于强电解质的是①⑦;在上述状态
2 2 3
下能导电的是①②⑤,故答案为:①⑦;①②⑤;
(2)属于弱电解质的是④,故答案为:④;
(3)属于非电解质,但溶于水后的水溶液能导电的是⑧⑨,故答案为:⑧⑨。
题型三:弱电解质的电离平衡
杨sir化学,侵权必究
【变3-1】在醋酸溶液中,CHCOOH电离达到平衡的标志是
3
A.溶液显电中性 B.溶液中检测出CHCOOH分子、CHCOO-共同存在
3 3C.c(H+)恒定不变 D.c(H+)=c(CHCOO-)
3
【答案】C
【详解】
A.不管CHCOOH电离是否达到平衡,CHCOOH溶液均显电中性,故A不是CHCOOH电离达到平衡的
3 3 3
标志;
B.不管CHCOOH电离是否达到平衡,溶液中CHCOOH分子、CHCOO-总是共同存在,故B不是
3 3 3
CHCOOH电离达到平衡的标志;
3
C.c(H+)恒定不变,表明CHCOOH电离达到平衡,故C是CHCOOH电离达到平衡的标志;
3 3
D.c(H+)与c(CHCOO-)之间的比值与CHCOOH的电离平衡之间没有一定关系,故D不是CHCOOH电
3 3 3
离达到平衡的标志。
故选C。
题型四:电离方程式的书写
杨sir化学,侵权必究
【例4】写出下列物质在水中的电离方程式:
(1)硝酸:___________
(2)醋酸:___________
(3)一水合氨:___________
(4)碳酸氢钠:___________
(5)NH NO :___________
4 3
(6)Al (SO ):___________
2 4 3
(7)Fe(OH) :___________
3
(8)HS:___________
2
【答案】
(1)HNO=H++NO
3
(2)CHCOOH CHCOO-+H+
3 3
(3)NH ·H O NH +OH-
3 2
(4)NaHCO =Na++HCO
3
(5)NH NO =NH +NO
4 3
(6)Al (SO )=2Al3++2SO
2 4 3
(7)Fe(OH) Fe3++3OH-
3
(8)HS H++HS-
2
【分析】强电解质电离的时候不可逆,弱电解质电离的时候要写可逆符号,且多元弱酸要分步电离,多元弱碱不用
分步,以此解题。
(1)
硝酸是强电解质,电离方程式为:HNO=H++NO ;
3
(2)
醋酸是弱电解质,电离方程式为:CHCOOH CHCOO-+H+;
3 3
(3)
一水合氨是弱电解质,电离方程式为:NH ·H O NH +OH-;
3 2
(4)
NaHCO 是盐,是强电解质,电离方程式为:NaHCO =Na++HCO ;
3 3
(5)
NH NO 是盐,是强电解质,电离方程式为:NH NO =NH +NO
4 3 4 3
(6)
Al (SO ) 是盐,是强电解质,电离方程式为:Al (SO )=2Al3++2SO ;
2 4 3 2 4 3
(7)
Fe(OH) 是弱碱,是弱电解质,电离方程式为:Fe(OH) Fe3++3OH-;
3 3
(8)
HS是二元弱酸,是弱电解质,电离方程式为:HS H++HS-。
2 2
题型五:弱电解质电离平衡的移动
杨sir化学,侵权必究
【变5-2】稀氨水中存在着下列平衡:NH ·H O NH +OH-,若要使平衡向左移动,同时使c(OH-)增大,
3 2
应加入的物质或采取的措施是( )
①NH Cl固体②硫酸③NaOH固体④水⑤加热⑥加入少量MgSO 固体
4 4
A.①②③⑤ B.③⑥ C.③ D.③⑤
【答案】C
【详解】
①加入NH Cl固体,NH 浓度增大,平衡逆向移动,c(OH-)减小,故①错误;
4
②加入硫酸会消耗OH-,OH-浓度减小,平衡正向移动,故②错误;
③加入NaOH固体,溶液中OH-浓度增大,电离平衡逆向移动,故③正确;
④加入水稀释,氨水的浓度减小,平衡正向移动,OH-浓度减小,故④错误;⑤弱电解质的电离为吸热过程,加热促进电离,平衡正向移动,故⑤错误;
⑥加入少量MgSO 固体,OH-与镁离子反应生成氢氧化镁沉淀,平衡正向移动,氢OH-浓度减小,故⑥错
4
误;
只有③正确,故答案为C。
【变5-4】化合物HIn在水溶液中存在以下电离平衡,故可作酸碱指示剂
HIn(aq) H+(aq)+In-(aq)
(红色) (黄色)
现把下列物质溶于水配成0.02 mol·L-1的水溶液,其中能使指示剂显黄色的是
①HCl ②SO ③NaCl ④NaHSO ⑤氨气 ⑥NaO ⑦NaCO
2 4 2 2 2 3
A.①②④ B.①④ C.⑤⑥⑦ D.⑤⑦
【答案】D
【详解】
①加入HCl,HCl电离产生H+,使溶液中c(H+)增大,电离平衡逆向移动,导致c(HIn)增大,c(In-)减小,溶
液显红色,①不符合题意;
②通入SO 气体,SO 与水反应产生HSO ,电离产生H+,使溶液中c(H+)增大,电离平衡逆向移动,导致
2 2 2 3
c(HIn)增大,c(In-)减小,溶液显红色,②不符合题意;
③加入NaCl,电离产生Na+、Cl-,不产生H+或OH-,溶液显中性,对电离平衡移动无影响,因此不能使指
示剂变为黄色,③不符合题意;
④NaHSO 电离方程式为:NaHSO=Na++H++ ,电离产生H+,使溶液中c(H+)增大,指示剂的电离平衡
4 4
逆向移动,导致c(HIn)增大,c(In-)减小,溶液显红色,④不符合题意;
⑤氨气溶于水反应产生NH ·H O,NH ·H O电离产生 、OH-,消耗溶液中的H+,使溶液中c(H+)减小,
3 2 3 2
电离平衡正向移动,导致c(In-)增大,溶液显黄色,⑤符合题意;
⑥NaO 溶于水反应产生NaOH和O,NaOH电离产生OH-,消耗溶液中的H+,使溶液中c(H+)减小,电离
2 2 2
平衡正向移动,导致c(In-)增大,溶液显黄色,但NaO 具有强氧化性,又将黄色物质氧化变为无色,因此
2 2
最终溶液显无色,⑥不符合题意;
⑦NaCO 是强碱弱酸盐,水解使溶液显碱性,水解产生的OH-消耗HIn电离产生的H+,使溶液中c(H+)减
2 3
小,电离平衡正向移动,导致c(In-)增大,溶液显黄色,⑦符合题意;
综上所述可知:能够使溶液显黄色的溶液序号是⑤⑦,故合理选项是D。
【例6】化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:
,向氨水中加入 固体时,平衡向____移动,OH-的浓度
_______,向浓氨水中加入少量NaOH固体,平衡向____移动。
【答案】右 减小 左
【详解】向氨水中加入MgCl 固体时,镁离子结合氢氧根生成氢氧化镁沉淀,平衡向右移动,OH-的浓度减小。向
2
浓氨水中加入少量NaOH固体,氢氧根浓度增大,则平衡向左移动。
故答案为:右;减小;左;
提分特训
小杨老师 15521324728 侵权必究
【题1】下列各组物质全部是强电解质的是
A.HSiO、HNO、HClO B.Ba(OH) 、CHCOOH、C HOH
2 3 3 2 3 2 5
C.HSO 、Ba(OH) 、BaCl D.HO、NH ∙H O、HPO
2 4 2 2 2 3 2 3 4
【答案】C
【详解】
A.HSiO、HClO在水溶液中部分电离,为弱电解质,A不符合题意;
2 3
B.CHCOOH在水溶液中部分电离,为弱电解质,C HOH在水溶液里或熔融状态下都不能电离,是非电
3 2 5
解质,B不符合题意;
C.HSO 、Ba(OH) 、BaCl 都是强电解质,C符合题意;
2 4 2 2
D.HO部分电离,NH ∙H O是弱碱,HPO 是中强酸,均属于弱电解质,D不符合题意;
2 3 2 3 4
答案为C。
【题2】下列组合正确的是
选项 强电解质 弱电解质 酸性氧化物 碱性氧化物
A Ca(OH) 乙醇 NO NaO
2 2 5 2
B CaSO HClO MnO CaO
4 2 7
C NaHCO 氨水 SO AlO
3 2 2 3
D HCl HF CO NaO
2 2 2
A.A B.B C.C D.D
【答案】B
【详解】
A.乙醇在水中和熔融状态下都不能导电,因此属于非电解质,A错误;
B.选项物质分类符合对应,因此分类合理,B正确;
C.氨水是混合物,不是纯净物,因此不属于电解质;Al O 是两性氧化物,不是碱性氧化物,C错误;
2 3
D.NaO 属于过氧化物,不是碱性氧化物,D错误;
2 2
故合理选项是B。
【题3】下列说法中,正确的是
A.强电解质溶液的导电能力一定比弱电解质强
杨sir化学,侵权必究
B.冰醋酸是弱电解质,但液态时不能导电
C.盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱D.硫酸钠是强电解质,硫酸钡是弱电解质
【答案】B
【详解】
A.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强,溶液的导电能力强弱与离子浓度成正
比,故A错误;
B.醋酸在溶液中部分电离,属于弱电解质,在液态时不发生电离,所以液态时不能导电,故B正确;
C.盐酸中加入固体NaCl,溶液中氯离子浓度增大,由于HCl在溶液中完全电离,所以溶液中氢离子浓度
不变,酸性不变,故C错误;
D.电解质的强弱与电解质的溶解性无关,硫酸钡在溶液中完全电离,属于强电解质,故D错误;
答案选B。
【题4】现有下列物质:①KSO 晶体;②液态SO ;③冰醋酸;④铜;⑤小苏打;⑥蔗糖;⑦乙醇;⑧熔
2 4 3
融的氯化钠;⑨NaOH溶液。其中:能导电的是___________(填序号,下同);属于电解质的是
___________;属于非电解质的是___________;属于强电解质的是___________;属于弱电解质的电离方
程式为___________。
【答案】④⑧⑨ ①③⑤⑧ ②⑥⑦ ①⑤⑧ CHCOOH CHCOO-+H+
3 3
【分析】
金属、石墨等因含有自由电子可导电,电解质水溶液或熔融的电解质因含可自由移动的离子可导电;水溶
液或熔融状态下能导电的化合物是电解质,水溶液和熔融状态下均不能导电的化合物是非电解质,碱性氧
化物、酸、碱和盐通常是电解质,绝大多数有机物是非电解质,二氧化碳等酸性氧化物溶于水生成酸溶液
会导电、因酸电离出可自由移动离子而导电、酸性氧化物自身不提供自由离子,故酸性氧化物属于非电解
质,强酸、强碱和大多数盐为强电解质、弱酸和弱碱为弱电解质,据此回答;
【详解】
①KSO 晶体不能导电、属于电解质、为强电解质;
2 4
②液态SO 不能导电、属于非电解质;
3
③冰醋酸不能导电、属于电解质、为弱电解质;
④铜能导电、是单质,既不属于电解质也不属于非电解质;
⑤小苏打不能导电、属于电解质、为强电解质;
⑥蔗糖不能导电、属于非电解质;
⑦乙醇不能导电、属于非电解质;
⑧熔融的氯化钠能导电、属于电解质、为强电解质;
⑨NaOH溶液能导电、是混合物,既不属于电解质也不属于非电解质。
其中:能导电的是④⑧⑨(填序号,下同);属于电解质的是①③⑤⑧;属于非电解质的是②⑥⑦;属于强
电解质的是①⑤⑧;属于弱电解质为醋酸,则其电离方程式为CHCOOH CHCOO-+H+。
3 3
【题6】下列物质在水中的电离方程式正确的是A.NaHCO =Na++H++CO
3
B.HClO H++ClO-
C.CuCl = Cu2++Cl-
2⇌
D.CHCOONH CHCOO-+NH
3 4 3
【答案】B ⇌
【详解】
A.NaHCO 是强电解质,完全电离, 是弱酸的酸式酸根离子,不能拆开,故正确的电离方程式为
3
NaHCO =Na++ ,故A错误;
3
B.HClO是一元弱酸,存在电离平衡,电离产生H+、ClO-,主要以电解质分子存在,电离方程式为
HClO H++ClO-,故B正确;
C.CuCl 是强电解质,完全电离,且电离产生的Cu2+、Cl-个数比为1:2,故正确的电离方程式为CuCl
⇌ 2 2
=Cu2++2Cl-,故C错误;
D.CHCOONH 是强电解质,完全电离变为离子,电离方程式为CHCOONH=CH COO-+ ,故D错误;
3 4 3 4 3
答案选B。
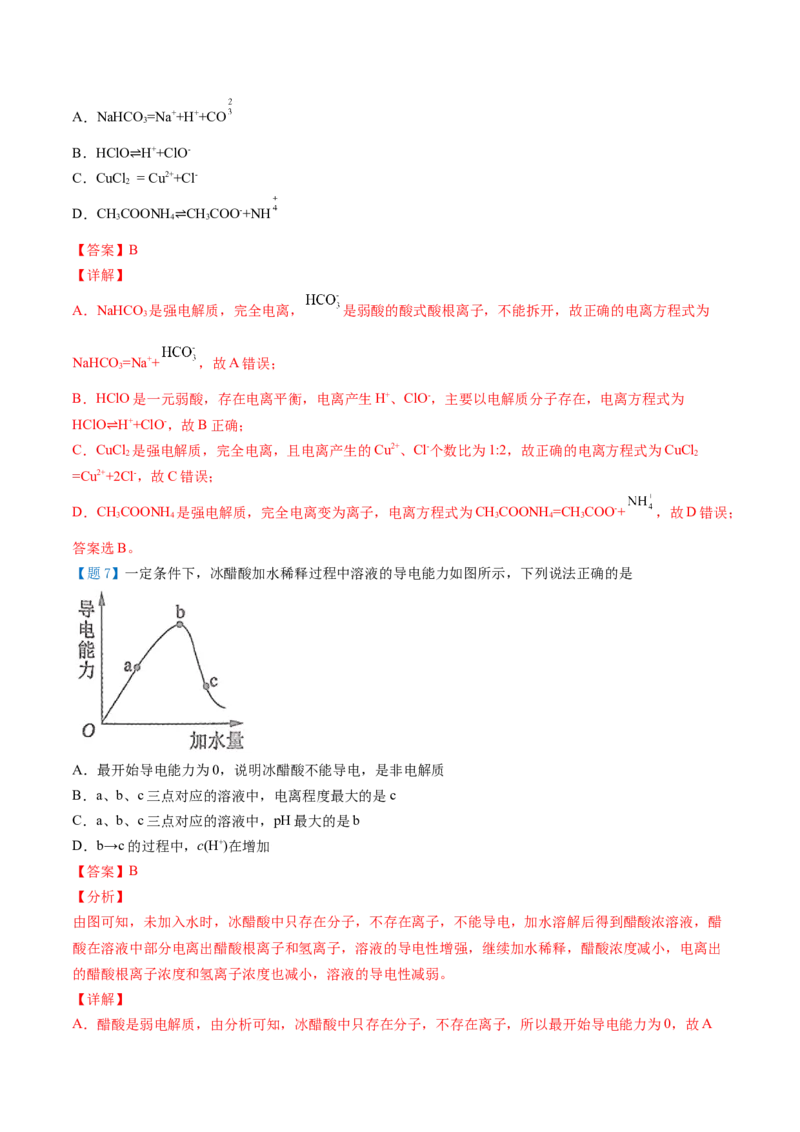
【题7】一定条件下,冰醋酸加水稀释过程中溶液的导电能力如图所示,下列说法正确的是
A.最开始导电能力为0,说明冰醋酸不能导电,是非电解质
B.a、b、c三点对应的溶液中,电离程度最大的是c
C.a、b、c三点对应的溶液中,pH最大的是b
D.b→c的过程中,c(H+)在增加
杨sir化学,侵权必究
【答案】B
【分析】
由图可知,未加入水时,冰醋酸中只存在分子,不存在离子,不能导电,加水溶解后得到醋酸浓溶液,醋
酸在溶液中部分电离出醋酸根离子和氢离子,溶液的导电性增强,继续加水稀释,醋酸浓度减小,电离出
的醋酸根离子浓度和氢离子浓度也减小,溶液的导电性减弱。
【详解】
A.醋酸是弱电解质,由分析可知,冰醋酸中只存在分子,不存在离子,所以最开始导电能力为0,故A错误;
B.醋酸是弱电解质,在溶液中部分电离出醋酸根离子和氢离子,醋酸浓度越小,电离程度越大,由图可
知,c点醋酸浓度最小,电离程度最大,故B正确;
C.醋酸溶液的导电能力越大,溶液中氢离子浓度越大,溶液pH越小,由图可知,b点导电能力最大,溶
液中氢离子浓度最大,溶液pH最小,故C错误;
D.醋酸溶液的导电能力越大,溶液中氢离子浓度越大,由图可知,b→c的过程中,导电能力减小,溶液
中氢离子浓度浓度减小,故D错误;
故选B。
【题9】25 ℃时,50 mL 0.10 mol·L-1醋酸中存在下述平衡:CHCOOH CHCOO-+H+,若分别作如
3 3
下改变,对上述平衡有何影响?
(1) 加入少量纯醋酸,电离平衡将___________(填“向左移动”“向右移动”或“不移动”),溶液中c(H+)将
___________(填“增大”“减小”或“不变”)。
(2)加入一定量蒸馏水,电离平衡将___________(填“向左移动”“向右移动”或“不移动”),溶液中c(H+)将
___________(填“增大”“减小”或“不变”)。
(3) 加入少量0.10 mol·L-1盐酸,电离平衡将___________(填“向左移动”“向右移动”或“不移动”),溶液中
c(H+)将___________(填“增大”“减小”或“不变”)。
(4) 加入20 mL 0.10 mol·L-1 NaCl溶液,平衡将___________(填“向左移动”“向右移动”或“不移动”),溶液中
c(H+)将___________(填“增大”“减小”或“不变”)。
杨sir化学,侵权必究
【答案】向右移动 增大 向右移动 减小 向左移动 增大 向右移动 减小
【详解】
(1)加入冰醋酸,醋酸浓度增大电离平衡向正反应方向移动,导致溶液中H+浓度增大;
(2)弱电解质浓度越小,其电离程度越大,所以加水稀释促进醋酸的电离,平衡向电离方向移动,但其电离
增大程度小于溶液体积增大程度,导致溶液中H+浓度减小;
(3)HCl是强电解质,电离出的氢离子抑制醋酸的电离,使电离平衡向左移动;平衡移动只是减弱H+浓度的
增大,最终结果还是增大;
(4)加入氯化钠溶液相当于稀释醋酸,促进醋酸的电离,则醋酸的电离平衡向右移动,但氢离子物质的量的
增加不如体积增加程度大,所以H+浓度减小。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是
选项 A B C D
强电解质 Fe NaCl
弱电解质 CO
2非电解质 (蔗糖)
A.A B.B C.C D.D
【答案】C
【详解】
A. 铁是单质,不是电解质,也不是非电解质,A不选;
B. 二氧化碳是非电解质,硫酸钡是强电解质,B不选;
C. 三种物质的分类均是正确的,C选;
D. 水是弱电解质,D不选;
答案选C。
【练2】下列说法正确的是
A.强酸和强碱一定是强电解质,不论其水溶液浓度大小,都能完全电离
B.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
C.强电解质不一定都是离子化合物
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
杨sir化学,侵权必究
【答案】C
【详解】
A.硫酸是强酸,98.3%的浓硫酸,由于水太少,硫酸大部分以分子形式存在,故A错误;
B.溶液导电能力与离子浓度有关,若强电解质溶液的浓度很小、弱电解质溶液中离子浓度很大,强电解
质溶液的导电能力可能比弱电解质溶液的导电能力弱,故B错误;
C.强电解质不一定都是离子化合物,如共价化合物HCl是强电解质,故C正确;
D.溶液导电能力与离子浓度、离子所带电荷有关,与几元酸无关,如磷酸是三元酸,其导电性不如同浓
度硫酸的导电性强,故D错误;
选C。
【练3】区分强弱电解质的标准是
A.在水中的溶解度 B.溶液的导电能力
C.电离是否完全 D.化学键的类型
【答案】C
【详解】
在水溶液或熔融状态下能完全电离的电解质是强电解质;在水溶液或熔融状态下只能部分电离的电解质是
弱电解质;区分强弱电解质的标准是电离是否完全,选C。
【练4】在醋酸溶液中存在电离平衡:CHCOOH CHCOO-+H+,要使电离平衡左移且c(H+)减小,应
3 3
采取的措施是
A.加入NaOH(s) B.加入盐酸 C.加蒸馏水 D.降低温度
【答案】D
【详解】A.加入NaOH固体会消耗氢离子,c(H+)减小,但平衡向右移动,A不符合题意;
B.加入盐酸氢离子的浓度可能会增大,B不符合题意;
C.加水稀释溶液酸性减弱c(H+)减小,但稀释会促进醋酸的电离,平衡向右移动,C不符合题意;
D.弱电解质的电离为吸热过程,降低温度平衡向左移动,c(H+)减小,D符合题意;
综上所述答案为D。
【练5】在含有酚酞的 氨水中加入少量 晶体,则溶液颜色
A.变为无色 B.变深 C.变浅 D.不变
【答案】C
【详解】
氨水中一水合氨部分电离出铵根离子和氢氧根离子,强电解质 电离出的 抑制了 的
电离,平衡左移,故 减小,颜色变浅,故C符合题意。
综上所述,答案为C。
【练6】在0.1mol∙L-1 CHCOOH溶液中存在如下电离平衡:CHCOOH⇌CHCOO-+H+对于该平衡,下列叙
3 3 3
述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向逆反应方向移动
杨sir化学,侵权必究
C.加入少量0.1mol∙L-1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小
D.加入少量CHCOONa固体,平衡向逆反应方向移动
3
【答案】D
【分析】
醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释促进醋酸电离,向醋酸溶液中加入含有氢离子或醋
酸根离子的物质抑制醋酸电离,加入和氢离子或醋酸根离子反应的物质促进醋酸电离,由此分析。
【详解】
A.加水促进弱电解质的电离,则电离平衡正向移动,故A不符合题意;
B.加入少量NaOH固体,与CHCOOH电离生成的H+结合,使电离平衡正向移动,故B不符合题意;
3
C.加入少量0.1mol∙L-1 HCl溶液,c(H+)增大,平衡逆向移动,但pH减小,故C不符合题意;
D.加入少量CHCOONa固体,由电离平衡可知,c(CHCOO-)增大,则电离平衡逆向移动,故D符合题意;
3 3
答案选D。
【练7】下列说法正确的是
A.电解质在溶液中存在电离平衡状态
B.电离平衡状态时v =v =0
结合 电离
C.弱电解质溶液中,既存在离子也存在分子
D.电解质的电离是可逆过程
【答案】C【详解】
A.弱电解质在溶液中存在电离平衡状态,而强电解质在溶液中不存在电离平衡,错误;
B.电离平衡状态时v =v ≠0,错误;
结合 电离
C. 弱电解质溶液中存在电离平衡,既存在离子,也存在未电离的电解质分子,正确;
D. 若电解质的电离是可逆过程,而强电解质在溶液中完全电离,不存在可逆过程,错误。
故答案为:C。
【练8】下列物质中,属于电解质的是_______,属于非电解质的是_______,属于强电解质的是_______,
属于弱电解质的是_______。
①氨气; ②氨水; ③盐酸; ④氢氧化钾; ⑤冰醋酸; ⑥氯化钠; ⑦醋酸铵; ⑧二氧化碳; ⑨氯化
钠溶液。
【答案】④⑤⑥⑦ ①⑧ ④⑥⑦ ⑤
【分析】
电解质是在水溶液中或熔融状态下能导电的化合物;非电解质是在水溶液中和融状态下不能导电的化合物;
在水溶液中能完全电离的电解质为强电解质,部分电离的为弱电解质;据此分析判断。
【详解】
①氨气为化合物,本身不能电离产生自由移动的离子,属于非电解质;
②氨水是混合物,既不是电解质也不是非电解质;
③盐酸是混合物,既不是电解质也不是非电解质;
④氢氧化钾是在水溶液中或熔融状态下能导电的化合物,属于电解质;且在水溶液中能完全电离,为强电
解质;
⑤冰醋酸是在水溶液中或熔融状态下能导电的化合物,属于电解质;且在水溶液中部分电离,属于弱电解
质;
⑥氯化钠是在水溶液中或熔融状态下能导电的化合物,属于电解质;且在水溶液中能完全电离,为强电解
质;
⑦醋酸铵是在水溶液中或熔融状态下能导电的化合物,属于电解质;且在水溶液中能完全电离,属于强电
解质;
⑧二氧化碳为化合物,本身不能电离,属于非电解质;
⑨氯化钠溶液是混合物,既不是电解质,也不是非电解质;
属于电解质的是④⑤⑥⑦,属于非电解质的是①⑧,属于强电解质的是④⑥⑦,属于弱电解质的是⑤,故
答案为:④⑤⑥⑦;①⑧;④⑥⑦;⑤。
【练9】从鲜花中可提取出一种简写为 的有机物,在其水溶液中因存在电离平衡:
,故可用作酸碱指示剂。在下列各物质的溶液(浓度均为
)中加入该指示剂,其中能使指示剂显黄色的有
① ② ③ ④ ⑤ ⑥A.①④⑤ B.②⑥ C.①④ D.⑤⑥
【答案】D
【详解】
①将指示剂加入到HCl溶液中后,由于溶液中氢离子较大,指示剂的平衡逆向移动,溶液显红色,故①错
误;
② 具有漂白性可以使有色物质漂白,溶液会变无色,故②错误;
③加入 后对平衡无影响,故③错误;
④ 在水溶液中能够完全解离为钠离子、氢离子和硫酸根,溶液呈酸性,加入指示剂后指示剂的电
离平衡逆向移动,溶液显红色,故④错误;
⑤ 的水溶液呈碱性,碳酸氢根的水解程度大于电离程度,溶液中存在大量氢氧根,加入指示剂
后指示剂的电离平衡正向移动,溶液显黄色,故⑤正确;
⑥ 形成的溶液呈碱性,溶液中存在大量氢氧根,加入指示剂后指示剂的电离平衡正向移动,溶液显黄
色,故⑥正确;
能使指示剂显黄色的是⑤⑥,故答案选:D。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育