文档内容
《原子结构与元素的性质》第二课时 教学设计
课题 《原子结构与元 单元 1 学科 化学 年级 高二
素的性质》
本节教学内容是人教版高中化学选择性必修第二册第一章《原子结构与性质》第二
节《原子结构与元素的性质》第三课时。这一课时的教学内容主要是电负性的概念以及
周期性变化规律。前一节已经学习了 “元素第一电离能”的概念及周期性变化相关内
容,了解了电离能随原子序数的变化而变化的周期性规律。本节内容在元素第一电离能
的基础上,进一步从电负性探究元素性质的周期性变化规律。重点探究电负性的周期性
教材 变化。
分析 本节安排了“电负性”这部分内容。学生通过学习这部分知识,了解电负性的概
念。
知道电负性的概念是由美国著名化学家鲍林提出。通过主动探究,理解电负性的周期性
变化趋势。通过思考讨论,学会应用电负性判断元素的原子半径大小、化合物元素化合
价正负、元素金属性与非金属性强弱、解释对角线规则。加深对元素周期律、元素周期
表及元素“位—构—性”三者关系的理解。
证据推理与模型认知:通过数据,主动绘制变化图探究元素电负性的变化趋势。理
教学目 解电负性的周期性变化趋势。通过综合比较与分析电离能与电负性的周期性变化异同
点,加深对元素周期律、元素周期表及元素“位—构—性”三者关系的理解。
标与核
心素养 科学精神与社会责任:通过了解电负性的概念是由美国著名化学家鲍林提出的,认
识到科学是在不断发展的,培养求真务实、不断进步的科学精神与社会责任感。
重点 电负性的周期性变化。
难点
教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 【旧知回顾】 复习旧知 通过之前
根据已学知识回顾:我们学过的化学键有哪几种类型? 已有知识
离子键、共价键。 的复习,
【思考】什么是化学键?如何理解? 给新内容
学习奠基
基础,提
高学生学
习 积 极
性。
讲授新课 第二节 原子结构与元素的性质
第三课时 电负性
一、电负性
1.化学键
元素相互化合,可理解为相邻原子之间产生化学作用 知道电负
力,形象地叫做化学键。 性 的 含
2.键合电子 义。
原子中用于形成化学键的电子称为键合电子。电负性的概念是由美国化学家鲍林提出的,用来描述不
同元素的原子对键合电子吸引力的大小。电负性越大的原
子,对键合电子的吸引力越大。鲍林利用实验数据进行了理
论计算,以氟的电负性为4.0和锂的电负性为1.0作为相对
标准,得出了各元素的电负性。
一、电负性
(1)定义
用来描述不同元素的原子对键合电子吸引力的大小。
(2)意义
电负性越大的原子,对键合电子的吸引力越大。
(3)大小标准
以氟的电负性为 4.0 和锂的电负性为 1.0 作为相对标
准,得出了各元素的电负性。
注意:电负性是相对值,没单位。
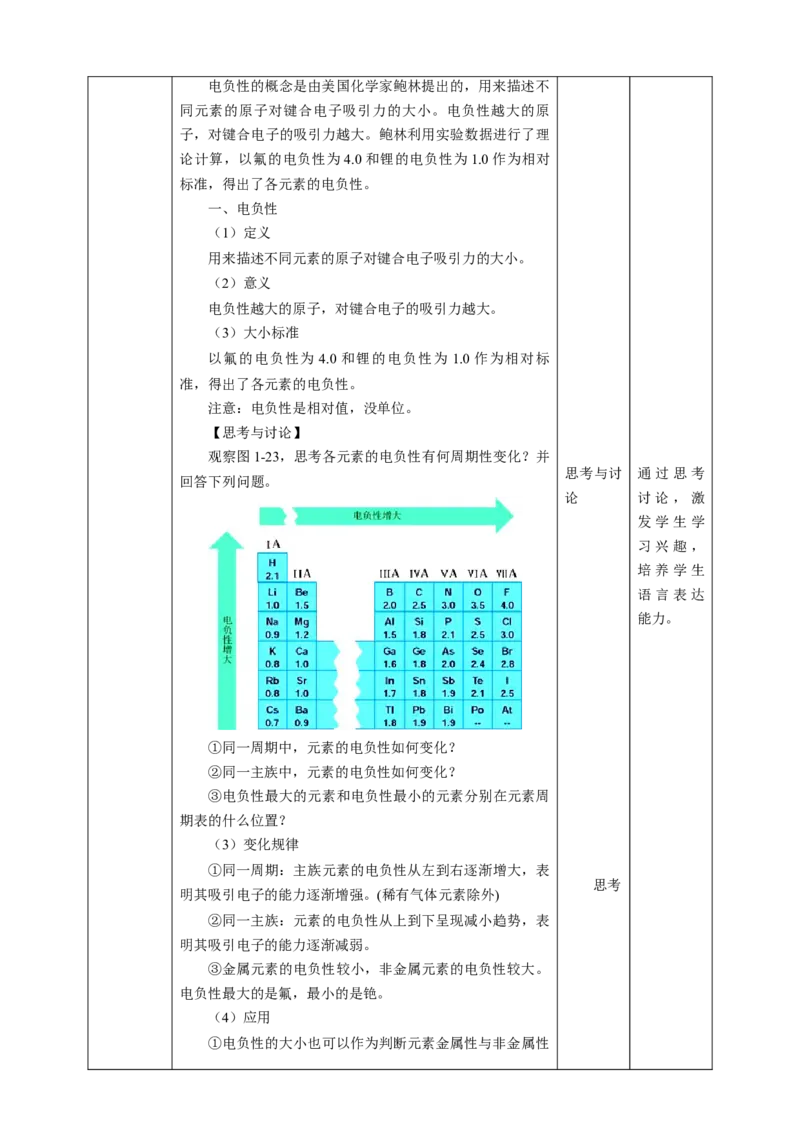
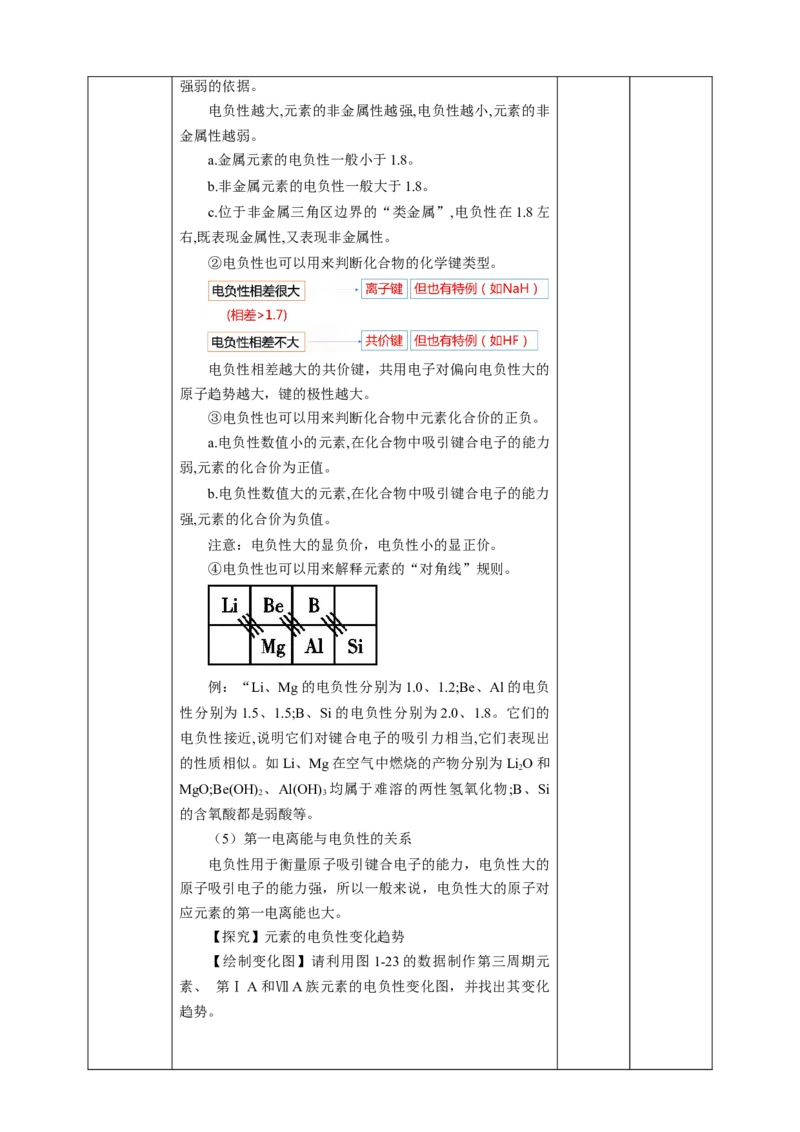
【思考与讨论】
观察图1-23,思考各元素的电负性有何周期性变化?并
思考与讨 通过思考
回答下列问题。
论 讨论,激
发学生学
习兴趣,
培养学生
语言表达
能力。
①同一周期中,元素的电负性如何变化?
②同一主族中,元素的电负性如何变化?
③电负性最大的元素和电负性最小的元素分别在元素周
期表的什么位置?
(3)变化规律
①同一周期:主族元素的电负性从左到右逐渐增大,表
思考
明其吸引电子的能力逐渐增强。(稀有气体元素除外)
②同一主族:元素的电负性从上到下呈现减小趋势,表
明其吸引电子的能力逐渐减弱。
③金属元素的电负性较小,非金属元素的电负性较大。
电负性最大的是氟,最小的是铯。
(4)应用
①电负性的大小也可以作为判断元素金属性与非金属性强弱的依据。
电负性越大,元素的非金属性越强,电负性越小,元素的非
金属性越弱。
a.金属元素的电负性一般小于1.8。
b.非金属元素的电负性一般大于1.8。
c.位于非金属三角区边界的“类金属”,电负性在1.8左
右,既表现金属性,又表现非金属性。
②电负性也可以用来判断化合物的化学键类型。
电负性相差越大的共价键,共用电子对偏向电负性大的
原子趋势越大,键的极性越大。
③电负性也可以用来判断化合物中元素化合价的正负。
a.电负性数值小的元素,在化合物中吸引键合电子的能力
弱,元素的化合价为正值。
b.电负性数值大的元素,在化合物中吸引键合电子的能力
强,元素的化合价为负值。
注意:电负性大的显负价,电负性小的显正价。
④电负性也可以用来解释元素的“对角线”规则。
例:“Li、Mg的电负性分别为1.0、1.2;Be、Al的电负
性分别为1.5、1.5;B、Si的电负性分别为2.0、1.8。它们的
电负性接近,说明它们对键合电子的吸引力相当,它们表现出
的性质相似。如Li、Mg在空气中燃烧的产物分别为LiO和
2
MgO;Be(OH) 、Al(OH) 均属于难溶的两性氢氧化物;B、Si
2 3
的含氧酸都是弱酸等。
(5)第一电离能与电负性的关系
电负性用于衡量原子吸引键合电子的能力,电负性大的
原子吸引电子的能力强,所以一般来说,电负性大的原子对
应元素的第一电离能也大。
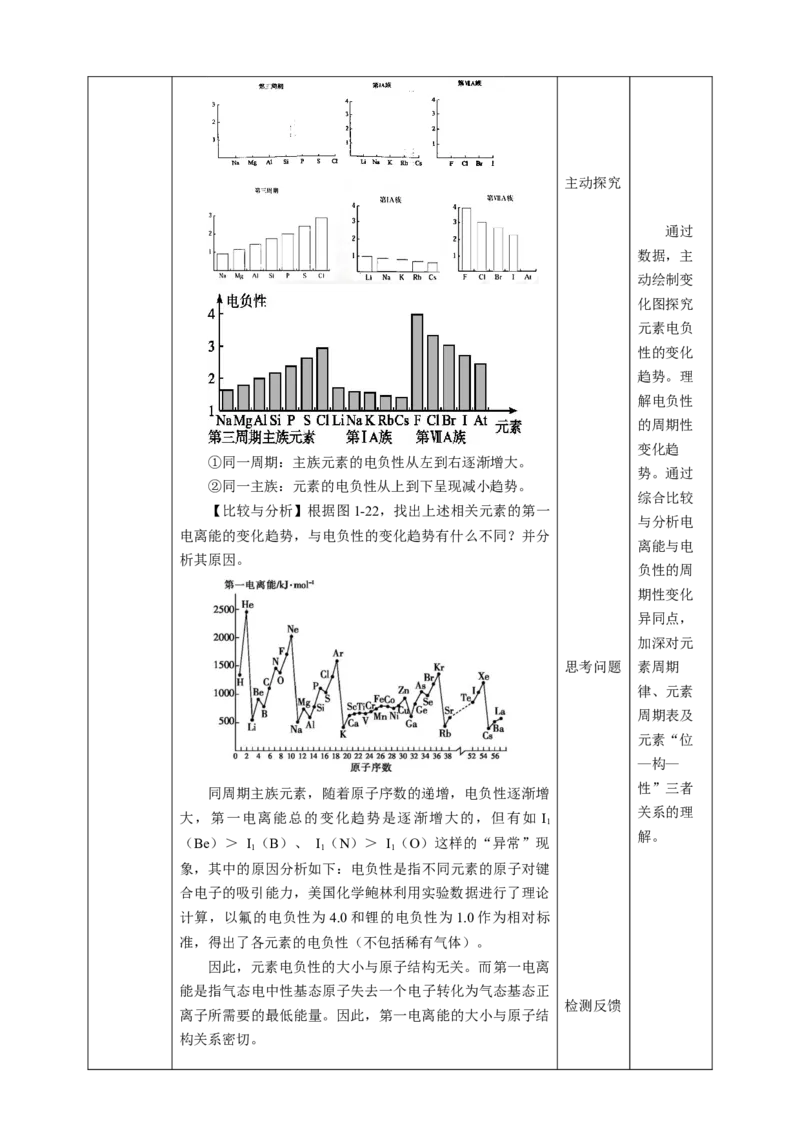
【探究】元素的电负性变化趋势
【绘制变化图】请利用图1-23的数据制作第三周期元
素、 第ⅠA和ⅦA族元素的电负性变化图,并找出其变化
趋势。主动探究
通过
数据,主
动绘制变
化图探究
元素电负
性的变化
趋势。理
解电负性
的周期性
变化趋
①同一周期:主族元素的电负性从左到右逐渐增大。
势。通过
②同一主族:元素的电负性从上到下呈现减小趋势。
综合比较
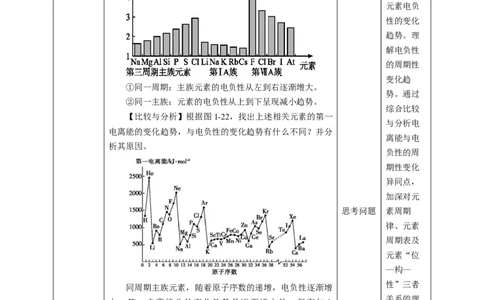
【比较与分析】根据图1-22,找出上述相关元素的第一
与分析电
电离能的变化趋势,与电负性的变化趋势有什么不同?并分
离能与电
析其原因。
负性的周
期性变化
异同点,
加深对元
思考问题 素周期
律、元素
周期表及
元素“位
—构—
性”三者
同周期主族元素,随着原子序数的递增,电负性逐渐增
关系的理
大,第一电离能总的变化趋势是逐渐增大的,但有如 I
1
解。
(Be)> I (B)、 I (N)> I (O)这样的“异常”现
1 1 1
象,其中的原因分析如下:电负性是指不同元素的原子对键
合电子的吸引能力,美国化学鲍林利用实验数据进行了理论
计算,以氟的电负性为4.0和锂的电负性为1.0作为相对标
准,得出了各元素的电负性(不包括稀有气体)。
因此,元素电负性的大小与原子结构无关。而第一电离
能是指气态电中性基态原子失去一个电子转化为气态基态正
检测反馈
离子所需要的最低能量。因此,第一电离能的大小与原子结
构关系密切。【课堂练习】
1.判断正误(正确的打“√”,错误的打“×”)
①原子半径:r(Si)>r(C)>r(B)。 ( )
②离子半径:r(Li+)O>C O>N>C课堂小结 原子结构与元素的性质
板书 原子结构与元素的性质