文档内容
3.1.2 晶胞(导学案)
1.认识简单的晶胞,能运用多种晶体模型和晶胞结构确定微粒个数和化学式,促进
“证据推理与模型认知”化学核心素养的发展。
2.了解晶体结构的测定方法。
重点:晶胞的形状、堆积方式以及结构特点;均摊法计算晶胞的化学组成。
难点:晶胞的无隙并置堆积方式及其结构特点。
1.晶胞
(1)概念:描述晶体结构的基本单元。
(2)晶胞与晶体的关系
常规的晶胞都是平行六面体,整块晶体可以看作是数量巨大的晶胞“无隙并置”而
成。
①“无隙”是指相邻晶胞之间没有任何间隙。
②“并置”是指所有晶胞都是平行排列的,取向相同。
③所有晶胞的形状及内部的原子种类、个数及几何排列(包括取向)是完全相同的。
(3)晶胞中粒子数目的计算(以铜的晶胞为例)
①位于顶角上的铜原子为8 个晶胞共用。
②位于面心上的铜原子为2 个晶胞共用。
③晶体铜中完全属于某一晶胞的铜原子数是4。
2.晶体结构的测定
测定晶体结构最常用的仪器是 X 射线衍射仪 。当单一波长的X射线通过晶体时,会在
记录仪上产生分立的斑点或者明锐的衍射峰,而非晶体图谱中没有。
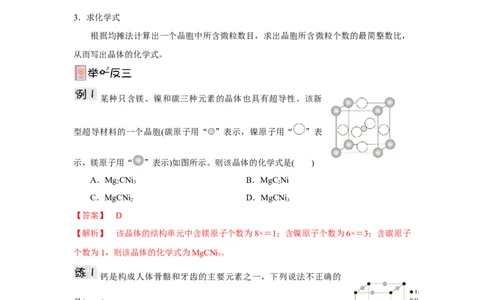
1.下列有关晶胞的叙述正确的是( )
A.晶胞的形状可以任意指定
B.不同的晶体中,晶胞的大小和形状都相同C.晶胞中的任何一个粒子都完全属于该晶胞
D.已知晶胞的组成就可推知晶体的组成
【答案】D
2.整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。对这句话的理解错误的是(
)
A.晶胞是描述晶体结构的基本单元
B.晶体是晶胞简单、随意堆积而成
C.晶胞排列时,取向相同
D.相邻晶胞之间没有任何间隙
【答案】B
3.下列六面体可作为晶胞的是( )
【答案】A
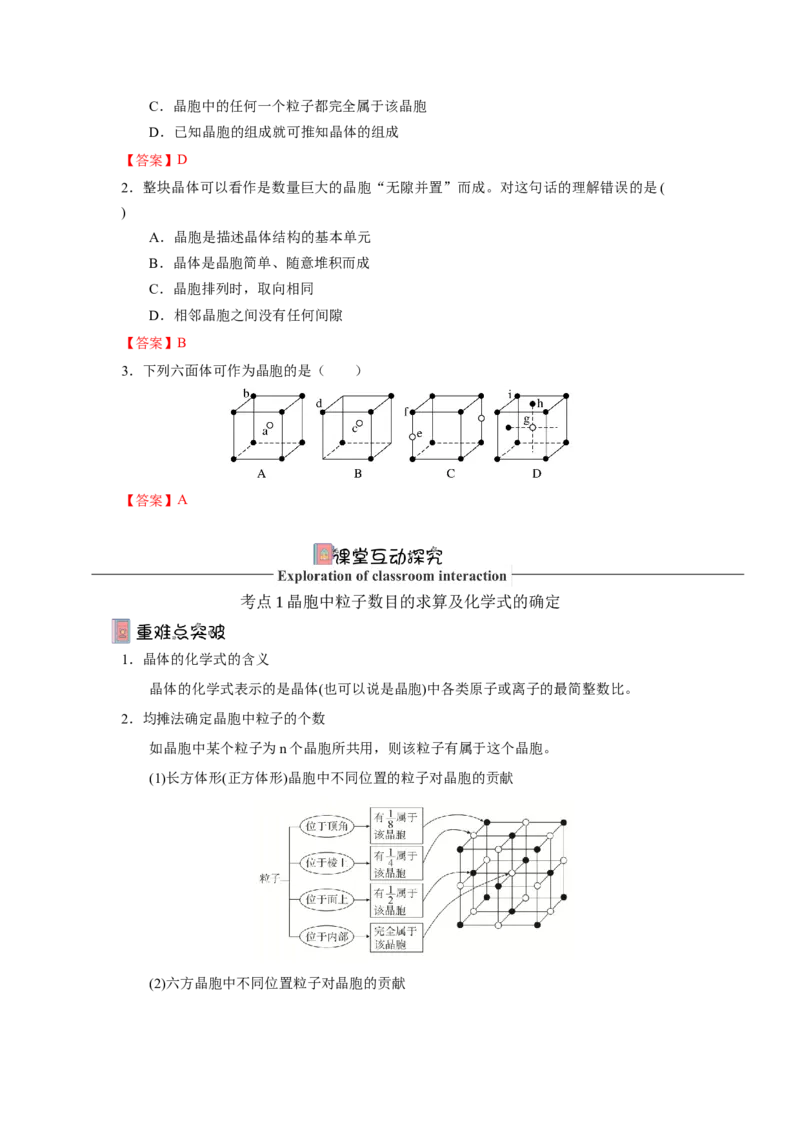
考点1晶胞中粒子数目的求算及化学式的确定
1.晶体的化学式的含义
晶体的化学式表示的是晶体(也可以说是晶胞)中各类原子或离子的最简整数比。
2.均摊法确定晶胞中粒子的个数
如晶胞中某个粒子为n个晶胞所共用,则该粒子有属于这个晶胞。
(1)长方体形(正方体形)晶胞中不同位置的粒子对晶胞的贡献
(2)六方晶胞中不同位置粒子对晶胞的贡献3.求化学式
根据均摊法计算出一个晶胞中所含微粒数目,求出晶胞所含微粒个数的最简整数比,
从而写出晶体的化学式。
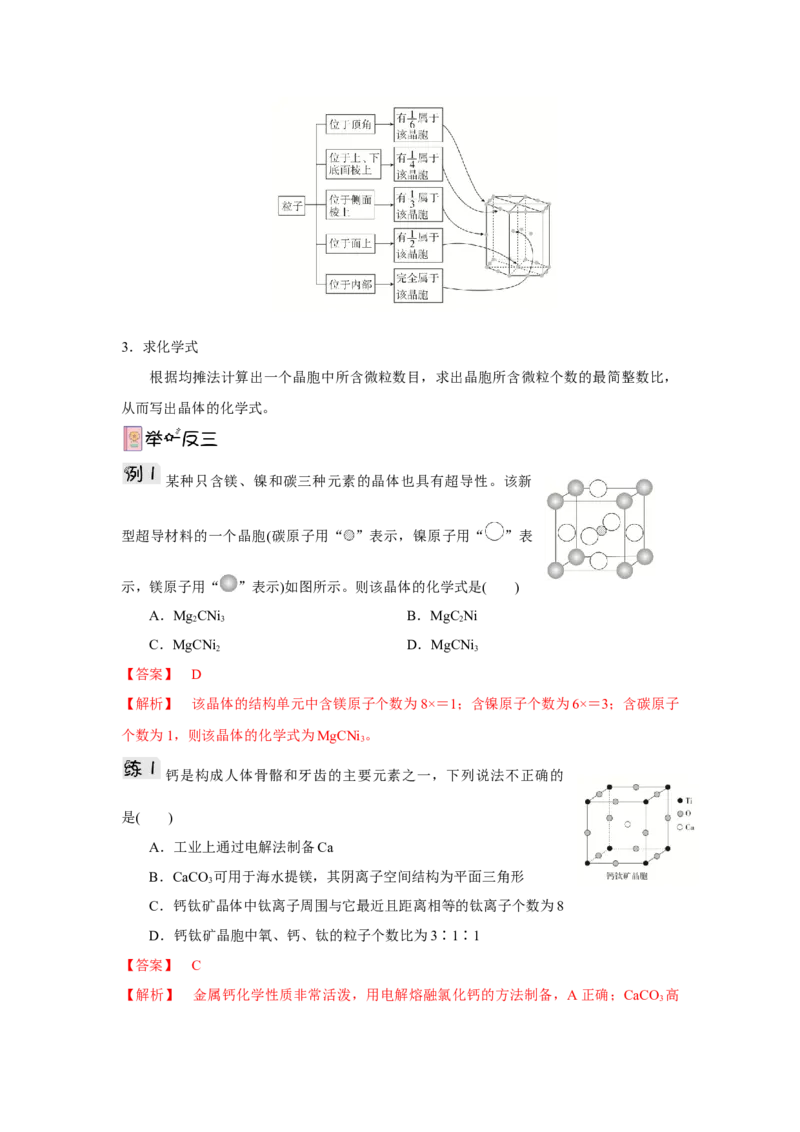
某种只含镁、镍和碳三种元素的晶体也具有超导性。该新
型超导材料的一个晶胞(碳原子用“ ”表示,镍原子用“ ”表
示,镁原子用“ ”表示)如图所示。则该晶体的化学式是( )
A.MgCNi B.MgC Ni
2 3 2
C.MgCNi D.MgCNi
2 3
【答案】 D
【解析】 该晶体的结构单元中含镁原子个数为8×=1;含镍原子个数为6×=3;含碳原子
个数为1,则该晶体的化学式为MgCNi 。
3
钙是构成人体骨骼和牙齿的主要元素之一,下列说法不正确的
是( )
A.工业上通过电解法制备Ca
B.CaCO 可用于海水提镁,其阴离子空间结构为平面三角形
3
C.钙钛矿晶体中钛离子周围与它最近且距离相等的钛离子个数为8
D.钙钛矿晶胞中氧、钙、钛的粒子个数比为3∶1∶1
【答案】 C
【解析】 金属钙化学性质非常活泼,用电解熔融氯化钙的方法制备,A正确;CaCO 高
3温分解得到氧化钙,CaO溶于水生成Ca(OH) ,Ca(OH) 可用于海水提镁,CO空间结构是
2 2
平面三角形,B正确;钙钛矿晶体中钛离子处于顶角位置,周围与它最近且距离相等的钛
离子个数为6,C错误;晶胞中氧原子位于棱上,钙原子位于体心,钛原子位于顶角,根
据均摊法知,钙钛矿晶胞中氧、钙、钛的粒子个数分别为12×、1、8×,D正确。
一、选择题(每小题只有1个选项符合题意)
1. 已知CsCl晶体的密度为ρ g/cm3,N 为阿伏加德罗常数的值,相
A
邻的两个Cs+的核间距为a cm,如图所示,则CsCl的相对分子质量
可以表示为( )
A.N a3ρ B.
A
C. D.
【答案】 A
【解析】 由题图可知,相邻的两个Cs+的核间距为a cm,即晶胞棱长为a cm,体积为
a3 cm3,顶点在空间被8个晶胞共用,体心为1个晶胞拥有,可知含1个氯离子,Cs+个数
为8×=1,则由ρV=可知,M==N a3ρ(g/mol),摩尔质量在以g/mol为单位时在数值上等
A
于其相对分子质量,所以其相对分子质量是N a3ρ。
A
2. CaC 晶体的晶胞结构(如图所示)与NaCl晶体的相似,但因为CaC 晶
2 2
体中含有的哑铃形C的存在,使晶胞沿一个方向拉长。下列关于 CaC
2
晶体的说法中正确的是( )
A.1个Ca2+周围距离最近且等距离的C数目为4
B.该晶体中的阴离子和O 所含电子数相同
2
C.6.4 g CaC 晶体中含阴离子0.2 mol
2
D.与每个Ca2+距离相等且最近的Ca2+共有12个
【答案】 A
【解析】 晶胞沿一个方向拉长,再由题图中体心可知,1个Ca2+周围距离最近的C有4
个,A正确;C含电子数为2×6+2=14,O 的电子数为16,二者电子数不同,B错误;6.4
2
g CaC 的物质的量为0.1 mol,CaC 晶体中含有的阴离子为C,则含阴离子的物质的量为
2 2
0.1 mol,C错误;晶胞沿一个方向拉长,与每个Ca2+距离相等且最近的Ca2+应为4个,D
错误。3.高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。
如图为超氧化钾晶体的一个晶胞,则下列说法中正确的是( )
A.超氧化钾的化学式为KO
2
B.每个晶胞中含有8个K+和4个O
C.晶体中与每个K+距离最近的K+有8个
D.晶体中0价氧原子和-2价氧原子个数比为1∶3
【答案】 A
【解析】 由题中的晶胞结构知,有8个K+位于晶胞顶角,6个K+位于晶胞面心,则晶
胞中含有K+的个数为8×+6×=4,O有12个位于棱上,1个处于体心,则晶胞中含有O的
个数为12×+1=4;超氧化钾的化学式为KO ;晶体中与每个K+距离最近的K+有12个;
2
设晶体中0价氧原子和-2价氧原子的个数分别为x、y,则有x+y=8,x×0+y×(-2)=-
4,得x∶y=3∶1。
4. 科学家合成了富集11B的非碳导热材料立方氮化硼晶体,晶胞结构如图。下列说法正确
的是( )
A.11BN和10BN的性质无差异
B.该晶体中含有σ键和π键
C.该晶胞中含有14个B原子,4个N原子
D.N原子周围等距且最近的N原子数为12
【答案】 D
【解析】 11B和10B互为同位素,11BN和10BN的性质相似,但不是完全相同,A错误;该
晶体中只含有σ键,B错误;该晶胞中B位于顶点和面心,个数为8×+6×=4,N位于体
内,个数为4,C错误。
5.热敏电阻的主要成分——钡钛矿晶体的晶胞结构如图所示,
晶胞棱长为a cm。顶点位置被Ti4+所占据,体心位置被Ba2+所
占据,所有棱心位置被O2-所占据。
(1)写出该晶体的化学式:____________。
(2)若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的________位
置。
(3)在该物质的晶体中,每个Ti4+周围距离相等且最近的Ti4+有________个;若将它们
连接起来,形成的空间结构为________。
(4)若晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为N ,则a=________。
A【答案】 (1)BaTiO (2)面心 (3)6 正八面体 (4)
3
【解析】 (1)在该晶胞中Ba2+、Ti4+和O2-的离子个数比为1∶(8×)∶(12×)=1∶1∶3,则
该晶体的化学式为BaTiO 。
3