文档内容
第一节 铁及其化合物
第3课时 铁盐和亚铁盐
基础巩固
1.(2022·广东韶关·高二期末)《新修本草》中描述“青矾”为“本来绿色,新出窟未见风者,正如琉
璃……烧之赤色……”。青矾加热时的反应为 。下列说法
正确的是
A.产物中含有3种酸性氧化物 B.所得赤色物质为
C.反应为分解反应 D.铁元素被还原
2.(2022·全国·高一)把Fe O 放入盐酸中能发生如下反应:Fe O +8HCl=2FeCl +FeCl +4H O,下列有关所
3 4 3 4 3 2 2
得溶液的说法正确的是
A.显蓝色 B.加入NaOH溶液只生成白色沉淀
C.加入Cu不反应 D.加入KSCN溶液后显红色
3.(2022·上海上海·模拟预测)硫酸铁溶液中加入少量Fe粉,溶液颜色变浅,要证明该过程发生了氧化
还原反应,加入下列试剂一定可行的是
A.KSCN溶液 B.酸性高锰酸钾溶液
C.NaOH溶液 D.铜粉
4.(2022·云南·弥勒市一中高一阶段练习)在无色溶液中下列离子能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
5.(2022·上海市七宝中学高一期末)① ② ③ ④ ,通过化合、置换、复分
解反应均能制得的是
A.只有①③ B.只有②④ C.只有① D.全部
6.(2022·全国·高一)(双选)已知下述三个实验均能发生化学反应:
① ② ③
向硫酸亚铁溶液中滴入几滴氯
将铁钉放入硫酸铜溶液中 将铜丝放入氯化铁溶液中
水
下列判断正确的是A.实验①中铁钉只作还原剂
B.实验②中Fe2+既显氧化性又显还原性
C.实验③中发生的是置换反应
D.上述实验证明氧化性:Fe3+>Cu2+>Fe2+
7.下列除杂方案错误的是
选
被提纯的物质 杂质 除杂试剂
项
学科网(北京)股份有限公司A 溶液
B 溶液 Fe粉
C 溶液 气体
D 溶液 KOH 加入 溶液
8.能正确表示下列反应的离子方程式是
A.在硫酸亚铁溶液中通入氧气:4Fe2++O +4H+=4Fe3++2H O
2 2
B.氯化铁溶液腐蚀铜电路板:Cu+Fe3+=Fe2++Cu2+
C.氢氧化亚铁溶于稀硝酸中:Fe(OH) +2H+=Fe2++2H O
2 2
D.澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO =CaCO ↓+H O
3 2
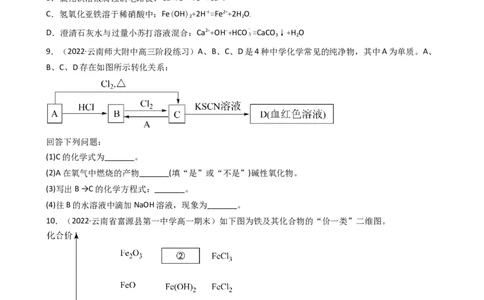
9.(2022·云南师大附中高三阶段练习)A、B、C、D是4种中学化学常见的纯净物,其中A为单质。A、
B、C、D存在如图所示转化关系:
回答下列问题:
(1)C的化学式为_______。
(2)A在氧气中燃烧的产物_______(填“是”或“不是”)碱性氧化物。
(3)写出B →C的化学方程式:_______。
(4)往B的水溶液中滴加NaOH溶液,现象为_______。
10.(2022·云南省富源县第一中学高一期末)如下图为铁及其化合物的“价一类”二维图。
(1)填写二维图缺失的类别①_______和化学式②_______。
(2)某同学利用以下试剂研究FeCl 性质,进行了如下预测:
3
①Cl ②Fe③NaOH④H SO ⑤AgNO
2 2 4 3
从物质类别上看,FeCl 属于_______,可能与_______发生反应(填序号)。
3
从化合价角度看,Fe3+具有_______性,可能与_______发生反应(填序号)。
(3)某工厂用FeCl 溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
3
学科网(北京)股份有限公司Cu+2FeCl =CuCl +2FeCl
3 2 2
①_______。
②在FeCl 反应中作_______剂。
3
③该反应的离子方程式为_______。
能力提升
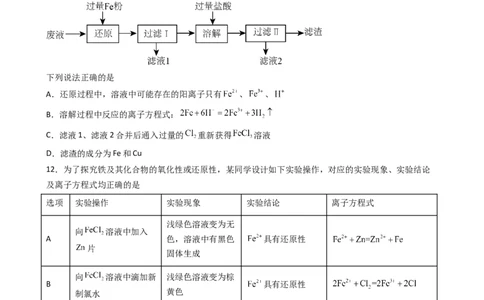
11.(2022·江苏连云港·高一期末)工业用 溶液刻蚀电路板的废液中主要含有 、 、 、
,实验室从废液中回收某些物质的流程如下:
下列说法正确的是
A.还原过程中,溶液中可能存在的阳离子只有 、 、
B.溶解过程中反应的离子方程式:
C.滤液1、滤液2合并后通入过量的 重新获得 溶液
D.滤渣的成分为Fe和Cu
12.为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论
及离子方程式均正确的是
选项 实验操作 实验现象 实验结论 离子方程式
浅绿色溶液变为无
向 溶液中加入
A 色,溶液中有黑色 具有还原性
片
固体生成
向 溶液中滴加新 浅绿色溶液变为棕
B 具有还原性
制氯水 黄色
向 溶液中加入铁 棕黄色溶液变为浅
C 具有还原性
粉 绿色
向 溶液中加入铜 蓝色溶液变为棕黄
D 具有氧化性
粉 色
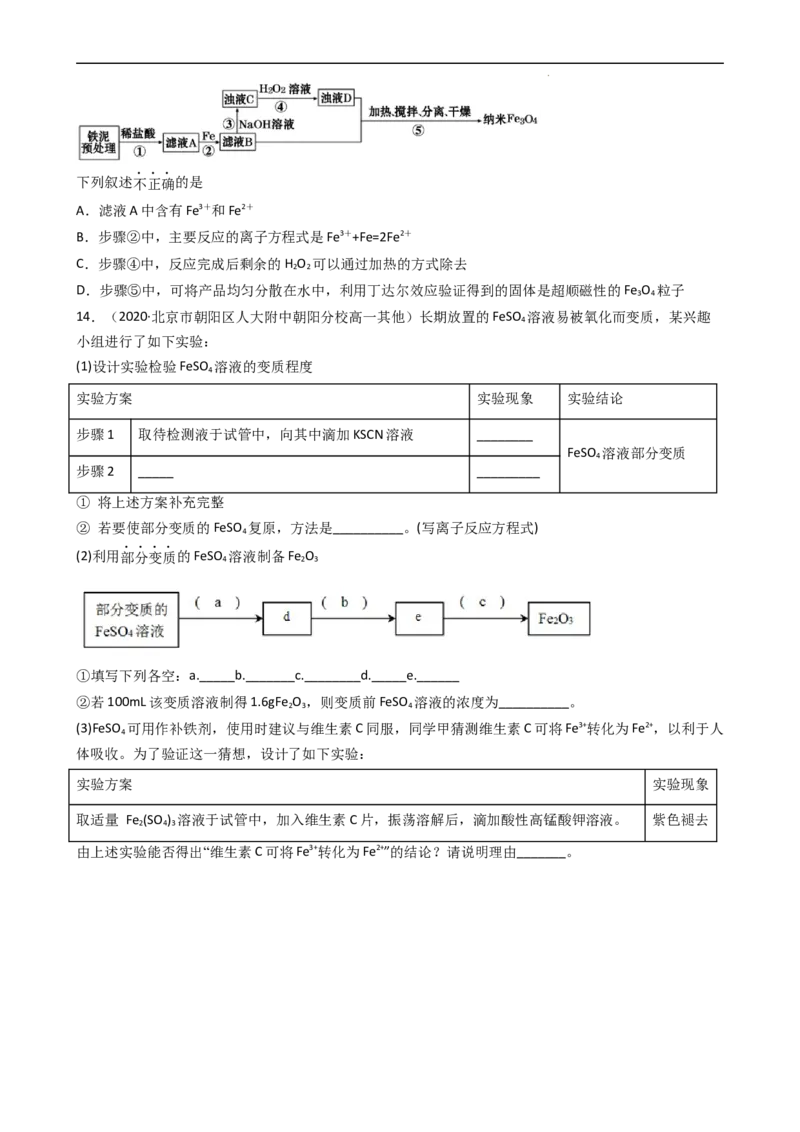
13.用铁泥(主要成分为Fe O 、FeO和少量Fe)制备超顺磁性(平均直径25nm)纳米Fe O 的流程示意图如下:
2 3 3 4
学科网(北京)股份有限公司下列叙述不正确的是
A.滤液A中含有Fe3+和Fe2+
B.步骤②中,主要反应的离子方程式是Fe3++Fe=2Fe2+
C.步骤④中,反应完成后剩余的H O 可以通过加热的方式除去
2 2
D.步骤⑤中,可将产品均匀分散在水中,利用丁达尔效应验证得到的固体是超顺磁性的Fe O 粒子
3 4
14.(2020·北京市朝阳区人大附中朝阳分校高一其他)长期放置的FeSO 溶液易被氧化而变质,某兴趣
4
小组进行了如下实验:
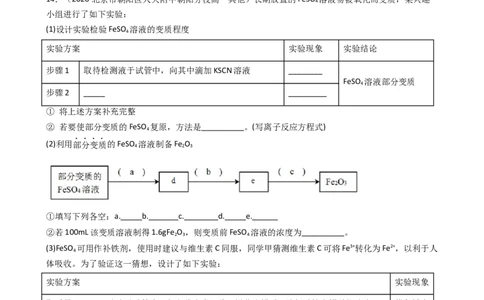
(1)设计实验检验FeSO 溶液的变质程度
4
实验方案 实验现象 实验结论
步骤1 取待检测液于试管中,向其中滴加KSCN溶液 ________
FeSO 溶液部分变质
4
步骤2 _____ _________
① 将上述方案补充完整
② 若要使部分变质的FeSO 复原,方法是__________。(写离子反应方程式)
4
(2)利用部分变质的FeSO 溶液制备Fe O
4 2 3
①填写下列各空:a._____b._______c.________d._____e.______
②若100mL该变质溶液制得1.6gFe O ,则变质前FeSO 溶液的浓度为__________。
2 3 4
(3)FeSO 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人
4
体吸收。为了验证这一猜想,设计了如下实验:
实验方案 实验现象
取适量 Fe (SO ) 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 紫色褪去
2 4 3
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由_______。
学科网(北京)股份有限公司学科网(北京)股份有限公司