文档内容
3.4 沉淀溶解平衡(精练)
题组一 沉淀溶解平衡
1.把NaCl晶体溶于水充分搅拌后,溶液中仍有晶体存在,下列说法正确的是
A.溶解过程停止 B.此时溶解速率等于结晶速率
C.此时溶质不再溶解 D.溶解过程停止
2.下列对沉淀溶解平衡的描述正确的是( )
A.沉淀达到溶解平衡时,溶液中溶质离子浓度一定相等,且保持不变
B.升高温度,沉淀溶解平衡一定向溶解方向移动
C.室温下,AgCl在水中的溶解度大于在食盐水中的溶解度
D.向NaSO 溶液中加入过量的BaCl 溶液,则SO 沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO
2 4 2
题组二 沉淀溶解平衡的影响因素
1.下列对沉淀溶解平衡的描述正确的是
A.达到平衡时,沉淀溶解和离子沉淀停止
B.达到平衡时,溶液中溶质的离子浓度相等
C.加水时,溶解平衡向溶解方向移动
D.升高温度,溶解平衡向溶解方向移动
2.(2022·全国·高二课时练习)下列有关BaSO 沉淀的溶解平衡状态的说法中,正确的是
4
A.BaSO 沉淀的生成和溶解不断进行,但速率相等
4
B.BaSO 难溶于水,溶液中没有Ba2+和SO
4
C.升高温度,BaSO 的溶解度不变
4
D.向BaSO 沉淀的溶解平衡体系中加入NaSO 固体,BaSO 的溶解度不变
4 4 4
3.在一定温度下,Fe(OH) 固体在水溶液中存在如下平衡:Fe(OH) (s) Fe3+(aq)+3OH-(aq),要使Fe(OH)
3 3 3
固体减少而c(Fe3+)不变,可采取的措施是
A.加少量水 B.加入少量盐酸 C.加入少量FeCl D.升高温度
3
4.石灰乳中存在下列平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq),加入下列溶液,不能使Ca(OH) 固体减
2 2
少的是( )
A.NaCO 溶液 B.加水 C.降温 D.CaCl 溶液
2 3 25.25 ℃时,在含有大量PbI 的饱和溶液中存在着平衡PbI (s) Pb2+(aq)+2I-(aq),加入KI溶液,下
2 2
列说法正确的是
A.溶液中Pb2+和I-浓度都增大 B.溶度积常数K 增大
sp
C.沉淀溶解平衡不移动 D.溶液中Pb2+浓度减小
6.已知溶液中存在平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq) H<0,下列有关该平衡体系的说法正确的是( )
2
①升高温度,平衡逆向移动 △
②向溶液中加入少量碳酸钠粉末能增大钙离子浓度
③恒温下向溶液中加入CaO,溶液的pH升高
④加热溶液,溶液的pH升高
⑤向溶液中加入NaCO 溶液,其中固体质量增加
2 3
⑥向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
A.仅①⑤ B.仅①⑤⑥ C.仅②③⑤ D.仅①②⑤⑥
7.已知 饱和溶液中存在沉淀溶解平衡 ,下列有关该平衡
体系的说法正确的是
①升高温度,该沉淀溶解平衡逆向移动
②向溶液中加入少量 粉末能增大 浓度
③恒温条件下,向溶液中加入 ,溶液的pH升高
④加热溶液,溶液的pH升高
⑤向溶液中加入 溶液,其中固体质量增加
⑥向溶液中加入少量 固体, 固体质量不变
A.①⑤ B.①④⑥ C.②③⑤ D.①②⑤⑥
8.(2022·黑龙江·嫩江市第一中学校高二开学考试)关于溶解平衡:Mg(OH) (s) Mg2+(aq)+2OH—
2
(aq),下列说法中正确的是
A.加入固体Mg(OH) ,可以增大溶液中镁离子的浓度
2
B.溶度积常数表示式:K =c(Mg2+)·c2 (OH—)
sp
C.加入NaOH浓溶液,可以增加Mg(OH) 的溶解量
2
D.升高温度,不会影响溶解平衡9.化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+: ,一定温
度下,下列有关该反应的推理正确的是
A.该反应达到平衡时c(Cu2+)=c(Mn2+)
B.往平衡体系中加入少量CuSO 固体后,c(Mn2+)变大
4
C.该反应的平衡常数
D.平衡体系中加入少量CuS(s)后,c(Mn2+)变小
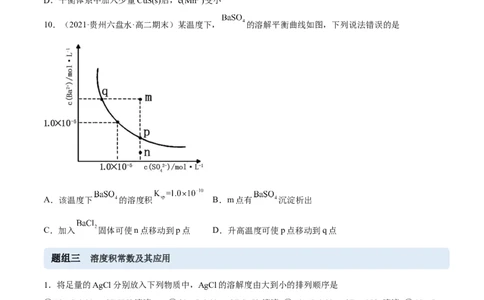
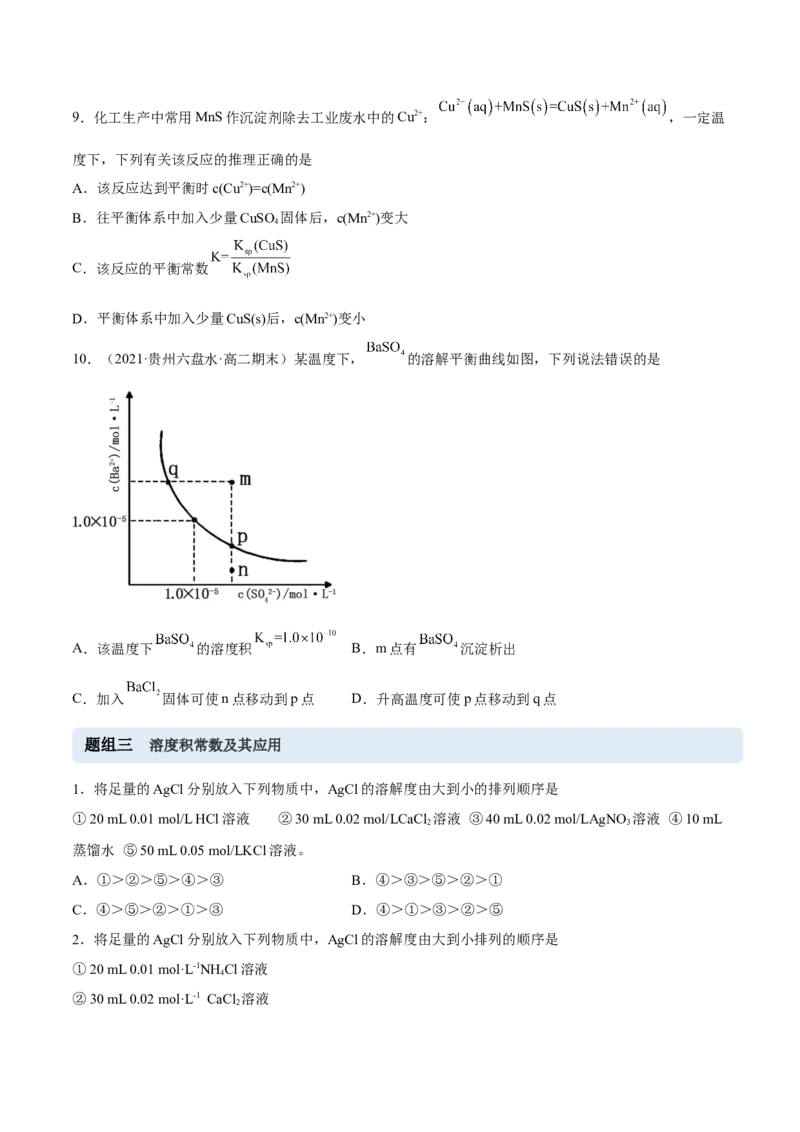
10.(2021·贵州六盘水·高二期末)某温度下, 的溶解平衡曲线如图,下列说法错误的是
A.该温度下 的溶度积 B.m点有 沉淀析出
C.加入 固体可使n点移动到p点 D.升高温度可使p点移动到q点
题组三 溶度积常数及其应用
1.将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①20 mL 0.01 mol/L HCl溶液 ②30 mL 0.02 mol/LCaCl 溶液 ③40 mL 0.02 mol/LAgNO 溶液 ④10 mL
2 3
蒸馏水 ⑤50 mL 0.05 mol/LKCl溶液。
A.①>②>⑤>④>③ B.④>③>⑤>②>①
C.④>⑤>②>①>③ D.④>①>③>②>⑤
2.将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小排列的顺序是
①20 mL 0.01 mol·L-1NH Cl溶液
4
②30 mL 0.02 mol·L-1 CaCl 溶液
2③40 mL 0.03 mol·L-1盐酸
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1AgNO 溶液
3
A.①②③④⑤ B.④①③②⑤ C.⑤④②①③ D.④③⑤②①
3.(2022·全国·高二课时练习)已知25℃时, 的平衡常数
, ,下列叙述中正确的是
A.25℃时,RSO 的K 的为
4 sp
B.将浓度均为 的RCl 、NaCO 溶液等体积混合后可得到RCO 沉淀
2 2 3 3
C.向c( )=c( )的混合液中滴加RCl 溶液,首先析出RSO 沉淀
2 4
D.相同温度下,RCO 在水中的K 大于在NaCO 溶液中的K
3 sp 2 3 sp
4.(2022·全国·高二课时练习)已知:Cr(OH) 在溶液中存在以下沉淀溶解平衡:Cr(OH) (s) Cr3+(aq)
3 3
+3OH-(aq) K =c(Cr3+)×c3(OH-)=10-32,下列有关说法不正确的是
sp
A.向5 mL 1.5×10-5 mol/L CrCl 溶液中,加入等体积等浓度的NaOH溶液,能观察到沉淀的产生
3
B.向 Cr(OH) 的悬浊液中加入NH Cl(s),Cr(OH) (s)的质量减小
3 4 3
C.当v (Cr3+)=3v (OH-)时,说明反应:Cr(OH) (s) Cr3+(aq)+3OH-(aq)达到平衡状态
正 逆 3
D.25℃时,将CrCl 溶液的pH调至5时,可认为溶液中的铬元素已基本沉淀完全(当溶液中c(Cr3+)≤10-5
3
mol/L时,可视作该离子沉淀完全)
5.(2021·河北·衡水市第十四中学高二阶段练习)关于沉淀溶解平衡和溶度积常数,下列说法不正确的是
A. 只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关
B. 时 在水中的溶解度大于其在CuCl 溶液中的溶解度
2
C.向 溶液中先滴加2滴 溶液,再滴加2滴 溶液,先生成
白色沉淀,后生成红褐色沉淀,说明
D.已知某温度下 ,则
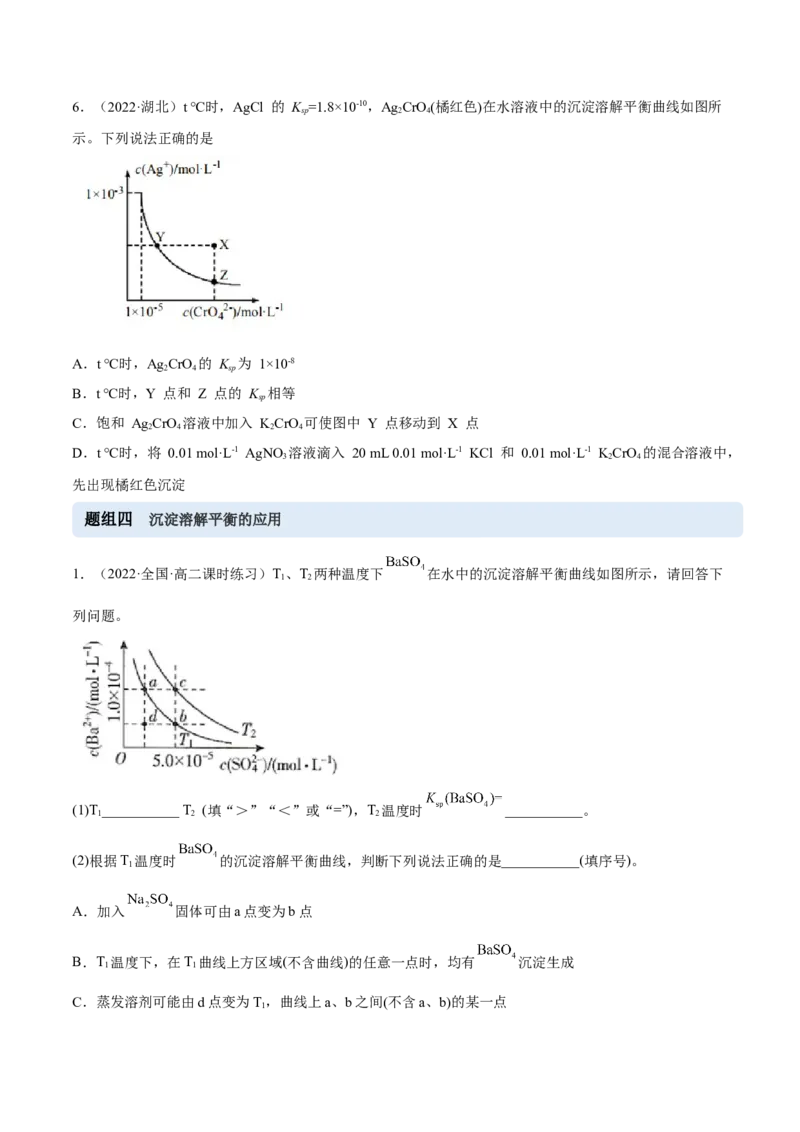
的平衡常数约为6.(2022·湖北)t ℃时,AgCl 的 K =1.8×10-10,Ag CrO(橘红色)在水溶液中的沉淀溶解平衡曲线如图所
sp 2 4
示。下列说法正确的是
A.t ℃时,Ag CrO 的 K 为 1×10-8
2 4 sp
B.t ℃时,Y 点和 Z 点的 K 相等
sp
C.饱和 Ag CrO 溶液中加入 KCrO 可使图中 Y 点移动到 X 点
2 4 2 4
D.t ℃时,将 0.01 mol·L-1 AgNO 溶液滴入 20 mL 0.01 mol·L-1 KCl 和 0.01 mol·L-1 KCrO 的混合溶液中,
3 2 4
先出现橘红色沉淀
题组四 沉淀溶解平衡的应用
1.(2022·全国·高二课时练习)T、T 两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下
1 2
列问题。
(1)T ___________ T (填“>”“<”或“=”),T 温度时 ___________。
1 2 2
(2)根据T 温度时 的沉淀溶解平衡曲线,判断下列说法正确的是___________(填序号)。
1
A.加入 固体可由a点变为b点
B.T 温度下,在T 曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
1 1
C.蒸发溶剂可能由d点变为T,曲线上a、b之间(不含a、b)的某一点
1D.升温可由b点变为d点
(3) T 温度时,现有0.2mol的 沉淀,每次用1 L饱和 溶液(浓度为1.7mol/L)处理。若使
2
中的 全部转化到溶液中,需要反复处理___________次[提示:
, ]。
2.(2022·西藏·拉萨那曲高级中学高二开学考试)回答下列问题:
(1)对于Ag S(s) 2Ag+(aq)+S2-(aq),其K =____。
2 sp
(2)在25℃下,向浓度均为0.1mol•L-1的MgCl 和CuCl 混合溶液中逐滴加入氨水,先生成____沉淀(填化学
2 2
式),生成该沉淀的离子方程式为_____。(已知25℃时K [Mg(OH) ]=1.8×10-11,K [Cu(OH) ]=2.2×10-20)。
sp 2 sp 2
(3)下列说法不正确的是____。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
C.对于Al(OH) (s) Al(OH) (aq) Al3++3OH-,前者为溶解平衡,后者为电离平衡
3 3
D.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO 效果好,说明Mg(OH) 的溶解度比MgCO 大
2 3
E.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全
3.(2022·云南省富源县第一中学高二期中)含氯化合物的应用越来越广泛,请完成下列有关问题:
(1)亚氯酸钠(NaClO)是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为_______,
2
其水溶液显碱性的原因为_______,其水溶液中离子浓度由大到小的顺序为_______。
(2)亚氯酸钠在碱性溶液中稳定,在酸性溶液中生成ClO 和氯元素的另一种稳定离子,写出亚氯酸钠在酸性
2
条件下反应的离子方程式_______。
(3)ClO 是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为SO 通入NaClO 中可得ClO ,
2 2 3 2
其氧化剂与还原剂的物质的量之比为_______。
(4)一定条件下,KClO 与硫酸酸化的草酸(H C O)溶液反应可制备ClO ,该反应的离子方程式为_______。
3 2 2 4 2
(5)AgNO 溶液可以用来检验水溶液中的Cl-或Br-。若向AgCl悬浊液中加入NaBr溶液,可把AgCl转化为
3
AgBr,已知AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)达到平衡时,c(Cl-)︰c(Br-)=23.4∶1,已知K (AgCl)=1.8×10-
sp
10,则K (AgBr)=_______。(不写单位)
sp4.(2021·内蒙古·巴彦淖尔市临河区第三中学高二阶段练习)回答下列问题
(1)已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,
再逐滴加入足量浓AgNO 溶液,充分反应后,下列说法正确的是_______
3
A.只有AgBr沉淀生成
B.AgCl与AgBr沉淀等量生成
C.AgCl与AgBr沉淀都有,但是以AgCl为主
D.AgCl与AgBr沉淀都有,但是以AgBr为主
(2)现向含AgBr的饱和溶液中:
①加入固体AgNO,则c(Ag+)_______(填“变大”“变小”或“不变”,下同);
3
②加入更多的AgBr固体,则c(Ag+)_______;
③加入NaBr固体,则 c(Ag+)_______。
(3)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8
时,c(Cu2+)=_______mol·L-1(Ksp[Cu(OH) ]=2.2×10-20)。
2
(4)若在0.1 mol·L-1硫酸铜溶液中通入过量HS气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是
2
_______mol·L-1
5.(2021·山东济宁·高二期中)下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为 )制备硫
酸锰及电解其溶液制锰的工艺流程图:
已知:①浸出液中主要含有 、 、 、 等杂质金属离子;
②生成氢氧化物的 见下表:
物质
开始沉淀的
7.5 2.7 7.7 7.6 8.3
完全沉淀的
9.7 3.7 8.4 8.2 9.8
③ , , , ,请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是___________。
(2)流程图中“①加入 ”的作用___________, 还可以用其他试剂___________(填化学式)代替。
(3)流程图中“②调节 ”可以除去某种金属离子,应将溶液 调节控制的范围是___________~7.6。
(4)向滤液I中加入 的作用是除去 、 等离子,其中可以发生反应为
等。当该反应完全后,滤液2中的 与 的物质的量浓度之比是
___________。
(5) 具有净水作用,其净水的原理是___________。(用离子方程式表示)
(6) 时 的溶液中, 浓度的最大值为 ___________ 。当溶液中加入 溶液
使 时 开始溶解,则 ___________。(溶液中 时 沉淀
完全)倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育