文档内容
《不同价态含硫物质的转化》教学设计
课题 《不同价态含硫 单元 5 学科 化学 年级 高一
物质的转化》
本节教学内容是人教版高中化学必修第二册第五章《化工生产中的重要非金属元素》
实验活动5《不同价态含硫物质的转化》。对关于含硫物质的学习是知识和用途相结合,理
论和实际相结合,着眼于对含硫物质性质的研究。例如二氧化硫是以大气污染物为背景学
习其性质,硫酸是以基础化工产品为背景学习其性质。在教材中,突出了“不同价态的硫元
素”及“硫的转化”的观点,从硫在自然界中的存在和转化,到实验室实现不同价态含硫
物质的相互转化,再到硫的转化在工业生产和环境保护中的体现和应用,多角度多层面介
绍硫及其化合物的有关知识。本节课的教学,希望学生能建立从另一种角度学习物质性质
的方法,即从转化的角度学习物质的性质,并在学习中体会物质之间转化和物质性质之间
教材
的关系。
分析
运用类比预测、启发探究、引导探究、问题探究法,使通过对不同价态硫元素之间转
化学习,加深学生对同一元素处于不同价态时相互转化规律的理解,不仅对金属元素知识
部分做了对比,更在知识面和思维品质上提高了要求。通过活动探究的形式使学生获取知
识,在关注获取知识结果的同时,也关注获取知识的过程。
本节安排了“硫的转化实验”,“硫元素转化规律”这两部分内容。学生通过学习这
部分知识,掌握硫元素的转化过程和化学反应原理,会根据硫元素的化合价变化,根据氧化
还原反应原理,实现对应的转化。
宏观辨识与微观探析:通过新旧知识的联系,培养学生知识迁移、拓展的能力,进一步激发
学生学习化学的兴趣和求知欲望,启发学生分析产生有关现象的因果关系和本质联系,从
而使学生了解学习和研究化学问题的一般方法和思维过程
证据推理与模型认知:通过揭示问题、讨论释疑、动手实验,学习对比、推断等多种科学探
教学目 究方法,学会由事物的表象分析事物的本质和变化,提高学生的实验能力、观察能力和对实
标与核 验现象的分析、推理及归纳总结能力。
心素养
科学探究与创新意识:从现象和结构出发,设计探究方案,探究硫的转化过程中的化学反应
原理,在探究中互利合作,培养团队精神。
科学精神与社会责任:激发学生透过现象探究本质的兴趣,尊重科学,认真学习科学的学习
方法;通过参与探究过程,培养自身严谨的科学态度和辩证分析能力。
重点 硫元素的相互转化。
难点
教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 步兵战车应用了一种新型才傲的发动机-------绝热陶瓷
发动机,可使其不易被红外探测器发现并被红外制导武器所
摧毁。那么你知道这种陶瓷在化学上属于什么材料吗?
讲授新课 实验活动5-----不同价态含硫物质的转化
一、硫的转化实验
【实验用品】
试管、托盘天平、量筒、酒精灯、铁架台、试管架、橡胶塞、
乳胶管、胶头滴管、玻璃导管、石棉网(或陶土网)、玻璃管、药
匙、棉花、镊子、火柴
浓硫酸、铜片、硫粉、铁粉、NaS溶液、酸性KMnO 溶
2 4
液、NaOH溶液、HSO 溶液、品红溶液
2 3
实验1.在两只试管中分别加入1mLNa S溶液,向其中
2一支边振荡边滴加HSO 溶液,另一支边振荡边滴加酸性
2 3
KMnO 溶液,用浸NaOH溶液的棉团分别塞住两个试管口,观
4
察并记录实验现象。
实验现象:加入HSO 溶液的试管中,出现淡黄色浑浊。加
2 3
入酸性KMnO 溶液的试管中,紫红色逐渐消失,并出现淡黄
4
色浑浊。
反 应 的 化 学 方 程 式 : 2NaS + 3H SO == 3S↓+
2 2 3
3HO+2Na SO
2 2 3
反应的离子方程式:5S2-+2MnO -+16H+==== 2Mn2++
4
8HO+5S↓
2
S元素化合价变化:S由-2价和+4价变为0价,-2价S具
有还原性,+4价S表现氧化性。
实验2.如下图所示连接仪器装置,向试管中加入1mL浓
硫酸和一小块铜片,塞上带导管的单孔橡胶塞,加热,观察并
记录实验现象。
实验现象:浓硫酸和铜片反应产生气泡,品红溶液颜色逐
渐变浅直至褪色。
实验:铜与浓硫酸反应(需要加热)
▲
原理:Cu +2HSO (浓) = = CuSO +SO↑+2H O
2 4 4 2 2
S元素化合价变化:由+6变为++44价,表现氧化性
实验3.将0.5g硫粉和1.0g铁粉均匀混合,放在石棉网
(或陶土网)上堆成条状,用灼热的玻璃棒触及混合粉末的一
端,当混合物呈红热状态时,移开玻璃棒,观察并记录实验现
象。
实验现象:刚开始无现象,玻璃棒呈红热状态后,反应迅
速,并有黑色固体生成。
硫粉与铁粉加热反应,得到硫化亚铁。
▲
Fe + S = = FeS,
S元元元素素素化化化合合合价价价变变变化化化:::由由由0价变为-2价,表现氧化性。
交流与讨论
1.在上述实验中,含硫物质中硫元素的价态发生了怎样
的变化?
实验1中.在NaS和HSO3反应中,NaS中S的化合价
2 2 2
由-2变为0价,HSO 化合价由+4变为0价;在NaS和酸性
2 3 2
KMnO 的反应中,S的化合价由-2变为0价。
4
实验2中.浓硫酸中S的化合价由+6变为+4.
实验3中.S的化合价由0价变为-2价。
2.铁粉和硫粉在空气中混合燃烧,可能发生哪些化学反应?
可能发生铁和氧气、铁和硫、硫和氧气的反应。
3.在实验过程中你遇到了哪些问题?你是如何解决的?
在实验1中可能遇到实验现象不明显,在操作中要注意
充分摇动;
实验2中反应过于剧烈,要注意控制加热温度;
实验3中不能引燃,要把玻璃棒加热到红热状态。
二、硫元素转化规律
1.硫元素的化合价及其化合物
FeS、H2S、HgS中S均为-2价;S单质的化合价为0价;
SO 、HSO 、NaSO 中S均为+4价;SO 、HSO 、NaSO 、
2 2 3 2 3 3 2 4 2 4
BaSO 中S均为+6价。
4
2.硫元素的氧化性和还原性
硫元素最高价(+6)只有氧化性,最低价(-2)只具有还
原性 ;中间价(0、+4)既具有氧化性,又具有还原性。使硫元
素由高价态向低价态转化需要加入还原剂,而硫元素低价态
向高价态转化需要加入氧化剂。
3.不同价态硫元素间的相互转化
HS S SO H SO
2 2 2 4
4.硫及其化合物之间相互转化
① 2H S + SO = 3S ↓ +H O
2 2 2
点燃
② S + O
2 ====
SO
2
加加热热
③ 2SO +O 2SO
2 2 3
催化剂
④ SO + H O = HSO
3 2 2 4
⑤ 2NaOH+SO=Na SO +H O
2 2 3 2
⑥ HO+SO HSO
2 2 2 3
⑦2Na SO +O =2NaSO
2 3 2 2 4
⑧2NaOH+H SO = Na SO +2H O
2 4 2 4 2
⑨BaCl +H SO = BaSO ↓+2HCl
2 2 4 4
相同价态含硫化合物间--酸碱反应规律转化
不同价态含硫化合物间--氧化还原反应规律
课堂练习
1、下列转化需要加入氧化剂才能实现的是( )A.HS SO B. H SO SO
2 2 2 4 2
C.SO 2- BaSO D. SO 2- SO
4 4 3 2
答案为:A
【解析】A.该反应中S元素化合价由-2价变为+4价,则
H2S是还原剂,需要氧化剂才能实现,如氧气,故A正确;
B.该反应中S元素化合价由+6价变为+4价,则HSO 是
2 4
氧化剂,需要还原剂才能实现,如Cu,故B错误;
C.该反应中各元素化合价不变,不发生氧化还原反应就
能实现,故C错误;
D.该反应中各元素化合价不变,不发生氧化还原反应就
能实现,故D错误;
2、下列化学品久置于空气中因发生氧化还原反应而变质
的是( )
A、NaOH B、浓HSO C、NaSO D、NaSO
2 4 2 3 2 4
答案为:C
【解析】A.NaOH与空气中的二氧化碳、水反应而变质,没
有元素的化合价变化,不发生氧化还原反应,故A不选;
B.HSO 在空气中不发生反应,故B不选;
2 4
C.Na SO 在空气中被氧气氧化为硫酸钠,有元素的化合
2 3
价变化,发生氧化还原反应,故C选;
D.NaSO 在空气中不发生反应,故D不选;
2 4
3、下列离子方程式书写正确的是( )
A、硫化亚铁与盐酸反应S2- + 2H+ == H2S↑
B、SO2通入溴水中 SO +Br +2H O==SO2- +2Br- +4H+
2 2 2 4
C.硫酸和氢氧化钡溶液H++SO2-+Ba2++OH-=BaSO ↓+H O
4 4 2
D、亚硫酸与氢氧化钠溶液混合 H+ + OH -==H O
2
答案为:B
4、已知下列氧化剂均能氧化+4价的硫元素,为了除去稀
硫酸中混有的亚硫酸,应选用的最合理的氧化剂是(
)
A. KMnO B. Ca(ClO) C. H O D. Cl
4 2 2 2 2
答案为:C
解析:除杂时不能引入新的杂质其他能够引入杂质的氧
化剂都不行,只能是过氧化氢(HO)了。
2 2
5、将SO 通入BaCl 溶液,未见沉淀,通入另一气体 X
2 2
仍无沉淀,则X可能是 ( )
A.HS B.NH C.Cl D.CO
2 3 2 2
答案为:D
【解析】A.SO 通入BaCl 溶液,未见沉淀,通入HS与二
2 2 2氧化硫反应生成S沉淀,故A不选;
B.通入NH 溶液呈碱性,溶液中生成大量的SO 2--离子,
3 3
生成沉淀BaSO,故B不选;
3
C.Cl 具有氧化性,在溶液中将SO 氧化为SO 2-离子,生
2 2 4
成沉淀BaSO,故C不选;
4
D.SO 与CO 都不与BaCl 反应,并且所对应的酸都比盐
2 2 2
酸弱,通入SO 与CO 都不会生成沉淀,故D选;
2 2
6.下列现象或事实可用同一原理解释的是( )
A.氯水和SO 使品红溶液退色
2
B.浓硫酸和浓硝酸长期暴露在空气中浓度降低
C.浓硫酸和浓硝酸都可以用铁质容器储运
D.SO 可使品红和酸性高锰酸钾溶液退色
2
答案为:C
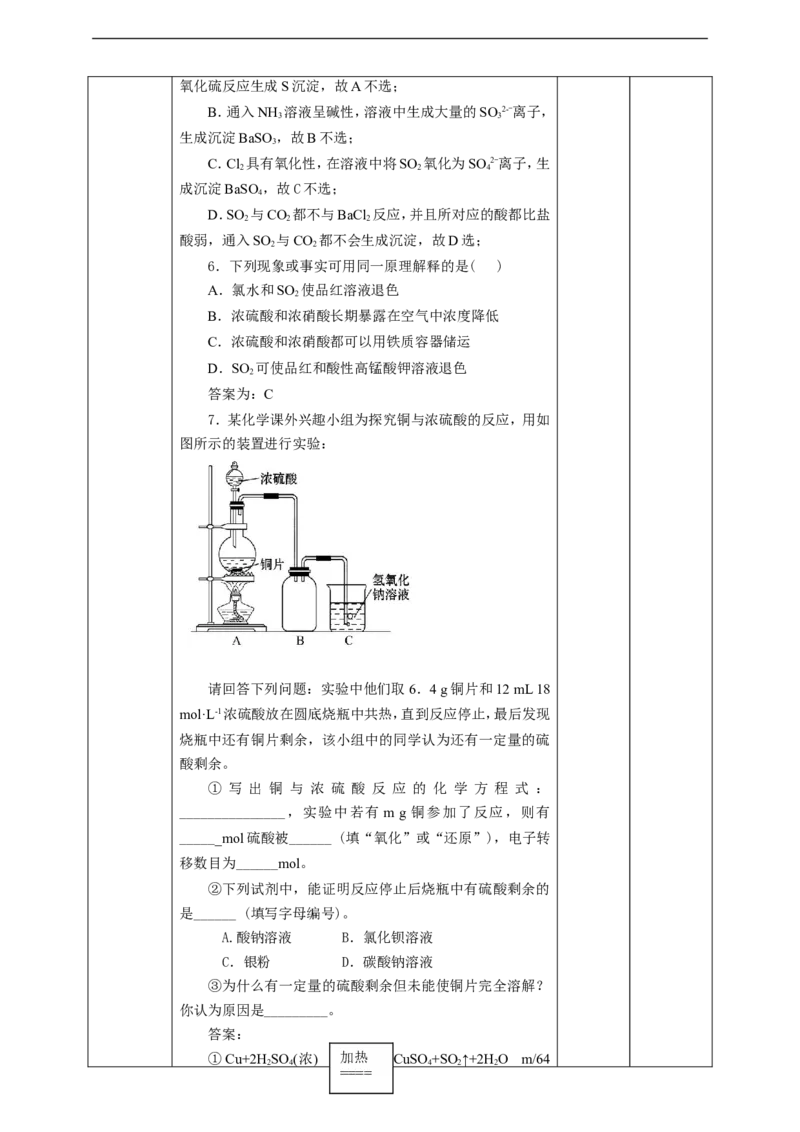
7.某化学课外兴趣小组为探究铜与浓硫酸的反应,用如
图所示的装置进行实验:
请回答下列问题:实验中他们取6.4 g铜片和12 mL 18
mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现
烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫
酸剩余。
① 写 出 铜 与 浓 硫 酸 反 应 的 化 学 方 程 式 :
_______________,实验中若有 m g 铜参加了反应,则有
______mol硫酸被______ (填“氧化”或“还原”),电子转
移数目为______mol。
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的
是______ (填写字母编号)。
A.酸钠溶液 B.氯化钡溶液
C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?
你认为原因是_________。
答案:
①Cu+2H SO (浓)) 加 热 CuSO +SO↑+2H O m/64
2 4 4 2 2
====还原 m/32
②D
③随着反应的进行,浓硫酸逐渐变为稀硫酸,稀硫酸不与
铜反应。
课堂小结 含硫物质的相互转化:
氧化剂
氧化剂 氧化剂
HSSSS SSSS SSSSOOOO H SSOO
2 2 2 4
还原剂 还原剂 还原剂
板书 一、硫的转化实验
二、 硫元素转化规律
1.硫元素的化合价及其化合物
2.硫元素的氧化性和还原性
3.不同价态硫元素间的相互转化
4.硫及其化合物之间相互转化