文档内容
第八、九单元测试题
(满分:100分 时间:90分钟)
相对原子质量:H—1 C—12 O—16 S—32 Fe—56 Cu—64
一、选择题(每小题3分,共45分)
1.(2017·湘潭)下列物质加入水中,不能形成溶液的是(D)
A.食盐 B.葡萄糖 C.氢氧化钠 D.植物油
2.(2017·江西)我省明代科学家宋应星所著的《天工开物》中,详细记述了金、铜、铁、锌
等金属的开采和冶炼方法,记述的金属中金属活动性最强的是(D)
A.金 B.铜 C.铁 D.锌
3.(2017·青岛)下列有关溶液的说法中,错误的是(C)
A.外界条件不改变,溶质不会从溶液中分离出来
B.物质的溶解过程通常会伴随着能量的变化
C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动,所以溶液具有
均一性和稳定性
D.改变条件,能够使饱和溶液与不饱和溶液相互转化
4.(2016·成都)在金属表面覆盖保护膜是普遍采用的金属防锈措施之一。下列自行车的
防锈措施中,不属于覆盖保护膜的是(A)
A.擦拭保持洁净与干燥 B.链条上油 C.轮圈镀铬 D.车架喷漆
5.(2016·枣庄)X、Y、Z为三种金属,已知:①X+HSO ===XSO +H↑;②Y+
2 4 4 2
2ZNO ===Y(NO )+2Z;③Y与稀硫酸不反应,则下列符合要求的X、Y、Z分别是(A)
3 3 2
A.Fe Cu Ag B.Cu Hg Ag C.Mg Zn Fe D.Fe Ag Cu
6.(2017·杭州)工业上可用如下反应制取金属钡:2Al+4BaO=====3Ba↑+Ba(AlO)。
2 2
下列说法正确的是(C)
A.反应物铝能被磁铁吸引 B.生成物Ba(AlO) 属于氧化物
2 2
C.反应前后铝元素的化合价发生改变 D.该反应属于复分解反应
7.(2017·江西)进行“一定溶质质量分数的氯化钠溶液的配制”实验活动时,常出现以
下错误操作,其中不影响所配溶液浓度的是(D)
A.氯化钠放在右盘 B.氯化钠洒出 C.俯视读数 D.配好的溶液
装瓶时溅出
8.(2017·贵港)下列实验现象描述错误的是(C)
A.向米饭上滴加几滴碘水后呈现蓝色
B.氢氧化钠固体溶于水,溶液温度升高
C.镁条在空气中燃烧,发出耀眼的白光,生成黑色固体
D.将铁片放入硫酸铜溶液中,铁片上出现红色物质
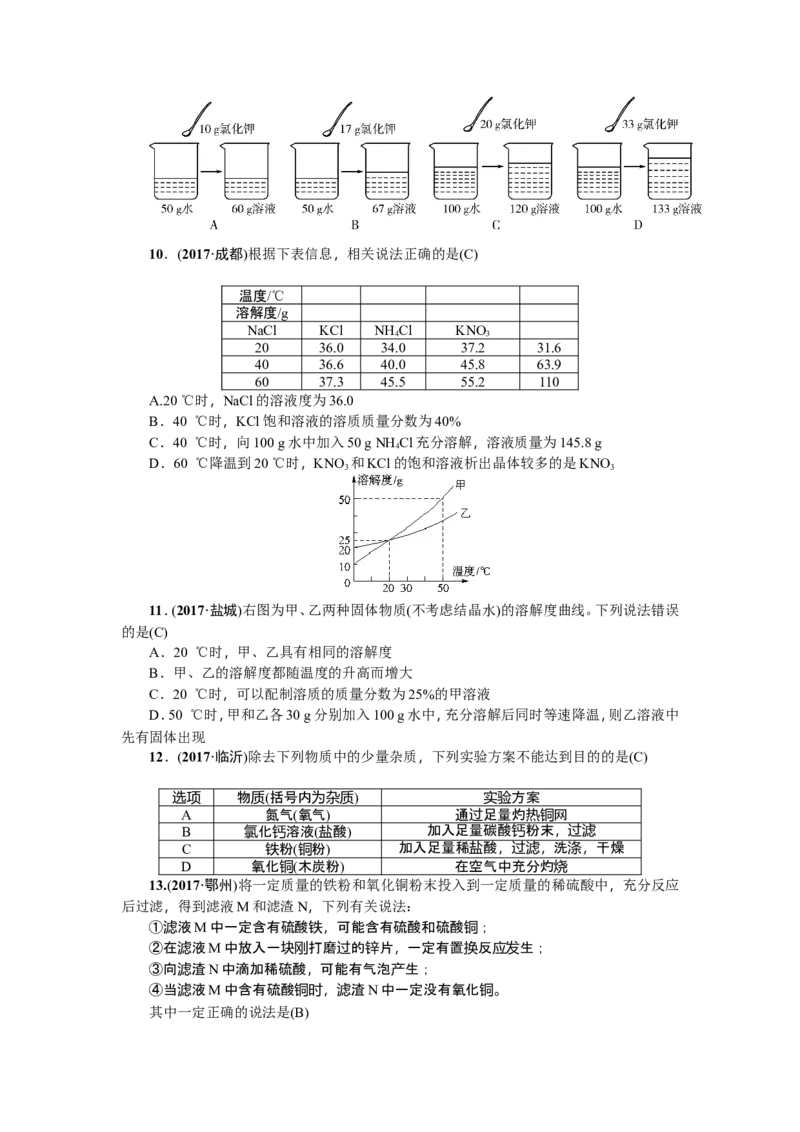
9.(2017·来宾)20 ℃时氯化钾的溶解度为34 g。下列是四位同学在20 ℃时配制的氯化钾
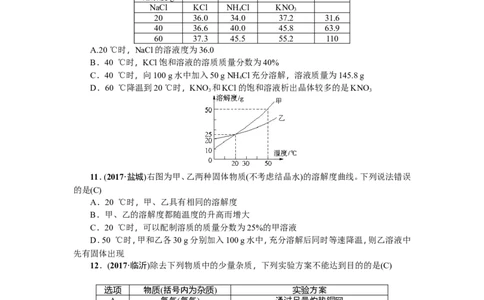
溶液,其中一定达到饱和的是(B)10.(2017·成都)根据下表信息,相关说法正确的是(C)
温度/℃
溶解度/g
NaCl KCl NH Cl KNO
4 3
20 36.0 34.0 37.2 31.6
40 36.6 40.0 45.8 63.9
60 37.3 45.5 55.2 110
A.20 ℃时,NaCl的溶液度为36.0
B.40 ℃时,KCl饱和溶液的溶质质量分数为40%
C.40 ℃时,向100 g水中加入50 g NH Cl充分溶解,溶液质量为145.8 g
4
D.60 ℃降温到20 ℃时,KNO 和KCl的饱和溶液析出晶体较多的是KNO
3 3
11.(2017·盐城)右图为甲、乙两种固体物质(不考虑结晶水)的溶解度曲线。下列说法错误
的是(C)
A.20 ℃时,甲、乙具有相同的溶解度
B.甲、乙的溶解度都随温度的升高而增大
C.20 ℃时,可以配制溶质的质量分数为25%的甲溶液
D.50 ℃时,甲和乙各30 g分别加入100 g水中,充分溶解后同时等速降温,则乙溶液中
先有固体出现
12.(2017·临沂)除去下列物质中的少量杂质,下列实验方案不能达到目的的是(C)
选项 物质(括号内为杂质) 实验方案
A 氮气(氧气) 通过足量灼热铜网
B 氯化钙溶液(盐酸) 加入足量碳酸钙粉末,过滤
C 铁粉(铜粉) 加入足量稀盐酸,过滤,洗涤,干燥
D 氧化铜(木炭粉) 在空气中充分灼烧
13.(2017·鄂州)将一定质量的铁粉和氧化铜粉末投入到一定质量的稀硫酸中,充分反应
后过滤,得到滤液M和滤渣N,下列有关说法:
①滤液M中一定含有硫酸铁,可能含有硫酸和硫酸铜;
②在滤液M中放入一块刚打磨过的锌片,一定有置换反应发生;
③向滤渣N中滴加稀硫酸,可能有气泡产生;
④当滤液M中含有硫酸铜时,滤渣N中一定没有氧化铜。
其中一定正确的说法是(B)A.①② B.②③ C.③④ D.①④
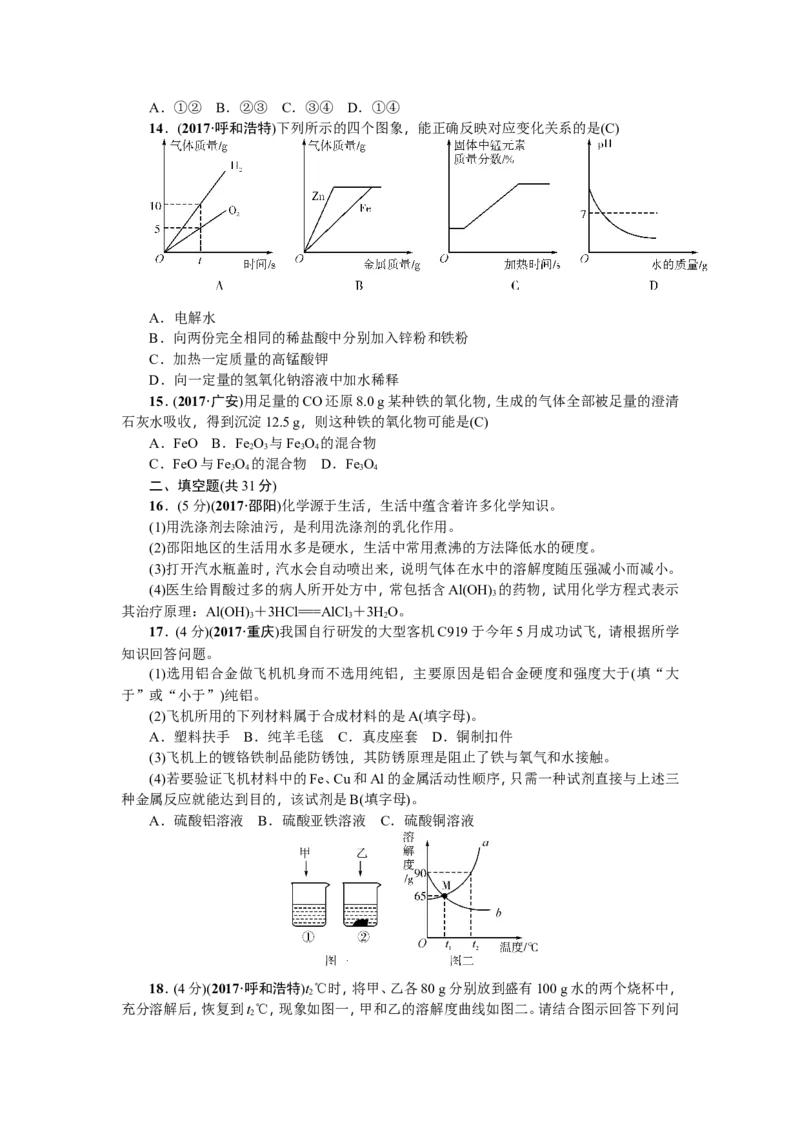
14.(2017·呼和浩特)下列所示的四个图象,能正确反映对应变化关系的是(C)
A.电解水
B.向两份完全相同的稀盐酸中分别加入锌粉和铁粉
C.加热一定质量的高锰酸钾
D.向一定量的氢氧化钠溶液中加水稀释
15.(2017·广安)用足量的CO还原8.0 g某种铁的氧化物,生成的气体全部被足量的澄清
石灰水吸收,得到沉淀12.5 g,则这种铁的氧化物可能是(C)
A.FeO B.Fe O 与Fe O 的混合物
2 3 3 4
C.FeO与Fe O 的混合物 D.Fe O
3 4 3 4
二、填空题(共31分)
16.(5分)(2017·邵阳)化学源于生活,生活中蕴含着许多化学知识。
(1)用洗涤剂去除油污,是利用洗涤剂的乳化作用。
(2)邵阳地区的生活用水多是硬水,生活中常用煮沸的方法降低水的硬度。
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随压强减小而减小。
(4)医生给胃酸过多的病人所开处方中,常包括含Al(OH) 的药物,试用化学方程式表示
3
其治疗原理:Al(OH) +3HCl===AlCl +3HO。
3 3 2
17.(4分)(2017·重庆)我国自行研发的大型客机C919于今年5月成功试飞,请根据所学
知识回答问题。
(1)选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度大于(填“大
于”或“小于”)纯铝。
(2)飞机所用的下列材料属于合成材料的是A(填字母)。
A.塑料扶手 B.纯羊毛毯 C.真皮座套 D.铜制扣件
(3)飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与氧气和水接触。
(4)若要验证飞机材料中的Fe、Cu和Al的金属活动性顺序,只需一种试剂直接与上述三
种金属反应就能达到目的,该试剂是B(填字母)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
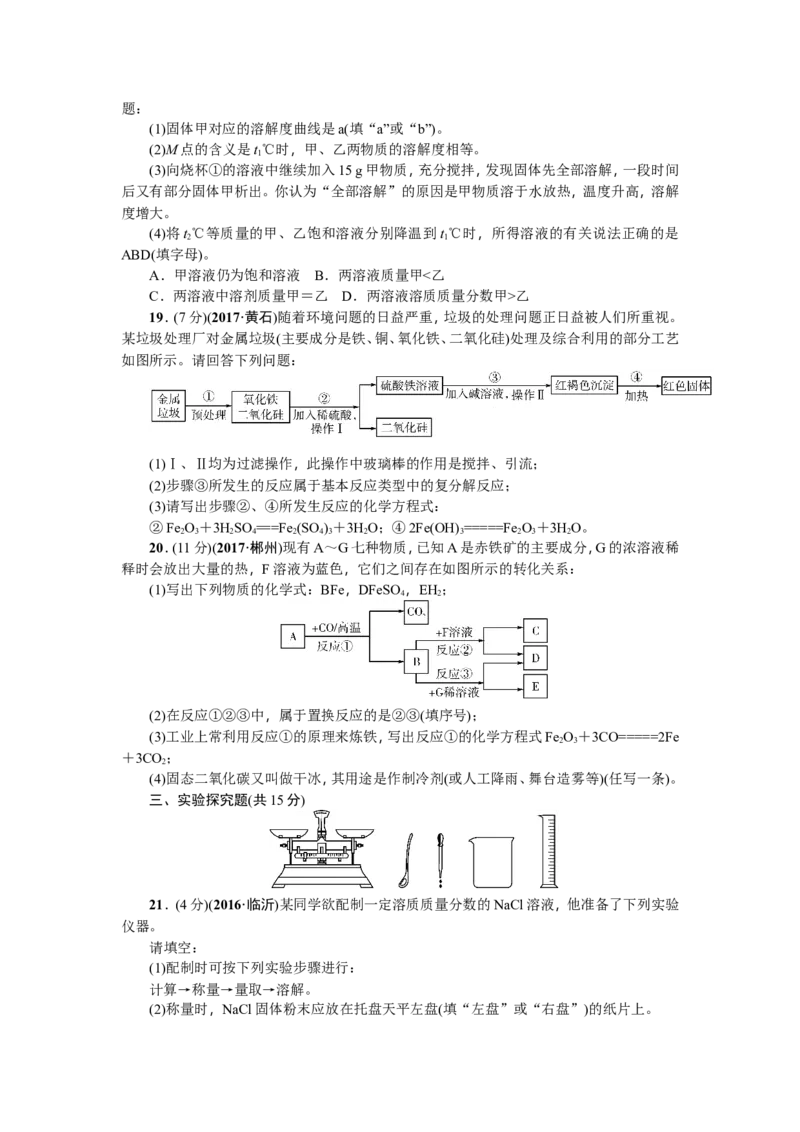
18.(4分)(2017·呼和浩特)t℃时,将甲、乙各80 g分别放到盛有100 g水的两个烧杯中,
2
充分溶解后,恢复到t℃,现象如图一,甲和乙的溶解度曲线如图二。请结合图示回答下列问
2题:
(1)固体甲对应的溶解度曲线是a(填“a”或“b”)。
(2)M点的含义是t℃时,甲、乙两物质的溶解度相等。
1
(3)向烧杯①的溶液中继续加入15 g甲物质,充分搅拌,发现固体先全部溶解,一段时间
后又有部分固体甲析出。你认为“全部溶解”的原因是甲物质溶于水放热,温度升高,溶解
度增大。
(4)将t℃等质量的甲、乙饱和溶液分别降温到t℃时,所得溶液的有关说法正确的是
2 1
ABD(填字母)。
A.甲溶液仍为饱和溶液 B.两溶液质量甲<乙
C.两溶液中溶剂质量甲=乙 D.两溶液溶质质量分数甲>乙
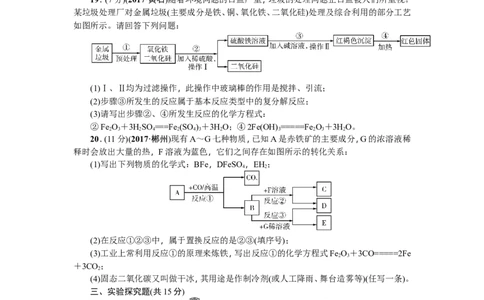
19.(7分)(2017·黄石)随着环境问题的日益严重,垃圾的处理问题正日益被人们所重视。
某垃圾处理厂对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)处理及综合利用的部分工艺
如图所示。请回答下列问题:
(1)Ⅰ、Ⅱ均为过滤操作,此操作中玻璃棒的作用是搅拌、引流;
(2)步骤③所发生的反应属于基本反应类型中的复分解反应;
(3)请写出步骤②、④所发生反应的化学方程式:
②Fe O+3HSO ===Fe (SO )+3HO;④2Fe(OH) =====Fe O+3HO。
2 3 2 4 2 4 3 2 3 2 3 2
20.(11分)(2017·郴州)现有A~G七种物质,已知A是赤铁矿的主要成分,G的浓溶液稀
释时会放出大量的热,F溶液为蓝色,它们之间存在如图所示的转化关系:
(1)写出下列物质的化学式:BFe,DFeSO ,EH;
4 2
(2)在反应①②③中,属于置换反应的是②③(填序号);
(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式Fe O+3CO=====2Fe
2 3
+3CO;
2
(4)固态二氧化碳又叫做干冰,其用途是作制冷剂(或人工降雨、舞台造雾等)(任写一条)。
三、实验探究题(共15分)
21.(4分)(2016·临沂)某同学欲配制一定溶质质量分数的NaCl溶液,他准备了下列实验
仪器。
请填空:
(1)配制时可按下列实验步骤进行:
计算→称量→量取→溶解。
(2)称量时,NaCl固体粉末应放在托盘天平左盘(填“左盘”或“右盘”)的纸片上。(3)配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是玻璃棒(填仪器名称)。
(4)量取一定体积的水,除了用量筒外,还需要用胶头滴管(填仪器名称)。
22.(11分)(2017·扬州)为测定钢铁中的含碳量,设计如图装置,钢铁样品在装置A中煅
烧时,气体产物只有CO 和SO 。
2 2
(1)钢样处理成粉末的主要目的是增大反应物的接触面积,使反应更充分。钢样中的Fe C
3
煅烧时的化学方程式为Fe C+3O=====Fe O+CO。
3 2 3 4 2
(2)实验室用KClO 和MnO 制备O 的化学方程式为2KClO=====2KCl+3O↑,MnO
3 2 2 3 2 2
中Mn的化合价为+4。
(3)KMnO 有强氧化性,装置B的作用是除尽SO ,装置B中的现象是紫色溶液逐渐变浅。
4 2
(4)装置C的作用是吸收水蒸气。若无装置C,则测定结果偏大(填“偏大”、“无影响”
或“偏小”)。
(5)装置D的作用是吸收产生的二氧化碳,装置E的作用是吸收空气中的二氧化碳和水
蒸气。
(6)钢样中加入某物质可降低煅烧温度。为不影响测定结果,该物质在组成上需满足的条
件是不含碳元素。
四、计算题(9分)
23.(2017·重庆)波尔多液是一种运用广泛的农药,由熟石灰和硫酸铜配制而成。某工厂
用以下反应:2Cu+O+2HSO ===2CuSO+2HO来生产硫酸铜,若要制得80 kg硫酸铜。试
2 2 4 4 2
计算:
(1)硫酸铜中S(填符号)元素的质量分数最小。
(2)若恰好消耗稀硫酸的质量是400 kg,则该稀硫酸溶质的质量分数是多少?
(3)上述过程中,所得硫酸铜溶液中溶质的质量分数是多少?(计算结果精确到0.1%)
解:设反应消耗的硫酸的质量为x,铜的质量为y,氧气的质量为z。
2Cu+O+2HSO ===2CuSO+2HO
2 2 4 4 2
128 32 196 320
y z x 80 kg
===
x=49 kg y=32 kg z=8 kg
稀硫酸中溶质的质量分数为×100%=12.25%
硫酸铜溶液中溶质的质量分数为×100%≈18.2%
答:(2)若恰好消耗稀硫酸的质量是400 kg,则该稀硫酸溶质的质量分数是12.25%。
(3)上述过程中,所得硫酸铜溶液中溶质的质量分数是18.2%。