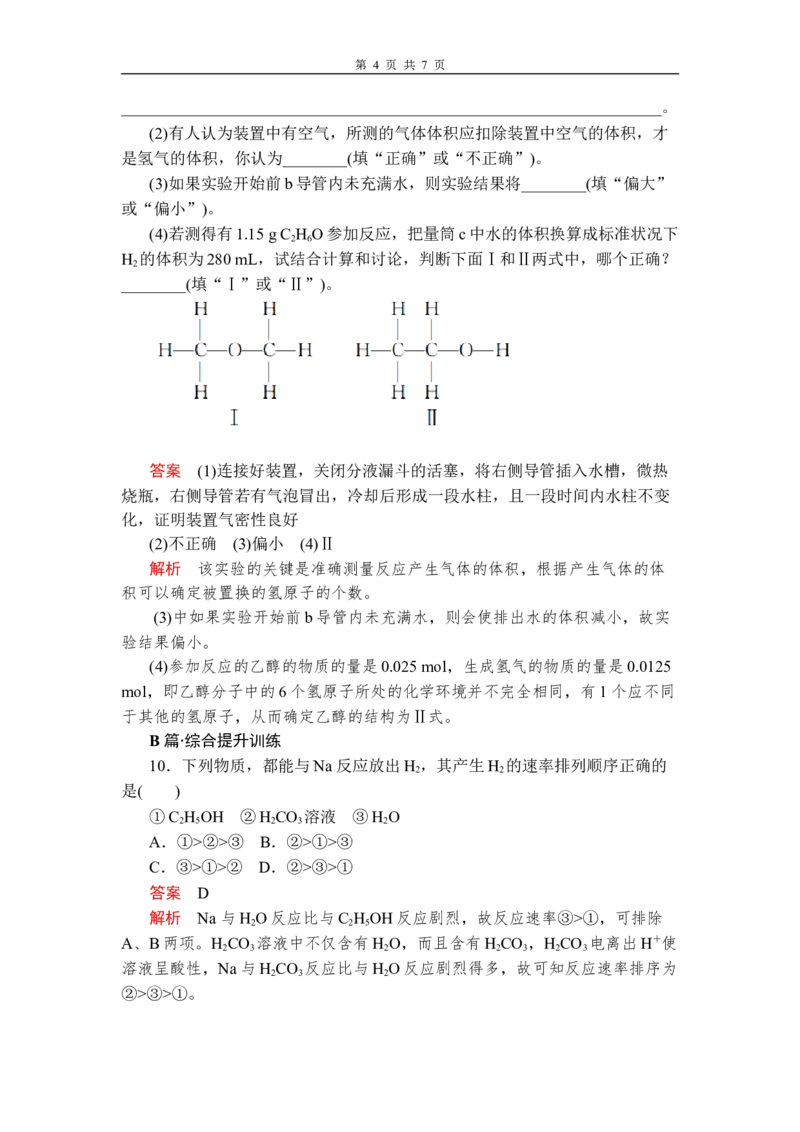文档内容
第 1 页 共 7 页
有机化合物第3节第1课时练习含解析
第七章 第三节 第一课时 乙醇
A篇·知识对点训练
知识点1 乙醇的物理性质及分子结构
1.下列物质中含有两种官能团的烃的衍生物为( )
答案 B
解析 A项官能团为—NO ;B中官能团为 和—Br;C项官能团
2
为—Cl,D项官能团为—Br。
2.下列有关乙醇的表达正确的是( )
答案 D
解析 甲基的结构简式为—CH ,含有1个单电子,其电子式为 ,
3
A错误;乙醇的分子式为C H O,结构简式为CH CH OH,B错误;羟基的结
2 6 3 2
构简式为—OH,其电子式为 是OH-的电子式,C错误。
知识点2 乙醇的化学性质
3.决定乙醇主要化学性质的原子或原子团是( )
A.羟基 B.乙基(—CH CH )
2 3
C.氢氧根离子 D.氢离子
答案 A
解析 羟基是乙醇的官能团,决定其主要化学性质。第 2 页 共 7 页
4.下列说法正确的是( )
A.无水乙醇可用于杀菌消毒
B.乙醇属于烃的衍生物
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L H
2
D.乙醇可使紫色的石蕊溶液变红
答案 B
解析 体积分数为75%的乙醇溶液可用来杀菌消毒,A错误;C中1 mol乙
醇与足量的Na反应生成0.5 mol H ,标准状况下的体积为11.2 L,C错误;乙
2
醇不具有酸性,D错误。
5.下列有关乙醇的说法正确的是( )
A.用酒精作燃料不会产生温室气体
B.通常状况下,不能与金属钠反应
C.在加热和有铜存在下,可与氧气反应生成乙醛
D.在水溶液中能够电离产生H+,呈现弱酸性
答案 C
解析 A项,乙醇中含有碳元素,燃烧会产生CO ,错误;B项,乙醇中含
2
有羟基,能与金属钠反应放出氢气,错误;C项,在加热和有铜或银存在下,
可与氧气反应生成乙醛,正确;D项,乙醇属于非电解质,在水溶液中不能电
离产生H+,错误。
6.下列方法中可以证明乙醇分子中羟基上的氢原子与其他氢原子不同的是
( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇跟足量的Na作用得0.5 mol H
2
D.1 mol乙醇可生成1 mol乙醛
答案 C
解析 乙醇分子中共有6个氢原子,其中羟基上的氢原子比较特殊,A项中
所有的氢原子参与反应,B项无法证明,D项中有C—H键参与了反应,只有C
项表明羟基上的氢原子与另外5个氢原子不同。
7.酒驾是引发交通事故的重要原因,醉驾要入刑。交警对驾驶员进行呼气
酒精检测的原理是橙色的酸性K Cr O 水溶液遇乙醇迅速生成蓝绿色Cr3+。下
2 2 7
列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性
④乙醇是烃的含氧衍生物
A.②④ B.②③ C.①③ D.①④
答案 C
解析 酒精用于对驾驶员酒驾的检测,是因为酒精沸点较低,易挥发,且第 3 页 共 7 页
具有还原性,酒精蒸气可使橙色的酸性K Cr O 溶液变为蓝绿色。
2 2 7
8.乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请回答
关于乙醇的若干问题。
(1)用物理、化学方法各一种鉴别乙醇和汽油。
若用物理方法,应选择的试剂为________;
若用化学方法,应选择的试剂为________。
(2)用乙醇为主要原料(无机试剂任选),根据要求,分别写出相应的化学方
程式(注明反应条件)。
①氧化反应__________________________________________;
②置换反应__________________________________________。
答案 (1)蒸馏水 金属钠
(2)①2CH CH OH+O ――→2H O+2CH CHO
3 2 2 2 3
②2CH CH OH+2Na―→2CH CH ONa+H ↑
3 2 3 2 2
解析 (1)物理方法鉴别乙醇和汽油,可利用它们在水中的溶解情况不同,
而化学方法鉴别,利用乙醇与Na反应而汽油与钠不反应。
(2)乙醇的催化氧化反应生成乙醛,化学方程式为
2CH CH OH+O ――→2H O+2CH CHO。乙醇的置换反应是指乙醇与Na
3 2 2 2 3
反应生成H ,反应的化学方程式为2CH CH OH+2Na―→2CH CH ONa+
2 3 2 3 2
H ↑。
2
9.为了测定乙醇的结构式是 还是
,利用乙醇和钠的反应,设计如图装置进行实验,在烧
瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水
的体积,就可知反应生成氢气的体积。
(1)实验前检验该装置的气密性的实验操作是__________________________第 4 页 共 7 页
___________________________________________________________________。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才
是氢气的体积,你认为________(填“正确”或“不正确”)。
(3)如果实验开始前b导管内未充满水,则实验结果将________(填“偏大”
或“偏小”)。
(4)若测得有1.15 g C H O参加反应,把量筒c中水的体积换算成标准状况下
2 6
H 的体积为280 mL,试结合计算和讨论,判断下面Ⅰ和Ⅱ两式中,哪个正确?
2
________(填“Ⅰ”或“Ⅱ”)。
答案 (1)连接好装置,关闭分液漏斗的活塞,将右侧导管插入水槽,微热
烧瓶,右侧导管若有气泡冒出,冷却后形成一段水柱,且一段时间内水柱不变
化,证明装置气密性良好
(2)不正确 (3)偏小 (4)Ⅱ
解析 该实验的关键是准确测量反应产生气体的体积,根据产生气体的体
积可以确定被置换的氢原子的个数。
(3)中如果实验开始前b导管内未充满水,则会使排出水的体积减小,故实
验结果偏小。
(4)参加反应的乙醇的物质的量是0.025 mol,生成氢气的物质的量是0.0125
mol,即乙醇分子中的6个氢原子所处的化学环境并不完全相同,有1个应不同
于其他的氢原子,从而确定乙醇的结构为Ⅱ式。
B篇·综合提升训练
10.下列物质,都能与Na反应放出H ,其产生H 的速率排列顺序正确的
2 2
是( )
①C H OH ②H CO 溶液 ③H O
2 5 2 3 2
A.①>②>③ B.②>①>③
C.③>①>② D.②>③>①
答案 D
解析 Na与H O反应比与C H OH反应剧烈,故反应速率③>①,可排除
2 2 5
A、B两项。H CO 溶液中不仅含有H O,而且含有H CO ,H CO 电离出H+使
2 3 2 2 3 2 3
溶液呈酸性,Na与H CO 反应比与H O反应剧烈得多,故可知反应速率排序为
2 3 2
②>③>①。第 5 页 共 7 页
11.某有机物的结构简式为 ,下列关于该有
机物的叙述不正确的是( )
A.能与金属钠发生反应并放出氢气
B.能在催化剂的作用下与H 发生加成反应
2
C.不能使酸性KMnO 溶液褪色
4
D.在铜作催化剂的条件下能发生催化氧化反应生成醛
答案 C
12.下列关于乙醇的说法中正确的是( )
A.乙醇在水溶液中能电离出少量的H+,所以乙醇是电解质
B.乙醇结构中有—OH,所以乙醇显碱性
C.乙醇分子中只有—C H 上的氢原子可被钠置换出来
2 5
D.乙醇是一种很好的溶剂,能溶解许多无机化合物和有机化合物,人们
用白酒浸泡中药制成药酒就是利用了这一性质
答案 D
解析 A项,乙醇属于非电解质,错误;B项,羟基(—OH)不是氢氧根离
子(OH-),乙醇不显碱性,错误;C项,金属钠与乙醇的反应中,是Na置换羟
基中的氢,错误。
13.向盛有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正
确的是( )
①钠块沉入乙醇液面的下面
②钠块熔化成小球
③钠块在乙醇的液面上游动
④钠块表面有气体放出第 6 页 共 7 页
A.①② B.②③ C.③④ D.①④
答案 D
解析 钠的密度比乙醇的密度大,故钠块会沉入乙醇液面以下,①正确,
③不正确;乙醇与钠反应比较平缓,放出的热量不足以使钠熔化,②不正确;
钠与乙醇反应有氢气放出,④正确。
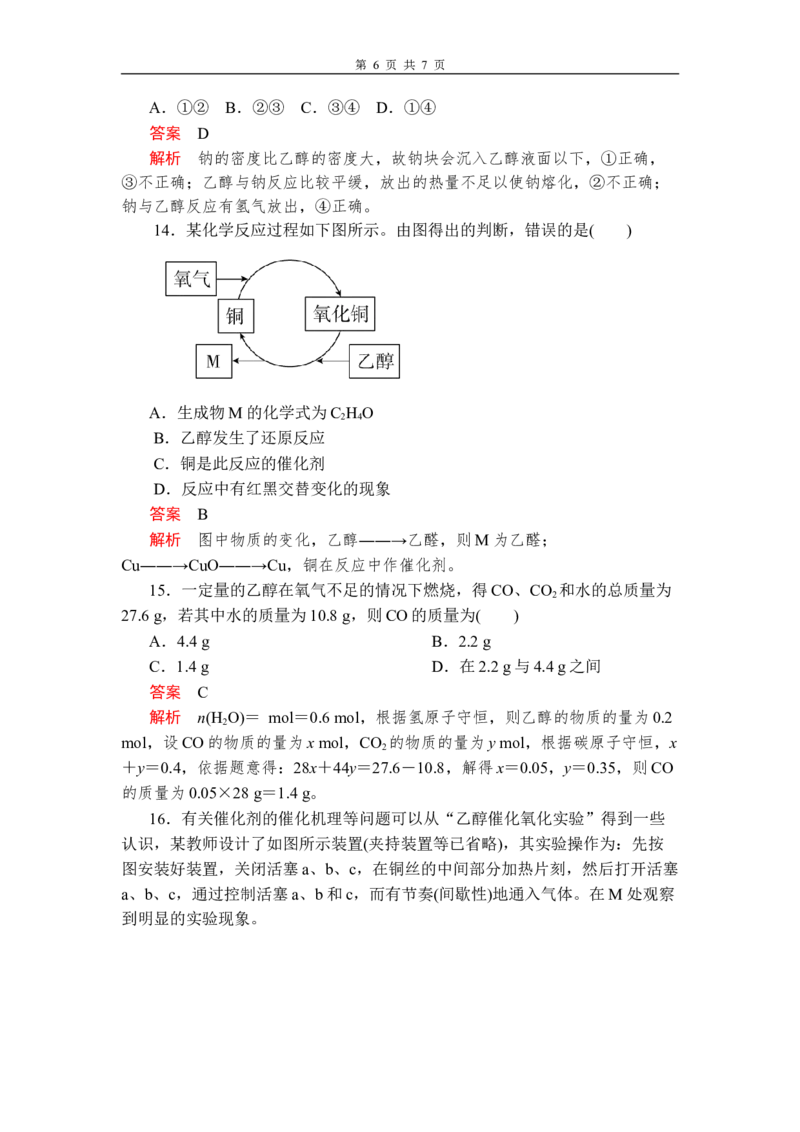
14.某化学反应过程如下图所示。由图得出的判断,错误的是( )
A.生成物M的化学式为C H O
2 4
B.乙醇发生了还原反应
C.铜是此反应的催化剂
D.反应中有红黑交替变化的现象
答案 B
解析 图中物质的变化,乙醇――→乙醛,则M为乙醛;
Cu――→CuO――→Cu,铜在反应中作催化剂。
15.一定量的乙醇在氧气不足的情况下燃烧,得CO、CO 和水的总质量为
2
27.6 g,若其中水的质量为10.8 g,则CO的质量为( )
A.4.4 g B.2.2 g
C.1.4 g D.在2.2 g与4.4 g之间
答案 C
解析 n(H O)= mol=0.6 mol,根据氢原子守恒,则乙醇的物质的量为0.2
2
mol,设CO的物质的量为x mol,CO 的物质的量为y mol,根据碳原子守恒,x
2
+y=0.4,依据题意得:28x+44y=27.6-10.8,解得x=0.05,y=0.35,则CO
的质量为0.05×28 g=1.4 g。
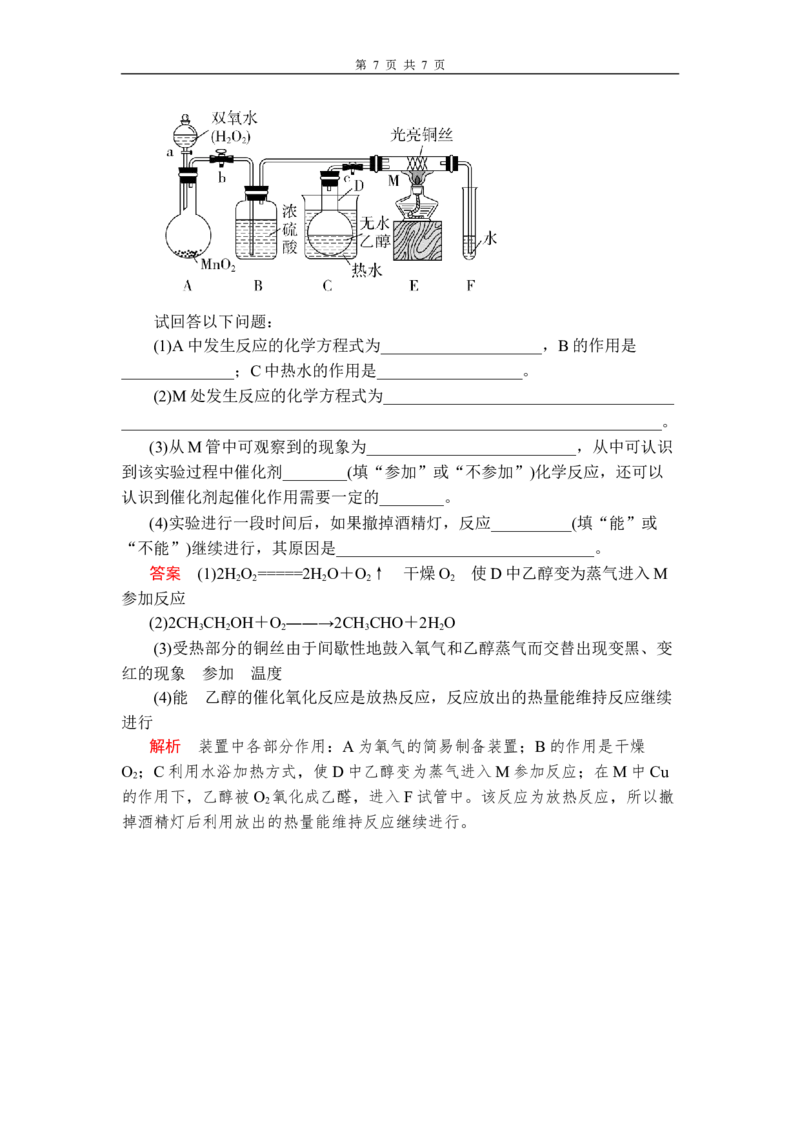
16.有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些
认识,某教师设计了如图所示装置(夹持装置等已省略),其实验操作为:先按
图安装好装置,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞
a、b、c,通过控制活塞a、b和c,而有节奏(间歇性)地通入气体。在M处观察
到明显的实验现象。第 7 页 共 7 页
试回答以下问题:
(1)A中发生反应的化学方程式为____________________,B的作用是
______________;C中热水的作用是__________________。
(2)M处发生反应的化学方程式为____________________________________
___________________________________________________________________。
(3)从M管中可观察到的现象为__________________________,从中可认识
到该实验过程中催化剂________(填“参加”或“不参加”)化学反应,还可以
认识到催化剂起催化作用需要一定的________。
(4)实验进行一段时间后,如果撤掉酒精灯,反应__________(填“能”或
“不能”)继续进行,其原因是________________________________。
答案 (1)2H O =====2H O+O ↑ 干燥O 使D中乙醇变为蒸气进入M
2 2 2 2 2
参加反应
(2)2CH CH OH+O ――→2CH CHO+2H O
3 2 2 3 2
(3)受热部分的铜丝由于间歇性地鼓入氧气和乙醇蒸气而交替出现变黑、变
红的现象 参加 温度
(4)能 乙醇的催化氧化反应是放热反应,反应放出的热量能维持反应继续
进行
解析 装置中各部分作用:A为氧气的简易制备装置;B的作用是干燥
O ;C利用水浴加热方式,使D中乙醇变为蒸气进入M参加反应;在M中Cu
2
的作用下,乙醇被O 氧化成乙醛,进入F试管中。该反应为放热反应,所以撤
2
掉酒精灯后利用放出的热量能维持反应继续进行。