文档内容
第十单元 酸和碱
课题1 常见的酸和碱
【培优训练题】
1.(河北初赛)下列物质长期暴露在空气中质量增加且变质的是( )
(1)浓硫酸 (2)浓盐酸 (3)粗盐 (4)生石灰 (5)氢氢化钠 (6)酒精
A.(1)(2)(3) B.(4)(5) C.(1)(2)(5) D.全部
2.( 多选)(湖北初赛)如下图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充
分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B可能是( )
A.氢氧化钠溶液和二氧化碳
B.硫酸和氮气
C.酒精和氧气
D.水和氯化氢
3. (全国复赛)工业品盐酸中因含有Fe3+而略带黄色,若某工业品盐酸中的H+和Cl-的个数
比为91﹕94,则该盐酸中Fe3+和Cl-的个数比为( )
A.1﹕1 B.1﹕3 C.91﹕94 D.1﹕94
4. (多选)(陕西初赛)如图所示,烧瓶内盛有X气体,若挤压滴管的胶头a ,
使液体Y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管插入滴有Z
的水,打开弹簧夹b,可见液体如喷泉一样喷入烧瓶,并出现颜色改变,
则X、Y、Z可能是( )
A.X是O,Y是硫酸溶液,Z是石蕊溶液
2
B.X是CO,Y是氢氧化钠溶液,Z是酚酞溶液
2
C.X是CO,Y是氢氧化钙溶液,Z是酚酞溶液
D.X是HCl ,Y是硝酸银溶液,Z是石蕊溶液
5.( 全国复赛)金属镁可与热水反应生成氢氧化镁,所得溶液呈碱性,可使酚酞溶液显红色。
某同学将镁条放在水中煮沸,趁热取出部分溶液,滴加酚酞溶液,变为红色,放置在空气
中一段时间后,发现溶液的红色褪去了。
(1)溶液的红色褪去说明溶液的碱性 。
(2)据你推测,导致溶液碱性变化的原因是 。
(3)设计一个实验来验证你的一种推测,简要说明操作、现象及结论。
。
【情景创新题】
6.资料一:通常食醋中含有3%~5%的醋酸。醋酸的化学式为CHCOOH,在常温下是一种无
3
色液体,易溶于水,醋酸具有酸的性质。
资料二:钙是人体的一种常量元素。动物骨头中含有磷酸钙,但磷酸钙难溶于水,却能跟
酸反应生成可溶性的钙盐。
阅读上述资料并回答问题:
(1)写出醋酸的两点物理性质 。
(2)不能用铝制品来盛放食醋的原因是
。
(3)熬骨头汤时,常常会加入少量食醋,这样做的理由是。
参考答案
1.B 【解析】生石灰能与空气中的水反应生成氢氧化钙;氢氧化钠能与空气中的CO 反应生
2
成碳酸钠。
2.AD 【解析】若使试管①中的水沸腾,必须保证②中气体压强减小;压强减小,液体沸点降
低,因此应保证试管②中的液体A和气体B反应或气体溶于液体A中。
3.D 【解析】溶液呈中性,是因为溶液中阳离子所带正电荷总数与阴离子所带负电荷总数相
等。91个H+带91个正电荷,94个Cl-带94个单位负电荷,还差3个单位正电荷,因1个
Fe3+带3个单位正电荷,所以该盐酸中Fe3+个数为1个,故该盐酸中Fe3+和Cl-的个数比为
1﹕94。
4.BD【 解析】气体X和液体Y反应使烧瓶内压强减小,且所得溶液呈酸性或碱性,从而使Z
(滴加酸碱指示剂)出现了颜色改变。
5. (1)减弱
(2)①溶液吸收了空气中的CO ②氢氧化镁的溶解度随温度的降低而变小
2
(3)做对比实验,让上述红色溶液分别在与空气接触和隔绝空气的条件下冷却,若前者褪
色,后者不褪色,则证明空气中的CO 使溶液碱性减弱,导致红色褪去
2
6.( 1)无色、液体 (2)醋酸会与铝发生反应,腐蚀铝制品 (3)磷酸钙与醋酸反应生成可
溶性钙盐,有利于吸收课题2 酸和碱的中和反应
【培优训练题】
1.(广东初赛) 下表为家庭中一些常见物质的pH。
物质 食醋 牙膏 食盐水 肥皂水 火碱液
pH 3 9 7 10 13
有些昆虫如蜜蜂、蚂蚁等叮咬人时,会向人体注入一种叫蚁酸(具有酸的性质)的物
质,使皮肤发红、瘙痒,甚至疼痛,要消除这种症状,可在叮咬处涂上下列物质中的(
)
A.牙膏或肥皂水 B.食盐水
C.火碱液 D.食醋
2.(全国复赛) 2008年诺贝尔化学奖授予钱永健等发明的绿色荧光蛋白标记技术,这项发
明为细胞生物学和神经生物学的发展带来一场革命,对我们理解绿色荧光蛋白如何发
光作出了贡献。绿色荧光蛋白分子中含有氨基(-NH ,具有碱的性质)和羧基(-
2
COOH,具有酸的性质)。该分子具有的性质是( )
A.只能与硫酸反应,不能与氢氧化钾反应
B.只能与氢氧化钾反应,不能与硫酸反应
C.既能与硫酸反应,又能与氢氧化钾反应
D.既不能与硫酸反应,又不能与氢氧化钾反应
3.(全国复赛)用石灰浆涂抹墙壁,一段时间以后,涂层表面物质的pH小于其内层物质的pH。下
列化学方程式可以解释这一现象的是( )
A.Ca(OH) +CO=== CaCO↓+H O
2 2 3 2
B.CaO+H O === Ca(OH)
2 2
C.CaCO =====CaO +CO↑
3 2
D.2HCl+Ca(OH) === CaCl+2H O
2 2 2
【情景创新题】
4.(原创题) 新华网沈阳2013年3月3日电,3月1日15时许,位于朝阳市建平县义成功乡
房申村一硫酸储存罐突然发生破裂,导致约2000立方米硫酸泄漏。造成7人死亡。事故
发生后有关部门调来100袋氢氧化钠对泄漏浓硫酸进行中和。十多名消防队员随后用水枪喷射稀释液体,稀释过程中冒出大量白雾。请根据材料回答下列问题:
(1)消防队员对泄漏的浓硫酸采取了“先中和,后用水稀释”的处理方法。下列是对此
方法的目的的解释,其中错误的是( )
A.若先用水稀释,则易造成酸液面积进一步蔓延,加重处理的难度
B.若先用水稀释,则易造成现场酸液飞溅
C.为了节省氢氧化钠
[来源:学_科_网]
D.为了降低危险
(2)冒出的“白雾”可能是( )
A.硫酸小液滴 B.水蒸气 C.受热产生的水汽 D.挥发出的硫酸
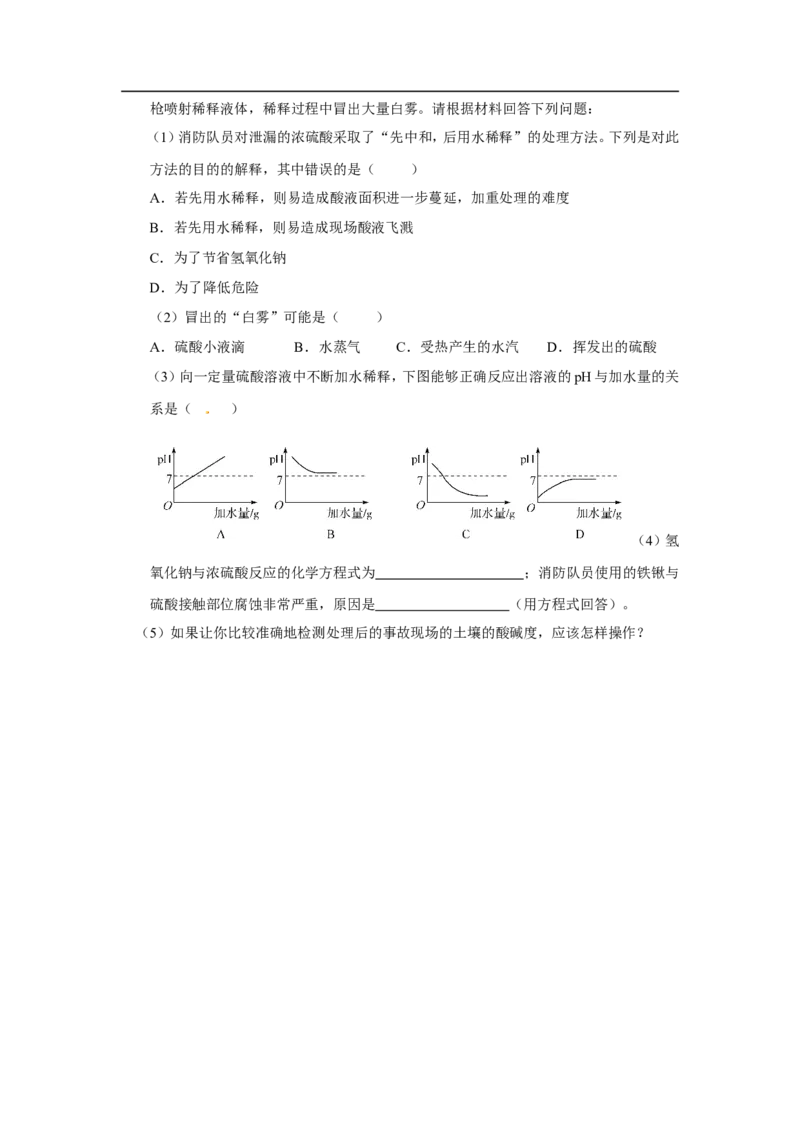
(3)向一定量硫酸溶液中不断加水稀释,下图能够正确反应出溶液的pH与加水量的关
系是( )
[来源:学&科&网Z&X&X&K]
[来源:学。科。 网Z。X。X。K]
(4)氢
氧化钠与浓硫酸反应的化学方程式为 ;消防队员使用的铁锹与
硫酸接触部位腐蚀非常严重,原因是 (用方程式回答)。
(5)如果让你比较准确地检测处理后的事故现场的土壤的酸碱度,应该怎样操作?参考答案
1.A 【解析】因蚁酸(具有酸的性质)呈酸性,利用酸碱中和反应原理,应该在叮咬处涂抹
弱碱性物质,如牙膏、肥皂水等,氢氧化钠具有强腐蚀性,对皮肤有腐蚀作用,因此
不能涂抹氢氧化钠。
2.C 【解析】由“绿色荧光蛋白分子中含有氨基(-NH ,具有碱的性质)和羧基(-COOH,具
2
有酸的性质)”推知,绿色荧光蛋白分子既能与酸反应又能与碱反应。
3.A 【解析】石灰浆的主要成分是氢氧化钙,氢氧化钙显碱性,但氢氧化钙露置在空气中能
与二氧化碳反应,生成碳酸钙和水,导致碱性减弱,pH变小。
4.(1)C (2)C (3)D
(4)HSO +2NaOH=== NaSO +2HO Fe+H SO === FeSO +H ↑
2 4 2 4 2 2 4 4 2
(5)从事故现场不同地点分别取土壤样品,分别加少量蒸馏水,配制土壤溶液备用;将pH
试纸放在玻璃片上,用玻璃棒分别蘸取土壤溶液滴到pH试纸上,再与标准比色卡对照,
分别记录不同地点的土壤的pH。
[来源:Z&xx&k.Com]第十单元 酸和碱综合训练
【培优训练题】
1.(广东初赛) 二氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H SO )。硫化氢
2 3
(H S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫
2
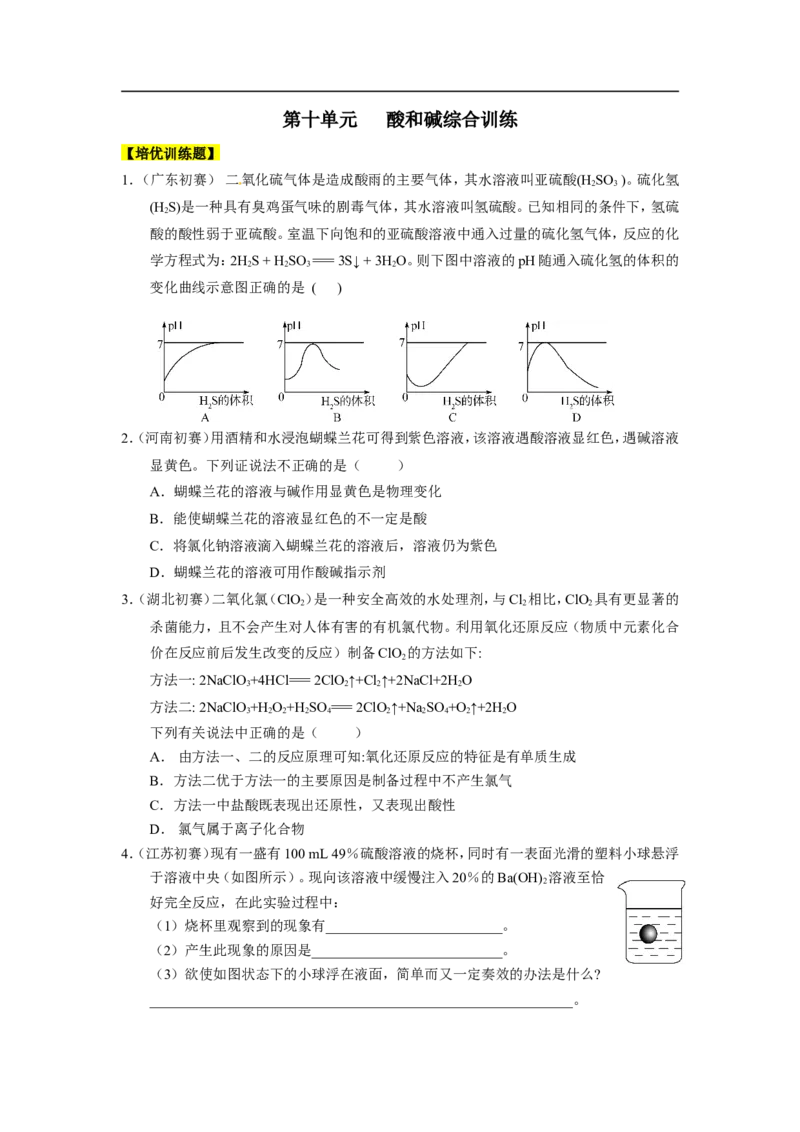
酸的酸性弱于亚硫酸。室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化
学方程式为:2HS + H SO === 3S↓ + 3H O。则下图中溶液的pH随通入硫化氢的体积的
2 2 3 2
变化曲线示意图正确的是 ( )
2.(河南初赛)用酒精和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显红色,遇碱溶液
显黄色。下列证说法不正确的是( )
A.蝴蝶兰花的溶液与碱作用显黄色是物理变化
B.能使蝴蝶兰花的溶液显红色的不一定是酸
C.将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D.蝴蝶兰花的溶液可用作酸碱指示剂
3.(湖北初赛)二氧化氯(ClO )是一种安全高效的水处理剂,与Cl 相比,ClO 具有更显著的
2 2 2
杀菌能力,且不会产生对人体有害的有机氯代物。利用氧化还原反应(物质中元素化合
价在反应前后发生改变的反应)制备ClO 的方法如下:
2
方法一: 2NaClO+4HCl=== 2ClO ↑+Cl↑+2NaCl+2HO
3 2 2 2
方法二: 2NaClO+H O+H SO === 2ClO ↑+Na SO +O ↑+2H O
3 2 2 2 4 2 2 4 2 2
下列有关说法中正确的是( )
A.由方法一、二的反应原理可知:氧化还原反应的特征是有单质生成
B.方法二优于方法一的主要原因是制备过程中不产生氯气
C.方法一中盐酸既表现出还原性,又表现出酸性
D.氯气属于离子化合物
4.(江苏初赛)现有一盛有100 mL 49%硫酸溶液的烧杯,同时有一表面光滑的塑料小球悬浮
于溶液中央(如图所示)。现向该溶液中缓慢注入20%的Ba(OH) 溶液至恰
2
好完全反应,在此实验过程中:
(1)烧杯里观察到的现象有_________________________。
(2)产生此现象的原因是___________________________。
(3)欲使如图状态下的小球浮在液面,简单而又一定奏效的办法是什么?
____________________________________________________________。【情景创新题】
5.( 原创题)近年来酸、碱泄漏事件频繁发生, 6月9日凌晨,位于杭州下沙14号大街的娃哈
哈乐维基地发生事故,一制冷机房内储量为30吨的液氨发生泄漏。接到报警后,下沙消
防中队赶到现场救援,根据现场情况,迅速疏散人员,深入泄漏现场,用喷雾水枪对泄漏
的氨气进行稀释。救援人员逐一关闭了所有的阀门,制止了本次泄漏。事后,公司技术人
员介绍:氨气是一种无色气体,有刺激性恶臭味,当它的蒸气与空气混合到一定比值时,
就会引起燃烧和爆炸,人和动物在短期内吸入大量氨气后会出现流泪、咳嗽、吐血、呼吸
困难等症状,严重者可引发肺水肿,如果吸入极高浓度能致人迅速死亡。此次泄漏可能
是因为设备陈旧而导致的,目前事件正在进一步调查中。
请回答下列问题:
(1)在发生氨气泄漏时,首先要切断泄漏源,由于 ,应迅速撤离泄漏污染区
的人员至上风,并立即隔离150米,还要切断火源。
(2)氨气是一种无色、有刺激性气味的气体,主要用作制冷剂,制取铵盐、硝酸和氮肥,
氨气易溶于水形成氨水,当温度升高时氨气又会逸出。
①下列产品能够体现氨气用途的是( )
A.NH Cl B.KNO C.CuSO D.HNO
4 3 4 3
②你认为保存氨水的方法是 。(写出一种即可)
(3)探究氨气的某些性质,进行以下实验。下图中从左到右依次是实验步骤及相应的现
象。
请根据上图中所示的信息,归纳出有关氨气的性质:
①物理性质: 。(写出一点即可)
②化学性质:氨气与水反应后所得氨水显_______。参考答案
1.B 【解析】向亚硫酸溶液中通入过量的硫化氢气体,溶液的酸性减弱,pH增大,当两者恰
好反应时,液体呈中性,pH=7,继续通入硫化氢气体,溶液由中性逐渐变为酸性,但其酸
性小于亚硫酸的酸性,故其pH应该大于亚硫酸的pH。
[来源:学.科.网Z.X.X.K]
2.A 【解析】酸碱指示剂遇到酸、碱溶液变色属于化学变化。
3.BC
4.(1)有白色沉淀生成,小球下沉 (2)反应产生沉淀,溶液密度变小
(3)加入浓度大于49%的硫酸
【解析】HSO 与Ba(OH) 恰好反应生成白色沉淀BaSO 和水,导致溶液密度减小,小球
2 4 2 4
所受浮力减小,小球下沉;欲使小球小球浮在液面,需要加入浓度比49%大的硫酸溶液。
5.(1)分子在不断运动 (2)①AD ②密封保存(或放在阴凉处) (3)①密度比空
气小(或易溶于水) ②碱性
【解析】分析题给材料归纳氨气的用途主要有:用作制冷剂,制取铵盐、硝酸和氮肥等;又
因“氨气易溶于水形成氨水,当温度升高时氨气又会逸出”推知应密封、低温保存氨气;
由于分子是不断运动的,因此应逆风撤离;问题(3)根据图A用向下排空气法收集氨气,
可知氨气的密度比空气的小;由图C和图D可以看出大气压将水槽中的液体压进试管
内,说明试管内的氨气溶于水,使试管内压强减小;再根据酚酞溶液变红,说明氨气和水
反应生成的氨水显碱性。