文档内容
第八章 化学与可持续发展
单元测试卷
(考试时间:90分钟 试卷满分:100分)
第Ⅰ卷(选择题 44 分)
一、选择题:本题包括22小题,每小题只有以个选项符合题意,每小题2分,共44分。
1.金属冶炼通常有热分解法、热还原法和电解法。金属汞和铜,冶炼的方法分别为( )
A.热分解法、电解法 B.热分解法、热还原法
C.电解法、热分解法 D.电解法、热还原法
【答案】B
【解析】金属冶炼方法的选择与金属的活动性顺序有关,非常活泼的金属选择电解法制备,大部分的金属
利用热还原法制备,不活泼金属用热分解法制备,极少数的金属利用物理方法获得。A项,不活泼金属汞
可用热分解法制备,但是电解法是用于制备非常活泼的金属的,而铜需要用热还原法冶炼,错误;B项,
不活泼金属汞可用热分解法制备,铜用热还原法冶炼,正确;C项,电解法用于制备非常活泼的金属,如
Na、Mg、Al;热分解法用于冶炼不活泼金属,如Hg、Ag,错误;D项,电解法不用于冶炼金属汞,铜可
用热还原法冶炼,错误。
2.下列食品添加剂的功能类别对应错误的是( )
A.抗坏血酸——抗氧化剂 B.亚硝酸钠——调味剂
C.碘酸钾——营养强化剂 D.柠檬黄——着色剂
【答案】B
【解析】A项,抗坏血酸(维生素C)具有还原性,可用做抗氧化剂,正确;B项,亚硝酸钠有毒,适量亚硝
酸钠可做食品防腐剂,长期食用会对身体有害,为防腐剂,不是调味剂,错误;C项,碘元素为人体需要
的营养元素,所以碘酸钾为营养强化剂,正确;D项,柠檬黄是着色剂,正确。
3.食品抗氧化剂是能阻止或延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。下列物质
不属于食品抗氧化剂的是( )
A.水果罐头中的维生素C B.葡萄酒中的少量二氧化硫
C.面包中的食用碳酸氢铵 D.植物油中的丁基羟基茴香醚
【答案】C
【解析】A项,水果罐头中的维生素C具有还原性,属于食品抗氧化剂,不符合题意;B项,葡萄酒中的
少量二氧化硫具有还原性,属于食品抗氧化剂,不符合题意;C项,面包中的食用碳酸氢铵,是膨松剂,不属于食品抗氧化剂,符合题意;D项,植物油中的丁基羟基茴香醚具有还原性,属于食品抗氧化剂,不
符合题意。
4.当今环境污染已成为人类面临的重大威胁,下列对应关系不完全正确的是( )
A.酸雨——SO 、NO 、CO 等
2 2 2
B.光化学烟雾——NO 、CH 等
2 x y
C.温室效应——CO、CH 等
2 4
D.白色污染——各种颜色的难降解的塑料膜、塑料袋等
【答案】A
【解析】A项,酸雨是由SO 、NO 的排放引起的,CO 排放过多引起温室效应,错误;B项,光化学烟雾
2 2 2
是由NO 、CH 等引起的,正确;C项,温室效应是由CO、CH 等引起的,正确;D项,各种颜色的难降
2 x y 2 4
解的塑料膜、塑料袋等会造成白色污染,正确。
5.下列有关物质的制备中,说法正确的是( )
A.高温加热氧化镁和碳的混合物可以冶炼镁
的
B.铁 冶炼过程是通过置换反应得到单质铁
C.海水提溴的过程中不发生氧化还原反应
D.利用电渗析的方法可以从海水中获取淡水
【答案】D
【解析】A项,冶炼镁是电解熔融氯化镁制备,错误;B项,3CO+Fe O====3CO+2Fe,不是置换反
2 3 2
应,错误;C项,海水提溴有反应Cl+2KBr=2KCl+Br 发生,是氧化还原反应,错误;D项,利用电
2 2
渗析的方法可以从海水中获得淡水,正确。
6.下列物质与用途对应不正确的是( )
A.苯甲酸钠:食品防腐剂 B.氧化钙:吸氧剂
C.碳酸氢钠:膨松剂 D.阿司匹林:解热镇痛药
【答案】B
【解析】A.苯甲酸钠可防止食品变质,延长保质期,是常用的食品防腐剂,故A正确;B.氧化钙不和
氧气反应,不能作吸氧剂,氧化钙能吸收水,常用作干燥剂,故B错误;C.碳酸氢钠加热分解产生二氧
化碳,常用作膨松剂,故C正确;D.阿司匹林是常用的解热镇痛药,故D正确;故答案选B。
7.随着人民生活水平的不断提高,人们更加讲究合理膳食。下列饮食习惯科学的是( )
A.多吃肉,少吃蔬菜水果 B.多喝碳酸饮料,少饮矿泉水
C.多食用含防腐剂的食品 D.注意饮食的合理搭配
【答案】D【解析】A.少吃蔬菜,会造成维生素缺乏,A项饮食习惯不科学;B.长期喝碳酸饮料会影响骨质、导致
肥胖、影响口腔健康、胃肠功能紊乱、增加肾脏负担等,矿泉水是地下水天然露出至地表或地下含水层露
出地表,有一定有机物、矿物质,能起到润肠通便、生津止渴的功效,应多喝矿泉水,少喝碳酸饮料,B
项饮食习惯不科学;C.含防腐剂的食物,食用过量会对人体有害,C项饮食习惯不科学;D.注意饮食的
合理搭配,合理膳食,有助于人体健康,D项饮食习惯科学;本题答案选D。
8.下列说法中不正确的是( )
A.生铁的含碳量比钢低
B.不锈钢是最常见的一种合金钢,它的合金元素主要是铬和镍
C.硬铝的密度小、强度高,是制造飞机和宇宙飞船的理想材料
D.储氢合金是一类能够大量吸收 ,并与 结合成金属氢化物的材料
【答案】A
【解析】A. 生铁中的含碳量为2%~4.3%,钢中的含碳量为0.03%~2%,生铁的含碳量比钢高,故A错
误;B. 不锈钢是最常见的一种合金钢,它的合金元素主要是铬和镍,故B正确;C. 硬铝是铝合金,硬
度大,硬铝的密度小、强度高,是制造飞机和宇宙飞船的理想材料,故C正确;D. 储氢合金是一类能够
大量吸收H,并与H 结合成金属氢化物的材料,便于氢的储运,故D正确;故选A。
2 2
9.雾霾严重地威胁着人们生存的生态环境。下列有关措施不可行的是( )
A.对燃煤进行脱硫,减少向大气排放SO
2
B.对含SO 等的工业废气进行无害处理后,再排放到大气中
2
C.为增加工业产值,大力兴建水泥厂、炼钢厂
D.对汽车等交通工具采用清洁燃料,如天然气、甲醇等
【答案】C
【解析】A.二氧化硫可导致酸雨的发生,则对燃煤进行脱硫,减少向大气排放SO ,有利于保护生态环
2
境,A项可行;B.SO 等工业废气污染环境,均可导致酸雨,二氧化氮还可导致光化学烟雾,则需对工业
2
废气进行无害处理后,再排放到大气中,B项可行;C.大力兴建水泥厂、炼钢厂,会排放粉尘、废水及
污染性气体,增加工业产值不能以破坏生态环境为代价,C项不可行;D.天然气、甲醇等的燃烧产物对
环境污染小,则对汽车等交通工具采用清洁燃料可保护环境,D项可行;故选C。
10.自然资源是人类社会发展不可或缺的自然物质基础,下列说法错误的是( )
A.石油的分馏、煤的气化和液化都是物理变化
B.天然气的主要成分甲烷是高效、较洁净的燃料
C.石油分馏得到的石油气常用来制造塑料或作为燃料
D.将铝土矿处理后通过电解的方法冶炼金属铝【答案】A
【解析】A项,石油的分馏是物理变化,煤的气化和液化都是化学变化,错误;B项,天然气的主要成分
为甲烷,属于高效、较洁净的燃料,正确;C项,石油分馏首先得到沸点较低的石油气,常用来制造塑料
或作为燃料,正确;D项,将铝土矿处理后,可通过电解熔融氧化铝的方法冶炼金属铝,正确。
11.现有以下几种措施:①煤燃烧前向煤中加适量生石灰;②少用原煤作燃料;③燃煤时鼓入足量空气;
④开发清洁能源。其中能减少酸雨产生的措施是
A.①②④ B.②③④ C.②③ D.②④
【答案】A
【解析】①煤燃烧前向煤中加适量生石灰,煤燃烧生成的二氧化硫与CaO反应生成CaSO3,能减少二氧化
硫的排放从而减少酸雨产生,①正确;②少用原煤作燃料可减少二氧化硫的排放,可减少酸雨产生,②正
确;③燃煤时鼓足空气,能使煤燃烧更充分但是生成的二氧化硫的量不会减少,不能减少酸雨产生,③错
误;④开发清洁能源能减少二氧化硫的排放从而减少酸雨的产生,④正确;根据以上分析①②④正确,故
答案选A。
12.海带中含有碘元素。从海带中提取碘的实验过程如下图所示,下列说法正确的是
A.步骤①主要在蒸发皿中进行
B.步骤④的离子方程式为2I-+H O =I +2OH-
2 2 2
C.步骤⑤中,先从分液漏斗下口放出水,再从下口放出含碘苯溶液
D.步骤⑥的操作为蒸馏
【答案】D
【分析】由流程可知,①为坩埚中灼烧,②为溶解、浸泡,③为过滤,分离出含碘离子的溶液,④中发生
2I-+H O+2H+═I +2H O,⑤中加苯萃取、分液,⑥中蒸馏分离出碘。
2 2 2 2
【解析】A. 步骤①为灼烧,需要坩埚、泥三角、三脚架、酒精灯,不需要蒸发皿,故A错误;B. 步
骤④的离子方程式为2I-+H O+2H+═I +2H O,故B错误;C. 碘不易溶于水,易溶于有机溶剂,苯密度小
2 2 2 2
于水溶液,步骤⑤中,先从分液漏斗下口放出水,再从上口放出含碘苯溶液,故C错误;D. 步骤⑥的操
作为蒸馏,分离出碘,回收苯,故D正确;故选D。
13.下列关于煤气、液化石油气和天然气的说法正确的是 ( )
A.煤气主要成分是氢气、甲烷、乙烯和一氧化碳
B.液化石油气是将甲烷压缩后成为液态的燃料
C.北京奥运会“祥云”火炬和家用打火机所用燃料均为丙烷,它是液化石油气的成分之一
D.家用液化石油气与天然气成分相同,但纯度不同【答案】C
【解析】焦炉气的主要成分为氢气、甲烷、乙烯和一氧化碳,而煤气的主要成分则为氢气和一氧化碳,A错;
液化石油气的主要成分为丙烷和丁烷,B、D错误。
14.下列关于农药和肥料的说法正确的是( )
A.草木灰含有KCO,可作为钾肥使用 B.含磷化合物都可以作为磷肥直接使用
2 3
C.氮肥只能通过人工合成而得到 D.农药都对人体无害,可以大量使用农药
【答案】A
【解析】A.草木灰含有KCO,KCO 属于可溶性钾盐,故可作为钾肥使用,故A正确;B.含磷化合物
2 3 2 3
不一定都可以作为磷肥直接使用,故B错误;C.氮肥不一定只能通过人工合成而得到,例如自然固氮
等,故C错误;D.农药都对人体有害,不可以大量使用农药,故D错误;故选:A。
15.化学与生产生活密切相关,下列说法错误的是( )
A.碳酸氢钠加入的量过多会使蒸出的馒头发黄
B.为防止富脂食品氧化变质,常在包装袋中放入生石灰
C.食用维生素C含量较高的食物有利于人体对铁元素的吸收
D.开发风能、氢能和太阳能等清洁能源,有利于从源头上防治酸雨
【答案】B
【解析】A.碳酸氢钠受热分解生成二氧化碳使馒头疏松,蒸馒头使用碳酸氢钠,碳酸氢钠加入的量过多会
使蒸出的馒头发黄,选项A正确;B.包装袋中的生石灰做干燥剂,选项B错误;C.维生素C具有还原
性,有利于人体对铁元素的吸收,选项C正确;D.开发风能、氢能和太阳能等清洁能源,有利于从源头
上防治酸雨,选项D正确;答案选B。
16.化学与生活息息相关。根据你的认知和体验,下列说法或做法正确的是( )
A.绿色食品就是不使用化肥、农药,不含任何化学物质的食品
B.酸雨是pH<5.6的雨水,主要是由大气中的SO 、NO 等造成的
2 x
C.医用酒精使用质量分数为75%酒精溶液
D.为了防止某些富脂食物因被氧化而变质,常在包装袋里放生石灰
【答案】B
【解析】A.绿色食品是指无污染、无公害的食品,A错误;B.酸雨是pH<5.6的雨水,包括硫酸型和硝
酸型酸雨,主要是由大气中的SO2、NOx等造成的,B正确;C.医用酒精使用体积分数为75%酒精溶
液,C错误;
D.为了防止某些富脂食物因被氧化而变质,常在包装袋里放还原铁粉,D错误; 故选B。
17.下列关于化学与职业的说法错误的是( )
A.营养师会根据食品科学、营养学和医学专业知识,结合服务对象的特殊需求进行膳脱食指导B.水质检验员对天然水、工业用水、生活用水等的物理性质、化学性质及生物性质进行检验评定
C.化学科研工作者是指从事与化学有关的基础研究和应用研究的专业技术人员
D.科技考古研究人员利用12C对文物进行年代测定
【答案】D
【解析】A.营养师会根据食品科学、营养学和医学专业知识,结合服务对象的特殊需求进行膳食指导,
保持营养均衡,故A正确;B.水质检验员是指对天然水、工业用水、生活用水等的物理性质、化学性质
及生物性质进行检验和评定的专业技术人员,一般检验氯离子、硫酸根离子、微生物、有机物等,故B正
确;C.化学科研工作者是指从事与化学有关的基础研究和应用研究的专业技术人员,故C正确;D.科
技考古研究人员利用14C对文物进行年代测定,故D错误;选D。
18.下列除去杂质的方法正确的是( )
A.除去CO 中混有的少量HCl气体:通过饱和NaHCO 溶液洗气
2 3
B.提纯含有少量硝酸钡杂质的硝酸钾溶液:先加入适量碳酸钠溶液,再过滤
C.除去粗盐水中的氯化镁及泥沙:先加入稍过量的NaOH溶液,再加入盐酸、过滤
D.除去硝酸钾中混有的氯化钠杂质:加水溶解、蒸发结晶、过滤
【答案】A
【解析】A.HCl气体与饱和NaHCO 反应生成二氧化碳、二氧化碳不与饱和NaHCO 反应、且难以溶解,
3 3
则除去CO 中混有的少量HCl气体:通过饱和NaHCO 溶液洗气,A正确;B. 提纯含有少量硝酸钡杂质
2 3
的硝酸钾溶液:先加入适量碳酸钠溶液,再过滤,所得滤液中引入新杂质(钠离子),B错误;C. 除去粗
盐水中的氯化镁及泥沙:先加入稍过量的NaOH溶液得到氢氧化镁沉淀后,过滤、再加入盐酸中和滤液中
多余的NaOH,C错误;D.硝酸钾的溶解度随温度升高而急剧增大,从溶液中提取硝酸钾晶体时,应采用
冷却结晶、氯化钠的溶解度随温度升高变化不大。除去硝酸钾中混有的少量氯化钠杂质:加水溶解、蒸发
浓缩、冷却结晶、过滤,D错误;答案选A。
19.中国传统文化对人类文明贡献巨大,下列对古文献记载内容或诗句谚语理解错误的是( )
A.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指铁的合金
B.“朝坛雾卷,曙岭烟沉”中的雾是一种胶体,能产生丁达尔效应
C.“水滴石穿、绳锯木断”不包含化学变化
D.《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应
【答案】C
【解析】A.铁中含碳量越高,硬度越大,含碳量越少,韧性越强,剂钢是铁与碳的合金,A正确;B.雾
是气溶胶,能产生丁达尔效应,B正确;C.“绳锯木断”,只是物质的形状发生了改变,没有新物质生
成,属于物理变化,“水滴石穿”,是指水滴在石头上,和碳酸钙、二氧化碳反应生成溶于水的碳酸氢
钙,使石头上出现了小孔,有新物质生成,属于化学变化,C错误;D.《天工开物》中“凡石灰,经火
焚炼为用”是指碳酸钙受热分解生成氧化钙和二氧化碳,是由一种物质生成多种物质的反应,反应类型是分解反应,D正确; 故选C。
20.“关爱生命,注意安全,拥抱健康”是人类永恒的主题。下列叙述正确的是
A.汽车尾气中含有一氧化碳、二氧化碳、二氧化硫等空气污染物,会危害人体健康
B.人体内血浆的正常pH范围是0.9~1.5,如果出现异常,则可能导致疾病
C.霉变的大米加热到280℃以上,再食用
D.利用活性炭来吸附装修产生的对人体有害的气体
【答案】D
【解析】A.汽车尾气的排放,主要的有害气体有:一氧化碳、二氧化氮、二氧化硫等,这三种气体都是
计入空气污染指数的项目的气体,会危害人体健康,而二氧化碳不属于空气污染物,选项 A错误;B.人
体内血浆的正常pH范围是7.35-7.45,血浆pH大于7,如果出现异常,则可能导致疾病,选项B错误;
C.霉变的大米含有黄曲霉素,黄曲霉素有毒且化学性质稳定,加热到280℃以上才能破坏它,但绝不能食
用霉变的大米,选项C错误;D.活性炭具有吸附性,用活性炭吸附装修后产生的对人体有害的气体,选
项D正确;答案选D。
21.铝元素是地壳中含量最多的金属元素(约占地壳总量的7.73%),主要以铝土矿形式存在(主要成分是
Al O)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝,主要的工艺流程如图所示:
2 3
下列说法正确的是( )
A.碱溶①后,溶液中主要含有的阳离子为Na+和Al3+
B.步骤②通入足量CO 反应的离子方程式为:2AlO2-+CO+3HO=2Al(OH) ↓+CO2-
2 2 2 3 3
C.Al(OH) 受热分解,生成高熔点物质和水,该高熔点物质常用作高温耐火材料
3
D.灼烧③一般在坩埚中进行,电解④添加冰晶石(Na AlF),目的是增强导电性
3 6
【答案】C
【解析】氧化铝和氢氧化钠溶液反应生成偏铝酸钠溶液,通入二氧化碳气体生成氢氧化铝沉淀,灼烧生成
氧化铝,电解得到铝单质。A项,碱溶①后,氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,溶液中主要
含有的阳离子为Na+,错误;B项,酸化②通足量的CO 应生成氢氧化铝沉淀和碳酸氢根,离子方程式为
2
AlO2-+CO+2HO=Al(OH) ↓+HCO -,错误;C项,Al(OH) 受热分解:2Al(OH) ====Al O+3HO,
2 2 3 3 3 3 2 3 2
生成高熔点的Al O 和水,Al O 常用作高温耐火材料,正确;D项,灼烧③一般在坩埚中进行,电解④添
2 3 2 3
加冰晶石(Na AlF),目的是降低Al O 熔融温度,错误。
3 6 2 3
22.科学家在己二酸现有工业路线基础上,提出了一条“绿色”合成路线(已知:卤代烃在氢氧化钠溶液中
可发生取代反应,卤原子可被羟基取代。):下列说法不正确的是
A.苯经取代、加成、取代三步反应可获得环己醇
B.用蒸馏的方法可将苯与环己醇进行分离
C.环己烷与氧气发生化合反应转化为己二酸
D.与传统工业路线相比,“绿色”合成路线可减少污染物排放
【答案】C
【解析】A项,苯经取代得到溴苯、溴苯催化加氢得到一溴环己烷、一溴环己烷在氢氧化钠水溶液中水解
(取代)可获得环己醇,正确;B项,苯与环己醇互溶且有一定沸点差,用蒸馏的方法可将苯与环己醇进行
分离,正确;C项,环己烷与氧气发生氧化反应转化为己二酸、同时有水生成:2C H +5O催化剂Δ2C H O+
6 12 2——— 6 10 4
2HO,不是化合反应,不正确;D项,传统工业路线中用硝酸氧化环己醇、硝酸的还原产物有可能是氮氧
2
化物、会污染空气,“绿色”合成路线的产物为己二酸、同时有水生成,故“绿色”合成路线可减少污染
物排放,正确。
第 II 卷(非选择题 共 56 分)
二、非选择题:本题共5个小题,共56分。
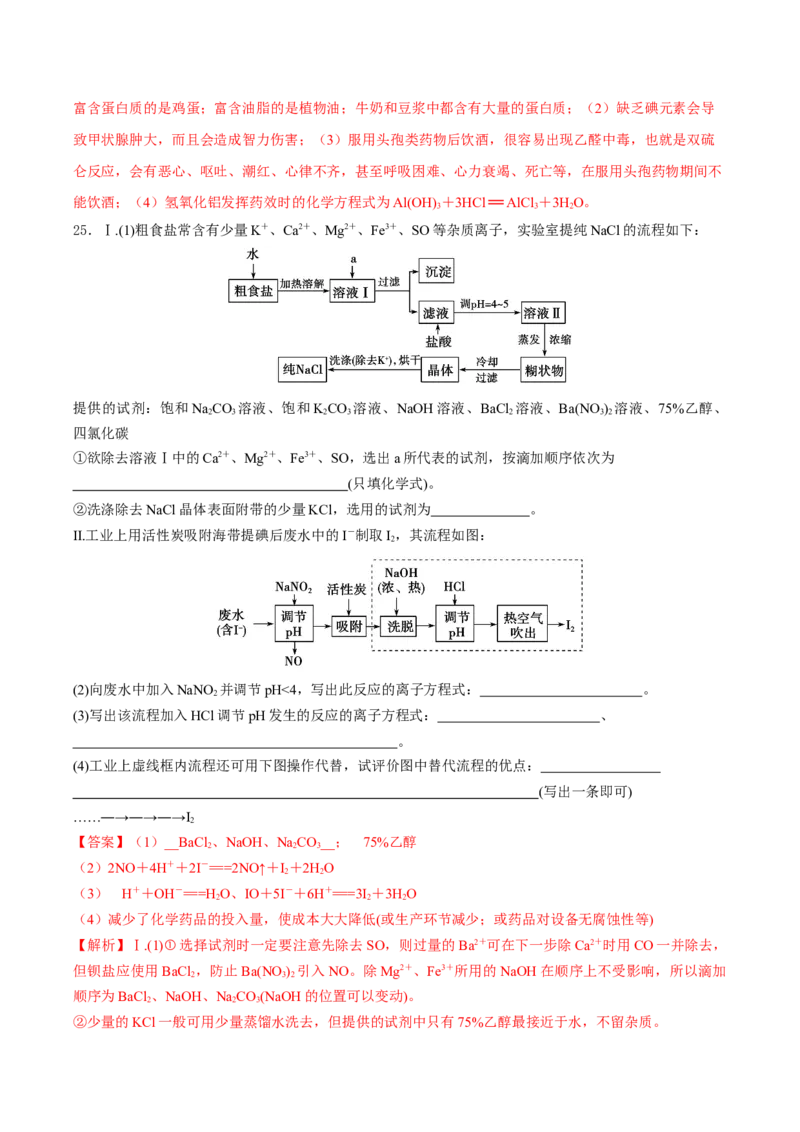
23.铝是一种重要金属,从铝土矿(主要成分为Al O,Fe O、SiO 等)中冶炼Al的工业生产流程如下图
2 3 2 3 2
(SiO 是酸性氧化物,不溶于盐酸):
2
(1)步骤I、II、III都要用到的分离方法是_______,该操作要用到的玻璃仪器有:烧杯、玻璃棒、
_______。
(2)写出向溶液C中通入少量CO 生成Al(OH) 沉淀的离子方程式_______________________________。
2 3
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有CO、________(填化学式)。
2(4)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al O 的纯度(质
2 3
量分数)______________(用含a、b的最简式表示)。
【答案】(1)过滤 漏斗 (2)2AlO2-+CO+3HO=2Al(OH) ↓+CO2- (3)NaOH (4)×100%
2 2 3 3
【解析】由工艺流程可知,铝土矿(主要成分为Al O ,Fe O 、SiO 等)与过量的盐酸反应得沉淀B和溶液
2 3 2 3 2
A,则固体B为SiO ,过滤得滤液A含有氯化铝、氯化铁、盐酸等,滤液中加入过量的NaOH,可推知沉
2
淀D为氢氧化铁,过滤得滤液C含有偏铝酸钠、氯化钠,所以向滤液C中通入二氧化碳,生成氢氧化铝沉
淀与溶液E为碳酸氢钠或碳酸钠溶液,过滤后向E溶液中加入氧化钙得沉淀G为碳酸钙,同时得到氢氧化
钠溶液,氢氧化钠溶液可以循环利用,碳酸钙煅烧分解得氧化钙和二氧化碳都可以循环利用,Al(OH) 灼
3
烧得氧化铝,电解熔融的氧化铝可得铝,据此解答。
(1)由上分析,步骤I、II、III都要用到的分离方法是过滤,该操作要用到的玻璃仪器有:烧杯、玻璃
棒、漏斗;(2)向溶液C中通入少量CO 生成Al(OH) 沉淀,即偏铝酸钠和少量CO 反应生成Al(OH) 沉
2 3 2 3
淀和碳酸钠溶液,离子方程式为2AlO2-+CO+3HO=2Al(OH) ↓+CO2-;(3)据分析,生产过程中,
2 2 3 3
除CaO可以循环使用外,还可以循环使用的物质有CO、NaOH;(4)经分析,a吨铝土矿可以冶炼出b
2
吨的铝(假设各生产环节中无损耗),则根据铝元素守恒可知2Al~Al O,m(AlO)= 吨,即需要纯氧化铝
2 3 2 3
的质量为 吨,所以原铝土矿中Al O 的纯度为×100%=×100%。
2 3
24.回答下列问题:
(1)下表是某食品包装袋上的说明
品名 早餐饼
配料 面粉 鸡蛋 植物油 白砂糖 食盐 苯甲酸钠
保质期 十二个月
生产日期 2022年11月8日
在配料中,富含淀粉的是_______;富含蛋白质的是_______;富含油脂的是_______;牛奶和豆浆中都含
有大量的_________。
(2)缺乏某种微量元素会导致甲状腺肿大,而且会造成智力伤害,该微量元素是_______。
(3)头孢药物是一种常见的抗生素,在服用期间_______(填“能”或“不能”)饮酒。
(4)人体的胃液中含有少量盐酸,秘为胃酸。含有碳酸氢钠、碳酸钙,氧化镁,氢氧化铝和氢氧化镁等
成分的抗酸药可缓解胃酸分泌过多而导致的胃部不适。写出氢氧化铝发挥药效时的化学方程式:
_________________________________________。
【答案】(1)面粉 鸡蛋 植物油 蛋白质 (2)碘 (3)不能 (4)Al(OH) +3HCl=AlCl +
3 3
3HO
2
【解析】(1)面粉的主要成分是淀粉,则在配料中,富含淀粉的是面粉;鸡蛋的主要成分为蛋白质,则富含蛋白质的是鸡蛋;富含油脂的是植物油;牛奶和豆浆中都含有大量的蛋白质;(2)缺乏碘元素会导
致甲状腺肿大,而且会造成智力伤害;(3)服用头孢类药物后饮酒,很容易出现乙醛中毒,也就是双硫
仑反应,会有恶心、呕吐、潮红、心律不齐,甚至呼吸困难、心力衰竭、死亡等,在服用头孢药物期间不
能饮酒;(4)氢氧化铝发挥药效时的化学方程式为Al(OH) +3HCl=AlCl +3HO。
3 3 2
25.Ⅰ.(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和NaCO 溶液、饱和KCO 溶液、NaOH溶液、BaCl 溶液、Ba(NO ) 溶液、75%乙醇、
2 3 2 3 2 3 2
四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO,选出a所代表的试剂,按滴加顺序依次为
(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为 。
Ⅱ.工业上用活性炭吸附海带提碘后废水中的I-制取I,其流程如图:
2
(2)向废水中加入NaNO 并调节pH<4,写出此反应的离子方程式: 。
2
(3)写出该流程加入HCl调节pH发生的反应的离子方程式: 、
。
(4)工业上虚线框内流程还可用下图操作代替,试评价图中替代流程的优点:
(写出一条即可)
……―→―→―→I
2
【答案】(1)__BaCl 、NaOH、NaCO__; 75%乙醇
2 2 3
(2)2NO+4H++2I-===2NO↑+I+2HO
2 2
(3) H++OH-===H O、IO+5I-+6H+===3I +3HO
2 2 2
(4)减少了化学药品的投入量,使成本大大降低(或生产环节减少;或药品对设备无腐蚀性等)
【解析】Ⅰ.(1)①选择试剂时一定要注意先除去SO,则过量的Ba2+可在下一步除Ca2+时用CO一并除去,
但钡盐应使用BaCl ,防止Ba(NO ) 引入NO。除Mg2+、Fe3+所用的NaOH在顺序上不受影响,所以滴加
2 3 2
顺序为BaCl 、NaOH、NaCO(NaOH的位置可以变动)。
2 2 3
②少量的KCl一般可用少量蒸馏水洗去,但提供的试剂中只有75%乙醇最接近于水,不留杂质。Ⅱ.(2)亚硝酸钠具有氧化性,碘离子具有还原性,酸性条件下,二者发生氧化还原反应生成一氧化氮、碘和
水,离子反应方程式为2NO+4H++2I-===2NO↑+I+2HO。
2 2
(3)加入HCl调节pH发生的反应主要是酸和碱反应生成水,碘离子和碘酸根离子在酸性溶液中发生归中反
应生成单质碘,反应的离子方程式为H++OH-===H O、IO+5I-+6H+===3I +3HO。
2 2 2
(4)工业上虚框内流程与图中操作流程比较,需氢氧化钠、盐酸对设备有一定的腐蚀性,化学药品的投入量
大,需热能成本高,而图中操作流程仅需高温,减少了化学药品的投入量,使成本大大降低(或生产环节减
少;或药品对设备无腐蚀性等)。
26.丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料,可以用乙烯、丙烯等石油化工产品为
原料进行合成。模拟石油深加工合成丙烯酸乙酯等化工原料的过程如下:
(1)B的化学名称是_________________________。
(2)丙烯酸分子中含有的含氧官能团名称为__________________。
(3)写出反应②的化学方程式_________________________________________________。
(4)已知石蜡油的分解产物中除含有A、丙烯外,还可能含有C H 等有机物。请写出C H 的同分异构
5 12 5 12
体中一氯代物只有一种的烃的结构简式:__________________________________。
(5)③的反应类型为________________。
(6)聚丙烯酸可用于配制某些高档商品的涂饰剂、制取丙烯酸树脂漆等。写出聚丙烯酸的结构简式:
______________________________。
【答案】(1)乙醇 (2)羧基
(3)CH=CHCOOH+CHCHOH CH=CHCOOCH CH+HO
2 3 2 2 2 3 2
(4)C(CH) (5)加聚反应 (6)
3 4
【解析】石蜡油经加热碎瓷片催化裂解为烯烃。A→B为烯烃与HO的加成反应生成醇。丙烯酸与B为酯
2
化反应。反应③为烯烃的加聚反应。
(1)由反应②与丙烯酸得到丙烯酸乙酯,则B为乙醇,答案为乙醇;(2)丙烯酸中的官能团-COOH含氧,答案为羧基;(3)反应②为酯化反应,酸脱羟基醇脱氢,方程式为:CH=CHCOOH+
2
CHCHOH CH=CHCOOCH CH+HO;(4)C H 一氯代物只有一种即该分子高度对称其他H
3 2 2 2 3 2 5 12
为等效,其结构为C(CH);(5)丙烯酸到聚丙烯酸高分子,应该为>C=C<的加聚反应,答案为加聚反
3 4
应;(6)聚丙烯酸为丙烯酸中>C=C<断裂连接,所以结构简式为 。
27.十九大报告中指出“持续实施大气污染防治行动,打赢蓝天保卫战”。汽车尾气中的CO、NOx以及燃
煤废气中的SO 都是大气污染物,研究它们的性质对环境治理具有重要意义。
2
(1)PM2.5是指大气中直径小于或等于2.5um(1um=103nm)的颗粒物。下列说法不正确的是_______(填字
母)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5um的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)直接排放含SO 的烟气会形成酸雨,危害环境。用化学方程式表示 形成硫酸型酸雨的过程
2
________________________________________________________(只写第一步)。
(3)洗涤含 的烟气,下列物质不能作为洗涤剂的是_________(填字母)。
a.Ca(OH) b.NaCO c.CaCl
2 2 3 2
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:
①该技术第一步反应的离子方程式为_______________________________________________。
②处理1kg含80%FeS 的黄铁矿,第二步消耗O(标准状况下)的体积为_________L(精确到0.01)。
2 2
(5)治理汽车尾气的NSR(NOx储存还原)技术均可有效降低柴油发动机工作过程中排放的NOx。柴油发
动机工作时在稀燃(O 充足、柴油较少)和富燃(O 不足、柴油较多)条件下交替进行,通过BaO和Ba(NO )
2 2 3 2
的相互转化实现 的储存和还原,原理如下:①BaO吸收NO 的反应中,氧化剂与还原剂的物质的量之比为________________。
2
②若柴油中硫含量较高,在稀燃过程中,BaO吸收氮氧化物的能力会下降至很低水平,结合化学方程式解
释其原因___________________________________________。
【答案】(1)bc (2)SO +H O==H SO
2 2 2 3
(3)c (4) 2FeS+7O +2H O=4H++2Fe2++4SO2- 37.35或37.33
2 2 2 4
(5)1∶4 稀燃过程中,柴油中的硫被氧化为SO ,发生反应2SO +O +2BaO=2BaSO ,BaSO 稳定,不易
2 2 2 4 4
分解,也难与NOx反应
【解析】(1)a.PM2.5是指大气中直径小于或等于2.5um的颗粒物。它的主要来源是日常发电、工业生
产、汽车尾气排放等过程中经过燃烧而排放的残留物,故a正确;
b.PM2.5表面积大,具有吸附性,能吸附大量有毒物质,故b错误;
c.胶体微粒直径在10-7m~10-9m之间,PM2.5粒子的大小不符合,故c错误;
d.减少机动车尾气排放,减少了烟尘,能降低空气中PM2.5,故d正确;
故选: bc;
(2)二氧化硫与水反应生成亚硫酸,SO 形成硫酸型酸雨的过程用化学式表示为:SO +H O==H SO ;
2 2 2 2 3
(3)SO 为酸性气体,可用碱性物质作为洗涤剂来吸收它;
2
a.Ca(OH) 显碱性,两者反应生成亚硫酸钠和水,故符合题意;
2
b.Na CO 显碱性,两者反应生成亚硫酸钠和二氧化碳,故符合题意;
2 3
c.CaCl 显中性,两者不反应,故不符合题意;
2
故选c;
(4)①第一步反应物为FeS、O、HO,生成物为Fe、SO 2-,根据氧化还原反应得失电子数目相等,电
2 2 2 4
荷守恒与原子守恒可知:2FeS+7O +2H O=4H++2Fe2++4SO2-;
2 2 2 4
②第二步发生的反应为:4Fe2++O +4H+=4Fe3++2H O, 1kg含80%FeS 的黄铁矿能生成Fe2+的物质的量为:
2 2 2
1000g×80%/120g/mol≈6.67mol,第二步消耗O 的物质的量为6.67mol÷4=1.6675mol,(标准状况下)的体积为
2
1.6675mol×22.4L/mol=37.35L;
(5)①根据题图乙所示,NO 和O,与BaO反应生成Ba(NO ),化学方程式为 2BaO +4 NO + O =2
2 2 3 2 2 2
Ba(NO ) 其中O 作氧化剂,NO 作还原剂,则氧化剂与还原剂的物质的量之比为 1:4;
3 2 2 2②稀燃过程中氧气充足,柴油中的硫被氧化为SO ,SO 进一步与O、BaO发生反应
2 2 2
2SO +O +2BaO=2BaSO ,BaSO 稳定,不易分解,也难与NOx反应,使BaO吸收氮氧化物的能力下降到
2 2 4 4
很低的水平。