文档内容
机密★启用前
2025 年天津市普通高中学业水平等级性考试
化学
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分。考试用时60
分钟。第Ⅰ卷1至4页,第Ⅱ卷5至6页,共100分。
答卷前,考生务必将自己的姓名、准考号填写在答题卡上,并在规定位置粘贴
考试用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。
考试结束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!
第Ⅰ卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。
2.本卷共12题,每题3分,共36分。在每题列出的四个选项中,只有一项是
最符合题目要求的。
1. 天津位于渤海之滨,地处“九河下梢”,因河而生,向海而兴,自古流传着“精卫填
海”“哪吒闹海”等传说,其海水资源丰富,下列说法错误的是
A. 海水可经蒸馏制备淡水
B. 海水经氯气氧化可直接得到液溴
C. 海水晒盐的过程涉及溶液的蒸发、结晶
D. 用离子交换膜法电解饱和 溶液可得到烧碱溶液
2. 下列可用作食品添加剂且属于无机物的是
A. 硫酸铅 B. 木糖醇 C. 葡萄糖酸-δ-内酯 D. 二氧化
硫
的
3. 下列离子在溶液中能大量共存 是
A. B.C. D.
的
4. 下列比较结果,错误 是
A. 熔点:石英>苯酚
B. 热稳定性:
C. 离子半径:
D. 分散系中分散质粒子的直径: 胶体 溶液
5. 下列叙述和反应方程式相对应且正确的是
A. 实验室制备氨气:
B. 与盐酸反应:
C. 常温下,将氯气通入 溶液中:
D. 氯化亚铁溶液中加入稀硝酸: (稀)
6. 仪器分析在化学研究中有重要应用。下列方法选择错误的是
A. 用pH计区分KCl溶液和NaNO 溶液 B. 用X射线衍射法区分玻璃和蓝宝
3
石
C. 用原子光谱鉴定样品中含有元素Li D. 用质谱区分正己醇和正庚醇
7. 利用反应 可
处理 。设 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有的电子数目为B. 消耗 ,生成 的体积为67.2 L
C. 处理6.5 g NaN ,至少需要
3
D. 处理1 mol NaN ,反应转移的电子数目为
3
8. 油脂、淀粉、纤维素和蛋白质是重要的物质。下列说法错误的是
A. 油脂为高级脂肪酸的甘油酯,属于高分子化合物
B. 油脂、淀粉、纤维素和蛋白质均可发生水解反应
C. 蛋白质是由多种氨基酸通过肽键等相互连接形成的有机分子
的
D. 淀粉和纤维素 分子式均可表示为(C H O),二者结构不同
6 10 5 n
9. 依据下列实验操作及现象,不能得出相应结论的是
实验操作及现象 结论
将稀盐酸滴入NaHCO 溶液中,产生的气体通入澄清的石
A 3 非金属性:Cl>C
灰水,石灰水变浑浊
硫化锌(ZnS,白色)、硫化镉(CdS,黄色)为难溶电解质。
B 向浓度均为0.1 mol/L的Zn2+、Cd2+混合液中,滴加NaS稀
2
溶液,先出现的沉淀是黄色的
向可能含有Fe2+的未知溶液中,滴加1滴
C 原未知溶液中含有Fe2+
溶液,有特征蓝色沉淀生成
向含有新制 的氢氧化铜的碱性溶液中,加入乙醛溶液并加
D 乙醛具有还原性
热,出现砖红色沉淀
A. A B. B C. C D. D
10. 我国科学家报道了如下反应。
有关该反应的说法错误的是
A. 反应物与产物的摩尔质量相同B. 反应物与产物的红外光谱相同
C. 反应物与产物均能使酸性高锰酸钾溶液褪色
D. 反应过程中有碳氢键的断裂和碳碳双键的形成
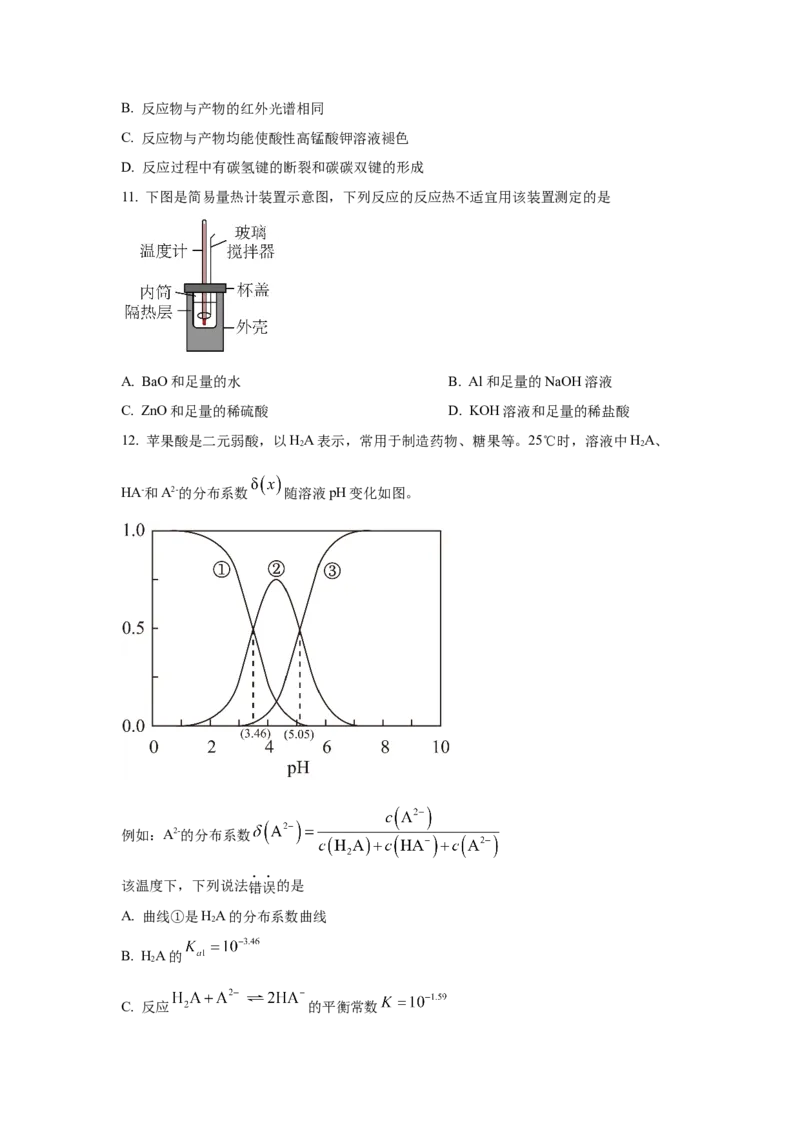
11. 下图是简易量热计装置示意图,下列反应的反应热不适宜用该装置测定的是
A. BaO和足量的水 B. Al和足量的NaOH溶液
C. ZnO和足量的稀硫酸 D. KOH溶液和足量的稀盐酸
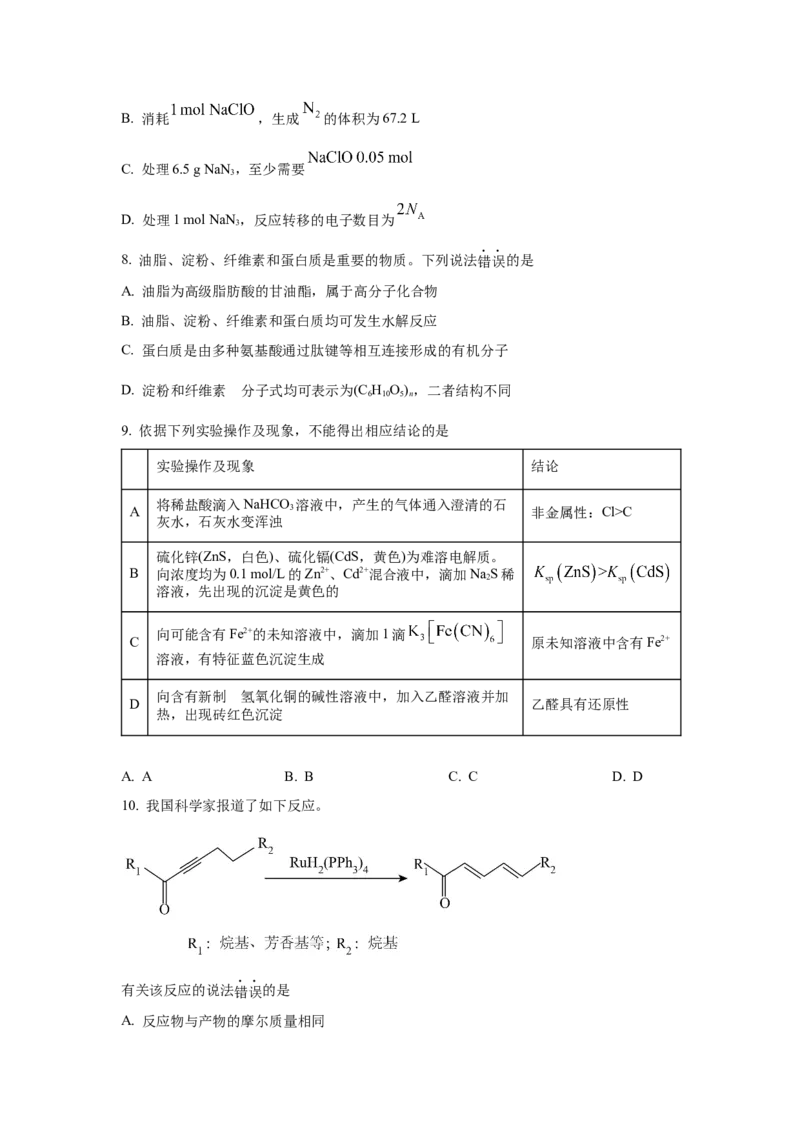
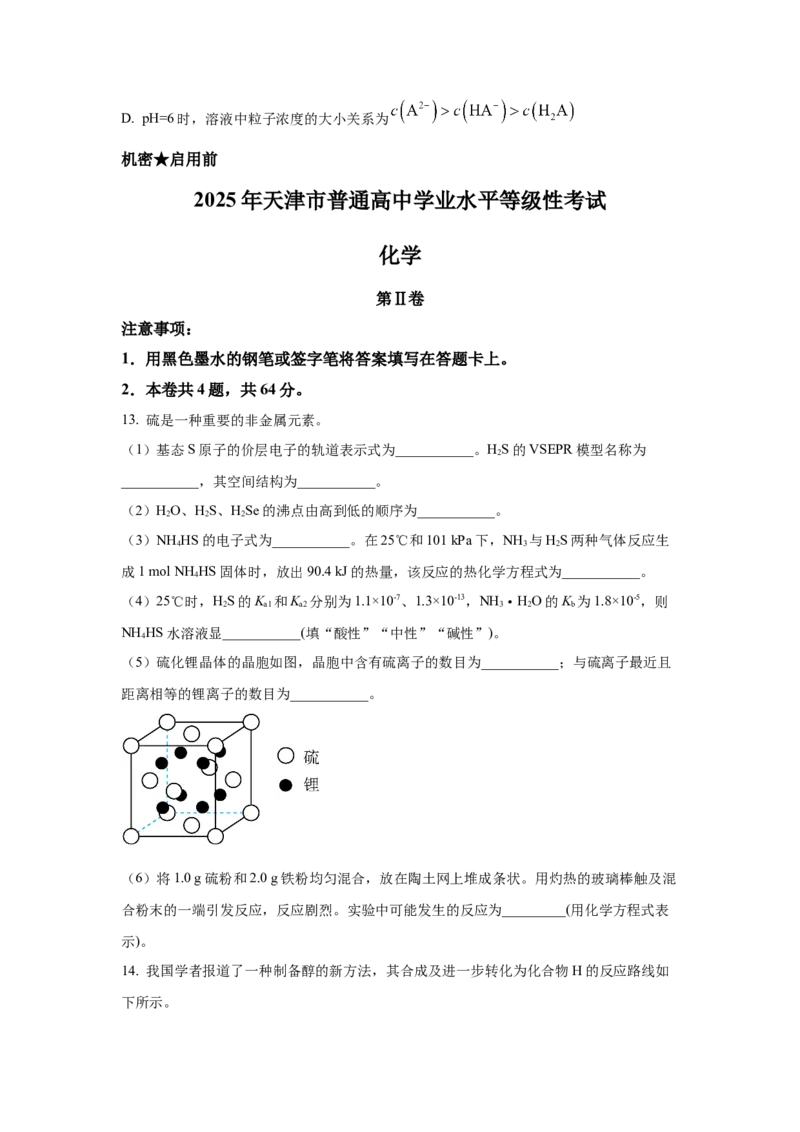
12. 苹果酸是二元弱酸,以HA表示,常用于制造药物、糖果等。25℃时,溶液中HA、
2 2
HA-和A2-的分布系数 随溶液pH变化如图。
例如:A2-的分布系数
该温度下,下列说法错误的是
A. 曲线①是HA的分布系数曲线
2
B. HA的
2
C. 反应 的平衡常数D. pH=6时,溶液中粒子浓度的大小关系为
机密★启用前
2025 年天津市普通高中学业水平等级性考试
化学
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案填写在答题卡上。
2.本卷共4题,共64分。
13. 硫是一种重要的非金属元素。
(1)基态S原子的价层电子的轨道表示式为___________。HS的VSEPR模型名称为
2
___________,其空间结构为___________。
(2)HO、HS、HSe的沸点由高到低的顺序为___________。
2 2 2
(3)NH HS的电子式为___________。在25℃和101 kPa下,NH 与HS两种气体反应生
4 3 2
成1 mol NH HS固体时,放出90.4 kJ的热量,该反应的热化学方程式为___________。
4
(4)25℃时,HS的K 和K 分别为1.1×10-7、1.3×10-13,NH ·HO的K 为1.8×10-5,则
2 a1 a2 3 2 b
NH HS水溶液显___________(填“酸性”“中性”“碱性”)。
4
(5)硫化锂晶体的晶胞如图,晶胞中含有硫离子的数目为___________;与硫离子最近且
距离相等的锂离子的数目为___________。
(6)将1.0 g硫粉和2.0 g铁粉均匀混合,放在陶土网上堆成条状。用灼热的玻璃棒触及混
合粉末的一端引发反应,反应剧烈。实验中可能发生的反应为_________(用化学方程式表
示)。
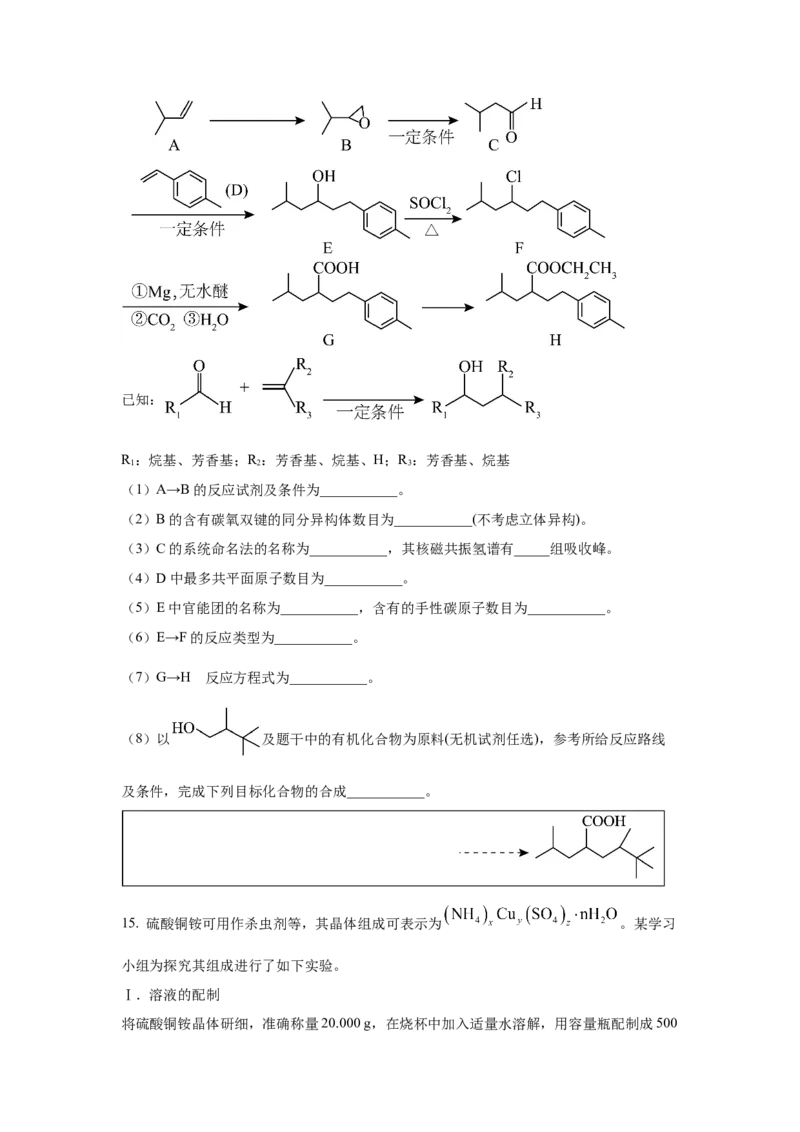
14. 我国学者报道了一种制备醇的新方法,其合成及进一步转化为化合物H的反应路线如
下所示。已知:
R :烷基、芳香基;R :芳香基、烷基、H;R :芳香基、烷基
1 2 3
(1)A→B的反应试剂及条件为___________。
(2)B的含有碳氧双键的同分异构体数目为___________(不考虑立体异构)。
(3)C的系统命名法的名称为___________,其核磁共振氢谱有_____组吸收峰。
(4)D中最多共平面原子数目为___________。
(5)E中官能团的名称为___________,含有的手性碳原子数目为___________。
(6)E→F的反应类型为___________。
的
(7)G→H 反应方程式为___________。
(8)以 及题干中的有机化合物为原料(无机试剂任选),参考所给反应路线
及条件,完成下列目标化合物的合成___________。
15. 硫酸铜铵可用作杀虫剂等,其晶体组成可表示为 。某学习
小组为探究其组成进行了如下实验。
Ⅰ.溶液的配制
将硫酸铜铵晶体研细,准确称量20.000 g,在烧杯中加入适量水溶解,用容量瓶配制成500mL溶液。
Ⅱ.组成的测定
①SO 定量分析:取25.00 mL硫酸铜铵溶液放入烧杯中,加入过量的经盐酸酸化的BaCl
2
溶液,使SO 完全沉淀,经过滤、洗涤、干燥至恒重,得到BaSO 固体并记录质量。重复
4
四次实验,结果分别为1.066 g、1.164 g、1.165 g和1.166 g。
②Cu2+定量分析:取25.00 mL硫酸铜铵溶液放入锥形瓶中,调节溶液的pH至3~4,加入过
量的KI溶液,用0.1000 mol/L Na SO 溶液滴定至浅黄色,加入指示剂,充分摇动后继续
2 2 3
滴定至终点。重复四次实验,消耗NaSO 溶液的平均体积为25.00 mL。
2 2 3
已知:
(1)研细晶体的仪器名称为___________。
(2)配制500 mL溶液定容时,操作的正确顺序为___________(填序号)。
a.将蒸馏水注入容量瓶
b.改用胶头滴管滴加蒸馏水
c.观察到液面离刻度线1~2 cm
d.至凹液面与刻度线相切
(3)分析 时,洗涤沉淀能否用稀硫酸作为洗涤试剂?___________(填“能”或“不
能”)。实验得到BaSO 的平均质量为___________。
4
(4)分析Cu2+时:①选用的指示剂为___________;②临近滴定终点时,需改为半滴滴加,
其具体操作为___________;③达到滴定终点的标志为___________。
(5)硫酸铜铵晶体中元素Cu的质量分数为___________。
(6)判断下列操作的影响(填“偏高”“偏低”或“无影响”);
①若在配制硫酸铜铵溶液时,烧杯中的溶液有少量溅出,则所配溶液浓度___________;
②若在滴定终点读数时,俯视液面,则Cu2+含量的测定结果___________。
(7)根据上述实验和结果,能否推断出硫酸铜铵晶体的化学式?说明理由。
___________(填“能”或“不能”),理由是________________。
16. 以苯为代表的挥发性有机污染物可以在Co O 的催化作用下,与O 反应生成CO 和
3 4 2 2
HO,进一步将CO 转化成高附加值的化学品,可减少污染和碳排放。
2 2
Ⅰ.CO 与苯的分子结构
2(1)CO 分子中碳原子的杂化轨道类型为___________,苯是___________(填“极性”或
2
“非极性”)分子。
Ⅱ.苯的催化氧化
Co O 做催化剂时,在有、无光照条件下,苯的催化氧化产物相同,但反应历程不同。无
3 4
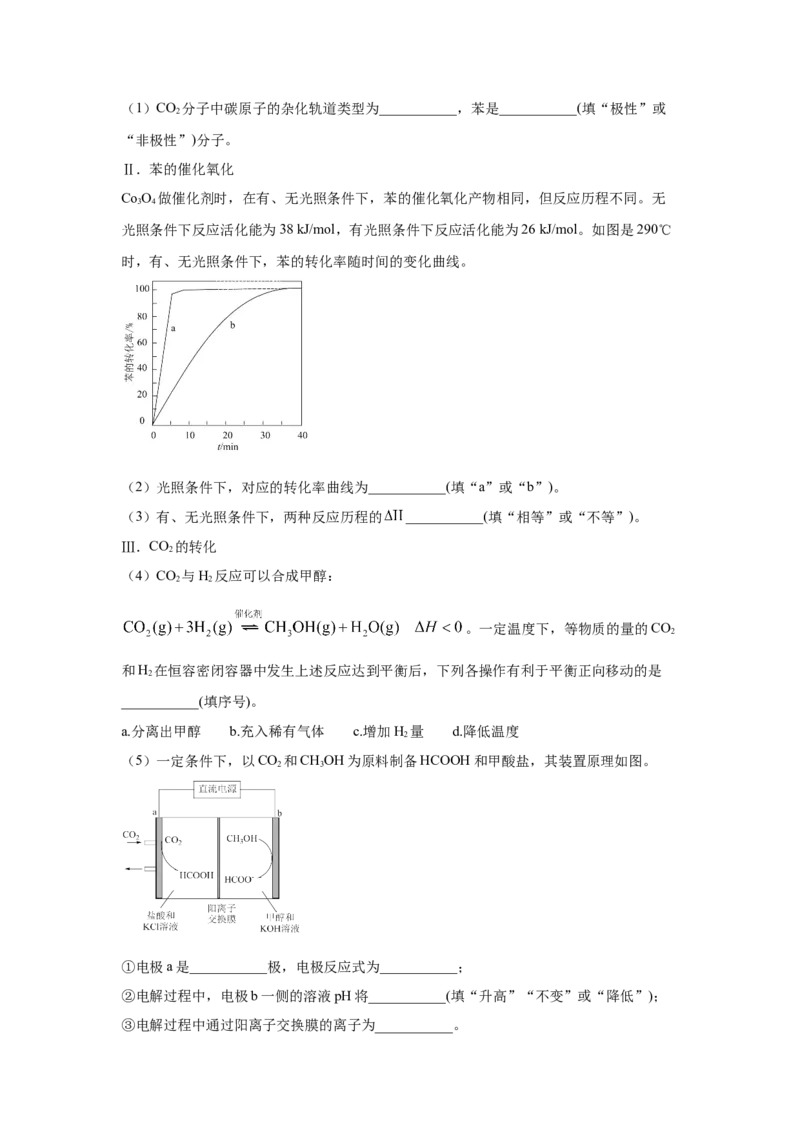
光照条件下反应活化能为38 kJ/mol,有光照条件下反应活化能为26 kJ/mol。如图是290℃
时,有、无光照条件下,苯的转化率随时间的变化曲线。
(2)光照条件下,对应的转化率曲线为___________(填“a”或“b”)。
(3)有、无光照条件下,两种反应历程的 ___________(填“相等”或“不等”)。
Ⅲ.CO 的转化
2
(4)CO 与H 反应可以合成甲醇:
2 2
。一定温度下,等物质的量的CO
2
和H 在恒容密闭容器中发生上述反应达到平衡后,下列各操作有利于平衡正向移动的是
2
___________(填序号)。
a.分离出甲醇 b.充入稀有气体 c.增加H 量 d.降低温度
2
(5)一定条件下,以CO 和CHOH为原料制备HCOOH和甲酸盐,其装置原理如图。
2 3
①电极a是___________极,电极反应式为___________;
②电解过程中,电极b一侧的溶液pH将___________(填“升高”“不变”或“降低”);
③电解过程中通过阳离子交换膜的离子为___________。