文档内容
2018年上海市普陀区中考化学二模试卷
六、选择题(共20分,每小题只有一个正确选项)
1.(1分)低碳环保应从我们身边做起,下列做法正确的是( )
A.出行以公共交通为主
B.空调一直开机维持室内温度
C.电池应扔在垃圾桶内
D.超市购物多使用塑料袋
2.(1分)属于混合物的是( )
A.蔗糖 B.胆矾 C.液态空气 D.蒸馏水
3.(1分)体现了“铁”的物理性质的是( )
A.铁易生锈 B.铁在纯氧中能燃烧
C.铁能与盐酸反应 D.铁能锻造成刀具
4.(1分)含“﹣4 价”碳元素的化合物是( )
A.CO B.CO C.CH D.Na CO
2 4 2 3
5.(1分)家庭中常见的物质在水中一般呈碱性的是( )
A.肥皂 B.食醋 C.食盐 D.酸奶
6.(1分)名称与化学式相对应的是( )
A.氯化亚铁FeCl B.硫酸钠 Na SO
3 2 4
C.胆矾CuSO D.氧化铝 AlO
4 2
7.(1分)地壳中含量最高的非金属元素是( )
A.氧 B.硅 C.铁 D.铝
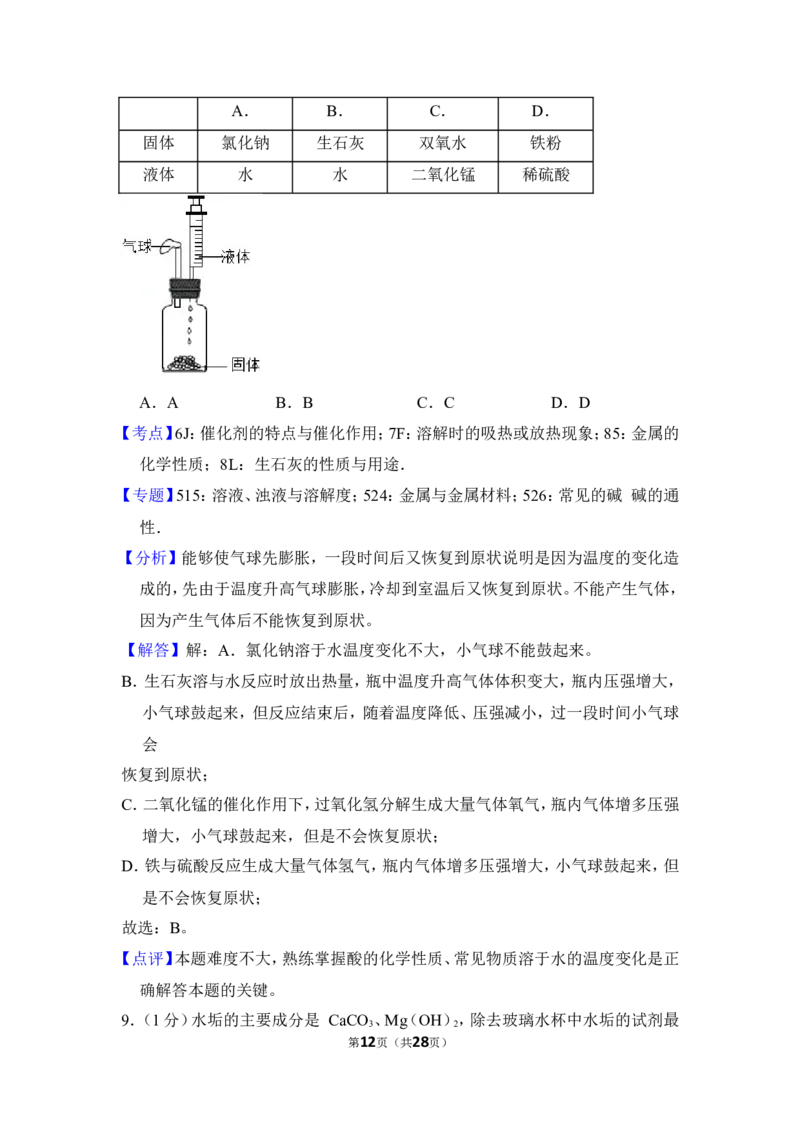
8.(1分)用如图所示的密闭装置进行实验,能够使气球先膨胀,慢慢又恢复(
)
A. B. C. D.
固体 氯化钠 生石灰 双氧水 铁粉
液体 水 水 二氧化锰 稀硫酸
第1页(共28页)A.A B.B C.C D.D
9.(1分)水垢的主要成分是 CaCO 、Mg(OH),除去玻璃水杯中水垢的试剂最
3 2
好是( )
A.盐酸 B.硫酸 C.食盐水 D.双氧水
10.(1分)物质露置在空气中一段时间后,质量会减轻的是( )
A.烧碱固体 B.浓盐酸 C.澄清石灰水 D.大理石
11.(1分)化学实验既要操作规范,更要保障安全。下列实验操作符合要求的是(
)
A.搅拌过滤器内的液体可以加快过滤速度
B.滴管伸入试管可以方便地把液体滴入试管
C.烧杯直接加热,可以更快地升温
D.粉末药品放入试管内,应平放试管用纸槽将粉末送入试管底部,再竖直试
管
12.(1分)有关“原子”说法错误的是( )
A.是化学变化中最小的微粒
B.是自然界中最小的微粒
C.是保持物质化学性质的一种微粒
D.是可以直接构成物质的一种微粒
13.(1分)有关燃烧说法正确的是( )
A.燃烧一定需要氧气 B.燃烧一定放热
C.燃烧一定生成二氧化碳 D.燃烧一定要点燃
14.(1分)一种高效消毒剂的主要成分为高氯精(C O N Cl ),下列有关高氯精的
3 3 3 3
说法正确的是( )
A.由 12 种元素组成
第2页(共28页)B.摩尔质量为 77.5
C.其中氧元素的质量分数最高
D.C、O、N、Cl 的原子个数比为 1:1:1:1
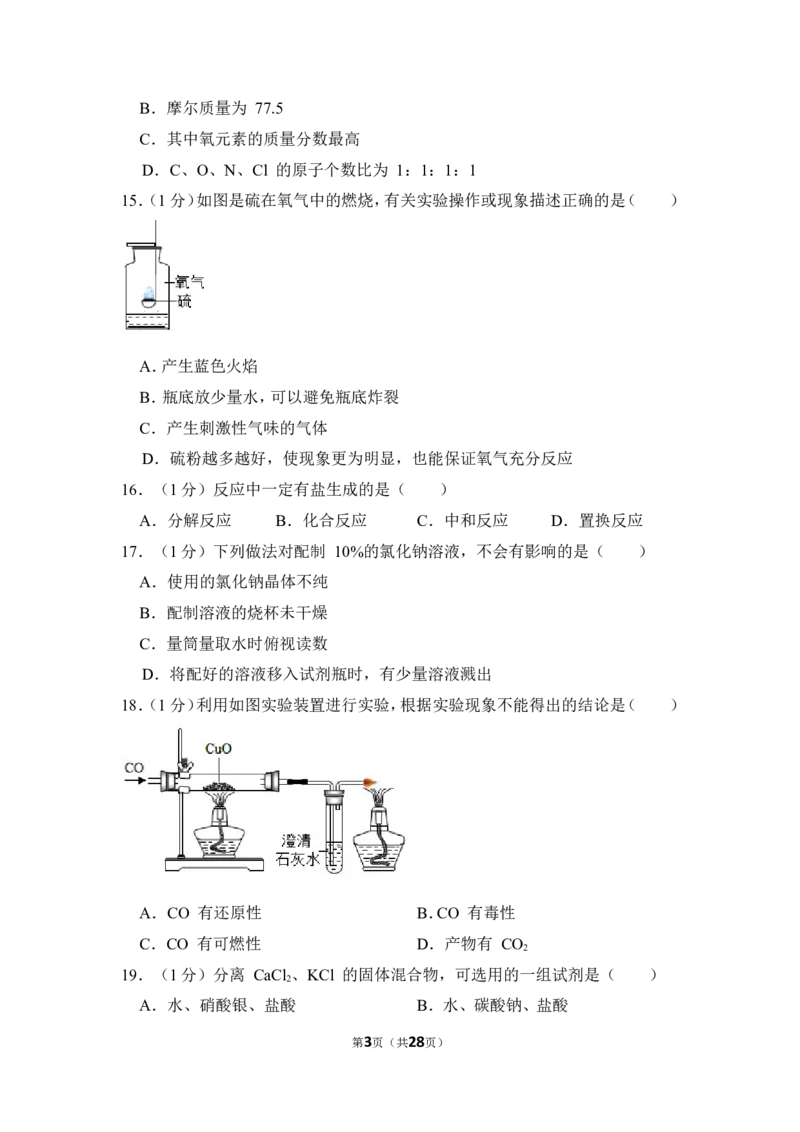
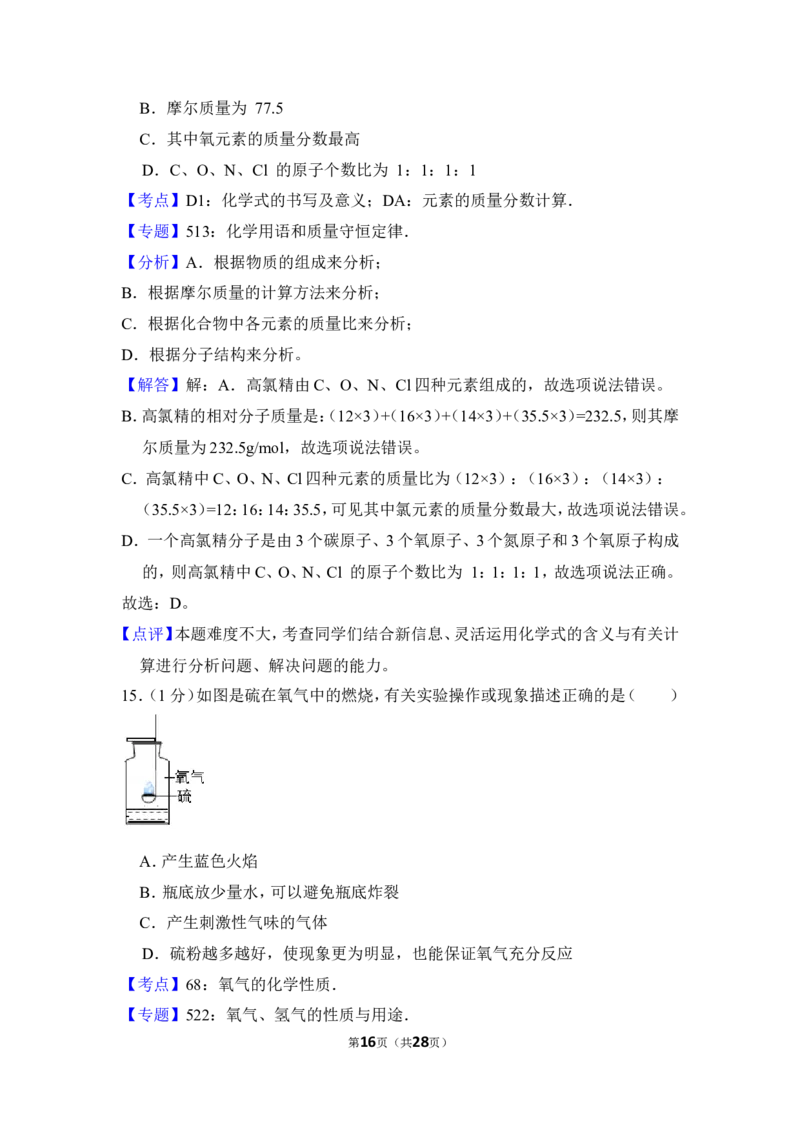
15.(1分)如图是硫在氧气中的燃烧,有关实验操作或现象描述正确的是( )
A.产生蓝色火焰
B.瓶底放少量水,可以避免瓶底炸裂
C.产生刺激性气味的气体
D.硫粉越多越好,使现象更为明显,也能保证氧气充分反应
16.(1分)反应中一定有盐生成的是( )
A.分解反应 B.化合反应 C.中和反应 D.置换反应
17.(1分)下列做法对配制 10%的氯化钠溶液,不会有影响的是( )
A.使用的氯化钠晶体不纯
B.配制溶液的烧杯未干燥
C.量筒量取水时俯视读数
D.将配好的溶液移入试剂瓶时,有少量溶液溅出
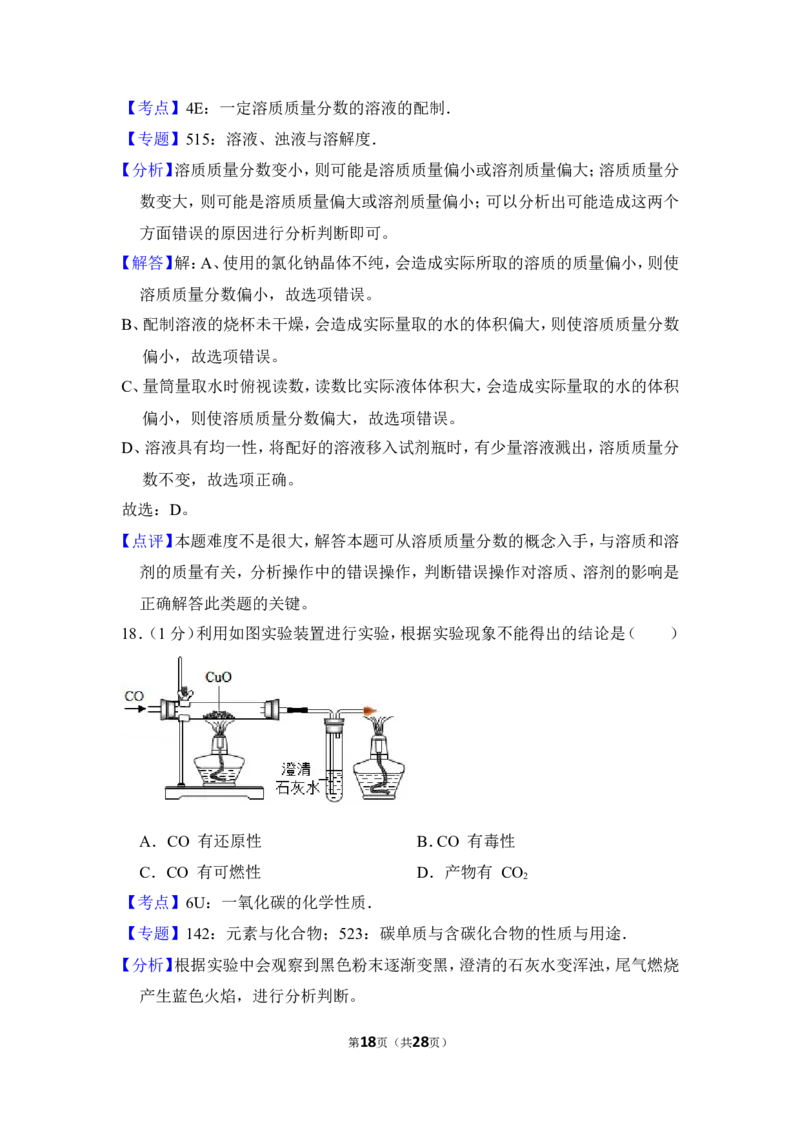
18.(1分)利用如图实验装置进行实验,根据实验现象不能得出的结论是( )
A.CO 有还原性 B.CO 有毒性
C.CO 有可燃性 D.产物有 CO
2
19.(1分)分离 CaCl 、KCl 的固体混合物,可选用的一组试剂是( )
2
A.水、硝酸银、盐酸 B.水、碳酸钠、盐酸
第3页(共28页)C.水、碳酸钾、硫酸 D.水、碳酸钾、盐酸
20.(1分)含 0.1mol NaOH 溶液中通入一定量的 CO 后,再滴入过量的盐酸
2
至溶液呈酸性,蒸干溶 液后,得到 NaCl 的物质的量n是( )
A.0.05<n<0.1mol B.n<0.1mol
C.0.05mol D.0.1mol
七、填空题(共21分)
21.(7分)普通电池(锌锰电池)含有多种材料,结构如图。 请你根据图示分析:
①图中金属单质有 种,化合物中除有机物外,无机物还含有 、
(填写物质种类名称)。
②写出氯化铵的化学式 ,在农业上它的 用途是 。
③碳棒起导电作用,这是利用了碳棒的 (选填“物理”或“化学”)性质
④拆解后经处理得到 65g 锌,则所含锌原子个数约为 (用科学记数法表
示)。
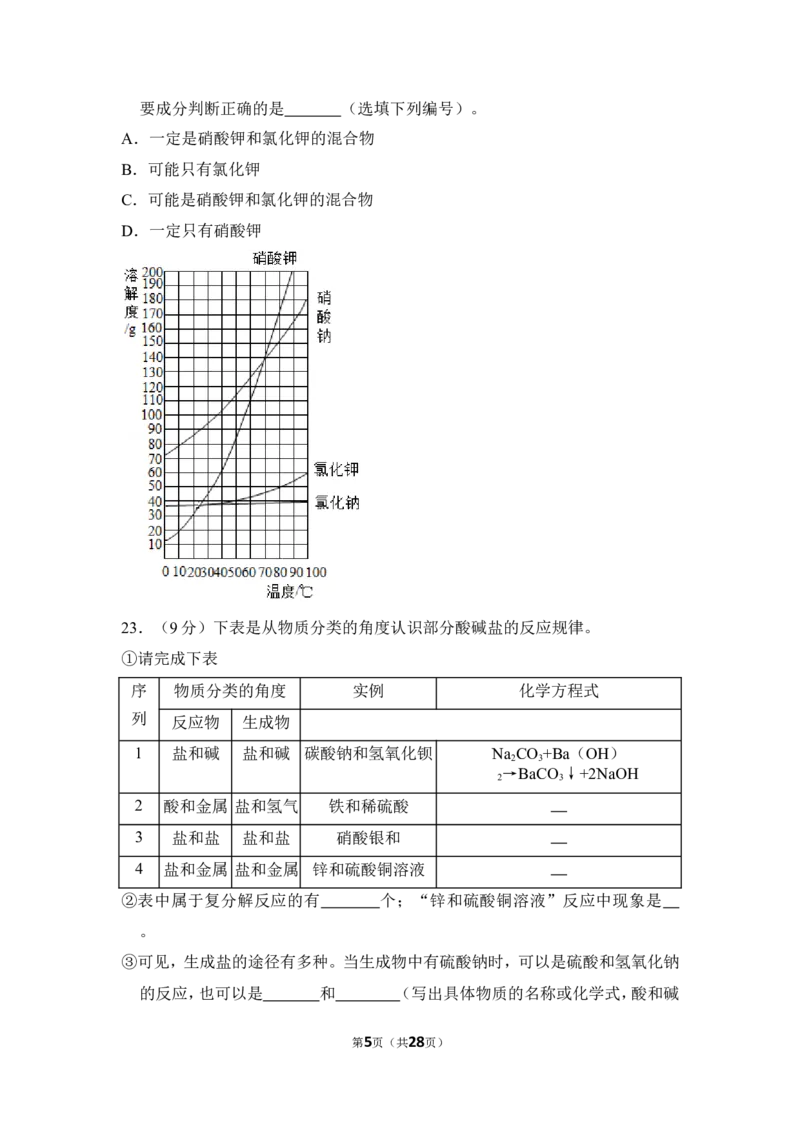
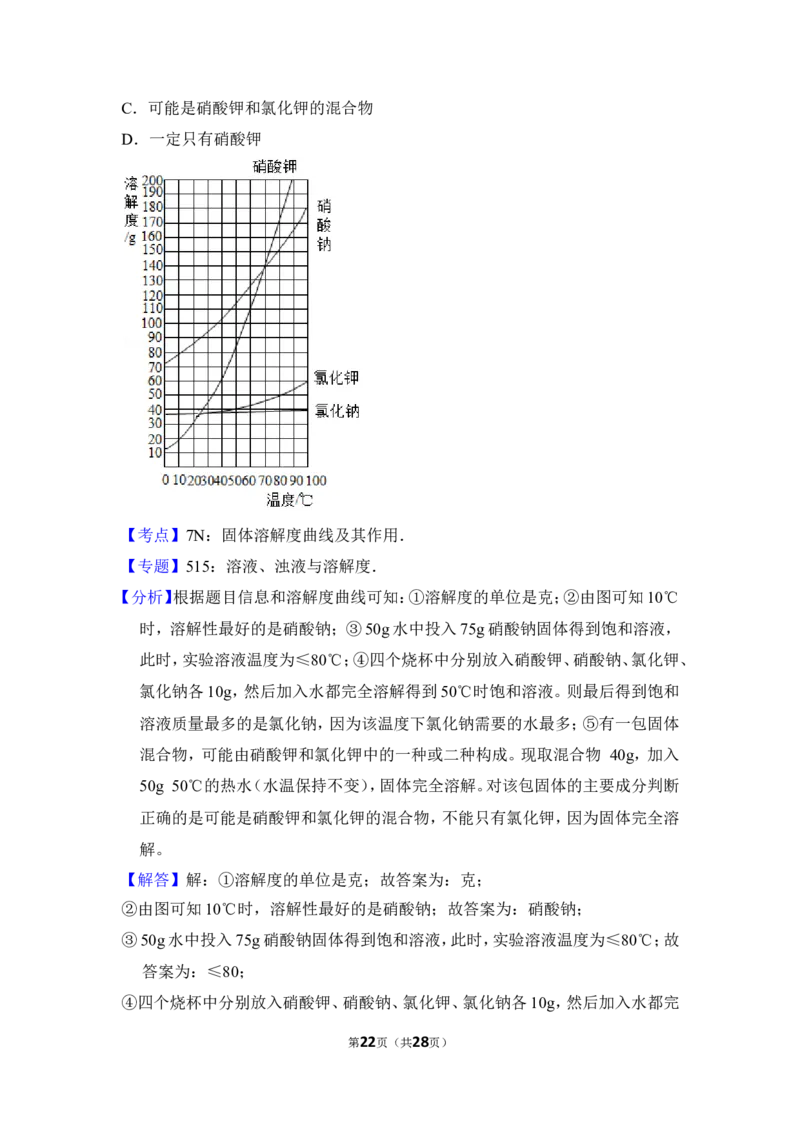
22.(5分)如图是四种物质的溶解度曲线图。
①溶解度的单位是 。
②由图可知 10℃时,溶解性最好的是 。
③ 50g 水中投入 75g 硝酸钠固体得到饱和溶液,此时,实验溶液温度为
℃。
④四个烧杯中分别放入硝酸钾、硝酸钠、氯化钾、氯化钠各 10g,然后加入水都完
全溶解得到 50℃时饱和溶液。则最后得到饱和溶液质量最多的是 (选
填下列编号)。
A.硝酸钾B.硝酸钠 C.氯化钾D.氯化钠
⑤有一包固体混合物,可能由硝酸钾和氯化钾中的一种或二种构成。现取混合物
40g,加入50g 50℃的热水(水温保持不变),固体完全溶解。对该包固体的主
第4页(共28页)要成分判断正确的是 (选填下列编号)。
A.一定是硝酸钾和氯化钾的混合物
B.可能只有氯化钾
C.可能是硝酸钾和氯化钾的混合物
D.一定只有硝酸钾
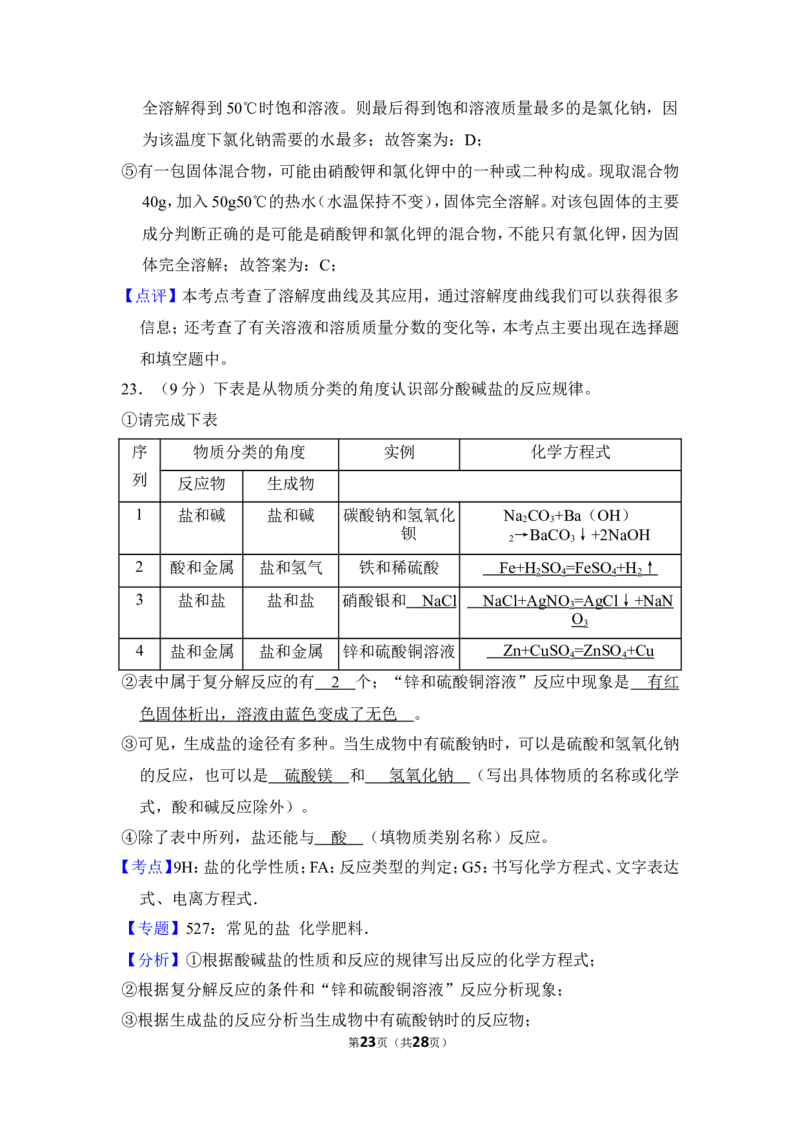
23.(9分)下表是从物质分类的角度认识部分酸碱盐的反应规律。
①请完成下表
序 物质分类的角度 实例 化学方程式
列 反应物 生成物
1 盐和碱 盐和碱 碳酸钠和氢氧化钡 Na CO +Ba(OH)
2 3
→BaCO ↓+2NaOH
2 3
2 酸和金属 盐和氢气 铁和稀硫酸
3 盐和盐 盐和盐 硝酸银和
4 盐和金属 盐和金属 锌和硫酸铜溶液
②表中属于复分解反应的有 个;“锌和硫酸铜溶液”反应中现象是
。
③可见,生成盐的途径有多种。当生成物中有硫酸钠时,可以是硫酸和氢氧化钠
的反应,也可以是 和 (写出具体物质的名称或化学式,酸和碱
第5页(共28页)反应除外)。
④除了表中所列,盐还能与 (填物质类别名称)反应。
八、简答题(共19分)
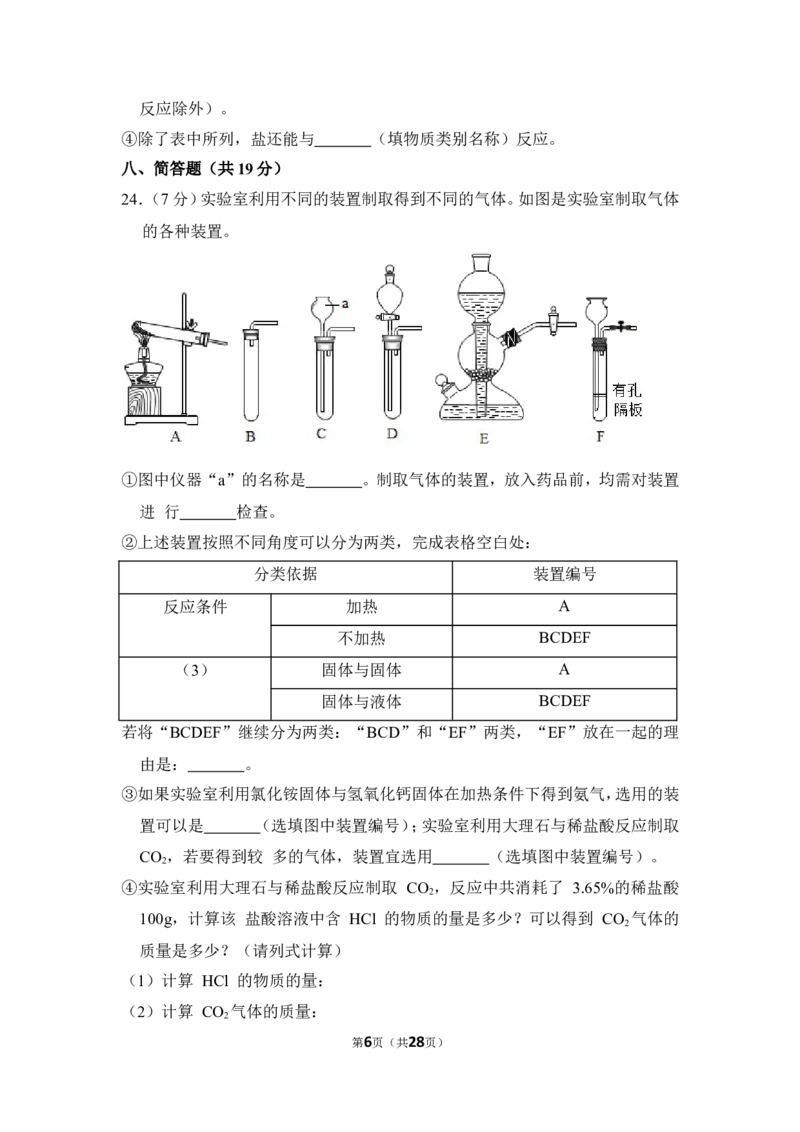
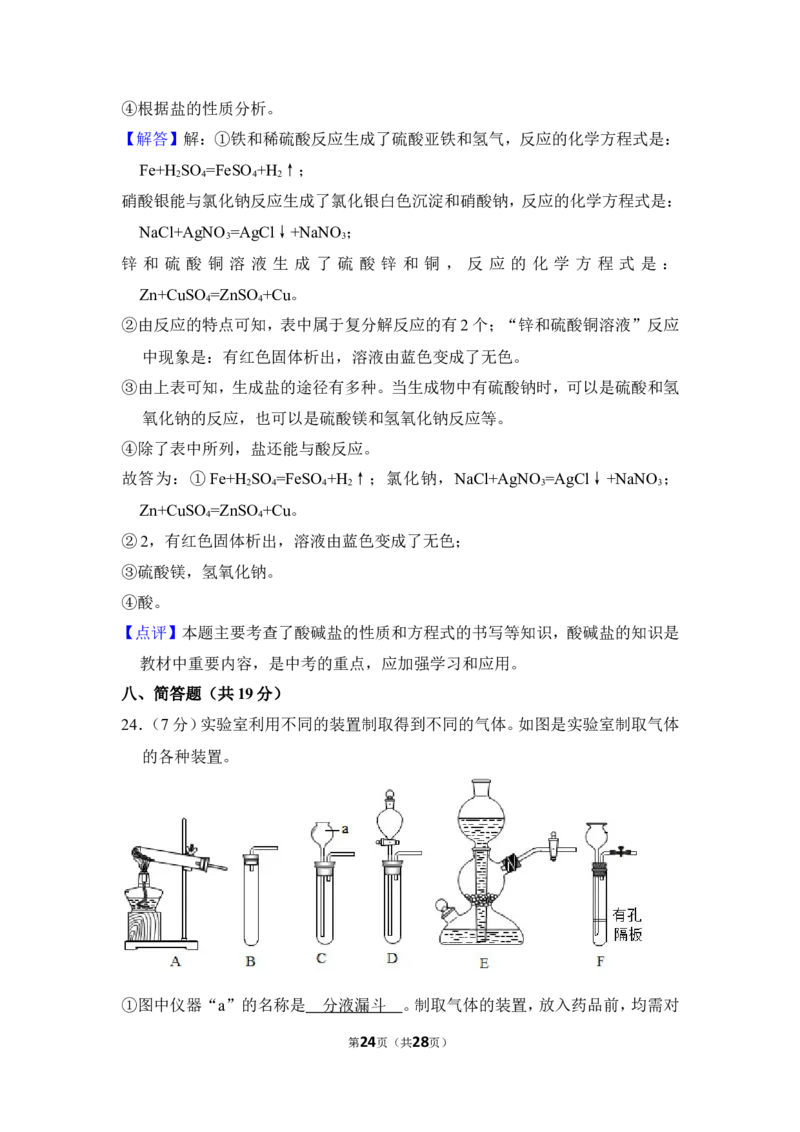
24.(7分)实验室利用不同的装置制取得到不同的气体。如图是实验室制取气体
的各种装置。
①图中仪器“a”的名称是 。制取气体的装置,放入药品前,均需对装置
进 行 检查。
②上述装置按照不同角度可以分为两类,完成表格空白处:
分类依据 装置编号
反应条件 加热 A
不加热 BCDEF
(3) 固体与固体 A
固体与液体 BCDEF
若将“BCDEF”继续分为两类:“BCD”和“EF”两类,“EF”放在一起的理
由是: 。
③如果实验室利用氯化铵固体与氢氧化钙固体在加热条件下得到氨气,选用的装
置可以是 (选填图中装置编号);实验室利用大理石与稀盐酸反应制取
CO ,若要得到较 多的气体,装置宜选用 (选填图中装置编号)。
2
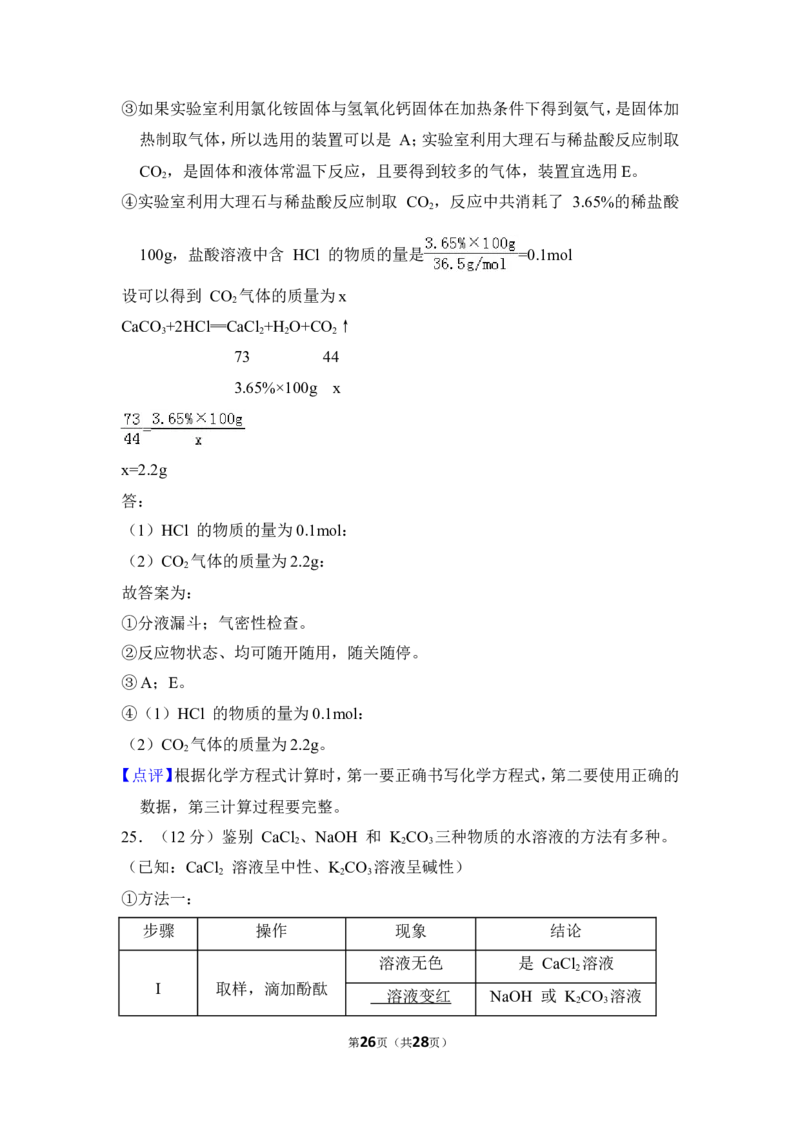
④实验室利用大理石与稀盐酸反应制取 CO ,反应中共消耗了 3.65%的稀盐酸
2
100g,计算该 盐酸溶液中含 HCl 的物质的量是多少?可以得到 CO 气体的
2
质量是多少?(请列式计算)
(1)计算 HCl 的物质的量:
(2)计算 CO 气体的质量:
2
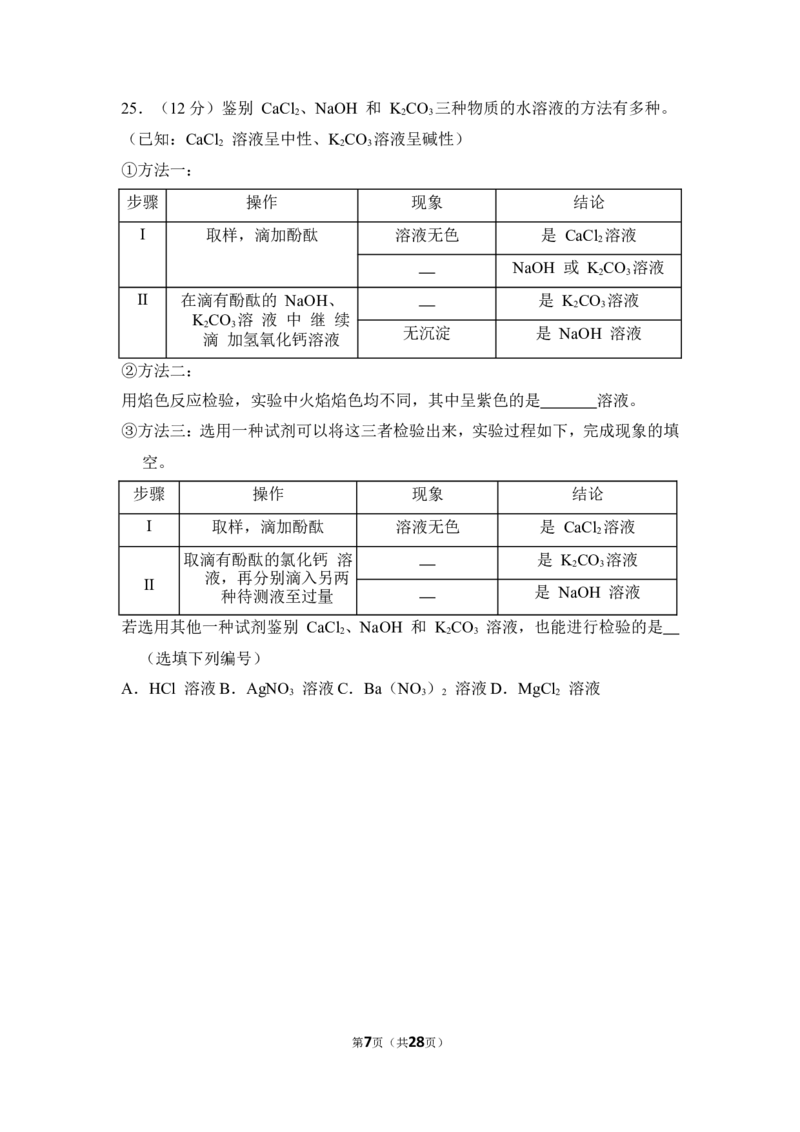
第6页(共28页)25.(12分)鉴别 CaCl 、NaOH 和 K CO 三种物质的水溶液的方法有多种。
2 2 3
(已知:CaCl 溶液呈中性、K CO 溶液呈碱性)
2 2 3
①方法一:
步骤 操作 现象 结论
I 取样,滴加酚酞 溶液无色 是 CaCl 溶液
2
NaOH 或 K CO 溶液
2 3
II 在滴有酚酞的 NaOH、 是 K CO 溶液
2 3
K CO 溶 液 中 继 续
2 3
无沉淀 是 NaOH 溶液
滴 加氢氧化钙溶液
②方法二:
用焰色反应检验,实验中火焰焰色均不同,其中呈紫色的是 溶液。
③方法三:选用一种试剂可以将这三者检验出来,实验过程如下,完成现象的填
空。
步骤 操作 现象 结论
I 取样,滴加酚酞 溶液无色 是 CaCl 溶液
2
取滴有酚酞的氯化钙 溶 是 K CO 溶液
2 3
液,再分别滴入另两
II
种待测液至过量 是 NaOH 溶液
若选用其他一种试剂鉴别 CaCl 、NaOH 和 K CO 溶液,也能进行检验的是
2 2 3
(选填下列编号)
A.HCl 溶液B.AgNO 溶液C.Ba(NO ) 溶液D.MgCl 溶液
3 3 2 2
第7页(共28页)2018 年上海市普陀区中考化学二模试卷
参考答案与试题解析
六、选择题(共20分,每小题只有一个正确选项)
1.(1分)低碳环保应从我们身边做起,下列做法正确的是( )
A.出行以公共交通为主
B.空调一直开机维持室内温度
C.电池应扔在垃圾桶内
D.超市购物多使用塑料袋
【考点】6I:自然界中的碳循环.
菁优网版权所有
【专题】212:化学与环境保护;523:碳单质与含碳化合物的性质与用途.
【分析】“低碳环保”代表着更健康、更自然、更安全的生活,同时也是一种低成
本、低代价的生活方式;可以从节电、节能和回收等环节来改变生活细节,据此
进行分析判断即可。
【解答】解:A、出行以公共交通为主,能减少燃油、燃气等交通工具的使用,从而
减少二氧化碳的排放,故选项符合“低碳环保”理念。
B、空调一直开机维持室内温度,浪费了大量的电能,增加了二氧化碳的排放量,
故选项不符合“低碳环保”理念。
C、电池应扔在垃圾桶内,会造成土壤、水体污染,应扔在专门回收电池的垃圾桶
内,故选项不符合“低碳环保”理念。
D、超市购物多使用塑料袋,会造成白色污染,故选项不符合“低碳生活”理念。
故选项不符合“低碳环保”理念。
故选:A。
【点评】低碳生活理念已成为人们的共识,节能减排的措施和观念是化学考查的
热点,要用低碳生活理念指导自己的活动,把节能减排的措施运用到生产、生
活中去。
2.(1分)属于混合物的是( )
A.蔗糖 B.胆矾 C.液态空气 D.蒸馏水
【考点】A5:纯净物和混合物的判别.
菁优网版权所有
第8页(共28页)【专题】516:物质的分类.
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,液态
空气中也有氧气、氮气等,属于混合物;纯净物是由一种物质组成。纯净物又分
为单质和化合物。由同种元素组成的纯净物叫单质;由两种或两种以上的元素
组成的纯净物叫化合物。
【解答】解:A、蔗糖属于纯净物中的化合物,故选项错误;
B、胆矾属于纯净物中的化合物,故选项错误;
C、混合物是由两种或两种以上的物质组成,液态空气中也有氧气、氮气等,属于
混合物;故选项正确;
D、蒸馏水属于纯净物中的化合物,故选项错误;
故选:C。
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物等基
本概念,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空
题中。
3.(1分)体现了“铁”的物理性质的是( )
A.铁易生锈 B.铁在纯氧中能燃烧
C.铁能与盐酸反应 D.铁能锻造成刀具
【考点】82:金属的物理性质及用途.
菁优网版权所有
【专题】524:金属与金属材料.
【分析】物质在化学变化中表现出来的性质叫化学性质,如可燃性、助燃性、氧化
性、还原性等;物质不需要发生化学变化就表现出来的性质,叫物理性质;物理
性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、
溶解性、挥发性等。
【解答】解:A、铁易生锈,铁生锈生成了新的物质,是在化学变化中表现出来的性
质,属于化学性质,故选项错误;
B、铁能在氧气中燃烧,生成了新的物质,是在化学变化中表现出来的性质,属于
化学性质,故选项错误;
C、铁能与稀硫酸反应,生成了新的物质,是在化学变化中表现出来的性质,属于
化学性质,故选项错误;
D、铁能锻造成刀具,是利用了铁硬度大的性质,属于物理性质,故选项正确。
第9页(共28页)故选:D。
【点评】本考点考查了物理性质和化学性质的区分,要记忆有关铁的性质,并能够
在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空
题中。
4.(1分)含“﹣4 价”碳元素的化合物是( )
A.CO B.CO C.CH D.Na CO
2 4 2 3
【考点】D6:有关元素化合价的计算.
菁优网版权所有
【专题】191:化学式的计算;541:有关化学式的计算.
【分析】根据在化合物中正负化合价代数和为零,结合的化学式进行解答即可。
【解答】解:A、氧元素显﹣2价,设碳元素的化合价是x,根据在化合物中正负化
合价代数和为零,可得:x+(﹣2)=0,则x=+2价。
B、氧元素显﹣2价,设碳元素的化合价是y,根据在化合物中正负化合价代数和
为零,可得:y+(﹣2)×2=0,则y=+4价。
C、氢元素显+1价,设碳元素的化合价是z,根据在化合物中正负化合价代数和为
零,可得:z+(+1)×4=0,则z=﹣4价。
D、钠元素显+1价,氧元素显﹣2价,设碳元素的化合价是w,根据在化合物中正
负化合价代数和为零,可得:(+1)×2+w+(﹣2)×3=0,则w=+4价。
故选:C。
【点评】本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为
零)计算指定元素的化合价的方法即可正确解答此类题。
5.(1分)家庭中常见的物质在水中一般呈碱性的是( )
A.肥皂 B.食醋 C.食盐 D.酸奶
【考点】9A:溶液的酸碱性测定.
菁优网版权所有
【专题】142:元素与化合物;525:常见的酸 酸的通性.
【分析】根据常见化学物质的酸碱性,进行分析判断。
【解答】解:A、肥皂水显碱性,故选项正确。
B、食醋中含有醋酸,显酸性,故选项错误。
C、食盐水显中性,故选项错误。
D、酸奶中含有酸性物质,显酸性,故选项错误。
故选:A。
第10页(共28页)【点评】本题难度不大,了解常见化学物质的酸碱性是正确解答本题的关键。
6.(1分)名称与化学式相对应的是( )
A.氯化亚铁FeCl B.硫酸钠 Na SO
3 2 4
C.胆矾CuSO D.氧化铝 AlO
4 2
【考点】D1:化学式的书写及意义.
菁优网版权所有
【专题】513:化学用语和质量守恒定律.
【分析】化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,
原子个数不能漏,正负化合价代数和为零。
【解答】解:A.氯化亚铁中,铁元素显+2价,氯元素显﹣1价,所以氯化亚铁的化
学式为FeCl ,故错误;
2
B.硫酸钠中,钠元素显+1价,硫酸根显﹣2价,所以硫酸钠的化学式为Na SO ,
2 4
故正确;
C.胆矾是五水硫酸铜的俗称,其化学式为CuSO •5H O,故错误;
4 2
D.氧化铝中,铝元素显+3价,氧元素显﹣2价,所以氧化铝的化学式为Al O ,故
2 3
错误。
故选:B。
【点评】本题难度不大,掌握化合物化学式的书写一般规律(金属在前,非金属在
后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此
类题的关键。
7.(1分)地壳中含量最高的非金属元素是( )
A.氧 B.硅 C.铁 D.铝
【考点】C2:地壳中元素的分布与含量;C4:元素的简单分类.
菁优网版权所有
【专题】511:物质的微观构成与物质的宏观组成.
【分析】根据地壳中各元素的含量及其种类来分析。
【解答】解:在地壳中,含量位于前五位的元素依次是氧、硅、铝、铁、钙,其中氧元
素是地壳中含量最高的非金属元素。
故选:A。
【点评】熟记地壳中含量较多的前五种元素即可顺利解答。
8.(1分)用如图所示的密闭装置进行实验,能够使气球先膨胀,慢慢又恢复(
)
第11页(共28页)A. B. C. D.
固体 氯化钠 生石灰 双氧水 铁粉
液体 水 水 二氧化锰 稀硫酸
A.A B.B C.C D.D
【考点】6J:催化剂的特点与催化作用;7F:溶解时的吸热或放热现象;85:金属的
化学性质;8L:生石灰的性质与用途.
菁优网版权所有
【专题】515:溶液、浊液与溶解度;524:金属与金属材料;526:常见的碱 碱的通
性.
【分析】能够使气球先膨胀,一段时间后又恢复到原状说明是因为温度的变化造
成的,先由于温度升高气球膨胀,冷却到室温后又恢复到原状。不能产生气体,
因为产生气体后不能恢复到原状。
【解答】解:A.氯化钠溶于水温度变化不大,小气球不能鼓起来。
B.生石灰溶与水反应时放出热量,瓶中温度升高气体体积变大,瓶内压强增大,
小气球鼓起来,但反应结束后,随着温度降低、压强减小,过一段时间小气球
会
恢复到原状;
C.二氧化锰的催化作用下,过氧化氢分解生成大量气体氧气,瓶内气体增多压强
增大,小气球鼓起来,但是不会恢复原状;
D.铁与硫酸反应生成大量气体氢气,瓶内气体增多压强增大,小气球鼓起来,但
是不会恢复原状;
故选:B。
【点评】本题难度不大,熟练掌握酸的化学性质、常见物质溶于水的温度变化是正
确解答本题的关键。
9.(1分)水垢的主要成分是 CaCO 、Mg(OH),除去玻璃水杯中水垢的试剂最
3 2
第12页(共28页)好是( )
A.盐酸 B.硫酸 C.食盐水 D.双氧水
【考点】95:碱的化学性质;9H:盐的化学性质.
菁优网版权所有
【专题】526:常见的碱 碱的通性;527:常见的盐 化学肥料.
【分析】根据食盐水、双氧水不会与碳酸盐、不溶性碱反应,硫酸和碳酸钙反应生
成微溶于水的硫酸钙进行分析。
【解答】解:食盐水、双氧水不会与碳酸盐、不溶性碱反应,硫酸和碳酸钙反应生成
微溶于水的硫酸钙,造成除垢不彻底,所以除去玻璃水杯中水垢的试剂最好是
盐酸,故选:A。
【点评】本题主要考查了碳酸盐、不溶性碱与酸的难度不大,加强记忆即可解答。
10.(1分)物质露置在空气中一段时间后,质量会减轻的是( )
A.烧碱固体 B.浓盐酸 C.澄清石灰水 D.大理石
【考点】9S:空气中常见酸碱盐的质量或性质变化及贮存法.
菁优网版权所有
【专题】525:常见的酸 酸的通性;526:常见的碱 碱的通性.
【分析】浓盐酸具有较强的挥发性,露置在空气中氯化氢挥发溶液质量减少;氢氧
化钠放在空气中易潮解以及和二氧化碳反应而质量增加;澄石灰水能与空气
中的二氧化碳反应生成碳酸钙和水;大理石在空气中没有变化而质量不变。
【解答】解:A、烧碱即氢氧化钠放在空气中易潮解以及和二氧化碳反应而质量增
加,故错。
B、浓盐酸易挥发质量会减小,故正确。
C、澄石灰水能与空气中的二氧化碳反应生成碳酸钙和水,总质量增加,故错误。
D、大理石在空气中没有变化而质量不变,故错误。
故选:B。
【点评】本题考查了初中化学中涉及到一些物质会因保存不当,发生质量的变化。
所以由此题我们联想到如何正确保存一些化学药品和它的用途。比如:苛性钠
放在空气中易潮解,故应放置在干燥的环境中,也可做一些物质的干燥剂。浓
盐酸具有较强挥发性,应密闭保存等。
11.(1分)化学实验既要操作规范,更要保障安全。下列实验操作符合要求的是(
)
A.搅拌过滤器内的液体可以加快过滤速度
第13页(共28页)B.滴管伸入试管可以方便地把液体滴入试管
C.烧杯直接加热,可以更快地升温
D.粉末药品放入试管内,应平放试管用纸槽将粉末送入试管底部,再竖直试
管
【考点】41:用于加热的仪器;48:固体药品的取用;49:液体药品的取用;4G:过滤
的原理、方法及其应用.
菁优网版权所有
【专题】341:化学学习中的实验思想;531:常见仪器及化学实验基本操作.
【分析】A、过滤液体时,注意“一贴、二低、三靠”的原则。
B、根据使用胶头滴管滴加少量液体的方法进行分析判断。
C、根据烧杯不能直接进行加热,进行分析判断。
D、根据向试管中装粉末状固体药品的方法(“一斜、二送、三直立”)进行分析
判断。
【解答】解:A、过滤液体时,注意“一贴、二低、三靠”的原则,不能搅拌过滤器内
的液体,以防止损坏滤纸,故选项说法错误。
B、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触
试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,故选项说
法错误。
C、烧杯不能直接加热,应垫上石棉网,故选项说法错误。
D、取用粉末状药品,试管横放,用药匙或纸槽把药品送到试管底部,再竖直试管
故选项说法正确。
故选:D。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本
操作的注意事项是解答此类试题的关键。
12.(1分)有关“原子”说法错误的是( )
A.是化学变化中最小的微粒
B.是自然界中最小的微粒
C.是保持物质化学性质的一种微粒
D.是可以直接构成物质的一种微粒
【考点】B4:原子的定义与构成.
菁优网版权所有
【专题】511:物质的微观构成与物质的宏观组成.
第14页(共28页)【分析】在化学变化中分子可分,原子不可分。原子是构成物质的一种微粒,原子
不是保持物质性质的一种微粒。
【解答】解:A、原子是化学变化中的最小微粒,故A说法正确。
B、原子还可以再分,分为原子核和和外电子,分子、原子不能笼统的比较大小,故
B说法错误。
C、由原子直接构成的物质中,原子是保持物质化学性质的一种微粒,故C说法正
确。
D、构成物质的基本微粒有:分子、原子和离子,所以原子是可以直接构成物质的
一种微粒,故D说法正确。
故选:B。
【点评】本题主要考查了原子的特征和性质方面是内容。可以依据原子的特征进
行。
13.(1分)有关燃烧说法正确的是( )
A.燃烧一定需要氧气 B.燃烧一定放热
C.燃烧一定生成二氧化碳 D.燃烧一定要点燃
【考点】H1:燃烧与燃烧的条件.
菁优网版权所有
【专题】213:化学与能源.
【分析】根据燃烧需要同时满足三个条件:①可燃物、②氧气或空气、③温度要达
到着火点,结合题意进行分析判断。
【解答】解:A、燃烧不一定需要氧气,如镁能在二氧化碳气体中燃烧,故选项说法
错误。
B、燃烧放出大量的热,一定放热,故选项说法正确。
C、燃烧不一定生成二氧化碳,如氢气燃烧生成水,故选项说法错误。
D、燃烧不一定要点燃,如白磷能自燃,故选项说法错误。
故选:B。
【点评】本题难度不大,灵活运用燃烧的特征、需要同时满足三个条件是正确解答
本题的关键。
14.(1分)一种高效消毒剂的主要成分为高氯精(C O N Cl ),下列有关高氯精的
3 3 3 3
说法正确的是( )
A.由 12 种元素组成
第15页(共28页)B.摩尔质量为 77.5
C.其中氧元素的质量分数最高
D.C、O、N、Cl 的原子个数比为 1:1:1:1
【考点】D1:化学式的书写及意义;DA:元素的质量分数计算.
菁优网版权所有
【专题】513:化学用语和质量守恒定律.
【分析】A.根据物质的组成来分析;
B.根据摩尔质量的计算方法来分析;
C.根据化合物中各元素的质量比来分析;
D.根据分子结构来分析。
【解答】解:A.高氯精由C、O、N、Cl四种元素组成的,故选项说法错误。
B.高氯精的相对分子质量是:(12×3)+(16×3)+(14×3)+(35.5×3)=232.5,则其摩
尔质量为232.5g/mol,故选项说法错误。
C.高氯精中C、O、N、Cl四种元素的质量比为(12×3):(16×3):(14×3):
(35.5×3)=12:16:14:35.5,可见其中氯元素的质量分数最大,故选项说法错误。
D.一个高氯精分子是由3个碳原子、3个氧原子、3个氮原子和3个氧原子构成
的,则高氯精中C、O、N、Cl 的原子个数比为 1:1:1:1,故选项说法正确。
故选:D。
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计
算进行分析问题、解决问题的能力。
15.(1分)如图是硫在氧气中的燃烧,有关实验操作或现象描述正确的是( )
A.产生蓝色火焰
B.瓶底放少量水,可以避免瓶底炸裂
C.产生刺激性气味的气体
D.硫粉越多越好,使现象更为明显,也能保证氧气充分反应
【考点】68:氧气的化学性质.
菁优网版权所有
【专题】522:氧气、氢气的性质与用途.
第16页(共28页)【分析】根据硫在氧气中燃烧的现象和注意事项分析判断有关的问题。
【解答】解:A、硫在氧气中燃烧产生蓝紫色火焰,故A错误;
B、硫在氧气中燃烧产生的二氧化硫有毒能污染空气,瓶底放少量水,可以吸收二
氧化硫,防止污染空气,故B错误;
C、硫在氧气中燃烧产生刺激性气味的气体,故C正确;
D、硫粉的量达到一定的量即可,并不是越多使现象更为明显,故D错误。
故选:C。
【点评】本题较为简单,了解硫在氧气中燃烧的现象和注意事项即可分析解答。
16.(1分)反应中一定有盐生成的是( )
A.分解反应 B.化合反应 C.中和反应 D.置换反应
【考点】97:中和反应及其应用;F1:化合反应及其应用;F2:分解反应及其应用;
F3:置换反应及其应用.
菁优网版权所有
【专题】332:化学反应的分类思想;514:化学反应的基本类型和能量变化.
【分析】根据分解反应、化合反应、中和反应、置换反应的特征,进行分析判断。
【解答】解:A、分解反应不一定有盐生成,如2H O 2H ↑+O ↑,故选项错
2 2 2
误。
B、化合反应不一定有盐生成,如C+O CO ,故选项错误。
2 2
C、中和反应是酸与碱作用生成盐和水的反应,中和反应一定有盐生成,故选项正
确。
D、置换反应不一定有盐生成,如C+2CuO 2Cu+CO ↑,故选项错误。
2
故选:C。
【点评】本题难度不大,掌握中和反应、分解反应、化合反应、置换反应的特征是正
确解答本题的关键。
17.(1分)下列做法对配制 10%的氯化钠溶液,不会有影响的是( )
A.使用的氯化钠晶体不纯
B.配制溶液的烧杯未干燥
C.量筒量取水时俯视读数
D.将配好的溶液移入试剂瓶时,有少量溶液溅出
第17页(共28页)【考点】4E:一定溶质质量分数的溶液的配制.
菁优网版权所有
【专题】515:溶液、浊液与溶解度.
【分析】溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大;溶质质量分
数变大,则可能是溶质质量偏大或溶剂质量偏小;可以分析出可能造成这两个
方面错误的原因进行分析判断即可。
【解答】解:A、使用的氯化钠晶体不纯,会造成实际所取的溶质的质量偏小,则使
溶质质量分数偏小,故选项错误。
B、配制溶液的烧杯未干燥,会造成实际量取的水的体积偏大,则使溶质质量分数
偏小,故选项错误。
C、量筒量取水时俯视读数,读数比实际液体体积大,会造成实际量取的水的体积
偏小,则使溶质质量分数偏大,故选项错误。
D、溶液具有均一性,将配好的溶液移入试剂瓶时,有少量溶液溅出,溶质质量分
数不变,故选项正确。
故选:D。
【点评】本题难度不是很大,解答本题可从溶质质量分数的概念入手,与溶质和溶
剂的质量有关,分析操作中的错误操作,判断错误操作对溶质、溶剂的影响是
正确解答此类题的关键。
18.(1分)利用如图实验装置进行实验,根据实验现象不能得出的结论是( )
A.CO 有还原性 B.CO 有毒性
C.CO 有可燃性 D.产物有 CO
2
【考点】6U:一氧化碳的化学性质.
菁优网版权所有
【专题】142:元素与化合物;523:碳单质与含碳化合物的性质与用途.
【分析】根据实验中会观察到黑色粉末逐渐变黑,澄清的石灰水变浑浊,尾气燃烧
产生蓝色火焰,进行分析判断。
第18页(共28页)【解答】解:A、实验中会观察到黑色粉末逐渐变黑,说明一氧化碳与氧化铜发生
了反应,说明CO 有还原性,故选项说法正确。
B、由图中实验,不能说明CO 有毒性,故选项说法错误。
C、尾气中含有一氧化碳,能燃烧产生蓝色火焰,说明CO 有可燃性,故选项说法
正确。
D、澄清的石灰水变浑浊,说明产物有CO ,故选项说法正确。
2
故选:B。
【点评】本题难度不大,掌握一氧化碳的化学性质(可燃性、还原性)并能灵活运用
是正确解答本题的关键。
19.(1分)分离 CaCl 、KCl 的固体混合物,可选用的一组试剂是( )
2
A.水、硝酸银、盐酸 B.水、碳酸钠、盐酸
C.水、碳酸钾、硫酸 D.水、碳酸钾、盐酸
【考点】4F:混合物的分离方法;9H:盐的化学性质.
菁优网版权所有
【专题】167:物质的分离和提纯;533:物质的分离、除杂、提纯与共存问题.
【分析】根据CaCl 、KCl 易溶于水,氯化钙能与碳酸钾溶液反应生成碳酸钙白色
2
沉淀和氯化钾,碳酸钙能与稀盐酸反应生成氯化钙、水和二氧化碳,进行分析
解答。
【解答】解:A、CaCl 、KCl均易溶于水,CaCl 、KCl均能与硝酸银溶液反应,不能
2 2
分离出CaCl 、KCl,故选项错误。
2
B、CaCl 、KCl 易溶于水,氯化钙能与碳酸钠溶液反应生成碳酸钙白色沉淀和氯
2
化钠,引入了新的杂质氯化钠,故选项错误。
C、CaCl 、KCl 易溶于水,氯化钙能与碳酸钾溶液反应生成碳酸钙白色沉淀和氯
2
化钾,再进行过滤,分离出氯化钾溶液和碳酸钙沉淀;最后向碳酸钙沉淀中滴
加稀硫酸,碳酸钙能与稀硫酸反应生成硫酸钙、水和二氧化碳;引入了新的杂
质硫酸钙,故选项错误。
D、CaCl 、KCl 易溶于水,氯化钙能与碳酸钾溶液反应生成碳酸钙白色沉淀和氯
2
化钾,再进行过滤,分离出氯化钾溶液和碳酸钙沉淀;最后向碳酸钙沉淀中滴
加稀盐酸,碳酸钙能与稀盐酸反应生成氯化钙、水和二氧化碳;能将混合物逐
一分离,故选项正确。
故选:D。
第19页(共28页)【点评】本题有一定难度,考查物质的分离,熟练掌握酸碱盐的化学性质并能灵活
运用是正确解答本题的关键,解题时要注意反应后不能引入新的杂质。
20.(1分)含 0.1mol NaOH 溶液中通入一定量的 CO 后,再滴入过量的盐酸
2
至溶液呈酸性,蒸干溶 液后,得到 NaCl 的物质的量n是( )
A.0.05<n<0.1mol B.n<0.1mol
C.0.05mol D.0.1mol
【考点】G1:质量守恒定律及其应用.
菁优网版权所有
【专题】411:元素质量守恒;513:化学用语和质量守恒定律.
【分析】根据质量守恒定律,反应前后钠元素的质量不变,进行分析解答。
【解答】解:含 0.1mol NaOH 溶液中,含有0.1mol钠离子;通入一定量的 CO
2
后,氢氧化钠与二氧化碳反应生成碳酸钠和水,再滴入过量的盐酸,稀盐酸与
碳酸钠、氢氧化钠反应能生成氯化钠;由质量守恒定律,反应前后钠元素的质
量不变,则蒸干溶 液后,得到NaCl 的物质的量n=0.1mol。
故选:D。
【点评】本题难度不大,明确反应前后钠元素的质量不变是正确解答本题的关键。
七、填空题(共21分)
21.(7分)普通电池(锌锰电池)含有多种材料,结构如图。 请你根据图示分析:
①图中金属单质有 二 种,化合物中除有机物外,无机物还含有 盐 、 氧
化物 (填写物质种类名称)。
②写出氯化铵的化学式 NH Cl ,在农业上它的 用途是 做化学肥料 。
4
③碳棒起导电作用,这是利用了碳棒的 物理 (选填“物理”或“化学”)性
质。
④拆解后经处理得到 65g 锌,则所含锌原子个数约为 6.02×1 0 2 3 (用科学记数
法表示)。
第20页(共28页)【考点】9J:常见化肥的种类和作用;A7:单质和化合物的判别;A9:常见的氧化物、
酸、碱和盐的判别;C6:碳单质的物理性质及用途;D1:化学式的书写及意义.
菁优网版权所有
【专题】516:物质的分类;527:常见的盐 化学肥料.
【分析】由题目的信息可知,①图中金属单质有二种,化合物中除有机物外,无机
物还含有盐、氧化物;②氯化铵的化学式是NH Cl,在农业上它的用途是做化
4
学肥料;③碳棒起导电作用,这是利用了碳棒的物理性质;④拆解后经处理得
到65g锌,即1mol,则所含锌原子个数约为:6.02×1023。
【解答】解:①图中金属单质有二种,化合物中除有机物外,无机物还含有盐、氧化
物;故答案为:二;盐;氧化物;
②氯化铵的化学式是 NH Cl,在农业上它的用途是做化学肥料;故答案为:
4
NH Cl;做化学肥料;
4
③碳棒起导电作用,这是利用了碳棒的物理性质;故答案为:物理;
④拆解后经处理得到65g锌,即1mol,则所含锌原子个数约为:6.02×1023;故答案
为:6.02×1023;
【点评】本考点考查了化学材料、化学肥料、物质的性质等,考查的知识点比较多,
要加强记忆,理解应用。
22.(5分)如图是四种物质的溶解度曲线图。
①溶解度的单位是 克 。
②由图可知 10℃时,溶解性最好的是 硝酸钠 。
③50g 水中投入75g硝酸钠固体得到饱和溶液,此时,实验溶液温度为 ≤ 80
℃。
④四个烧杯中分别放入硝酸钾、硝酸钠、氯化钾、氯化钠各 10g,然后加入水都完
全溶解得到 50℃时饱和溶液。则最后得到饱和溶液质量最多的是 D (选填
下列编号)。
A.硝酸钾B.硝酸钠 C.氯化钾D.氯化钠
⑤有一包固体混合物,可能由硝酸钾和氯化钾中的一种或二种构成。现取混合物
40g,加入50g 50℃的热水(水温保持不变),固体完全溶解。对该包固体的主
要成分判断正确的是 C (选填下列编号)。
A.一定是硝酸钾和氯化钾的混合物
B.可能只有氯化钾
第21页(共28页)C.可能是硝酸钾和氯化钾的混合物
D.一定只有硝酸钾
【考点】7N:固体溶解度曲线及其作用.
菁优网版权所有
【专题】515:溶液、浊液与溶解度.
【分析】根据题目信息和溶解度曲线可知:①溶解度的单位是克;②由图可知10℃
时,溶解性最好的是硝酸钠;③50g水中投入75g硝酸钠固体得到饱和溶液,
此时,实验溶液温度为≤80℃;④四个烧杯中分别放入硝酸钾、硝酸钠、氯化钾、
氯化钠各10g,然后加入水都完全溶解得到50℃时饱和溶液。则最后得到饱和
溶液质量最多的是氯化钠,因为该温度下氯化钠需要的水最多;⑤有一包固体
混合物,可能由硝酸钾和氯化钾中的一种或二种构成。现取混合物 40g,加入
50g 50℃的热水(水温保持不变),固体完全溶解。对该包固体的主要成分判断
正确的是可能是硝酸钾和氯化钾的混合物,不能只有氯化钾,因为固体完全溶
解。
【解答】解:①溶解度的单位是克;故答案为:克;
②由图可知10℃时,溶解性最好的是硝酸钠;故答案为:硝酸钠;
③50g水中投入75g硝酸钠固体得到饱和溶液,此时,实验溶液温度为≤80℃;故
答案为:≤80;
④四个烧杯中分别放入硝酸钾、硝酸钠、氯化钾、氯化钠各10g,然后加入水都完
第22页(共28页)全溶解得到50℃时饱和溶液。则最后得到饱和溶液质量最多的是氯化钠,因
为该温度下氯化钠需要的水最多;故答案为:D;
⑤有一包固体混合物,可能由硝酸钾和氯化钾中的一种或二种构成。现取混合物
40g,加入50g50℃的热水(水温保持不变),固体完全溶解。对该包固体的主要
成分判断正确的是可能是硝酸钾和氯化钾的混合物,不能只有氯化钾,因为固
体完全溶解;故答案为:C;
【点评】本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多
信息;还考查了有关溶液和溶质质量分数的变化等,本考点主要出现在选择题
和填空题中。
23.(9分)下表是从物质分类的角度认识部分酸碱盐的反应规律。
①请完成下表
序 物质分类的角度 实例 化学方程式
列 反应物 生成物
1 盐和碱 盐和碱 碳酸钠和氢氧化 Na CO +Ba(OH)
2 3
钡 →BaCO ↓+2NaOH
2 3
2 酸和金属 盐和氢气 铁和稀硫酸 Fe+H SO =FeSO +H ↑
2 4 4 2
3 盐和盐 盐和盐 硝酸银和 NaC l NaCl+AgNO =AgCl ↓ +NaN
3
O
3
4 盐和金属 盐和金属 锌和硫酸铜溶液 Zn+CuSO =ZnSO +Cu
4 4
②表中属于复分解反应的有 2 个;“锌和硫酸铜溶液”反应中现象是 有红
色固体析出,溶液由蓝色变成了无色 。
③可见,生成盐的途径有多种。当生成物中有硫酸钠时,可以是硫酸和氢氧化钠
的反应,也可以是 硫酸镁 和 氢氧化钠 (写出具体物质的名称或化学
式,酸和碱反应除外)。
④除了表中所列,盐还能与 酸 (填物质类别名称)反应。
【考点】9H:盐的化学性质;FA:反应类型的判定;G5:书写化学方程式、文字表达
式、电离方程式.
菁优网版权所有
【专题】527:常见的盐 化学肥料.
【分析】①根据酸碱盐的性质和反应的规律写出反应的化学方程式;
②根据复分解反应的条件和“锌和硫酸铜溶液”反应分析现象;
③根据生成盐的反应分析当生成物中有硫酸钠时的反应物;
第23页(共28页)④根据盐的性质分析。
【解答】解:①铁和稀硫酸反应生成了硫酸亚铁和氢气,反应的化学方程式是:
Fe+H SO =FeSO +H ↑;
2 4 4 2
硝酸银能与氯化钠反应生成了氯化银白色沉淀和硝酸钠,反应的化学方程式是:
NaCl+AgNO =AgCl↓+NaNO ;
3 3
锌 和 硫 酸 铜 溶 液 生 成 了 硫 酸 锌 和 铜 , 反 应 的 化 学 方 程 式 是 :
Zn+CuSO =ZnSO +Cu。
4 4
②由反应的特点可知,表中属于复分解反应的有2个;“锌和硫酸铜溶液”反应
中现象是:有红色固体析出,溶液由蓝色变成了无色。
③由上表可知,生成盐的途径有多种。当生成物中有硫酸钠时,可以是硫酸和氢
氧化钠的反应,也可以是硫酸镁和氢氧化钠反应等。
④除了表中所列,盐还能与酸反应。
故答为:① Fe+H SO =FeSO +H ↑;氯化钠,NaCl+AgNO =AgCl↓+NaNO ;
2 4 4 2 3 3
Zn+CuSO =ZnSO +Cu。
4 4
②2,有红色固体析出,溶液由蓝色变成了无色;
③硫酸镁,氢氧化钠。
④酸。
【点评】本题主要考查了酸碱盐的性质和方程式的书写等知识,酸碱盐的知识是
教材中重要内容,是中考的重点,应加强学习和应用。
八、简答题(共19分)
24.(7分)实验室利用不同的装置制取得到不同的气体。如图是实验室制取气体
的各种装置。
①图中仪器“a”的名称是 分液漏斗 。制取气体的装置,放入药品前,均需对
第24页(共28页)装置进 行 气密性 检查。
②上述装置按照不同角度可以分为两类,完成表格空白处:
分类依据 装置编号
反应条件 加热 A
不加热 BCDEF
(3) 固体与固体 A
固体与液体 BCDEF
若将“BCDEF”继续分为两类:“BCD”和“EF”两类,“EF”放在一起的理
由是: 反应物状态、均可随开随用,随关随停 。
③如果实验室利用氯化铵固体与氢氧化钙固体在加热条件下得到氨气,选用的装
置可以是 A (选填图中装置编号);实验室利用大理石与稀盐酸反应制取
CO ,若要得到较 多的气体,装置宜选用 E (选填图中装置编号)。
2
④实验室利用大理石与稀盐酸反应制取 CO ,反应中共消耗了 3.65%的稀盐酸
2
100g,计算该 盐酸溶液中含 HCl 的物质的量是多少?可以得到 CO 气体的
2
质量是多少?(请列式计算)
(1)计算 HCl 的物质的量:
(2)计算 CO 气体的质量:
2
【考点】4K:检查装置的气密性;4N:实验室制取气体的思路;G6:根据化学反应
方程式的计算.
菁优网版权所有
【专题】193:有关化学方程式的计算;534:常见气体的实验室制法、检验、干燥与
净化.
【分析】①根据常见仪器的名称和使用注意事项分析;
②根据给出的仪器装置特点进行分析和归纳;
③根据对应的气体的制取方法进行回答;
④根据HCl的质量和对应的化学方程式求算生成的二氧化碳的质量。
【解答】解:
①图中仪器“a”的名称是分液漏斗,方便液体药品的添加以及滴加量和速率的
控制。制取气体的装置,放入药品前,均需对装置进行气密性检查。
②“EF”是能实现固体和液体分离从而实验反应控制,所以放在一起的理由是:
反应物状态、均可随开随用,随关随停。
第25页(共28页)③如果实验室利用氯化铵固体与氢氧化钙固体在加热条件下得到氨气,是固体加
热制取气体,所以选用的装置可以是 A;实验室利用大理石与稀盐酸反应制取
CO ,是固体和液体常温下反应,且要得到较多的气体,装置宜选用E。
2
④实验室利用大理石与稀盐酸反应制取 CO ,反应中共消耗了 3.65%的稀盐酸
2
100g,盐酸溶液中含 HCl 的物质的量是 =0.1mol
设可以得到 CO 气体的质量为x
2
CaCO +2HCl═CaCl +H O+CO ↑
3 2 2 2
73 44
3.65%×100g x
=
x=2.2g
答:
(1)HCl 的物质的量为0.1mol:
(2)CO 气体的质量为2.2g:
2
故答案为:
①分液漏斗;气密性检查。
②反应物状态、均可随开随用,随关随停。
③A;E。
④(1)HCl 的物质的量为0.1mol:
(2)CO 气体的质量为2.2g。
2
【点评】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的
数据,第三计算过程要完整。
25.(12分)鉴别 CaCl 、NaOH 和 K CO 三种物质的水溶液的方法有多种。
2 2 3
(已知:CaCl 溶液呈中性、K CO 溶液呈碱性)
2 2 3
①方法一:
步骤 操作 现象 结论
溶液无色 是 CaCl 溶液
2
I 取样,滴加酚酞
溶液变红 NaOH 或 K CO 溶液
2 3
第26页(共28页)在滴有酚酞的 产生白色沉淀 是 K CO 溶液
2 3
NaOH、K CO 溶
2 3
液 中 继 续 滴
II
加氢氧化钙溶液 无沉淀 是 NaOH 溶液
②方法二:
用焰色反应检验,实验中火焰焰色均不同,其中呈紫色的是 碳酸钾 溶液。
③方法三:选用一种试剂可以将这三者检验出来,实验过程如下,完成现象的填
空。
步骤 操作 现象 结论
I 取样,滴加酚酞 溶液无色 是 CaCl 溶液
2
II 取滴有酚酞的氯化钙 产生白色沉淀,溶液变红 是 K CO 溶液
2 3
溶液,再分别滴入另
两 种待测液至过量 溶液变红 是 NaOH 溶液
若选用其他一种试剂鉴别 CaCl 、NaOH 和 K CO 溶液,也能进行检验的是
2 2 3
ACD (选填下列编号)
A.HCl 溶液B.AgNO 溶液C.Ba(NO ) 溶液D.MgCl 溶液
3 3 2 2
【考点】AE:物质的鉴别、推断.
菁优网版权所有
【专题】182:物质的鉴别题.
【分析】根据物质的性质以及性质差异、物质间反应的实验现象进行分析解答即
可。
【解答】解:①方法一:氢氧化钠和碳酸钾的溶液是碱性的,能使酚酞试液变红,碳
酸钾能与氢氧化钙反应产生白色沉淀,故填:
步骤 操作 现象 结论
溶液无色 是 CaCl 溶液
2
I 取样,滴加酚酞
溶液变红 NaOH 或 K CO 溶液
2 3
在滴有酚酞的 NaOH、 产生白色沉淀 是 K CO 溶液
2 3
K CO 溶 液 中 继
2 3
续 滴 加氢氧化钙
II
溶液 无沉淀 是 NaOH 溶液
②方法二:
用焰色反应检验,碳酸钾中的钾离子的焰色反应是紫色的,故填:碳酸钾。
③方法三:选碳酸钾能与氯化钙反应产生白色沉淀,过量的碳酸钾会使溶液呈碱
性,能使酚酞试液变红,而氢氧化钠溶液中加入氯化钙溶液仅仅会出现溶液变
第27页(共28页)红的现象,故填:
步骤 操作 现象 结论
I 取样,滴加酚酞 溶液无色 是 CaCl 溶液
2
取滴有酚酞的氯化钙 溶 产生白色沉淀,溶液变红 是 K CO 溶液
2 3
液,再分别滴入另两
II
种待测液至过量 溶液变红 是 NaOH 溶液
A.HCl 溶液能与碳酸钾反应产生气泡,将碳酸钾溶液加入剩余的两种溶液中,
产生白色沉淀的是氯化钙,无现象的是氢氧化钠,可以鉴别;
B.AgNO 溶液能与氯化钙和碳酸钾溶液反应产生白色沉淀,只能鉴别出氢氧化
3
钠溶液,无法确定氯化钙和碳酸钾溶液,不能鉴别;
C.Ba(NO ) 溶液能与碳酸钾溶液反应产生白色沉淀,将碳酸钾溶液加入剩余
3 2
的两种溶液中,产生白色沉淀的是氯化钙,无现象的是氢氧化钠,可以鉴别;
D.MgCl 溶液能与氢氧化钠溶液产生白色沉淀,能与碳酸钾溶液产生白色沉淀,
2
在等量的情况下,由于碳酸镁的溶解度小于氢氧化镁,会产生的沉淀减少,能
区别出来,可以鉴别;
故填:ACD。
【点评】本题考查的是常见的物质的鉴别,完成此题,可以依据已有的知识进行。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2018/12/24 22:29:41;用户:初中化学;邮箱:xdjyhx002@xyh.com;学号:25905210
第28页(共28页)