文档内容
2021年上海市宝山区中考化学二模试卷
一、选择题(共20分)
1.(1分)汞的元素符号是( )
A.Ag B.Hg C.Mg D.He
2.(1分)属于物理变化的是( )
A.食物腐败 B.金属生锈 C.冰雪消融 D.酒精燃烧
3.(1分)灼烧氯化钾时,火焰呈( )
A.紫色 B.黄色 C.蓝色 D.绿色
4.(1分)属于纯净物的是( )
A.矿泉水 B.冰水混合物 C.河水 D.自来水
5.(1分)属于有机物的是( )
A.CO B.CaCO C.H CO D.CH
2 3 2 3 4
6.(1分)下列物质在氧气中燃烧,产生淡蓝色火焰的是( )
A.红磷 B.硫 C.木炭 D.氢气
7.(1分)碘化银(AgI)常用作人工降雨剂,其中碘元素的化合价是( )
A.﹣1 B.+1 C.+2 D.﹣2
8.(1分)CuSO •5H O的俗名是( )
4 2
A.石碱 B.胆矾 C.烧碱 D.纯碱
9.(1分)下列液体中滴加紫色石蕊试液,变红的是( )
A.柠檬水 B.食盐水 C.石灰水 D.蒸馏水
10.(1分)与石墨互为同素异形体的是( )
A.碳﹣60 B.活性炭 C.炭黑 D.一氧化碳
11.(1分)有关物质的命名正确的是( )
A.HNO ﹣﹣硝酸氢 B.N O ﹣﹣氧化氮
3 2 5
C.Fe(OH) ﹣﹣氢氧化铁 D.NaHCO ﹣﹣碳酸氢钠
2 3
12.(1分)下列物质可做复合肥的是( )
A.(NH ) PO B.NH NO C.K SO D.CO(NH )
4 3 4 4 3 2 4 2 2
13.(1分)工业上常把液态燃料喷成雾状,从而提高燃料的利用率,其原理是( )
A.使可燃物分子变小
B.增加空气中的氧气含量
第1页(共19页)C.增大可燃物与氧气的接触面积
D.降低可燃物着火点
14.(1分)鉴别稀盐酸和稀硫酸,可选用的试剂是( )
A.酚酞试液 B.锌粒 C.NaOH溶液 D.Ba(NO )
3 2
第15~17题,每题有一个或两个正确选项
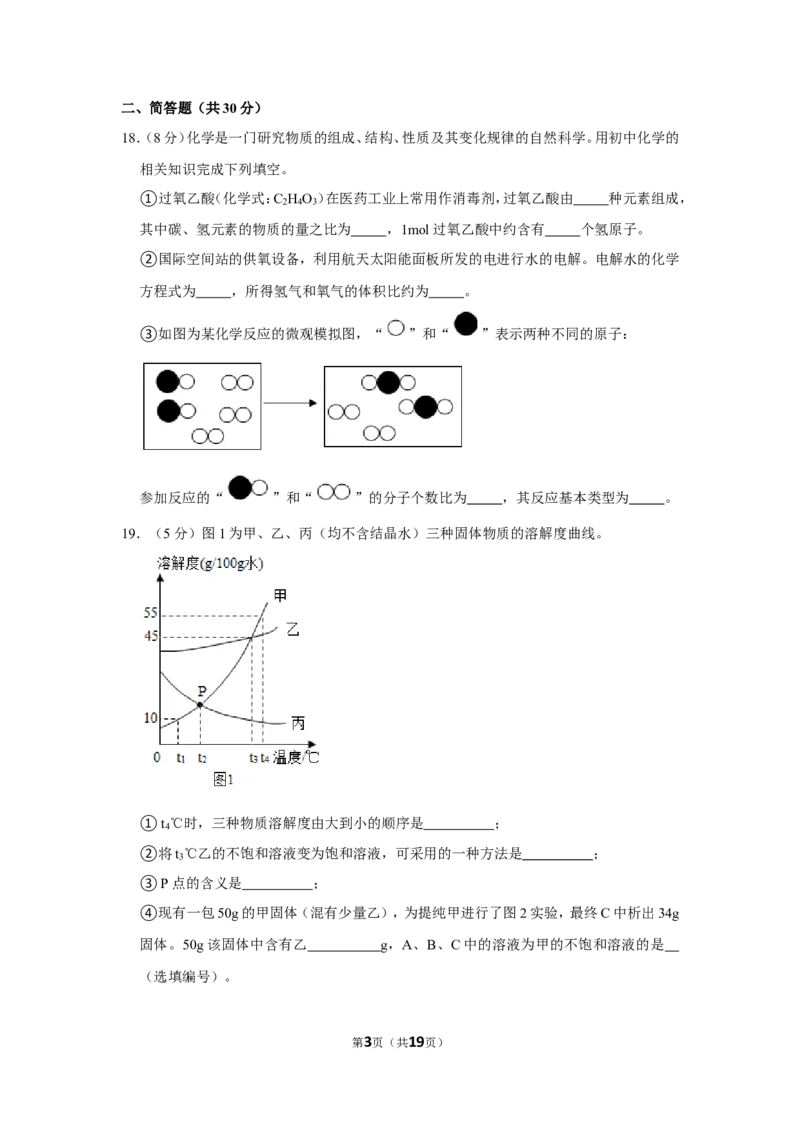
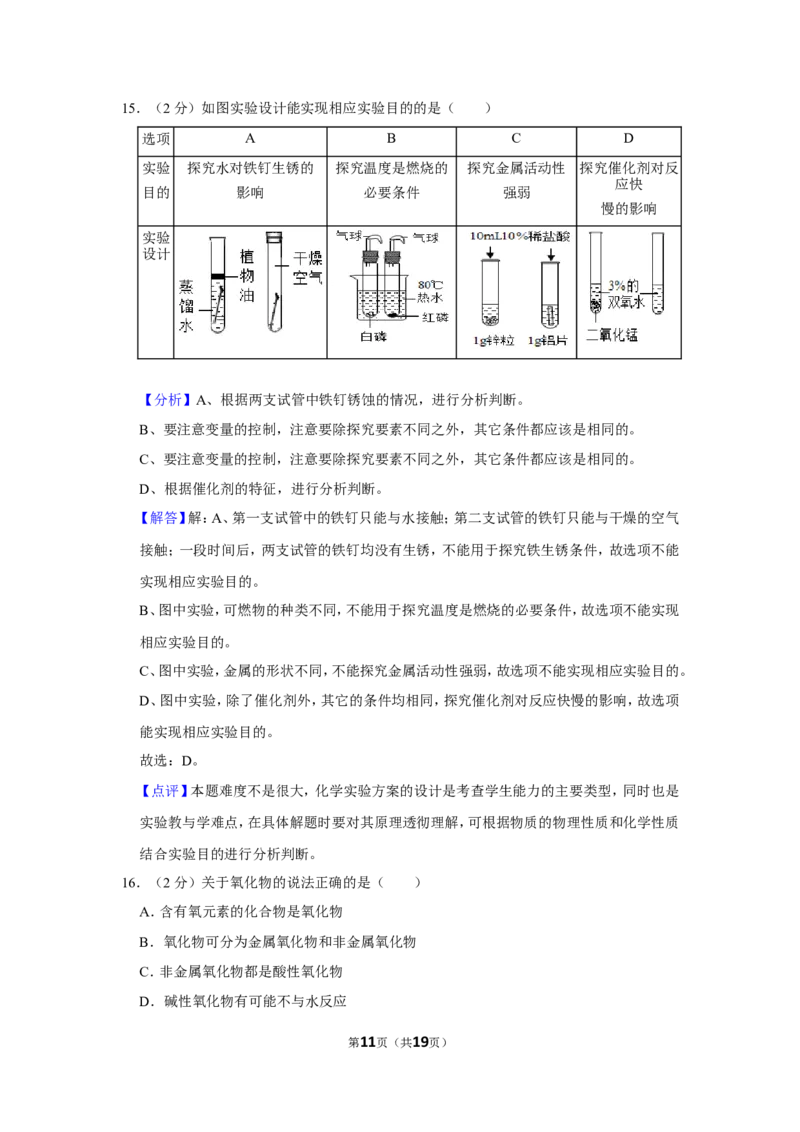
15.(2分)如图实验设计能实现相应实验目的的是( )
选项 A B C D
实验 探究水对铁钉生锈的 探究温度是燃烧的 探究金属活动性 探究催化剂对反
应快
目的 影响 必要条件 强弱
慢的影响
实验
设计
A.A B.B C.C D.D
16.(2分)关于氧化物的说法正确的是( )
A.含有氧元素的化合物是氧化物
B.氧化物可分为金属氧化物和非金属氧化物
C.非金属氧化物都是酸性氧化物
D.碱性氧化物有可能不与水反应
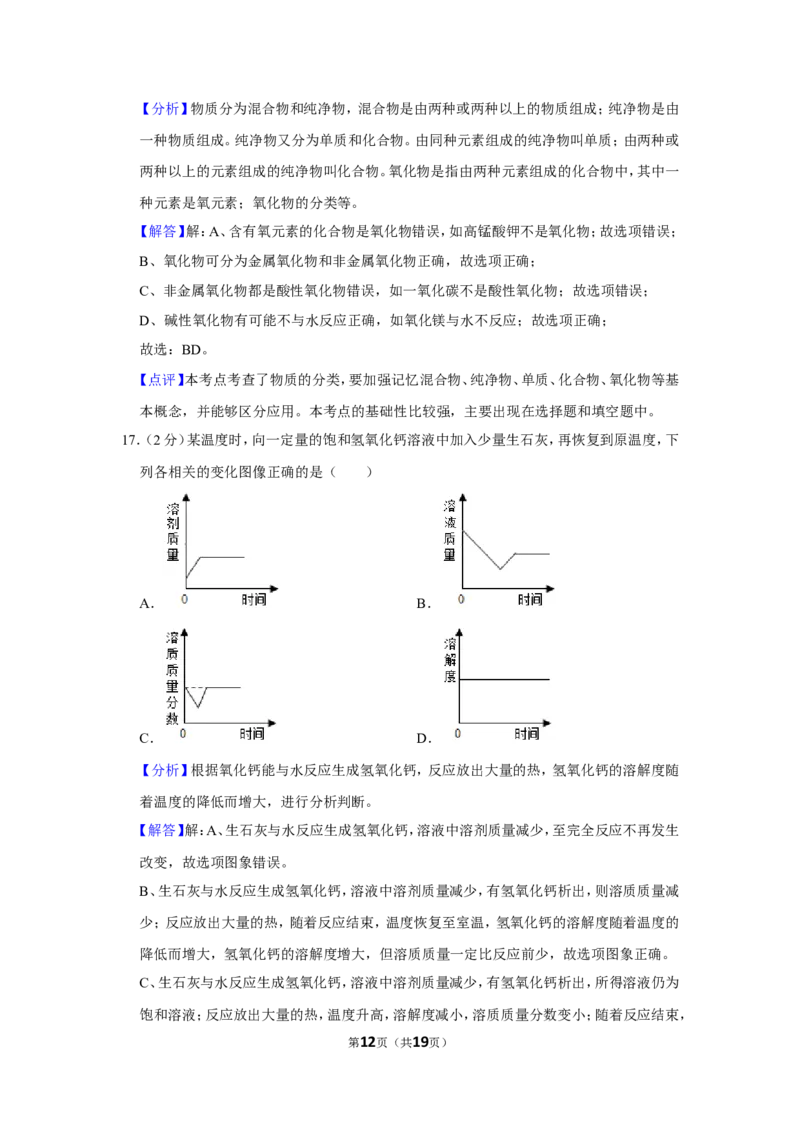
17.(2分)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,再恢复到原温度,下
列各相关的变化图像正确的是( )
A. B.
C. D.
第2页(共19页)二、简答题(共30分)
18.(8分)化学是一门研究物质的组成、结构、性质及其变化规律的自然科学。用初中化学的
相关知识完成下列填空。
①过氧乙酸(化学式:C H O )在医药工业上常用作消毒剂,过氧乙酸由 种元素组成,
2 4 3
其中碳、氢元素的物质的量之比为 ,1mol过氧乙酸中约含有 个氢原子。
②国际空间站的供氧设备,利用航天太阳能面板所发的电进行水的电解。电解水的化学
方程式为 ,所得氢气和氧气的体积比约为 。
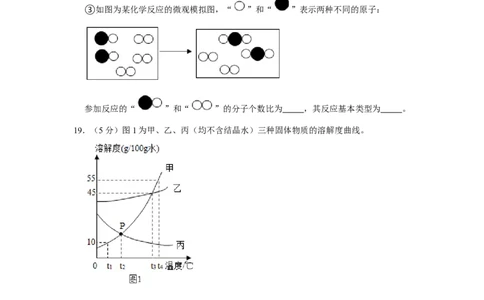
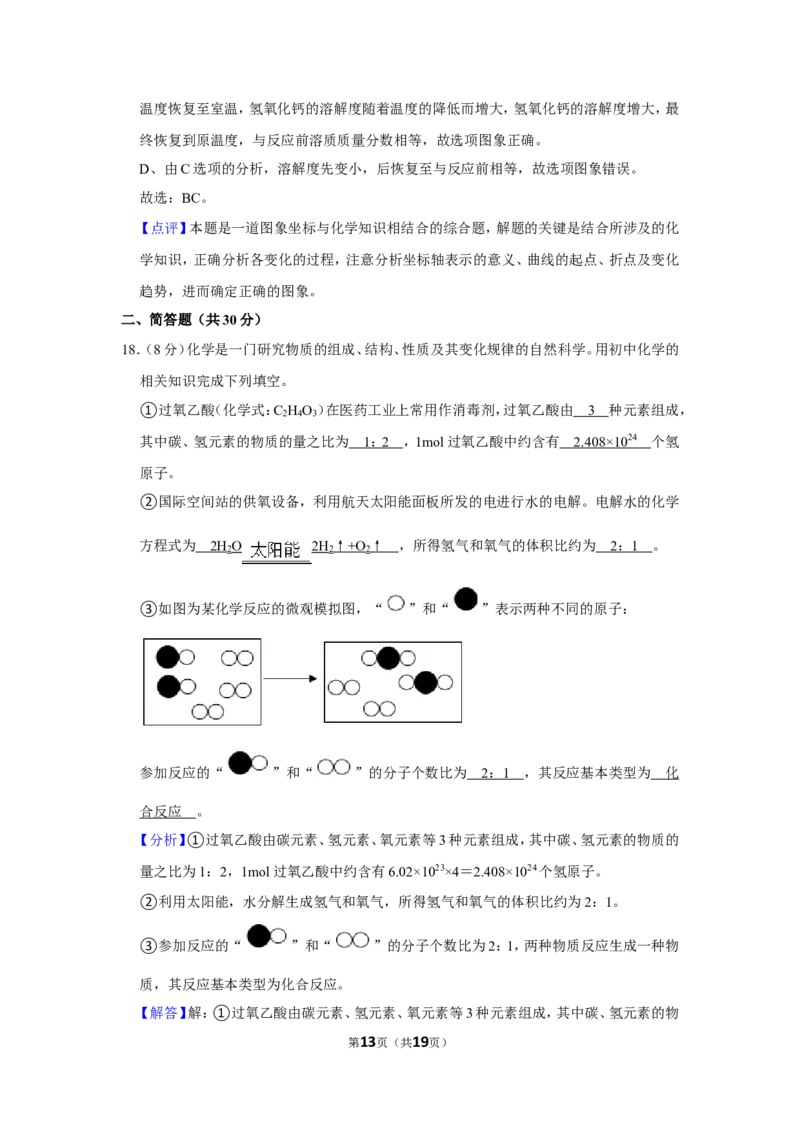
③如图为某化学反应的微观模拟图,“ ”和“ ”表示两种不同的原子:
参加反应的“ ”和“ ”的分子个数比为 ,其反应基本类型为 。
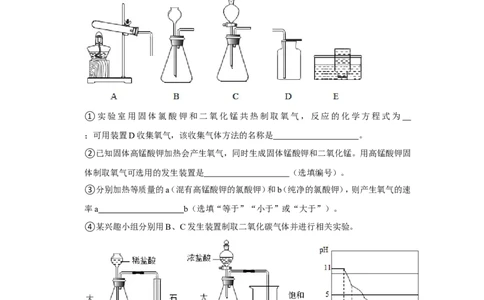
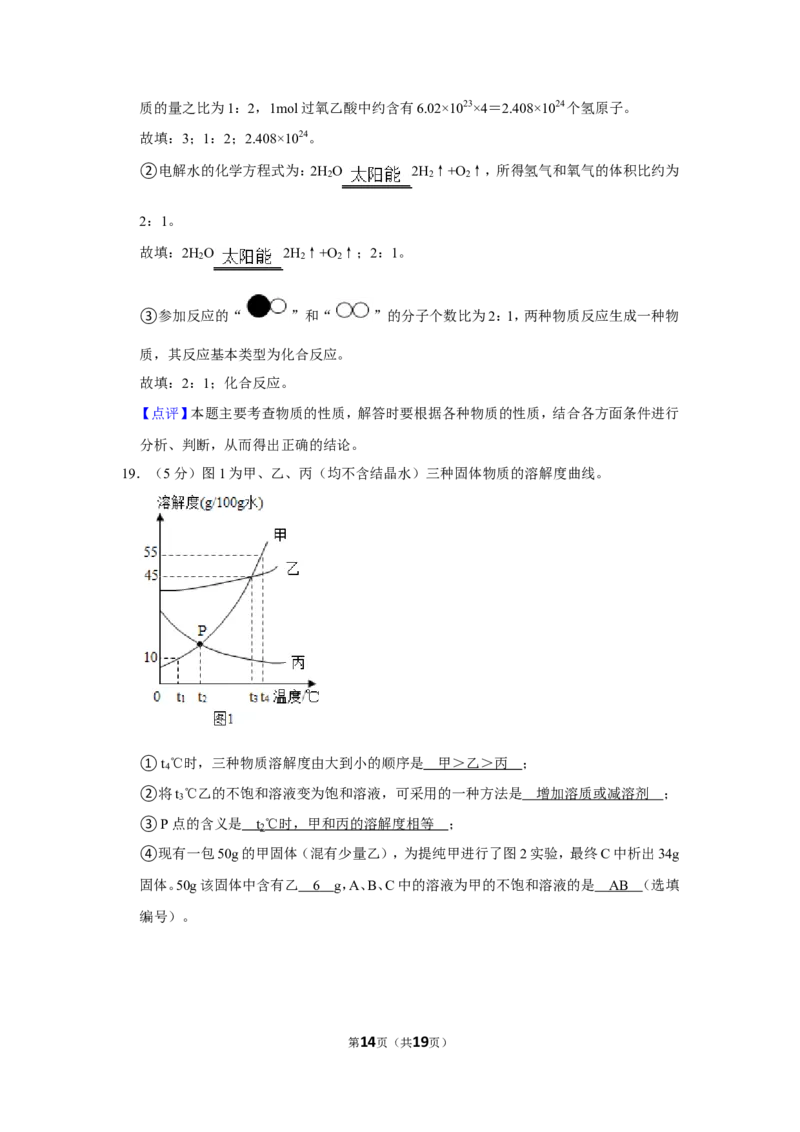
19.(5分)图1为甲、乙、丙(均不含结晶水)三种固体物质的溶解度曲线。
①t ℃时,三种物质溶解度由大到小的顺序是 ;
4
②将t ℃乙的不饱和溶液变为饱和溶液,可采用的一种方法是 ;
3
③P点的含义是 ;
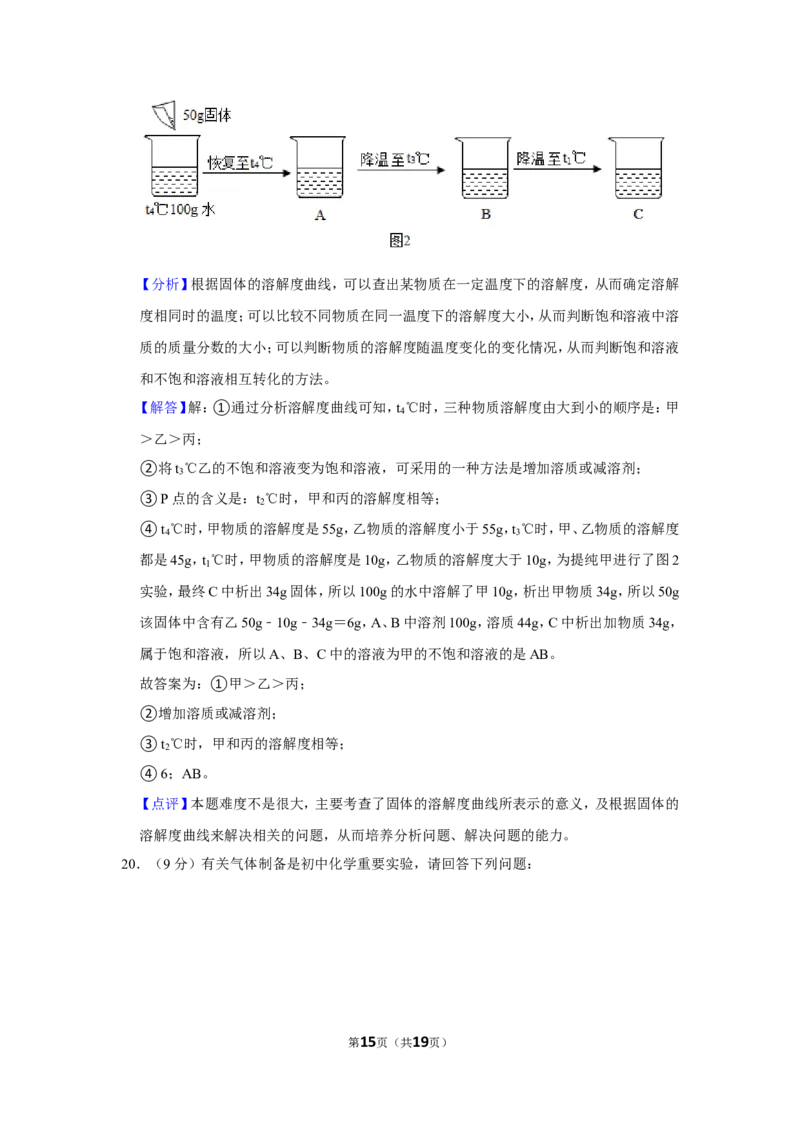
④现有一包50g的甲固体(混有少量乙),为提纯甲进行了图2实验,最终C中析出34g
固体。50g该固体中含有乙 g,A、B、C中的溶液为甲的不饱和溶液的是
(选填编号)。
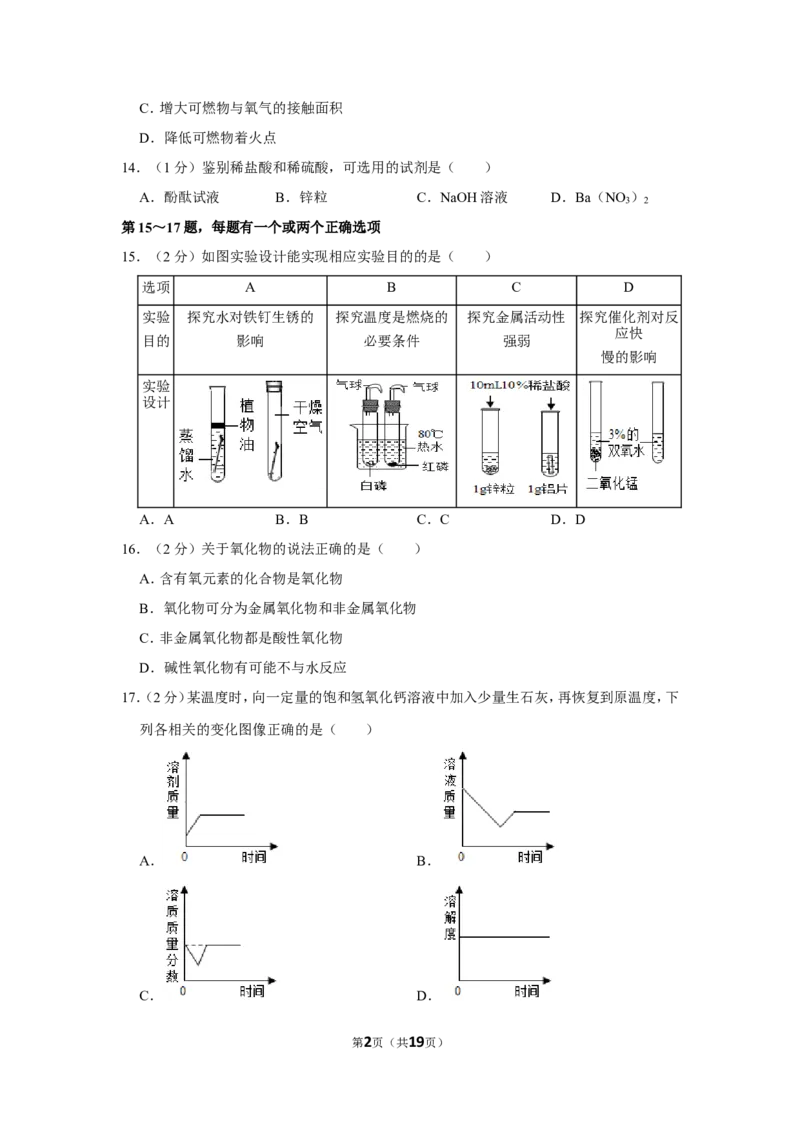
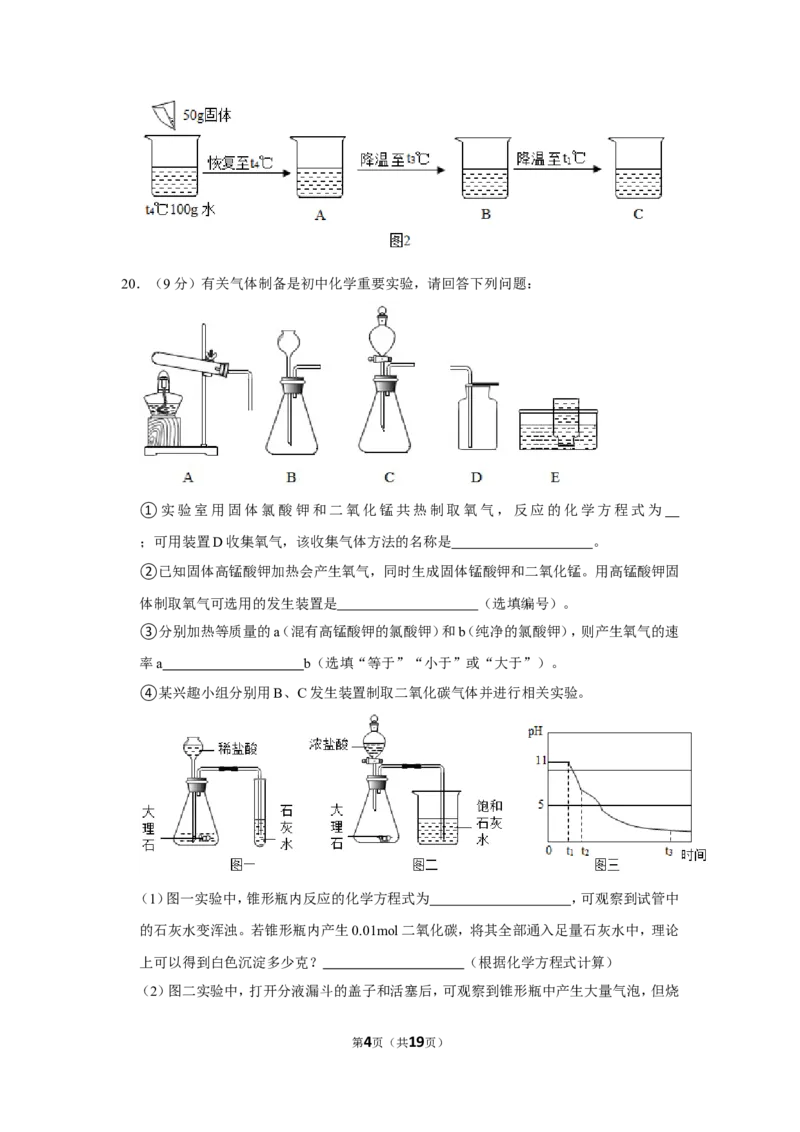
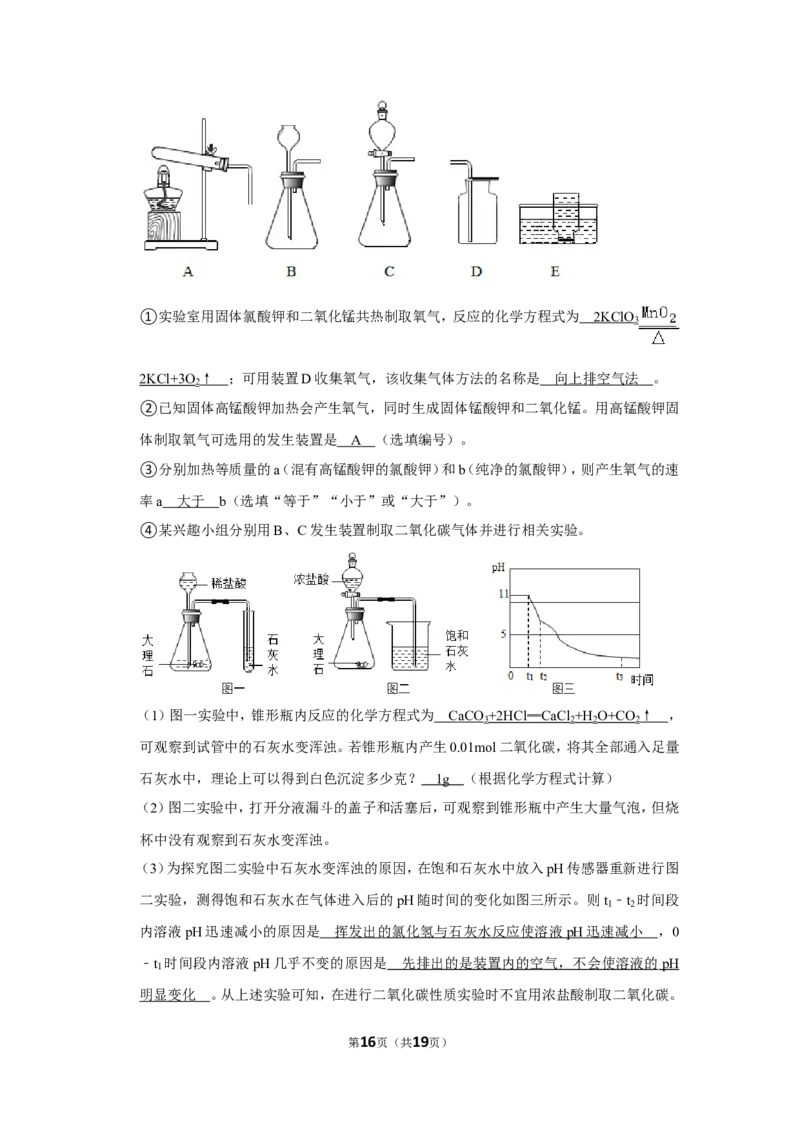
第3页(共19页)20.(9分)有关气体制备是初中化学重要实验,请回答下列问题:
①实验室用固体氯酸钾和二氧化锰共热制取氧气,反应的化学方程式为
;可用装置D收集氧气,该收集气体方法的名称是 。
②已知固体高锰酸钾加热会产生氧气,同时生成固体锰酸钾和二氧化锰。用高锰酸钾固
体制取氧气可选用的发生装置是 (选填编号)。
③分别加热等质量的a(混有高锰酸钾的氯酸钾)和b(纯净的氯酸钾),则产生氧气的速
率a b(选填“等于”“小于”或“大于”)。
④某兴趣小组分别用B、C发生装置制取二氧化碳气体并进行相关实验。
(1)图一实验中,锥形瓶内反应的化学方程式为 ,可观察到试管中
的石灰水变浑浊。若锥形瓶内产生0.01mol二氧化碳,将其全部通入足量石灰水中,理论
上可以得到白色沉淀多少克? (根据化学方程式计算)
(2)图二实验中,打开分液漏斗的盖子和活塞后,可观察到锥形瓶中产生大量气泡,但烧
第4页(共19页)杯中没有观察到石灰水变浑浊。
(3)为探究图二实验中石灰水变浑浊的原因,在饱和石灰水中放入pH传感器重新进行图
二实验,测得饱和石灰水在气体进入后的pH随时间的变化如图三所示。则t ﹣t 时间段
1 2
内溶液pH迅速减小的原因是 ,0﹣t 时间段内溶液pH几乎不变的
1
原因是 。从上述实验可知,在进行二氧化碳性质实验时不宜用浓盐
酸制取二氧化碳。
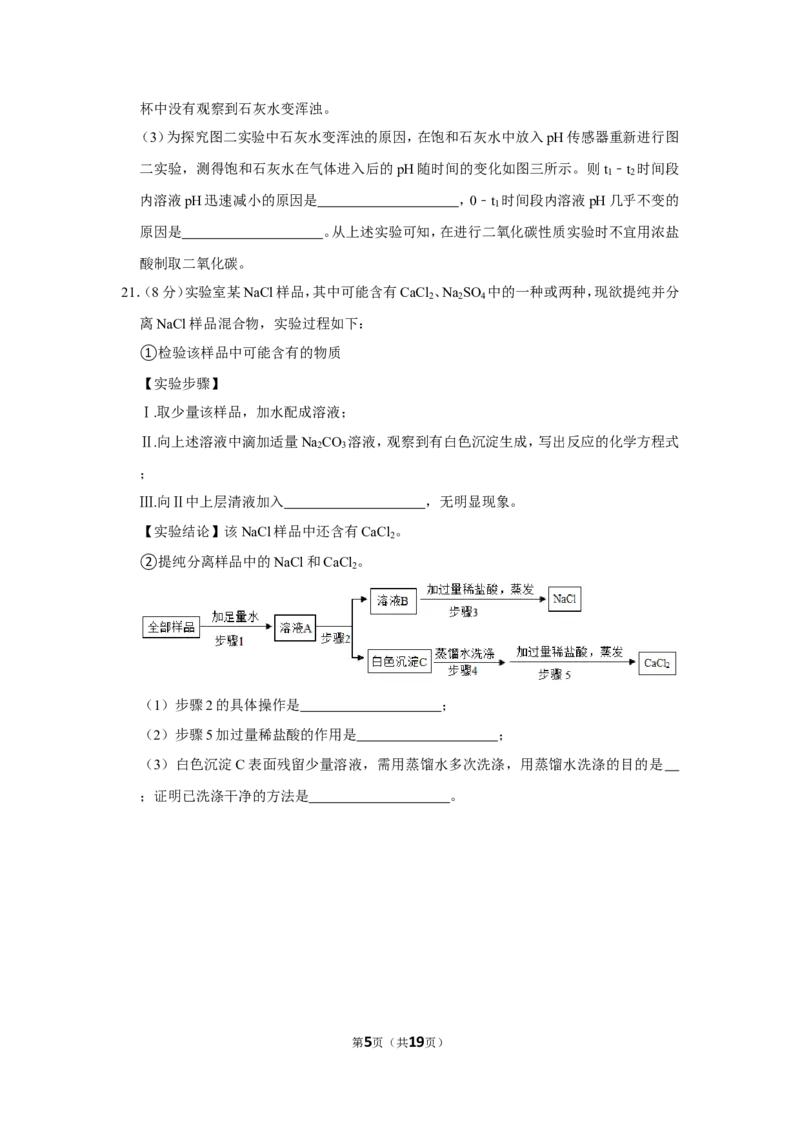
21.(8分)实验室某NaCl样品,其中可能含有CaCl 、Na SO 中的一种或两种,现欲提纯并分
2 2 4
离NaCl样品混合物,实验过程如下:
①检验该样品中可能含有的物质
【实验步骤】
Ⅰ.取少量该样品,加水配成溶液;
Ⅱ.向上述溶液中滴加适量Na CO 溶液,观察到有白色沉淀生成,写出反应的化学方程式
2 3
;
Ⅲ.向Ⅱ中上层清液加入 ,无明显现象。
【实验结论】该NaCl样品中还含有CaCl 。
2
②提纯分离样品中的NaCl和CaCl 。
2
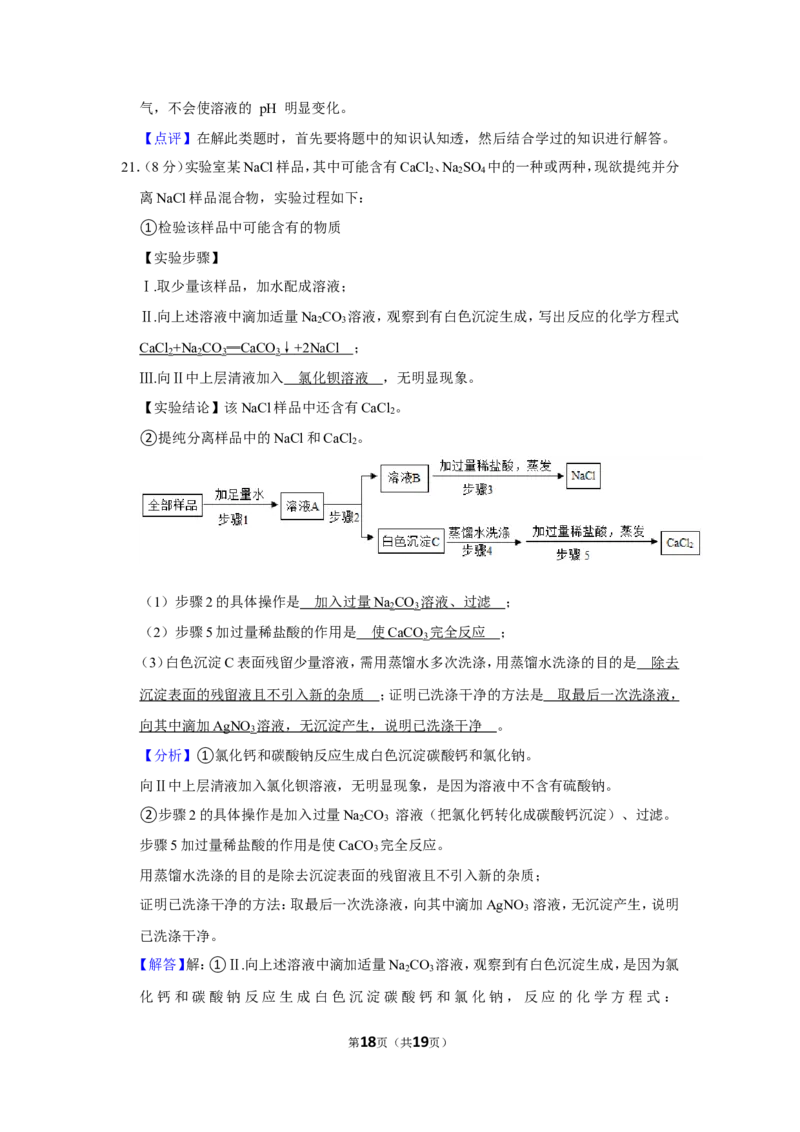
(1)步骤2的具体操作是 ;
(2)步骤5加过量稀盐酸的作用是 ;
(3)白色沉淀C表面残留少量溶液,需用蒸馏水多次洗涤,用蒸馏水洗涤的目的是
;证明已洗涤干净的方法是 。
第5页(共19页)2021年上海市宝山区中考化学二模试卷
参考答案与试题解析
一、选择题(共20分)
1.(1分)汞的元素符号是( )
A.Ag B.Hg C.Mg D.He
【分析】书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表
示的元素符号,第一个字母大写,第二个字母小写。
【解答】解:书写元素符号注意“一大二小”,汞的元素符号是Hg。
故选:B。
【点评】本题难度不大,考查元素符号的书写方法(“一大二小”),熟记常见的元素符号
是正确解答本题的关键。
2.(1分)属于物理变化的是( )
A.食物腐败 B.金属生锈 C.冰雪消融 D.酒精燃烧
【分析】有新物质生成的变化叫化学变化,食物腐败、金属生锈、酒精燃烧都属于化学变化;
没有新物质生成的变化叫物理变化。化学变化的特征是:有新物质生成。判断物理变化和
化学变化的依据是:是否有新物质生成。
【解答】解:A、食物腐败生成有害物质,属于化学变化;故选项错误;
B、金属生锈,铁锈是新物质,属于化学变化;故选项错误;
C、冰雪消融没有新物质生成,属于物理变化;故选项正确;
D、酒精燃烧生成二氧化碳和水,属于化学变化;故选项错误;
故选:C。
【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否
有新物质生成,问题就很容易解决。本考点主要出现在选择题和填空题中。
3.(1分)灼烧氯化钾时,火焰呈( )
A.紫色 B.黄色 C.蓝色 D.绿色
【分析】根据钾元素的焰色反应是紫色进行分析。
【解答】解:钾元素的焰色反应是紫色,所以灼烧氯化钾时,火焰呈紫色,故选:A。
【点评】本题主要考查了常见元素的焰色反应颜色,难度不大,在平时的学习中加强记忆
即可完成。
第6页(共19页)4.(1分)属于纯净物的是( )
A.矿泉水 B.冰水混合物 C.河水 D.自来水
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由
一种物质组成。纯净物又分为单质和化合物。由同种元素组成的纯净物叫单质;由两种或
两种以上的元素组成的纯净物叫化合物。氧化物是指由两种元素组成的化合物中,其中一
种元素是氧元素。
【解答】解:A、矿泉水中含有矿物质,属于混合物;故选项错误;
B、冰水混合物只是状态上的混合,属于纯净物;故选项正确;
C、河水中含有很多杂质以及微生物等,属于混合物;故选项错误;
D、自来水中含有消毒剂等,属于混合物;故选项错误;
故选:B。
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物等基本概念,
并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
5.(1分)属于有机物的是( )
A.CO B.CaCO C.H CO D.CH
2 3 2 3 4
【分析】根据含有碳元素的化合物叫有机化合物,简称有机物;不含碳元素的化合物叫无
机化合物;碳的氧化物、碳酸盐、碳酸虽含碳元素,但其性质与无机物类似,因此把它们看
作无机物;进行分析判断。
【解答】解:A、二氧化碳是碳的氧化物,由于化学性质与无机物相似,归为无机物,不属于
有机物;故A错;
B、碳酸钙虽然是含碳的化合物,由于化学性质与无机物相似,归为无机物,不属于有机物;
故B错;
C、碳酸虽然是含碳的化合物,由于化学性质与无机物相似,归为无机物,不属于有机物;
故C错误;
D、甲烷由碳、氢两种元素组成,属于有机物,故D正确。
故选:D。
【点评】本题难度不大,考查有机物与无机物的判别,抓住有机物与无机物的特征是正确
解答本题的关键。
6.(1分)下列物质在氧气中燃烧,产生淡蓝色火焰的是( )
A.红磷 B.硫 C.木炭 D.氢气
【分析】A、根据红磷在氧气中燃烧的现象进行分析判断.
第7页(共19页)B、根据硫在氧气中燃烧的现象进行分析判断.
C、根据木炭在氧气中燃烧的现象进行分析判断.
D、根据氢气在氧气中燃烧的现象进行分析判断.
【解答】解:A、红磷在氧气中燃烧,产生大量的白烟,故错误。
B、硫在氧气中燃烧,发出明亮的蓝紫色火焰,故错误。
C、木炭在氧气中燃烧,发出白光,故错误。
D、氢气在氧气中燃烧,淡蓝色火焰,故正确。
故选:D。
【点评】本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象
时,需要注意光和火焰、烟和雾的区别.
7.(1分)碘化银(AgI)常用作人工降雨剂,其中碘元素的化合价是( )
A.﹣1 B.+1 C.+2 D.﹣2
【分析】根据在化合物中正负化合价代数和为零,结合碘化银的化学式进行解答本题.
【解答】解:银元素显+1价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为
零,可得:(+1)+x=0,则x=﹣1价。
故选:A。
【点评】本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解
答.
8.(1分)CuSO •5H O的俗名是( )
4 2
A.石碱 B.胆矾 C.烧碱 D.纯碱
【分析】根据常见化学物质的名称、俗称、化学式,进行分析判断即可。
【解答】解:A、石碱是十水合碳酸钠的俗称,其化学式为:Na CO •10H O,故选项错误。
2 3 2
B、CuSO •5H O的俗名胆矾或蓝矾,故选项正确。
4 2
C、烧碱是氢氧化钠的俗称,故选项错误。
D、纯碱是碳酸钠的俗称,故选项错误。
故选:B。
【点评】本题难度不大,熟练掌握常见化学物质(特别是常见的酸碱盐)的名称、俗称、化学
式是正确解答此类题的关键。
9.(1分)下列液体中滴加紫色石蕊试液,变红的是( )
A.柠檬水 B.食盐水 C.石灰水 D.蒸馏水
【分析】石蕊试液遇酸性溶液变红,因此不能使石蕊变红则是溶液不显酸性。
第8页(共19页)【解答】解:A、柠檬水呈酸性,能使石蕊变红,故正确;
B、食盐水是氯化钠溶液,呈中性,石蕊不变色,故错误;
C、石灰水是氢氧化钙溶液,呈碱性,能使石蕊变蓝,故错误;
B、蒸馏水呈中性,石蕊不变色,故错误;
故选:A。
【点评】本题主要考查溶液的酸碱性和酸碱指示剂的变色情况,属于基础考查。
10.(1分)与石墨互为同素异形体的是( )
A.碳﹣60 B.活性炭 C.炭黑 D.一氧化碳
【分析】由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以
下两个条件:同种元素形成,不同单质;据此进行分析判断。
【解答】解:判断同素异形体的关键把握两点:①同种元素形成,②不同单质。
石墨、金刚石、碳﹣60是由碳元素形成的不同单质,互为同素异形体。
故选:A。
【点评】本题难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,
②不同单质,这是解决此类题的关键之所在。
11.(1分)有关物质的命名正确的是( )
A.HNO ﹣﹣硝酸氢 B.N O ﹣﹣氧化氮
3 2 5
C.Fe(OH) ﹣﹣氢氧化铁 D.NaHCO ﹣﹣碳酸氢钠
2 3
【分析】化合物化学式的读法:一般是从右向左读,读作“某化某”或“某酸某”等,进行
分析判断。
【解答】解:A、HNO 读作硝酸,故选项说法错误。
3
B、N O 从右向左读,读作五氧化二氮,故选项说法错误。
2 5
C、Fe(OH)中铁元素显+2价,氢氧根显﹣1价,从右向左读,读作氢氧化亚铁,故选项说
2
法错误。
D、NaHCO 从右向左读,读作碳酸氢钠,故选项说法正确。
3
故选:D。
【点评】本题难度不大,掌握化合物化学式的读法是正确解答本题的关键。
12.(1分)下列物质可做复合肥的是( )
A.(NH ) PO B.NH NO C.K SO D.CO(NH )
4 3 4 4 3 2 4 2 2
【分析】含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称
为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。
第9页(共19页)【解答】解:A、(NH ) PO 中含有磷元素和氮元素,属于复合肥,故选项正确。
4 3 4
B、NH NO 中含有氮元素,属于氮肥,故选项错误。
4 3
C、K SO 中含有钾元素,属于钾肥,故选项错误。
2 4
D、CO(NH ) 中含有氮元素,属于氮肥,故选项错误。
2 2
故选:A。
【点评】本题难度不大,主要考查化肥的分类方面的知识,确定化肥中营养元素的种类、化
肥的分类方法是正确解答此类题的关键。
13.(1分)工业上常把液态燃料喷成雾状,从而提高燃料的利用率,其原理是( )
A.使可燃物分子变小
B.增加空气中的氧气含量
C.增大可燃物与氧气的接触面积
D.降低可燃物着火点
【分析】根据物质的变化和使燃料充分燃烧的因素分析有关有关的说法。
【解答】解:A、把液态燃料喷成雾状,可燃物分子的大小没有变化,故A错误;
B、空气中的氧气含量一般不变,故B错误;
C、把液态燃料喷成雾状,增大可燃物与氧气的接触面积,故C正确;
D、可燃物着火点属于物质的属性,一般不会改变,故D错误。
故选:C。
【点评】本题的难度不大,了解物质的变化特征、使燃料充分燃烧的因素即可分析解答。
14.(1分)鉴别稀盐酸和稀硫酸,可选用的试剂是( )
A.酚酞试液 B.锌粒 C.NaOH溶液 D.Ba(NO )
3 2
【分析】根据盐酸与硫酸的不同性质分析回答此题。
【解答】解:A、稀盐酸和稀硫酸都是酸,加入酚酞都不变色,选项A不符合题意;
B、锌与盐酸和硫酸都发生反应生成氢气,看到气泡,无法区分两种酸,选项B不符合题意;
C、稀盐酸和稀硫酸都是酸,与氢氧化钠都发生反应生成盐和水,无明显现象,无法区分两
种酸,选项C不符合题意;
D、稀硫酸与硝酸钡反应生成硫酸钡沉淀和硝酸,而稀盐酸与硝酸钡不反应,无明显现象,
可以区分两种酸,选项D符合题意;
故选:D。
【点评】在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答
第15~17题,每题有一个或两个正确选项
第10页(共19页)15.(2分)如图实验设计能实现相应实验目的的是( )
选项 A B C D
实验 探究水对铁钉生锈的 探究温度是燃烧的 探究金属活动性 探究催化剂对反
应快
目的 影响 必要条件 强弱
慢的影响
实验
设计
【分析】A、根据两支试管中铁钉锈蚀的情况,进行分析判断。
B、要注意变量的控制,注意要除探究要素不同之外,其它条件都应该是相同的。
C、要注意变量的控制,注意要除探究要素不同之外,其它条件都应该是相同的。
D、根据催化剂的特征,进行分析判断。
【解答】解:A、第一支试管中的铁钉只能与水接触;第二支试管的铁钉只能与干燥的空气
接触;一段时间后,两支试管的铁钉均没有生锈,不能用于探究铁生锈条件,故选项不能
实现相应实验目的。
B、图中实验,可燃物的种类不同,不能用于探究温度是燃烧的必要条件,故选项不能实现
相应实验目的。
C、图中实验,金属的形状不同,不能探究金属活动性强弱,故选项不能实现相应实验目的。
D、图中实验,除了催化剂外,其它的条件均相同,探究催化剂对反应快慢的影响,故选项
能实现相应实验目的。
故选:D。
【点评】本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是
实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质
结合实验目的进行分析判断。
16.(2分)关于氧化物的说法正确的是( )
A.含有氧元素的化合物是氧化物
B.氧化物可分为金属氧化物和非金属氧化物
C.非金属氧化物都是酸性氧化物
D.碱性氧化物有可能不与水反应
第11页(共19页)【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由
一种物质组成。纯净物又分为单质和化合物。由同种元素组成的纯净物叫单质;由两种或
两种以上的元素组成的纯净物叫化合物。氧化物是指由两种元素组成的化合物中,其中一
种元素是氧元素;氧化物的分类等。
【解答】解:A、含有氧元素的化合物是氧化物错误,如高锰酸钾不是氧化物;故选项错误;
B、氧化物可分为金属氧化物和非金属氧化物正确,故选项正确;
C、非金属氧化物都是酸性氧化物错误,如一氧化碳不是酸性氧化物;故选项错误;
D、碱性氧化物有可能不与水反应正确,如氧化镁与水不反应;故选项正确;
故选:BD。
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基
本概念,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
17.(2分)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,再恢复到原温度,下
列各相关的变化图像正确的是( )
A. B.
C. D.
【分析】根据氧化钙能与水反应生成氢氧化钙,反应放出大量的热,氢氧化钙的溶解度随
着温度的降低而增大,进行分析判断。
【解答】解:A、生石灰与水反应生成氢氧化钙,溶液中溶剂质量减少,至完全反应不再发生
改变,故选项图象错误。
B、生石灰与水反应生成氢氧化钙,溶液中溶剂质量减少,有氢氧化钙析出,则溶质质量减
少;反应放出大量的热,随着反应结束,温度恢复至室温,氢氧化钙的溶解度随着温度的
降低而增大,氢氧化钙的溶解度增大,但溶质质量一定比反应前少,故选项图象正确。
C、生石灰与水反应生成氢氧化钙,溶液中溶剂质量减少,有氢氧化钙析出,所得溶液仍为
饱和溶液;反应放出大量的热,温度升高,溶解度减小,溶质质量分数变小;随着反应结束,
第12页(共19页)温度恢复至室温,氢氧化钙的溶解度随着温度的降低而增大,氢氧化钙的溶解度增大,最
终恢复到原温度,与反应前溶质质量分数相等,故选项图象正确。
D、由C选项的分析,溶解度先变小,后恢复至与反应前相等,故选项图象错误。
故选:BC。
【点评】本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化
学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化
趋势,进而确定正确的图象。
二、简答题(共30分)
18.(8分)化学是一门研究物质的组成、结构、性质及其变化规律的自然科学。用初中化学的
相关知识完成下列填空。
①过氧乙酸(化学式:C H O )在医药工业上常用作消毒剂,过氧乙酸由 3 种元素组成,
2 4 3
其中碳、氢元素的物质的量之比为 1 : 2 ,1mol过氧乙酸中约含有 2.408×1 0 2 4 个氢
原子。
②国际空间站的供氧设备,利用航天太阳能面板所发的电进行水的电解。电解水的化学
方程式为 2H O 2H ↑ +O ↑ ,所得氢气和氧气的体积比约为 2 : 1 。
2 2 2
③如图为某化学反应的微观模拟图,“ ”和“ ”表示两种不同的原子:
参加反应的“ ”和“ ”的分子个数比为 2 : 1 ,其反应基本类型为 化
合反应 。
【分析】①过氧乙酸由碳元素、氢元素、氧元素等3种元素组成,其中碳、氢元素的物质的
量之比为1:2,1mol过氧乙酸中约含有6.02×1023×4=2.408×1024个氢原子。
②利用太阳能,水分解生成氢气和氧气,所得氢气和氧气的体积比约为2:1。
③参加反应的“ ”和“ ”的分子个数比为2:1,两种物质反应生成一种物
质,其反应基本类型为化合反应。
【解答】解:①过氧乙酸由碳元素、氢元素、氧元素等3种元素组成,其中碳、氢元素的物
第13页(共19页)质的量之比为1:2,1mol过氧乙酸中约含有6.02×1023×4=2.408×1024个氢原子。
故填:3;1:2;2.408×1024。
②电解水的化学方程式为:2H O 2H ↑+O ↑,所得氢气和氧气的体积比约为
2 2 2
2:1。
故填:2H O 2H ↑+O ↑;2:1。
2 2 2
③参加反应的“ ”和“ ”的分子个数比为2:1,两种物质反应生成一种物
质,其反应基本类型为化合反应。
故填:2:1;化合反应。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
19.(5分)图1为甲、乙、丙(均不含结晶水)三种固体物质的溶解度曲线。
①t ℃时,三种物质溶解度由大到小的顺序是 甲>乙>丙 ;
4
②将t ℃乙的不饱和溶液变为饱和溶液,可采用的一种方法是 增加溶质或减溶剂 ;
3
③P点的含义是 t ℃时,甲和丙的溶解度相等 ;
2
④现有一包50g的甲固体(混有少量乙),为提纯甲进行了图2实验,最终C中析出34g
固体。50g该固体中含有乙 6 g,A、B、C中的溶液为甲的不饱和溶液的是 AB (选填
编号)。
第14页(共19页)【分析】根据固体的溶解度曲线,可以查出某物质在一定温度下的溶解度,从而确定溶解
度相同时的温度;可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶
质的质量分数的大小;可以判断物质的溶解度随温度变化的变化情况,从而判断饱和溶液
和不饱和溶液相互转化的方法。
【解答】解:①通过分析溶解度曲线可知,t ℃时,三种物质溶解度由大到小的顺序是:甲
4
>乙>丙;
②将t ℃乙的不饱和溶液变为饱和溶液,可采用的一种方法是增加溶质或减溶剂;
3
③P点的含义是:t ℃时,甲和丙的溶解度相等;
2
④t ℃时,甲物质的溶解度是55g,乙物质的溶解度小于55g,t ℃时,甲、乙物质的溶解度
4 3
都是45g,t ℃时,甲物质的溶解度是10g,乙物质的溶解度大于10g,为提纯甲进行了图2
1
实验,最终C中析出34g固体,所以100g的水中溶解了甲10g,析出甲物质34g,所以50g
该固体中含有乙50g﹣10g﹣34g=6g,A、B中溶剂100g,溶质44g,C中析出加物质34g,
属于饱和溶液,所以A、B、C中的溶液为甲的不饱和溶液的是AB。
故答案为:①甲>乙>丙;
②增加溶质或减溶剂;
③t ℃时,甲和丙的溶解度相等;
2
④6;AB。
【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的
溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
20.(9分)有关气体制备是初中化学重要实验,请回答下列问题:
第15页(共19页)①实验室用固体氯酸钾和二氧化锰共热制取氧气,反应的化学方程式为 2KClO
3
2KCl+3O ↑ ;可用装置D收集氧气,该收集气体方法的名称是 向上排空气法 。
2
②已知固体高锰酸钾加热会产生氧气,同时生成固体锰酸钾和二氧化锰。用高锰酸钾固
体制取氧气可选用的发生装置是 A (选填编号)。
③分别加热等质量的a(混有高锰酸钾的氯酸钾)和b(纯净的氯酸钾),则产生氧气的速
率a 大于 b(选填“等于”“小于”或“大于”)。
④某兴趣小组分别用B、C发生装置制取二氧化碳气体并进行相关实验。
(1)图一实验中,锥形瓶内反应的化学方程式为 CaCO +2HCl ═ CaCl +H O+CO ↑ ,
3 2 2 2
可观察到试管中的石灰水变浑浊。若锥形瓶内产生0.01mol二氧化碳,将其全部通入足量
石灰水中,理论上可以得到白色沉淀多少克? 1 g (根据化学方程式计算)
(2)图二实验中,打开分液漏斗的盖子和活塞后,可观察到锥形瓶中产生大量气泡,但烧
杯中没有观察到石灰水变浑浊。
(3)为探究图二实验中石灰水变浑浊的原因,在饱和石灰水中放入pH传感器重新进行图
二实验,测得饱和石灰水在气体进入后的pH随时间的变化如图三所示。则t ﹣t 时间段
1 2
内溶液pH迅速减小的原因是 挥发出的氯化氢与石灰水反应使溶液 pH 迅速减小 ,0
﹣t 时间段内溶液pH几乎不变的原因是 先排出的是装置内的空气,不会使溶液的 pH
1
明显变化 。从上述实验可知,在进行二氧化碳性质实验时不宜用浓盐酸制取二氧化碳。
第16页(共19页)【分析】①氯酸钾在二氧化锰催化作用下加热反应生成氯化钾和氧气,据此书写化学方程
式;根据装置特点总结收集气体方法;
②根据反应物状态和反应条件选择反应装置;
③根据高锰酸钾性质分析回答此题;
④(1)盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,据此书写化学方程式;根据化学方
程式计算此题;
(3)根据盐酸性质分析回答此题;根据反应特点分析回答此题。
【解答】解:①氯酸钾在二氧化锰催化作用下加热反应生成氯化钾和氧气,书写化学方程
式注意配平及气体符号,所以化学方程式为2KClO 2KCl+3O ↑;D为向上排空气
3 2
法收集装置,所以采用方法为向上排空气法;
故答案为:2KClO 2KCl+3O ↑;向上排空气法。
3 2
②反应物为固体,且需要加热,故选A为发生装置;
故答案为:A。
③高锰酸钾分解生成二氧化锰,可以加快氯酸钾分解,所以反应速度为a大于b;
故答案为:大于。
④(1)盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,书写化学方程式注意配平及气体符
号,所以化学方程式为 CaCO +2HCl═CaCl +H O+CO ↑;生成二氧化碳质量=
3 2 2 2
0.01mol×44g=0.44g,设碳酸钙的质量为m,
CO +Ca(OH) =CaCO ↓+H O
2 2 3 2
44 100
0.44g m
m=1g
故答案为:CaCO +2HCl═CaCl +H O+CO ↑;1g。
3 2 2 2
(3)浓盐酸具有挥发性,挥发出氯化氢,进气澄清石灰水与氢氧化钙反应,溶液碱性减弱,
pH减小;氯化氢密度比空气大,从底部向上逸出,则上部的空气先排出,此时排出的是空
气,进入溶液不会引起溶液pH的变化;
故答案为:挥发出的氯化氢与石灰水反应使溶液 pH 迅速减小;先排出的是装置内的空
第17页(共19页)气,不会使溶液的 pH 明显变化。
【点评】在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答。
21.(8分)实验室某NaCl样品,其中可能含有CaCl 、Na SO 中的一种或两种,现欲提纯并分
2 2 4
离NaCl样品混合物,实验过程如下:
①检验该样品中可能含有的物质
【实验步骤】
Ⅰ.取少量该样品,加水配成溶液;
Ⅱ.向上述溶液中滴加适量Na CO 溶液,观察到有白色沉淀生成,写出反应的化学方程式
2 3
CaCl +Na CO ═ CaCO ↓ +2NaC l ;
2 2 3 3
Ⅲ.向Ⅱ中上层清液加入 氯化钡溶液 ,无明显现象。
【实验结论】该NaCl样品中还含有CaCl 。
2
②提纯分离样品中的NaCl和CaCl 。
2
(1)步骤2的具体操作是 加入过量 N a CO 溶液、过滤 ;
2 3
(2)步骤5加过量稀盐酸的作用是 使 CaCO 完全反应 ;
3
(3)白色沉淀C表面残留少量溶液,需用蒸馏水多次洗涤,用蒸馏水洗涤的目的是 除去
沉淀表面的残留液且不引入新的杂质 ;证明已洗涤干净的方法是 取最后一次洗涤液,
向其中滴加 AgNO 溶液,无沉淀产生,说明已洗涤干净 。
3
【分析】①氯化钙和碳酸钠反应生成白色沉淀碳酸钙和氯化钠。
向Ⅱ中上层清液加入氯化钡溶液,无明显现象,是因为溶液中不含有硫酸钠。
②步骤2的具体操作是加入过量Na CO 溶液(把氯化钙转化成碳酸钙沉淀)、过滤。
2 3
步骤5加过量稀盐酸的作用是使CaCO 完全反应。
3
用蒸馏水洗涤的目的是除去沉淀表面的残留液且不引入新的杂质;
证明已洗涤干净的方法:取最后一次洗涤液,向其中滴加AgNO
3
溶液,无沉淀产生,说明
已洗涤干净。
【解答】解:①Ⅱ.向上述溶液中滴加适量Na CO 溶液,观察到有白色沉淀生成,是因为氯
2 3
化钙和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,反应的化学方程式:
第18页(共19页)CaCl +Na CO ═CaCO ↓+2NaCl。
2 2 3 3
故填:CaCl +Na CO ═CaCO ↓+2NaCl。
2 2 3 3
Ⅲ.向Ⅱ中上层清液加入氯化钡溶液,无明显现象,是因为溶液中不含有硫酸钠。
故填:氯化钡溶液。
②(1)步骤2的具体操作是加入过量Na CO 溶液(把氯化钙转化成碳酸钙沉淀)、过滤。
2 3
故填:加入过量Na CO 溶液、过滤。
2 3
(2)步骤5加过量稀盐酸的作用是使CaCO 完全反应。
3
故填:使CaCO 完全反应。
3
(3)白色沉淀C表面残留少量溶液,需用蒸馏水多次洗涤,用蒸馏水洗涤的目的是除去沉
淀表面的残留液且不引入新的杂质;
证明已洗涤干净的方法:取最后一次洗涤液,向其中滴加AgNO
3
溶液,无沉淀产生,说明
已洗涤干净。
故填:除去沉淀表面的残留液且不引入新的杂质;取最后一次洗涤液,向其中滴加AgNO
3
溶液,无沉淀产生,说明已洗涤干净。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
第19页(共19页)