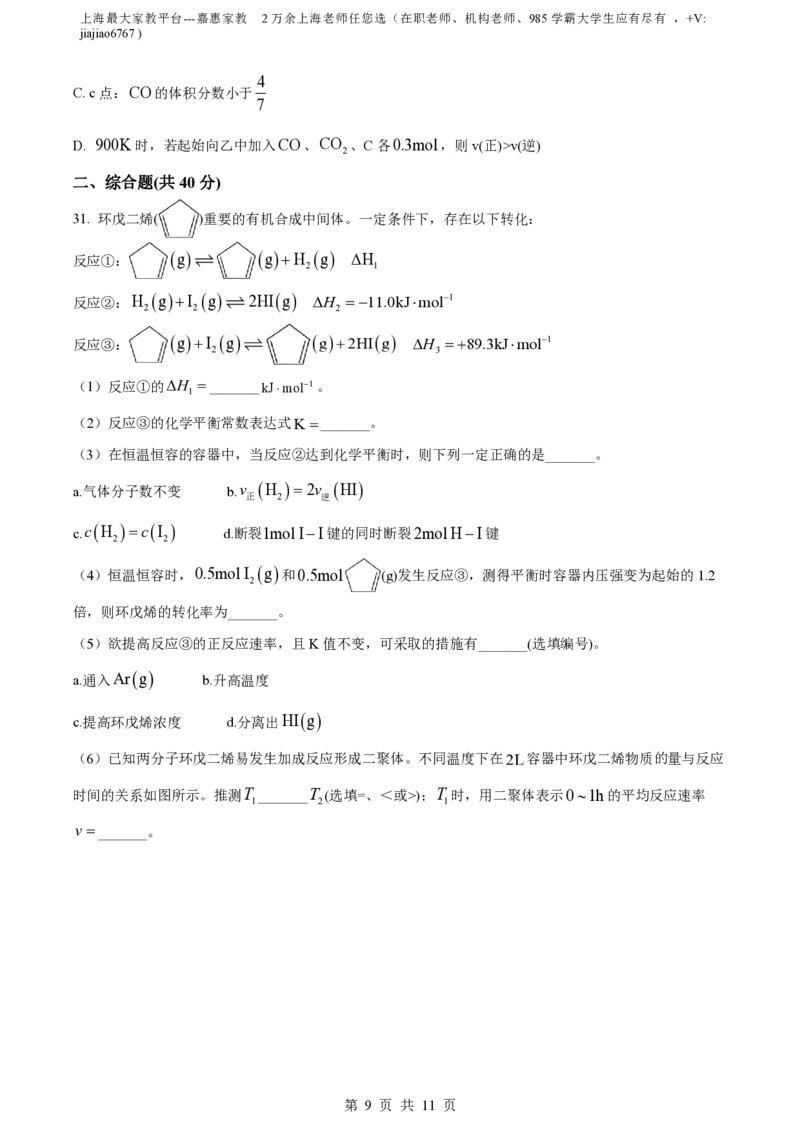文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海市七宝中学 2022 学年第一学期
高二化学期末考试
相对原子质量:H1 C12
一、选择题(共 60分,每题只有一个正确答案)
1. 苏轼的《格物粗谈》中记有:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”。推测文中
的“气”是指
A. 甲烷 B. 乙烯 C. 乙炔 D. 苯
2. 酸碱中和滴定是用来测定
A. 溶液酸碱性 B. 溶液pH C. 酸或碱的浓度 D. 电解质电离程度
3. 下列煤化工过程属于物理变化的是
A. 煤的干馏 B. 煤的液化 C. 煤的气化 D. 煤焦油制苯
4. 石油化工在国民经济中占有极其重要的地位。下列关于石油化工说法正确的是
A. 石油分馏塔的顶部获得重馏分
B. 石油分馏时获得各种馏分均为纯净物
C. 石油裂化主要是为提高轻质液体燃料的产量
D. 石油裂解的原理是将长链烃断裂成短链的烷烃
5. 下列可证明甲烷分子是正四面体结构,而非平面结构的是
A. CH键的键长均相同 B. CH键的键能均相同
C. CH键的键角均相同 D. CH Cl 只有一种结构
2 2
6. 硫酸铵溶液中,离子浓度最大的是
A. NH B. SO2 C. H D. OH
4 4
7. 下列过程或现象与盐类水解无关的是
A. 钢铁在潮湿的环境下易生锈 B. 氯化铵溶液加入镁粉有气泡产生
C. 加热氯化铁溶液颜色变深 D. 硫化钠浓溶液有臭味
8. 下列关于溴乙烷的说法正确的是
A. 电子式为 B. 密度比水小
C. 发生取代反应时CBr键一定会断裂 D. 发生消去反应时CBr键一定会断裂
第 1 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
9. 加热纯水时,下列叙述正确的是
A. pH变小、呈酸性 B. pH不变、呈中性
C. K 变大、呈中性 D. K 变小、呈碱性
w w
10. 下列分子式一定表示纯净物的是
A. C H B. C H C. C H Cl D. C H O
3 6 3 8 3 7 3 8
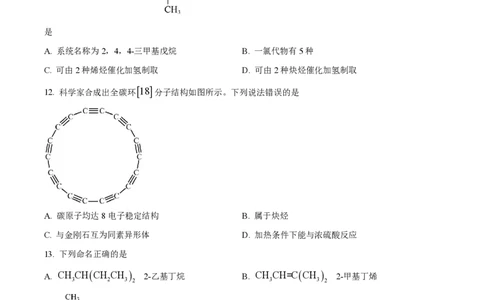
11. 异辛烷( )含量是汽油抗爆性能的重要指标,下列关于异辛烷说法正确的
是
A. 系统名称为2,4,4-三甲基戊烷 B. 一氯代物有5种
C. 可由2种烯烃催化加氢制取 D. 可由2种炔烃催化加氢制取
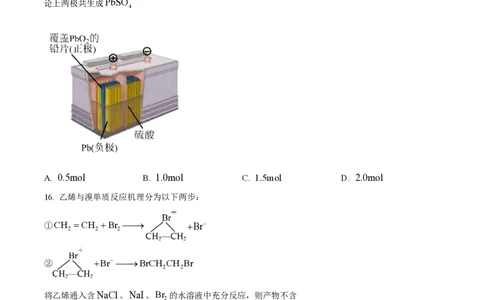
12. 科学家合成出全碳环
18
分子结构如图所示。下列说法错误的是
A. 碳原子均达8电子稳定结构 B. 属于炔烃
C. 与金刚石互为同素异形体 D. 加热条件下能与浓硫酸反应
13. 下列命名正确的是
A. CH CHCH CH 2-乙基丁烷 B. CH CH=CCH 2-甲基丁烯
3 2 3 2 3 3 2
C. 1,2,4-三甲苯 D. CH CH CHCH Br 1-甲基溴丙烷
3 2 3
14. 现代医学证明“痛风”的病因与关节滑液中形成尿酸钠
NaUr
晶体有关,尤其在寒冷季节易诱发关节
疼痛。主要原理为:
①HUr(尿酸)H
2
O
Ur(尿酸离子)H
3
O
第 2 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
②UraqNaaq
NaUrs
下列叙述错误的是
A. ①是尿酸的电离方程式
B. 反应②的H 0,因此热敷能减轻关节疼痛
C. 饮食中摄入过多食盐,容易诱发痛风
D. “痛风”患者应控制摄入产生较多尿酸的食物
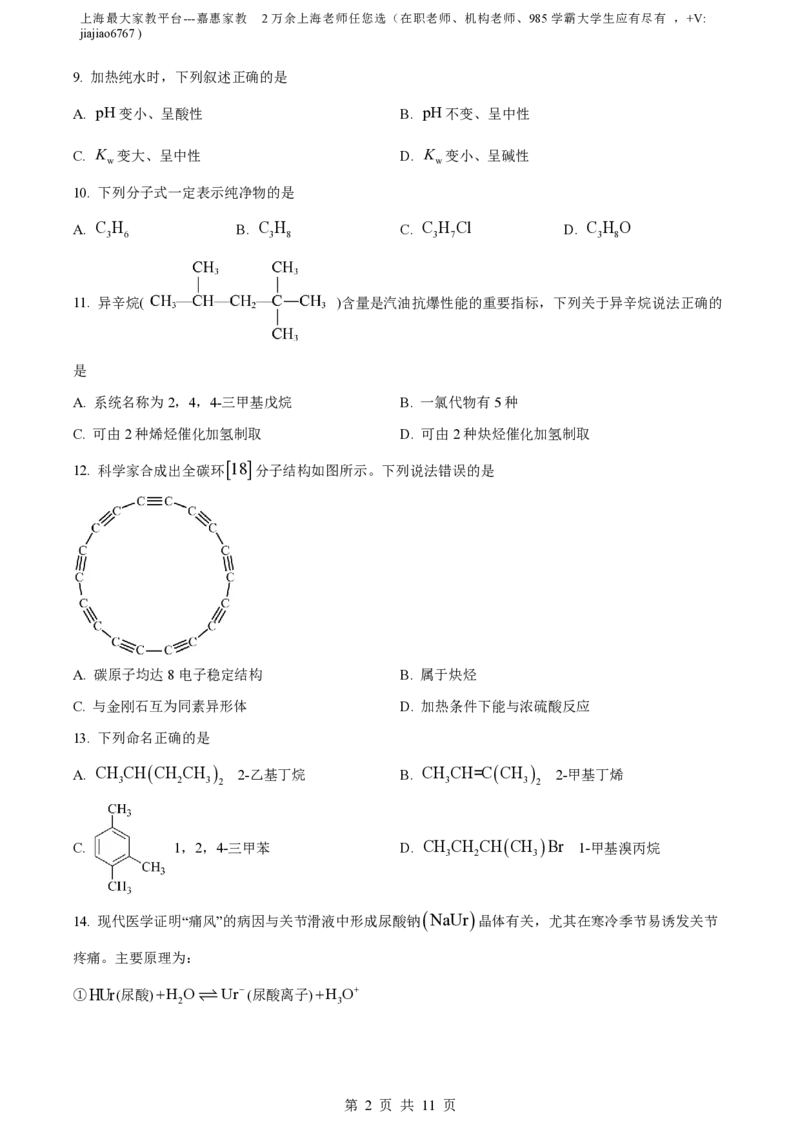
15. 铅蓄电池构造如图所示,放电时正极和负极均会生成PbSO 。当导线中有1.0mol电子通过时,则理
4
论上两极共生成PbSO
4
A. 0.5mol B. 1.0mol C. 1.5mol D. 2.0mol
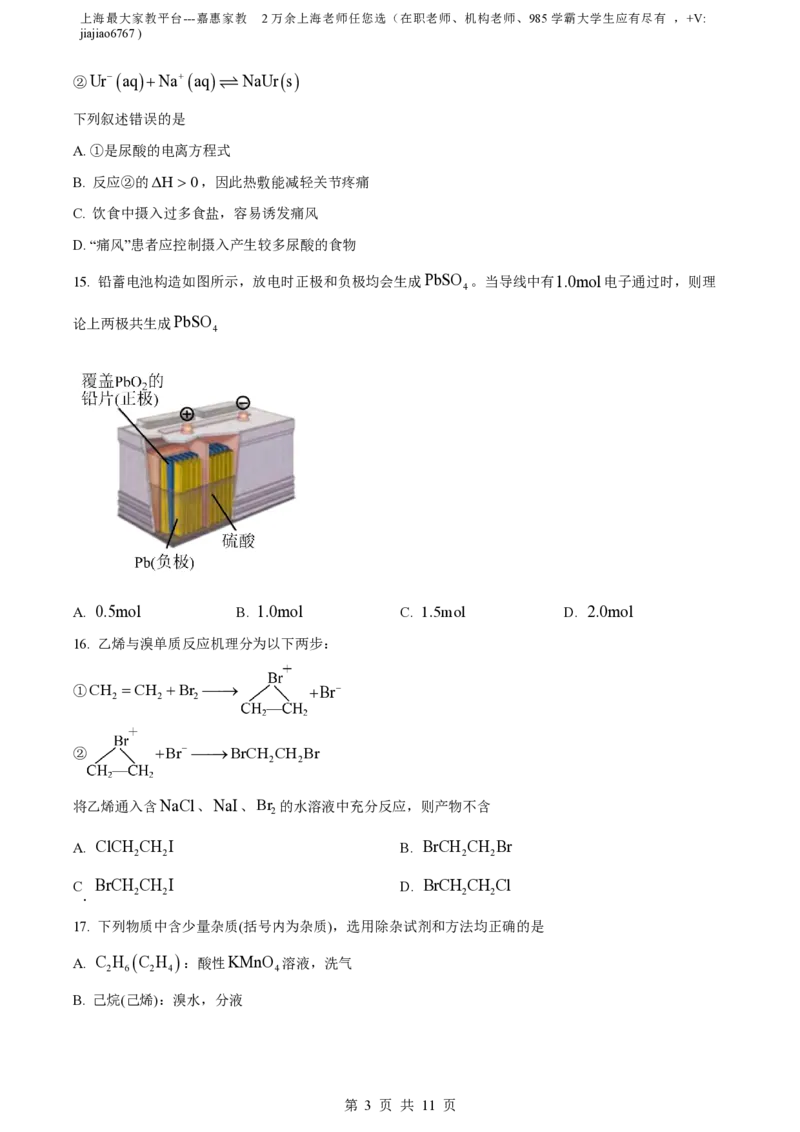
16. 乙烯与溴单质反应机理分为以下两步:
①CH CH Br Br
2 2 2
② Br BrCH CH Br
2 2
将乙烯通入含NaCl、NaI、Br 的水溶液中充分反应,则产物不含
2
A. ClCH CH I B. BrCH CH Br
2 2 2 2
C BrCH CH I D. BrCH CH Cl
. 2 2 2 2
17. 下列物质中含少量杂质(括号内为杂质),选用除杂试剂和方法均正确的是
A. C H C H :酸性KMnO 溶液,洗气
2 6 2 4 4
B. 己烷(己烯):溴水,分液
第 3 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. 硝基苯 NO :NaOH溶液,分液
2
D. C H BrBr :NaOH溶液,蒸馏
2 5 2
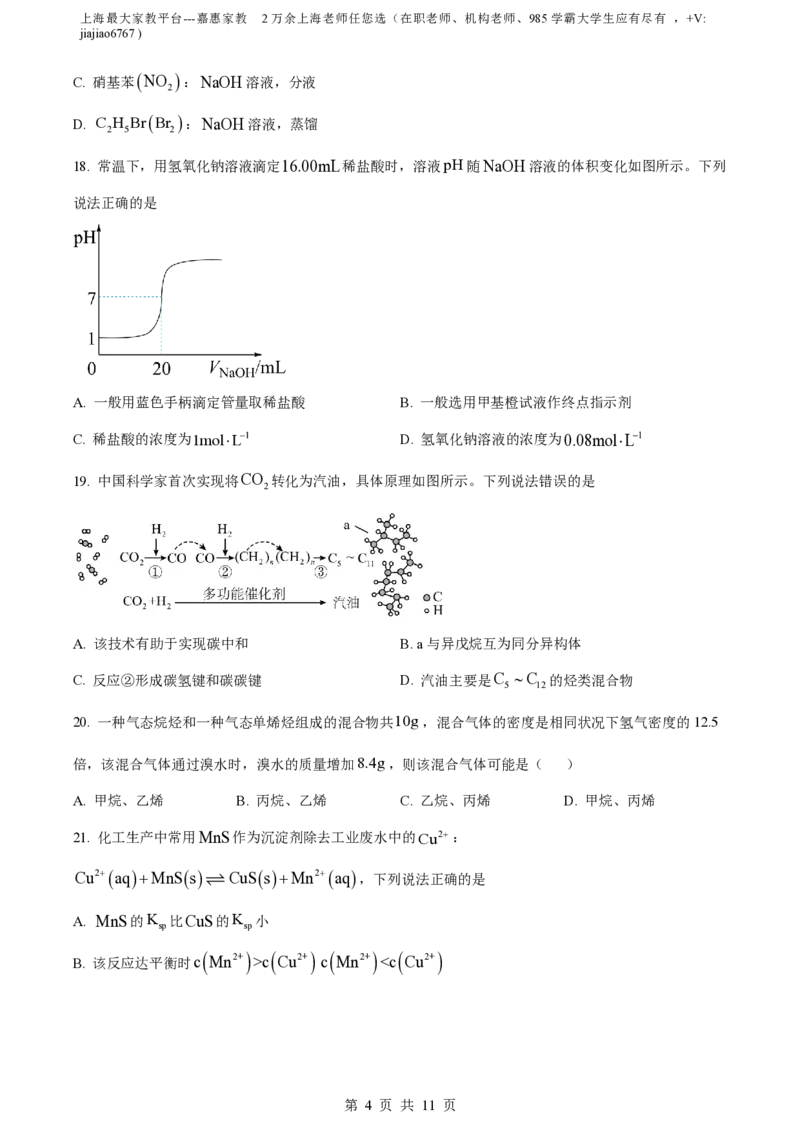
18. 常温下,用氢氧化钠溶液滴定16.00mL稀盐酸时,溶液pH随NaOH溶液的体积变化如图所示。下列
说法正确的是
A. 一般用蓝色手柄滴定管量取稀盐酸 B. 一般选用甲基橙试液作终点指示剂
C. 稀盐酸的浓度为1molL1 D. 氢氧化钠溶液的浓度为0.08molL1
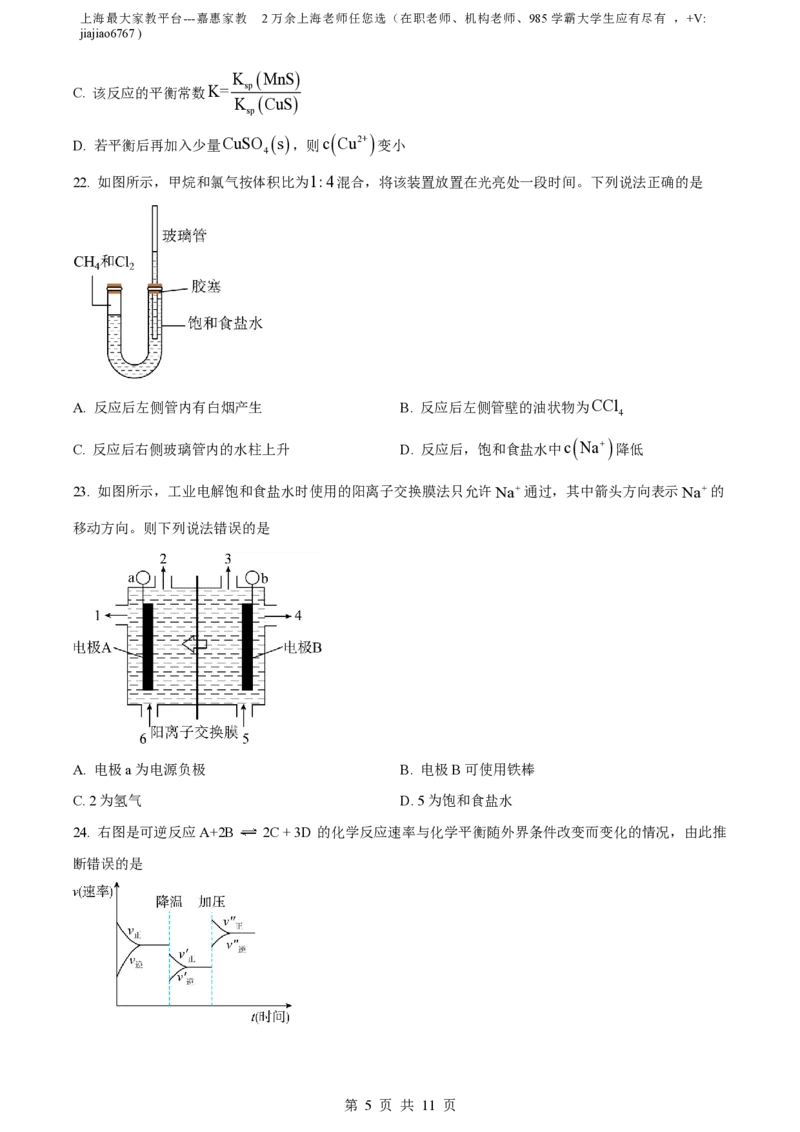
19. 中国科学家首次实现将CO 转化为汽油,具体原理如图所示。下列说法错误的是
2
A. 该技术有助于实现碳中和 B. a与异戊烷互为同分异构体
C. 反应②形成碳氢键和碳碳键 D. 汽油主要是C C 的烃类混合物
5 12
20. 一种气态烷烃和一种气态单烯烃组成的混合物共10g,混合气体的密度是相同状况下氢气密度的12.5
倍,该混合气体通过溴水时,溴水的质量增加8.4g,则该混合气体可能是( )
A. 甲烷、乙烯 B. 丙烷、乙烯 C. 乙烷、丙烯 D. 甲烷、丙烯
21. 化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2:
Cu2aqMnSs
CuSsMn2aq
,下列说法正确的是
A. MnS的K 比CuS的K 小
sp sp
B. 该反应达平衡时c
Mn2+
>c
Cu2+
c
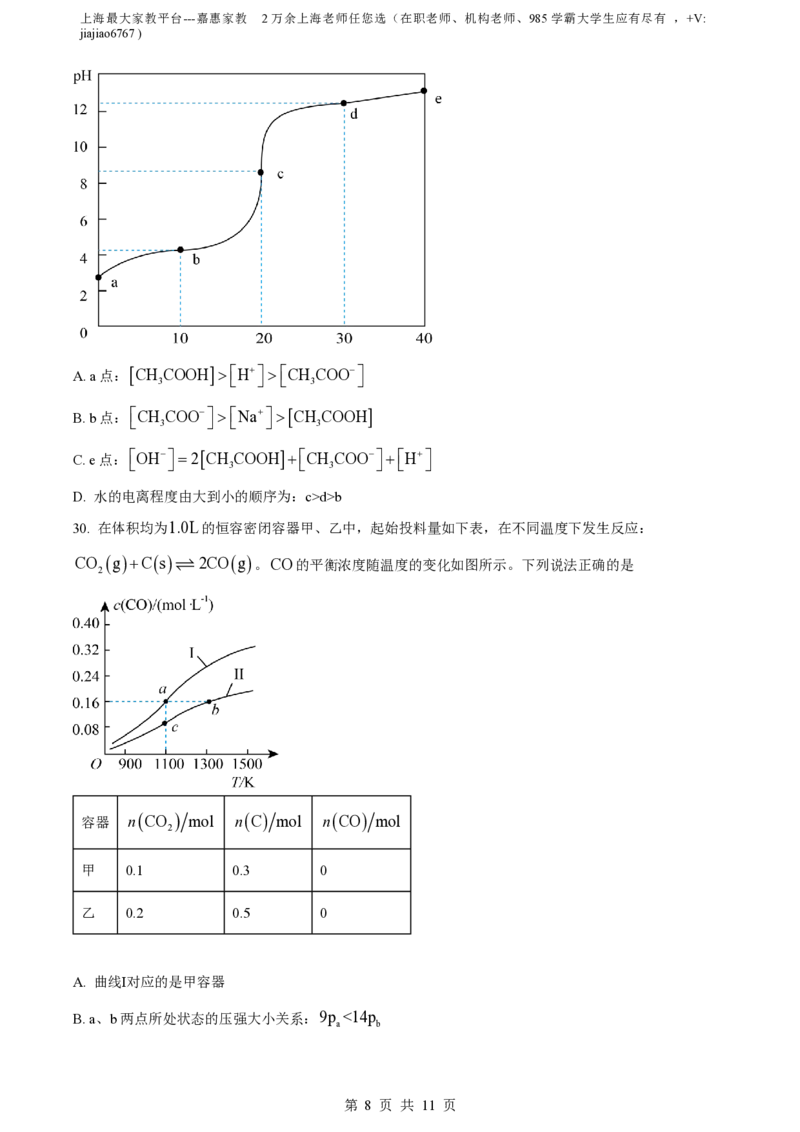
Mn2+
d>b
30. 在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如下表,在不同温度下发生反应:
CO
2
gCs
2COg 。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
容器 nCO mol nC mol nCO mol
2
甲 0.1 0.3 0
乙 0.2 0.5 0
A. 曲线Ⅰ对应的是甲容器
B. a、b两点所处状态的压强大小关系:9p <14p
a b
第 8 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
4
C. c点:CO的体积分数小于
7
D. 900K时,若起始向乙中加入CO、CO 、C各0.3mol,则v(正)>v(逆)
2
二、综合题(共 40分)
31. 环戊二烯( )重要的有机合成中间体。一定条件下,存在以下转化:
反应①: g gH 2 g ΔH 1
反应②:H
2
gI
2
g
2HIg H
2
11.0kJmol1
反应③: gI 2 g g2HIg H 3 89.3kJmol1
(1)反应①的H _______kJmol1。
1
(2)反应③的化学平衡常数表达式K _______。
(3)在恒温恒容的容器中,当反应②达到化学平衡时,则下列一定正确的是_______。
a.气体分子数不变 b.v H 2v HI
正 2 逆
c.cH cI d.断裂1mol II键的同时断裂2mol HI键
2 2
(4)恒温恒容时,0.5mol I g 和0.5mol (g)发生反应③,测得平衡时容器内压强变为起始的1.2
2
倍,则环戊烯的转化率为_______。
(5)欲提高反应③的正反应速率,且K值不变,可采取的措施有_______(选填编号)。
a.通入Arg
b.升高温度
c.提高环戊烯浓度
d.分离出HIg
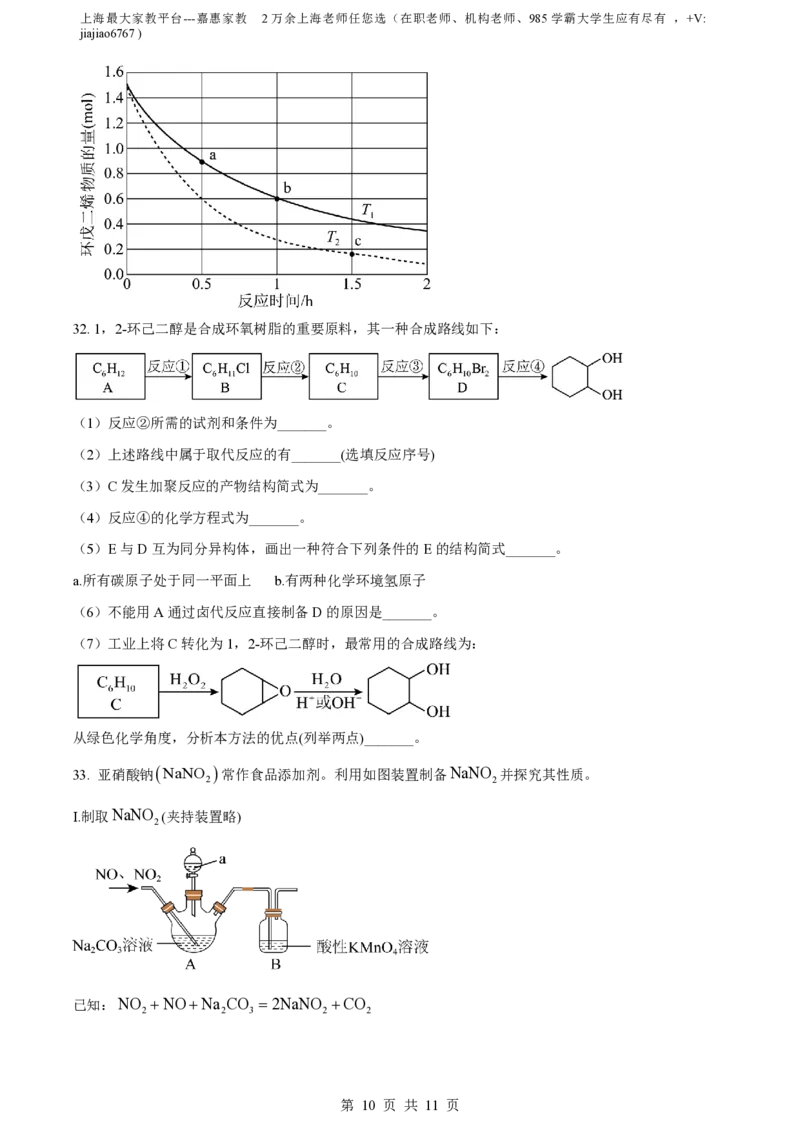
(6)已知两分子环戊二烯易发生加成反应形成二聚体。不同温度下在2L容器中环戊二烯物质的量与反应
时间的关系如图所示。推测T _______T (选填=、<或>);T 时,用二聚体表示01h的平均反应速率
1 2 1
v _______。
第 9 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
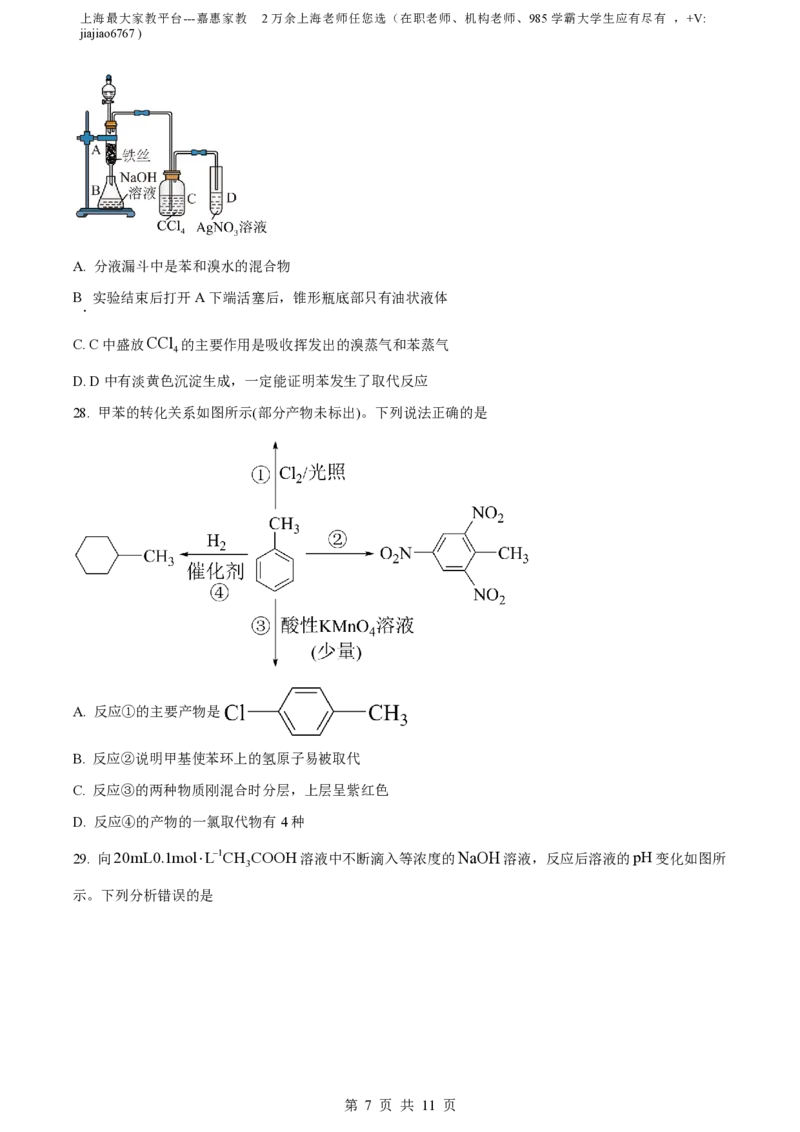
32. 1,2-环己二醇是合成环氧树脂的重要原料,其一种合成路线如下:
(1)反应②所需的试剂和条件为_______。
(2)上述路线中属于取代反应的有_______(选填反应序号)
(3)C发生加聚反应的产物结构简式为_______。
(4)反应④的化学方程式为_______。
(5)E与D互为同分异构体,画出一种符合下列条件的E的结构简式_______。
a.所有碳原子处于同一平面上 b.有两种化学环境氢原子
(6)不能用A通过卤代反应直接制备D的原因是_______。
(7)工业上将C转化为1,2-环己二醇时,最常用的合成路线为:
从绿色化学角度,分析本方法的优点(列举两点)_______。
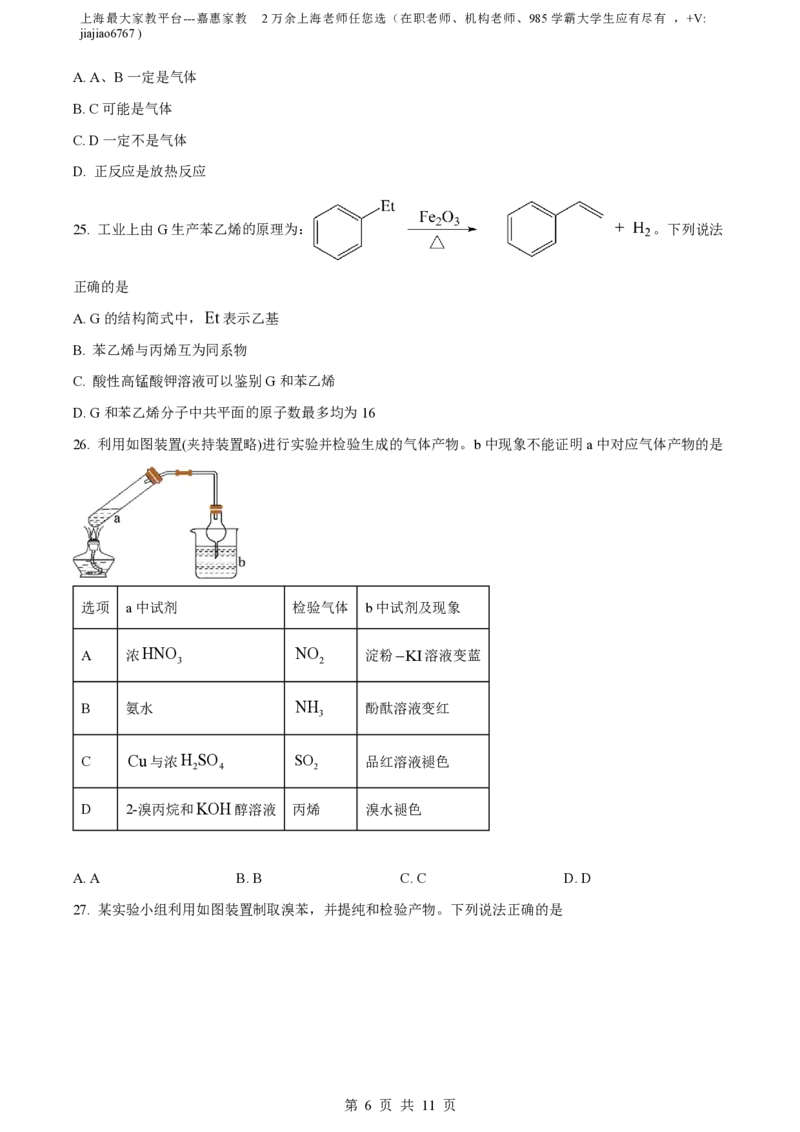
33. 亚硝酸钠 NaNO 常作食品添加剂。利用如图装置制备NaNO 并探究其性质。
2 2
Ⅰ.制取NaNO (夹持装置略)
2
已知:NO NONa CO 2NaNO CO
2 2 3 2 2
第 10 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2NO Na CO NaNO NaNO CO
2 2 3 2 3 2
(1)仪器a的名称是_______。
(2)已知HNO 为弱酸。判断NaNO 溶液的酸碱性,并结合离子方程式进行解释_______。
2 2
(3)反应前需通入N ,其作用是_______。
2
(4)A中反应后溶液经蒸发浓缩、_______、_______、洗涤干燥等,制得NaNO 晶体。
2
(5)等浓度的NaNO 和NaNO 的混合溶液中,微粒浓度关系正确的是_______(选填编号)。
2 3
a.c Na c NO c NO b.c NO c NO cHNO
3 2 3 2 2
c.c
Na
2c
NO
2c
NO
d.c
NO
c
H
c
NO
c
OH
3 2 3 2
Ⅱ.NaNO 性质探究
2
配制0.1molL1NaNO 溶液进行以下实验:
2
已知:Ag与NO反应,可生成AgNO 白色沉淀或无色络合离子。
2 2
(6)由实验现象得出结论:是否产生白色沉淀与_______有关。
(7)仅用上述实验中的试剂,设计不同实验方案进一步证实上述结论。实验操作及现象是_______。
第 11 页 共 11 页