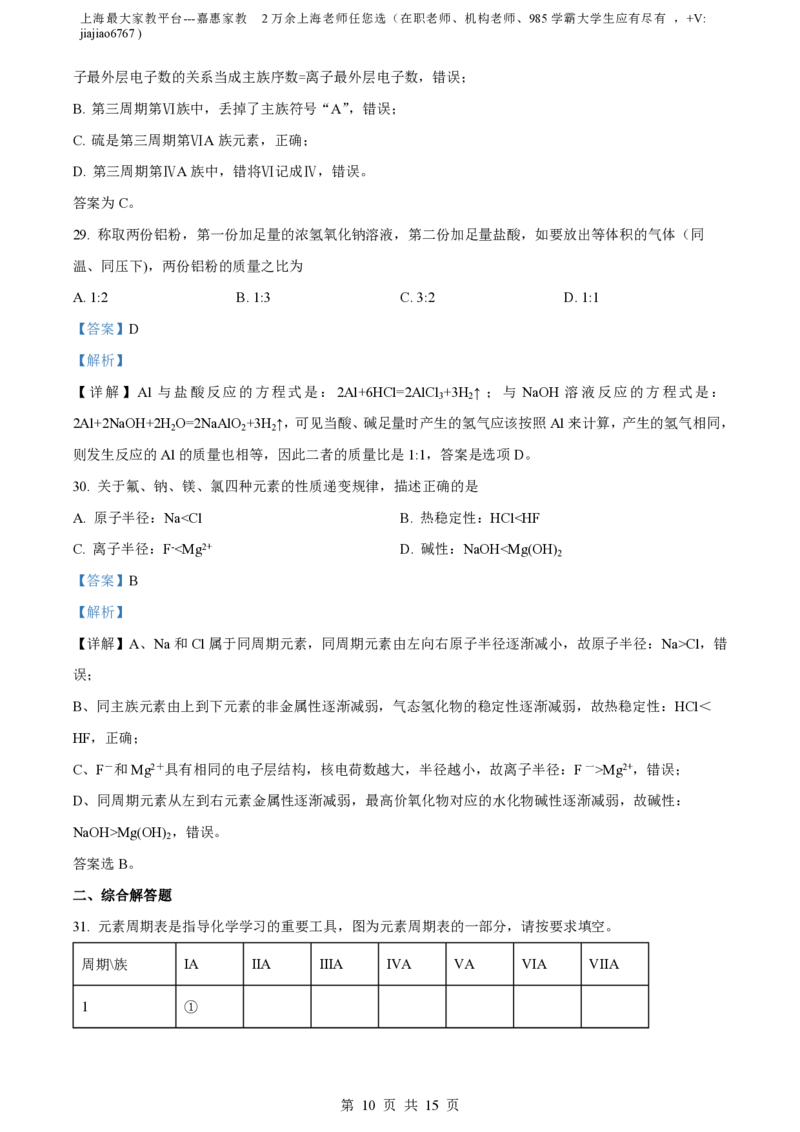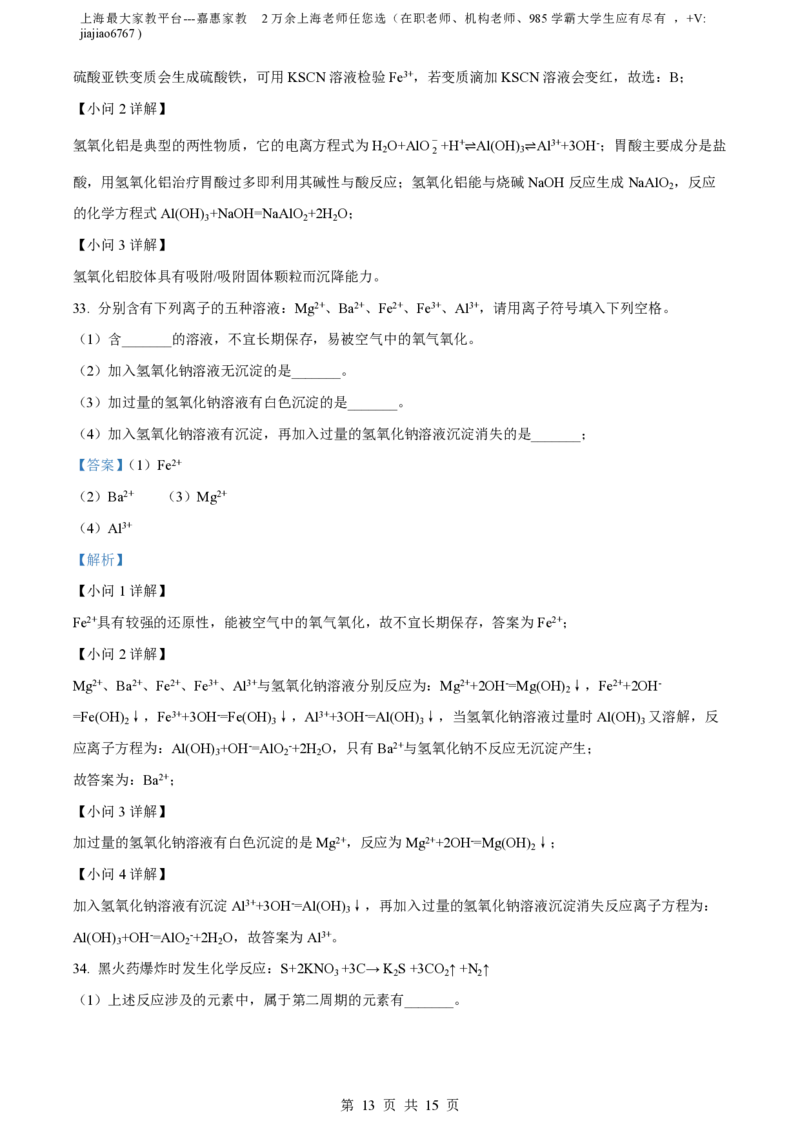文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
徐汇中学 2021 学年第一学期期中考试
高二年级化学(合格考)试卷
相对原子质量:H-1 O-16 Na-23 Al-27 Cl-35.5
一、选择题(每小题只有一个选项符合题意)
1. 提出元素周期律并根据周期律编制第一个元素周期表的科学家是()
A. 道尔顿 B. 门捷列夫 C. 普利斯特里 D. 阿佛加德罗
【答案】B
【解析】
【分析】1869年,俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,使得化学学习和研究变
得有规律可循。
【详解】A.道尔顿提出了近代原子学说,A项错误;
B.俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,B项正确;
C.普利斯特里加热氧化汞时,发现了氧气,C项错误;
D.阿佛加德罗提出了分子学说,D项错误;
答案选B。
2. 下列物质中,含有金属键的是( )
A. 干冰 B. 金刚石 C. 食盐 D. 白银
【答案】D
【解析】
【分析】金属键是化学键的一种,主要在金属中存在。由自由电子及排列成晶格状的金属离子之间的静电
吸引力组合而成。
【详解】A. 干冰中碳和氧之间是共价键,故A不符;
B. 金刚石中碳与碳之间是共价键,故B不符;
C. 食盐中钠离子和氯离子间以离子键结合,故C不符;
D. 白银由银离子和自由电子形成金属键,故D符合;
故选D。
3. 下列各元素中,化合价的最高正价数最大的是
A. F B. S C. N D. Al
【答案】B
【解析】
第 1 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【分析】主族元素其最高正化合价等于其族序数,但F无正价,O无最高正价,据此解答即可.
【详解】A、F只有负价,无正价,故A不选;
B、S原子的最外层有6个电子,全部失去得最高价为+6价,故B选;
C、N原子的最外层有5个电子,全部失去得最高价为+5价,故C不选;
D、Al原子的最外层有3个电子,故最高价为+3价,故D不选.
故选B.
4. 利用新技术能将不锈钢加工成为柔软的金属丝,它和棉纤维一起编织成为防辐射的劳防服装,这是利用
了金属的
A. 耐腐蚀性 B. 还原性 C. 热传导性 D. 延展性
【答案】D
【解析】
【详解】不锈钢能加工成为柔软的金属丝说明不锈钢具有很好的延展性,故选D。
5. 属于短周期元素的是( )
A. K B. Ca C. I D. Cl
【答案】D
【解析】
【详解】原子序数第1到18号的元素是短周期元素,Cl符合;
答案选D。
6. 原子核外L电子层最多能容纳的电子数是
A. 4 B. 6 C. 8 D. 10
【答案】C
【解析】
【详解】每个电子层最多容纳的2n2个电子,原子核外的电子层按照K、L、M……等排列,L电子层为第2
电子层,最多能容纳的电子数是2×22=8,故选C。
7. 下列各物质中,不能由组成它的两种元素的单质直接化合得到的是
A. FeS B. SO C. Cu S D. Fe O
3 2 3 4
【答案】B
【解析】
【详解】A.Fe和S在点燃下反应生成FeS,能由单质直接化合得到,A不选;
B.S具有弱还原性,S与O 反应只生成SO ,SO 再和O 反应生成SO ,不能由单质直接化合得到,B
2 2 2 2 3
选;
第 2 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.S具有弱还原性,S与Cu反应生成Cu S,能由单质直接化合得到,A不选;
2
D.Fe在O 中点燃能生成Fe O ,能由单质直接化合得到,A不选;
2 3 4
故选:B。
8. 元素性质呈现周期性变化的根本原因是( )
A. 元素原子电子层数增大
B. 元素原子最外层电子数呈现周期性变化
C. 元素的化合价呈现周期性变化
D. 核电荷数依次增大
【答案】B
【解析】
【详解】元素性质呈现周期性变化的根本原因是元素原子最外层电子数呈现周期性变化,最外层电子数决
定元素的性质,元素的化合价为元素的性质,而电子层数、核电荷数不具有周期性变化;
答案选B。
9. 易形成简单阴离子的元素是
A. O B. Mg C. Na D. He
【答案】A
【解析】
【详解】Mg、Na为金属,最外层电子数较少,容易形成阳离子,不能形成简单阴离子;O原子最外层电子
数较多,易得到电子形成阴离子;He为惰性气体,性质稳定,不容易形成阳离子,也不容易形成阴离子,
故选A。
10. 在周期表中金属和非金属的分界线附近能找到
A. 制农药的元素 B. 制催化剂的元素
C. 制耐高温合金材料的元素 D. 做半导体的元素
【答案】D
【解析】
【分析】
【详解】金属导电性强,非金属导电性弱,在金属与非金属的分界线附近的元素导电性介于金属和非金属
之间,属于半导体,比如硅。合金和催化剂在过渡金属元素里面寻找,农药在非金属元素里面寻找,故选
D。
11. 既能与盐酸反应又能和氢氧化钠反应的氧化物是( )
第 3 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. Al O B. Fe O C. Al(OH) D. Fe(OH)
2 3 2 3 3 3
【答案】A
【解析】
【详解】Al O 是两性氧化物,Fe O 是碱性氧化物,Al(OH) 和Fe(OH) 都不是氧化物;
2 3 2 3 3 3
答案选A。
【点睛】此题C容易错选,因为有同学审题时只注意到“既能与盐酸反应又能和氢氧化钠反应”没有注意到
“氧化物”。
12. 为除去铁粉中混有的少量铝粉,所选试剂和操作都合理的是
A. 盐酸,蒸发 B. NaOH溶液,蒸发
C. 盐酸,过滤 D. NaOH溶液,过滤
【答案】D
【解析】
【详解】A. 盐酸既能与铝反应,也能与铁反应,不能用盐酸除去铁粉中混有的少量铝粉,故A错误;
B. NaOH溶液能够与铝反应,而不能与铁反应,可以用氢氧化钠溶解铝,除去铁粉中混有的少量铝粉,然
后过滤即可,故B错误;
C. 盐酸既能与铝反应,也能与铁反应,不能用盐酸除去铁粉中混有的少量铝粉,故C错误;
D. NaOH溶液能够与铝反应,而不能与铁反应,可以用氢氧化钠溶解铝,除去铁粉中混有的少量铝粉,然
后过滤即可,故D正确;
故选D。
【点睛】本题的易错点为B,要注意溶解铝之后,应该通过过滤,洗涤得到纯净的铁粉。
13. 下列各元素中,原子半径依次增大的是
A. Na、Mg、Al B. N、O、F
C. P、Si、Al D. C、Si、P
【答案】C
【解析】
【详解】A.Na、Mg、Al属于同一周期,且Na、Mg、Al的原子序数依次增大,所以原子半径依次减小,A
错误;
B.N、O、F属于同一周期,且N、O、F的原子序数依次增大,所以原子半径依次减小,B错误;
C.P、Si、Al属于同一周期,且P、Si、Al的原子序数依次减小,所以原子半径依次增大,C正确;
D.C、Si属于同一主族,C的原子序数小于Si的,所以碳的原子半径小于硅的原子半径;Si、P属于同一
周期,且Si的原子序数小于P的原子序数,所以Si的原子半径大于P的原子半径,P的电子层数比碳的
第 4 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
多,所以P的原子半径大于C的原子半径,C、Si、P的原子半径从小到大的顺序为C、P、Si,D错误;
故选C。
14. 下列物质跟铁发生反应能生成三价铁盐的是
A. 稀硫酸 B. 硫酸铜 C. 硫磺 D. 氯气
【答案】D
【解析】
【详解】A.铁和稀硫酸反应生成硫酸亚铁和氢气,不能得到三价铁盐,A错误;
B.铁和硫酸铜发生置换反应生成铜和硫酸亚铁,B错误;
C.硫磺S的氧化性较弱,与铁反应生成FeS,不能得到三价铁盐,C错误;
D.氯气具有强氧化性,与铁点燃下反应生成FeCl ,能得到三价铁盐,D正确;
3
故选:D。
15. 关于合金的叙述:①合金中至少含两种金属;②合金硬度低于各组分的硬度;③合金中一定含金属;
④合金熔点低于各组分。其中正确的是
A. ①②③④ B. ①③④ C. ②③④ D. ③④
【答案】D
【解析】
【详解】合金是指一种金属与另一种或几种金属或非金属经过混合熔化,冷却凝固后得到的具有金属性质
的混合物,则合金中至少有一种金属,同时合金硬度一般高于各组分的硬度,熔点低于各组分,所以①②
说法错误,③④说法正确,答案选D。
16. 铝热剂为混合物,其中铝的作用是
A. 催化剂 B. 氧化剂 C. 还原剂 D. 填充剂
【答案】C
【解析】
【详解】铝和某些金属氧化物(如Fe O )组成的混合物称为铝热剂,铝热剂在高温下发生铝热反应时,
2 3
铝元素的化合价从0价升到+3价,Al被氧化,是还原剂;
答案选C。
17. 常温下铝具有较强的抗腐蚀性,主要原因是
A. 铝不活泼
B. 铝与氧气在常温下不反应
C. 常温下铝表面能形成一层致密的氧化物薄膜
D. 铝单质既可与强酸作用,又可与强碱溶液反应
第 5 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】C
【解析】
【详解】A.铝很活泼,在空气中易被氧化,选项A错误;
B.铝和氧气在常温下反应生成氧化铝,选项B错误;
C.常温下,铝易被氧气氧化生成一层致密的氧化物薄膜而阻止进一步被氧化,所以铝具有较强的抗腐蚀
性,选项C正确;
D.铝能和强酸、强碱反应生成氢气,但不是铝具有抗腐蚀性的原因,选项D错误;
答案选C。
18. 由短周期元素和长周期元素共同组成的族可能是
A. 主族 B. 副族 C. Ⅷ族 D. ⅦB族
【答案】A
【解析】
【详解】A.主族元素均由短周期元素和长周期元素共同组成,故A正确;
B.副族元素均为长周期元素,故B错误;
C.Ⅷ族为元素周期表中的第8、9、10三个纵列,均在长周期,故C错误;
D.没有Ⅶ族,若为ⅦA族,则符合题意,若为ⅦB族,不符合题意,故D错误;
故选A.
19. 某元素R,其原子的最外层有2个电子,该元素是
A. 金属元素 B. 稀有气体元素
C. ⅡA族元素 D. 无法确定为哪一类元素
【答案】D
【解析】
【详解】元素R的原子的最外层有2个电子,若R只有1个电子层,则为2号元素He稀有气体,若有2
个电子层,为4号元素Be,是IIA族元素,若有3个电子层,为12号元素Mg,为金属元素,则无法确定
为哪一类元素,故选:D。
20. 下列物质属于电解质的是
A. Cl B. KNO C. SO D. Al
2 3 2
【答案】B
【解析】
【详解】电解质就是在水溶液中或熔融状态下能够导电的化合物,常见的电解质主要有酸、碱、盐、活泼
金属氧化物等。所以B正确。
第 6 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
21. 下列离子方程式正确的是
A. 醋酸与氢氧化钠溶液反应:CH COOH+OH—= CH COO—+H O
3 3 2
B. 铁与盐酸反应:2Fe+6H+ =2Fe3++3H ↑
2
C. 氯化铁溶液和氨水反应:Fe3+ +3OH— = Fe(OH) ↓
3
D. 氯化铝溶液中滴入过量氢氧化钠溶液:Al3+ + 3OH—= Al(OH) ↓
3
【答案】A
【解析】
【详解】A.醋酸与氢氧化钠溶液反应生成醋酸钠和水,反应的离子方程式为CH COOH+OH—=
3
CH COO—+H O,故A正确;
3 2
B.铁与盐酸反应生成氯化亚铁和氢气,反应的离子方程式为Fe+2H+ =Fe2++H ↑,故B错误;
2
C.氯化铁溶液和氨水反应生成氢氧化铁沉淀和氯化铵,反应的离子方程式为Fe3+ +3NH ·H O =
3 2
Fe(OH) ↓+3NH+,故C错误;
3 4
D.氯化铝溶液与过量氢氧化钠溶液反应生成偏铝酸钠、氯化钠和水,反应的离子方程式为Al3+ +4OH—=
AlO- +2 H O,故D错误;
2 2
故选A。
22. 铝在人体中积累可使人慢性中毒,世界卫生组织将铝确定为食品污染源之-而加以控制,铝在下列使用
场合中,必须加以控制的是
A. 制造电线 B. 制饮料罐 C. 制铝合金窗 D. 炼铝厂制造铝锭
【答案】B
【解析】
【分析】铝在人体内积累可使人慢性中毒,铝进入人体的主要途径是通过消化系统,既然铝是食品污染源
之一,凡与人的食用物品及口腔接触的物品都必须控制铝的使用。
【详解】A. 制造电线,铝与人的消化系统不直接接触,铝不会因使用电缆进入人体,与人体健康无关,无
需控制,选项A不符合题意;
B. 制饮料罐,可使铝通过饮料进入人体,需要加以控制,选项B符合题意;
C. 用铝制门窗,铝与人的消化系统不直接接触,铝不会因使用电缆进入人体,与人体健康无关,无需控
制,选项C不符合题意;
D. 炼铝厂制造铝锭与人体健康无关,无需控制,选项D不符合题意;
答案选B。
23. 元素性质的周期性变化不包括
第 7 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 原子半径 B. 主要化合价 C. 原子核外电子层数 D. 金属性和非金属性
【答案】C
【解析】
【详解】随原子序数的递增,元素的原子半径、主要化合价、金属性和非金属性都呈现出周期性变化规
律,称为元素周期律;元素性质的周期性变化不包括原子核外电子层数的变化,故选C。
24. 主族元素R的最高价氧化物对应水化物的化学式为H RO ,则其氢化物的化学式为( )
2 3
A. HR B. H R C. RH D. RH
2 3 4
【答案】D
【解析】
【详解】R元素的最高价氧化物对应的水化物的化学式为H RO ,则R的最高正价为+4价,说明RX原子
2 3
最外层有4个电子,最低化合价为-4价,形成的氢化物为RH ,故选D。
4
25. 将除去表面氧化膜的铝条投入Hg(NO ) 溶液中,反应片刻后将铝条取出置于表面皿上,铝条上长出白
3 2
色的“毛刷”。下列说法错误的是
A. 发生了置换反应
B. 离子方程式为 Al + Hg2+= Al3++ Hg
C. 白色的“毛刷”是氧化铝
D. 实验证明了铝条表面氧化膜的保护作用
【答案】B
【解析】
【详解】A.Al的金属活泼性比Hg强,则铝投入Hg(NO ) 溶液中发生置换反应,A正确;
3 2
B.铝能与Hg2+发生置换反应得到Hg,离子方程式为:2Al + 3Hg2+= 2Al3++ 3Hg,B错误;
C.Al与O 反应生成的Al O 不再是均匀致密地覆盖在铝表面,而是呈白色的“毛刷”, “毛刷”是氧化铝,
2 2 3
C正确;
D.置换出的Hg附在铝表面,使Al与O 反应生成的Al O 不再是均匀致密地覆盖在铝表面,而是呈白色
2 2 3
的“毛刷”,该实验证明了铝条表面氧化膜的保护作用,D正确;
故选:B。
26. 能够大量共存的离子组合是
A. H+、SO2-、NO-、Ba2+ B. K+、Cl-、CO2-、Na+
4 3 3
C. Fe3+、NO-、OH-、Na+ D. K+、SO2-、CO2-、H+
3 4 3
【答案】B
第 8 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【详解】A.SO2-、Ba2+结合成沉淀,不能共存,A错误;
4
B.四种离子之间互不反应,能共存,B正确;
C.Fe3+、OH-结合成沉淀,不能共存,C错误;
D.CO2-、H+反应生成二氧化碳和水,不能共存,D错误;
3
故选:B。
27. 要使氯化铝溶液中的Al3+完全转化为Al(OH) 沉淀,应选用的最佳试剂是
3
A. NaOH溶液 B. 稀盐酸 C. 氨水 D. AgNO 溶液
3
【答案】C
【解析】
【分析】根据题意,Al3+转化为不溶于水的物质是Al(OH) ,Al(OH) 具有两性,既能和强酸酸反应又
3 3
能和强碱反应,要使明矾溶液中的Al3+完全沉淀,选取试剂时就不能选强碱,只能是弱碱。
【详解】A.氢氧化钠溶液是强碱溶液,沉淀Al3+时生成的氢氧化铝能溶解在过量的强碱溶液中,所以Al3+
不能全部沉淀出来,故A不符合;
B.盐酸不与氯化铝反应,故B不符合;
C.氨水与氯化铝反应生成氢氧化铝沉淀,氨水是弱碱溶液,不能溶解Al(OH) ,可以全部沉淀Al3+,
3
故C符合;
D.氯化铝与硝酸银溶液反应生成氯化银沉淀,故D不符合;
答案选C。
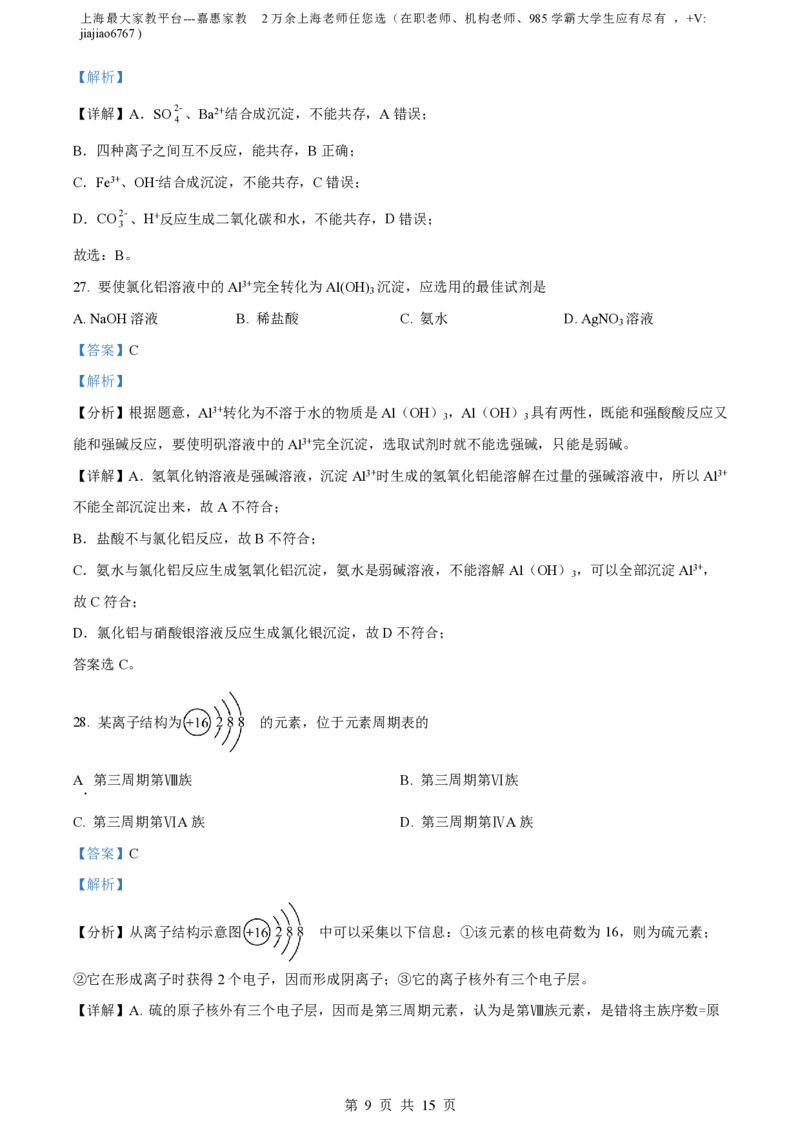
28. 某离子结构为 的元素,位于元素周期表的
A 第三周期第Ⅷ族 B. 第三周期第Ⅵ族
.
C. 第三周期第ⅥA族 D. 第三周期第ⅣA族
【答案】C
【解析】
【分析】从离子结构示意图 中可以采集以下信息:①该元素的核电荷数为16,则为硫元素;
②它在形成离子时获得2个电子,因而形成阴离子;③它的离子核外有三个电子层。
【详解】A. 硫的原子核外有三个电子层,因而是第三周期元素,认为是第Ⅷ族元素,是错将主族序数=原
第 9 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
子最外层电子数的关系当成主族序数=离子最外层电子数,错误;
B. 第三周期第Ⅵ族中,丢掉了主族符号“A”,错误;
C. 硫是第三周期第ⅥA族元素,正确;
D. 第三周期第ⅣA族中,错将Ⅵ记成Ⅳ,错误。
答案为C。
29. 称取两份铝粉,第一份加足量的浓氢氧化钠溶液,第二份加足量盐酸,如要放出等体积的气体(同
温、同压下),两份铝粉的质量之比为
A. 1:2 B. 1:3 C. 3:2 D. 1:1
【答案】D
【解析】
【详解】Al 与盐酸反应的方程式是:2Al+6HCl=2AlCl +3H ↑ ;与 NaOH 溶液反应的方程式是:
3 2
2Al+2NaOH+2H O=2NaAlO +3H ↑,可见当酸、碱足量时产生的氢气应该按照Al来计算,产生的氢气相同,
2 2 2
则发生反应的Al的质量也相等,因此二者的质量比是1:1,答案是选项D。
30. 关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是
A. 原子半径:NaCl,错
误;
B、同主族元素由上到下元素的非金属性逐渐减弱,气态氢化物的稳定性逐渐减弱,故热稳定性:HCl<
HF,正确;
C、F-和Mg2+具有相同的电子层结构,核电荷数越大,半径越小,故离子半径:F一>Mg2+,错误;
D、同周期元素从左到右元素金属性逐渐减弱,最高价氧化物对应的水化物碱性逐渐减弱,故碱性:
NaOH>Mg(OH) ,错误。
2
答案选B。
二、综合解答题
31. 元素周期表是指导化学学习的重要工具,图为元素周期表的一部分,请按要求填空。
周期\族 IA IIA IIIA IVA VA VIA VIIA
1 ①
第 10 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2 ② ③ ④ ⑤ ⑥
3 ⑦ ⑧ ⑨ ⑩
(1)写出下列元素的符号:③_______ ④_______⑤_______⑦_______
(2)⑤和⑥处于同一行,是由于它们的_______相同。
(3)以上元素中,原子半径最小的是_______(填元素符号);最高价氧化物对应水化物中酸性最强的是
_______(填最高价氧化物对应水化物的化学式)。
(4)写出由⑤⑥⑧三种元素组成的化合物的化学式_______。
(5)S和Cl两种元素中,非金属性较强的是_______,不能说明该结论的事实是_______。(填选项)
A.氯气与铁反应生成FeCl ,硫与铁反应生成FeS
3
B.把Cl 通入H S溶液中能发生置换反应
2 2
C.受热时H S易分解,HCl不易分解
2
D.单质硫是固体,氯的单质是气体
【答案】(1) ①. Be ②. B ③. N ④. Mg
(2)电子层数 (3) ①. H ②. HClO
4
(4)Al(NO ) 或Al(NO )
3 3 2 3
(5) ①. Cl ②. D
【解析】
【分析】由周期表中各元素的相对位置可知,①为H元素、②为Li元素、③为Be元素、④为B元素、
⑤为N元素、⑥为O元素、⑦为Mg元素、⑧为Al元素、⑨为S元素、⑩为Cl元素。
【小问1详解】
由分析可知,③为Be元素、④为B元素、⑤为N元素、⑦为Mg元素,故答案为:Be;B;N;Mg;
【小问2详解】
电子层数相同的元素在周期表中位于同一周期,N元素和O元素的电子层数都为2,都位于元素周期表第
二周期,故答案为:电子层数;
【小问3详解】
以上元素中,原子半径最小的是氢元素;最高价氧化物对应水化物中酸性最强的是高氯酸,故答案为:
H;HClO ;
4
【小问4详解】
氮、氧、铝三种元素组成的化合物可能为硝酸铝或亚硝酸铝,故答案为:Al(NO ) 或Al(NO ) ;
3 3 2 3
第 11 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【小问5详解】
氯元素的原子半径小于硫元素,得到电子的能力强于硫元素,非金属性强于硫元素;
A.氯气与铁反应生成FeCl ,硫与铁反应生成FeS说明氯元素得到电子的能力强于硫元素,非金属性强于
3
硫元素,故不符合题意;
B.氧化剂的氧化性强于氧化产物,非金属单质的氧化性越强,元素的非金属性越强,把Cl 通入H S溶
2 2
液中能发生置换反应说明氯气的氧化性强于硫,氯元素的非金属性强于硫元素,故不符合题意;
C.元素的非金属性越强,氢化物的稳定性越强,受热时H S易分解,HCl不易分解说明氯元素的非金属
2
性强于硫元素,故不符合题意;
D.单质的熔沸点高低与元素的非金属性强弱无关,则单质硫是固体,氯的单质是气体不能判断元素的非
金属性强弱,故符合题意;
D符合题意,故答案为:Cl;D。
32. 人类生活离不开化学,如:①硫酸亚铁片用于治疗贫血(图是其说明书);②复方氢氧化铝用于治疗胃
酸过多;③明矾用作净水剂等。
阅读“硫酸亚铁片”的标签说明,请回答:
(1)硫酸亚铁易被氧化而变质,为检验某补血剂中硫酸亚铁是否变质,可向该补血剂配成的溶液中加入
A. AgNO 溶液 B. KSCN溶液
3
C. 盐酸酸化的BaCl 溶液 D. HNO 酸化的Ba(NO ) 溶液
2 3 3 2
(2)氢氧化铝是典型的两性物质,它的电离方程式为_______;复方氢氧化铝在治疗胃酸过多时,氢氧化
铝作为_______(填“酸”或“碱”)中和过多胃酸;当然氢氧化铝也能与烧碱反应,反应的化学方程式
_______。
(3)明矾能净水是因为①Al3+能水解,②水解产物氢氧化铝胶体具有_______能力。
【答案】(1)B (2) ①. H O+AlO+H+⇌Al(OH) ⇌Al3++3OH- ②. 碱 ③.
2 2 3
Al(OH) +NaOH=NaAlO +2H O
3 2 2
(3)吸附/吸附固体颗粒而沉降
【解析】
【小问1详解】
第 12 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
硫酸亚铁变质会生成硫酸铁,可用KSCN溶液检验Fe3+,若变质滴加KSCN溶液会变红,故选:B;
【小问2详解】
氢氧化铝是典型的两性物质,它的电离方程式为H O+AlO+H+⇌Al(OH) ⇌Al3++3OH-;胃酸主要成分是盐
2 2 3
酸,用氢氧化铝治疗胃酸过多即利用其碱性与酸反应;氢氧化铝能与烧碱NaOH反应生成NaAlO ,反应
2
的化学方程式Al(OH) +NaOH=NaAlO +2H O;
3 2 2
【小问3详解】
氢氧化铝胶体具有吸附/吸附固体颗粒而沉降能力。
33. 分别含有下列离子的五种溶液:Mg2+、Ba2+、Fe2+、Fe3+、Al3+,请用离子符号填入下列空格。
(1)含_______的溶液,不宜长期保存,易被空气中的氧气氧化。
(2)加入氢氧化钠溶液无沉淀的是_______。
(3)加过量的氢氧化钠溶液有白色沉淀的是_______。
(4)加入氢氧化钠溶液有沉淀,再加入过量的氢氧化钠溶液沉淀消失的是_______;
【答案】(1)Fe2+
(2)Ba2+ (3)Mg2+
(4)Al3+
【解析】
【小问1详解】
Fe2+具有较强的还原性,能被空气中的氧气氧化,故不宜长期保存,答案为Fe2+;
【小问2详解】
Mg2+、Ba2+、Fe2+、Fe3+、Al3+与氢氧化钠溶液分别反应为:Mg2++2OH-=Mg(OH) ↓,Fe2++2OH-
2
=Fe(OH) ↓,Fe3++3OH-=Fe(OH) ↓,Al3++3OH-=Al(OH) ↓,当氢氧化钠溶液过量时Al(OH) 又溶解,反
2 3 3 3
应离子方程为:Al(OH) +OH-=AlO -+2H O,只有Ba2+与氢氧化钠不反应无沉淀产生;
3 2 2
故答案为:Ba2+;
【小问3详解】
加过量的氢氧化钠溶液有白色沉淀的是Mg2+,反应为Mg2++2OH-=Mg(OH) ↓;
2
【小问4详解】
加入氢氧化钠溶液有沉淀Al3++3OH-=Al(OH) ↓,再加入过量的氢氧化钠溶液沉淀消失反应离子方程为:
3
Al(OH) +OH-=AlO -+2H O,故答案为Al3+。
3 2 2
34. 黑火药爆炸时发生化学反应:S+2KNO +3C→ K S +3CO ↑ +N ↑
3 2 2 2
(1)上述反应涉及的元素中,属于第二周期的元素有_______。
第 13 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(2)上述反应的生成物中,属于非电解质的是_______,其电子式是_______。
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式:_______。
【答案】(1)C、N、O
(2) ①. CO ②.
2
(3)KOH+HNO =KNO +H O
3 3 2
【解析】
【小问1详解】
属于第二周期的元素有C、N、O,K属于第三周期;
【小问2详解】
在水溶液和熔融状态下都不能导电的化合物属于非电解质,即非电解质为:CO ,其中C和O分别共用2
2
对共用电子对,电子式为 ;
【小问3详解】
K、N最高价氧化物对应的水化物分别为KOH、HNO ,两者发生酸和碱的中和反应,反应的化学方程
3
式:KOH+HNO =KNO +H O。
3 3 2
Δ
35. 铁在常温下遇浓硫酸发生钝化,在加热条件下发生反应生成SO 气体,方程式:2Fe+6H SO (浓)
2 2 4
Fe (SO ) +3SO ↑+6H O
2 4 3 2 2
(1)请标出上述反应中电子转移的方向和数目_______。
(2)该反应的氧化剂是_______,被氧化的元素是_______。
【答案】(1) (2) ①. (浓)H SO ②. 0价的铁
2 4
元素
【解析】
【小问1详解】
该反应中,铁元素的化合价由0价→+3价升高3,失电子被氧化,硫元素的化合价由+4价→+2价降低
2,所以部分硫元素被氧化,最小公倍数为6,故反应中电子转移的方向和数目用单线桥表示如下
;
【小问2详解】
硫元素的化合价由+4价→+2价,化合价降作为氧化剂,氧化剂为(浓)H SO ;铁元素的化合价由0价→+3
2 4
第 14 页 共 15 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
价,化合价升高,被氧化的元素是0价的铁元素。
第 15 页 共 15 页