文档内容
化学答案第1
页(共5页)
化学参考答案及评分意见
1.
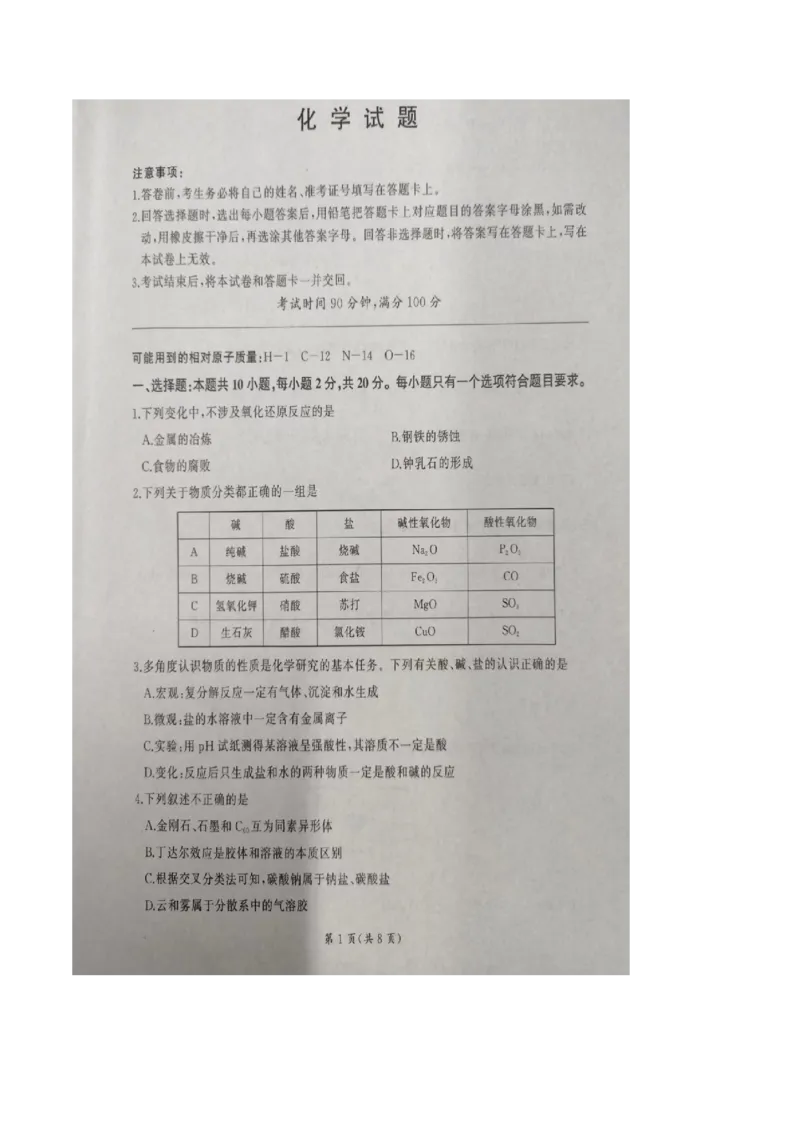
D 【解析】金属的冶炼是金属元素由化合态变为游离态,金属元素被还原,涉及氧化还原反应,A 不符合题意;钢
铁的锈蚀是铁失电子发生氧化反应,涉及氧化还原反应,B不符合题意;食物的腐败是食物被氧气氧化,涉及氧化
还原反应,C 不符合题意;钟乳石的形成涉及的化学反应有CaCO3+H2O +CO2Ca(HCO3)
2、
Ca(HCO3)
2CaCO3↓+H2O+CO2↑,反应中没有元素化合价的变化,不涉及氧化还原反应,D 符合题意.
2.
C 【解析】纯碱是碳酸钠,属于盐;盐酸属于混合物,烧碱是氢氧化钠,属于碱,A 错误;CO 和酸碱都不能反
应,CO 属于不成盐氧化物,B错误;氢氧化钾属于碱;硝酸属于含氧酸;苏打是碳酸钠,属于盐;MgO 能与盐酸反
应生成氯化镁和水,MgO 属于碱性氧化物;SO3和氢氧化钠反应生成硫酸钠和水,SO3属于酸性氧化物,C 正确;
生石灰是氧化钙,属于碱性氧化物,D 错误.
3.
C 【解析】一般来说,复分解反应的发生需要有沉淀、气体或水生成,而不是三者都生成,也可以利用“强制弱”的
原理发生复分解反应,如HCl+CH3COONaNaCl+CH3COOH,A 错误;铵盐(如氯化铵)的水溶液中不含
有金属离子,B 错误;酸式盐(如NaHSO4的溶液)可能呈强酸性,C 正确;酸式盐与碱反应(如NaHCO3与
NaOH 反应)也可能只生成盐和水,D 错误.
4.
B 【解析】金刚石、石墨和C60都是碳的单质,互为同素异形体,A 正确;丁达尔效应是区分胶体和溶液的方法,本
质区别是分散质粒子直径不同,B错误;根据交叉分类法,碳酸钠属于钠盐、碳酸盐,C 正确;云、雾是大气中的水
蒸气遇冷液化成的小水滴或凝华成的小冰晶漂浮在空中的可见物质,它们都形成气溶胶,D 正确.
5.
B 【解析】NaCl在熔融状态和溶于水时发生电离:NaCl=Na
++Cl
-,A 正确;氯化钠是电解质,溶于水或在熔融
状态下才能导电,固体不导电,B错误;图a表示固体NaCl,图b表示熔融NaCl的导电情况,图c表示NaCl在水
溶液中的导电情况,表示NaCl水溶液中的微粒迁移,C 正确;根据异性相吸的原则由图c可判断水合离子中H
和O 原子的朝向受到离子所带电荷种类的影响,D 正确.
6.
C 【解析】NaNO3不能与其它物质反应而生成氯化钠,无法一步实现图示的转化,A 错误;氧化铜不能与水反应
生成氢氧化铜,无法一步实现图示的转化,B错误;各步都能实现转化,C正确;硫酸钡无法转化为硫酸钠,所以无
法实现乙到丙的转化,D 错误.
7.A 【解析】Br
-→Br2时,Br元素化合价升高,需加入氧化剂才可以实现物质的转化,A 符合题意;HSO
-
3→SO
2-
3
时,元素化合价不变,不需要加入氧化剂或还原剂就可以实现物质的转化,B不符合题意;H2O2→O2时,加热就
可以转化,不需要加入氧化剂,C不符合题意;MnO
-
4→Mn
2+时,Mn元素化合价降低,则需要加入还原剂才可以
实现物质的转化关系,D 不符合题意.
8.
B 【解析】某溶液中含有Fe
3+、SO
2-
4、Al
3+和X 四种离子,且各离子的数目之比为2∶4∶1∶1,根据电荷守恒可
知,X 所带的负电荷数为2×3+1×3-2×4
1
=1;结合离子共存,铁离子和氢氧根离子生成氢氧化铁沉淀,选B.
{#{QQABYYwQggAAAIAAABgCQQ0QCkCQkBGCCYoGRBAYMAAAiRFABAA=}#}
化学答案第2
页(共5页)
9.
C 【解析】CuO 与C反应,铜元素得电子,C 元素失电子,则电子转移的方向和数目为
,A
错误;反应中Na共失去2e
-,Cl
2共得到2e
-,电子转移数目正确,但电子转移方向有误,B错误;反应中电子转移
的方向和数目均正确,C正确;该反应中C1元素化合价降低得电子,氧元素化合价升高失电子,转移电子数为
12,则电子转移的方向和数目为
,选项D 错误.
10.A 【解析】各离子之间互不反应,能共存,A 正确;使紫色石蕊试液呈红色的溶液呈酸性,CO
2-
3
与Ca
2+、H
+均
反应,不能大量共存,B 错误;OH
-与NH
+
4反应生成NH3H2O,不能大量共存,OH
-与Mg
2+反应生成
Mg(OH)
2沉淀,C错误;强碱性溶液中OH
-与HCO
-
3反应生成碳酸根离子和水,不能大量共存,D 错误.
11.
CD 【解析】熔融状态下的NaHSO4的电离方程式为NaHSO4Na
++HSO
-
4,A 错误;水溶液中的KNO3
的电离方程式为KNO3K
++NO
-
3,B错误;水溶液中的NaHCO3电离:NaHCO3Na
++HCO
-
3,C正
确;水溶液中的Al
2(SO4)
3的电离方程式为Al
2(SO4)
32Al
3++3SO
2-
4,D 正确.
12.
B 【解析】Cu与稀硫酸不反应,A 错误;少量二氧化碳通入澄清石灰水产生碳酸钙沉淀,石灰水变浑浊,离子方
程式为CO2+Ca
2++2OH
-CaCO3↓+H2O,B正确;H2CO3不稳定会分解为CO2和H2O,稀硝酸滴在大
理石上离子方程式为:CaCO3+2H
+Ca
2++H2O+CO2↑,C错误;氧化铁为Fe2O3,氧化铁与稀盐酸混合
的离子方程式为:Fe2O3+6H
+2Fe
3++3H2O,D 错误.
13.
D 【解析】由(1)取少量粉末加入水中,振荡,有白色沉淀生成,可知白色沉淀为碳酸钡或碳酸钙,则一定有
K2CO3;由(2)向悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;(3)向少量(2)的溶液中加入AgNO3
溶液,有白色沉淀生成,可知(3)中白色沉淀为AgCl,则原粉末一定含CaCl
2,不能确定是否含Ba(NO3)
2.根据
以上分析可知不一定有Ba(NO3)
2,A 错误、B错误;肯定有K2CO3、CaCl
2,C错误、D 正确.
14.
D 【解析】已知氧化性:氧化剂>氧化产物,则ClO
-
3+5Cl
-+6H
+3Cl
2↑+3H2O 中氧化性:ClO
-
3>Cl
2;
2FeCl
3+2KI2FeCl
2+2KCl+I
2中氧化性:Fe
3+>I
2;再结合2FeCl
2+Cl
22FeCl
3可知氧化性:Cl
2>
Fe
3+,即氧化性:ClO
-
3>Cl
2>Fe
3+>I
2,选D.
15.AD 【解析】反应2KNO3+3C+SK2S+N2↑+3CO2↑中,N 的化合价降低得电子,KNO3是氧化剂,S的
化合价降低得电子,S是氧化剂,A 正确;反应2KNO3+3C+SK2S+N2↑+3CO2↑中,S发生还原反应,B
错误;C到CO2,C 的化合价升高,CO2是氧化产物,C 错误;CO2中C 的化合价为+4价,C 单质中的C 为0
价,一般情况下,同种元素化合价越高氧化性越强,氧化性CO2>C,D 正确.
16.(12分)
(1)②⑤⑧⑩(2分) ①⑦(1分) ③④⑥⑧(1分)
(2)CE(2分)
{#{QQABYYwQggAAAIAAABgCQQ0QCkCQkBGCCYoGRBAYMAAAiRFABAA=}#}
化学答案第3
页(共5页)
(3)红褐色(2分) FeCl
3+3H2O
△
Fe(OH)
3(胶体)+3HCl(2分)
(4)ABC(2分)
【解析】(1)电解质是水溶液或熔融状态可以导电的化合物,属于电解质的是②⑤⑧⑩;非电解质是水溶液中或
熔融状态都不能导电的化合物,属于非电解质的是①⑦;可以导电的是金属或者有可自由移动的离子的物
质,为③④⑥⑧.
(2)属于如图所示化学概念交叉部分的物质是非电解质,水溶液可以导电,液态不导电的物质,选CE.
(3)制备氢氧化铁胶体是将饱和氯化铁溶液滴入沸水中,继续煮沸至溶液呈红褐色,停止加热.化学方程式为
FeCl
3+3H2O
△
Fe(OH)
3(胶体)+3HCl.
(4)关于FeCl
3溶液和Fe(OH)
3胶体这两种分散系,一种是溶液,一种是胶体:溶液稳定性大于胶体,稳定性:
FeCl
3溶液>Fe(OH)
3胶体,A 正确;胶体中分散质粒子直径为1~100nm,B正确;FeCl
3溶液和Fe(OH)
3胶体
都能透过滤纸,C正确.
17.(12分)
(1)Ca(OH)
2(2分)
(2)干燥剂(2分)
(3)Na2CO3+CaCl
2CaCO3↓+2NaCl(2分,合理即可)
(4)CO
2-
3、SO
2-
4、Na
+(2分)
(5)H
+、Ba
2+(2分)
(6)Cl
-(2分)
【解析】Ⅰ.石灰石(主要成分为碳酸钙)高温分解生成CaO 和CO2,CaO 能与水反应生成Ca(OH)
2,故A 是
CaO,C是CO2,B是Ca(OH)
2,CaO 易吸水,可用作干燥剂,Ca(OH)
2能与CO2反应生成CaCO3和H2O.
Ⅱ.①向溶液中加入过量的BaCl
2溶液,有白色沉淀产生,说明可能是碳酸钡、硫酸钡,说明不含有Ba
2+.②向
①中滤液里加入AgNO3溶液,有白色沉淀产生,不能说明含有氯离子,因为加入了氯化钡.③将①中的沉淀加
入稀盐酸中,沉淀部分消失,有气体产生,说明沉淀为碳酸钡、硫酸钡,即原溶液含硫酸根和碳酸根,说明不含氢
离子.
18.(12分)
(1)Ba(OH)
2Ba
2++2OH
-(1分)
(2)红色变浅直到消失(1分) Ba(OH)
2+2HClBaCl
2+2H2O(2分)
(3)Ba
2+、Cl
-(2分)
(4)①(1分)
(5)H
++SO
2-
4+OH
-+Ba
2+BaSO4↓+H2O(2分) H
++OH
-H2O(1分)
(6)ad(2分)
{#{QQABYYwQggAAAIAAABgCQQ0QCkCQkBGCCYoGRBAYMAAAiRFABAA=}#}
化学答案第4
页(共5页)
【解析】(1)Ba(OH)
2为强电解质,完全电离,电离方程式:Ba(OH)
2Ba
2++2OH
-.
(2)滴有酚酞的氢氧化钡溶液显示红色,烧杯里的现象是红色变浅直到消失,溶液导电能力与离子浓度成正
比,A、B段酸碱发生中和反应生成氯化钡和水,化学方程式为Ba(OH)
2+2HClBaCl
2+2H2O.
(3)B点溶质为BaCl
2,BaCl
2完全电离,则溶液中除了含有H2O 外还含有Ba
2+、Cl
-.
(4)由分析可知代表滴加H2SO4溶液的变化曲线为①.
(5)曲线②为Ba(OH)
2溶液和NaHSO4溶液的反应,根据图知,b点溶液溶质为NaOH:
H
++SO
2-
4+OH
-+Ba
2+BaSO4↓+H2O;②中d点溶质为Na2SO4:H
++OH
-H2O.
(6)由分析知①中a点硫酸和氢氧化钡恰好完全反应,溶液中只含水;②中b点溶液溶质为NaOH;①中c点稀
硫酸过量,溶质为硫酸,②中d点溶质为Na2SO4,a、b、c、d四点对应的溶液中呈中性的是ad.
19.(12分)
(1)氧化(1分) 还原(1分)
(2)K2Cr2O7(1分) CrCl
3(1分)
(3)3∶4(2分)
(4)6(2分)
(5)15∶14(2分)
(6)44(2分)
【解析】(1)NaNO2能将Fe
2+转化为Fe
3+,铁元素化合价升高被氧化,Fe
2+是还原剂,则NaNO2是氧化剂,具有
氧化性,服用维生素C来缓解中毒状况,则维生素C可将Fe
3+转化为Fe
2+,维生素C 做还原剂,这说明维生素
C具有还原性.
(2)反应中Cr元素化合价降低被还原,氯元素化合价升高被氧化,所以K2Cr2O7为氧化剂,Cl
2是氧化产物,
CrCl
3是还原产物.
(3)被氧化的HCl与未被氧化的HCl的个数比为6∶8=3∶4.
(4)HCl生成氯气中氯元素化合价从-1升高至0价,该反应中每生成3个Cl
2转移6个电子.
(5)2NO+2CO
催化剂
N2+2CO2,NO 中N 元素化合价降低,NO 是氧化剂,CO 中C 元素化合价升高,CO 是
还原剂,氧化剂和还原剂的质量之比为(30×2)∶(28×2)15∶14.
(6)2NO+2CO
催化剂
N2+2CO2反应中,CO 中C 元素化合价升高被氧化为CO2,CO2是氧化产物,NO 和
CO2的质量比为30∶44,若消耗3gNO 得到氧化产物的质量为44g.
20.(12分)
(1)①+1(1分)
②正盐(1分)
③H3PO4(2分)
{#{QQABYYwQggAAAIAAABgCQQ0QCkCQkBGCCYoGRBAYMAAAiRFABAA=}#}
化学答案第5
页(共5页)
(2)6H2O+2P4+3Ba(OH)
22PH3↑+3Ba(H2PO2)
2(2分)
(3)①漏斗、烧杯、玻璃棒(2分)
②CaCO3(2分)
③加热浓缩,冷却结晶(2分)
【解析】(1)①次磷酸中氢元素化合价为+1价、氧元素的化合价为-2价,由化合价的代数和为0可知,分子中
磷元素的化合价为+1价;②由题意可知,次磷酸与足量的氢氧化钠溶液反应,只生成NaH2PO2,说明
NaH2PO2是正盐;③由题意可知,利用次磷酸进行化学镀银反应时,银元素的化合价降低被还原,银离子是反应
的氧化剂,磷元素的化合价升高被氧化,次磷酸是还原剂,设氧化产物中磷元素的化合价为+a价,反应中氧化
剂与还原剂的粒子个数之比为4∶1,由得失电子数目守恒可得:1×4=(a-1)×1,解得a=5,则氧化产物为磷
酸,化学式为H3PO4.
(2)由题意可知,白磷与氢氧化钡溶液反应生成磷化氢气体和次磷酸钡,反应的化学方程式为6H2O+2P4+
3Ba(OH)
22PH3↑+3Ba(H2PO2)
2.
(3)①过滤操作所用到的玻璃仪器为漏斗、烧杯、玻璃棒;②滤渣2的主要成分为碳酸钙;③从滤液获得晶体的
操作是加热浓缩、冷却结晶、过滤、洗涤、干燥.
{#{QQABYYwQggAAAIAAABgCQQ0QCkCQkBGCCYoGRBAYMAAAiRFABAA=}#}