文档内容
1
答案:D
解析:
废旧电池回收可减少环境污染并实现金属资源再利用(A正确)。
正极片含可回收金属元素 Al、Fe、Li(B正确)。
硝酸将亚铁离子氧化为 Fe³⁺,故沉淀成分为 Fe(OH)₃(C正确)。
硫酸钠无法沉淀锂离子,不可替代碳酸钠(D错误)。
———
2
答案:AB
解析:
果糖为单糖,蔗糖和麦芽糖是双糖(A错误)。
酶的本质主要是蛋白质,但存在非蛋白类生物催化剂(B错误)。
植物油含不饱和脂肪酸酯,可与溴发生加成反应(C正确)。
淀粉和纤维素水解终产物均为葡萄糖(D正确)。
———
3
答案:D
解析:
乙酸乙酯的制备及纯化流程包括:
1. 试管中加热反应混合液(涉及);
2. 导气管通入饱和 Na₂CO₃ 溶液吸收杂质(涉及);
3. 分液分离酯层(涉及);
未涉及蒸发结晶操作(D选项)。
———
4
答案:B
解析:
胶体粒子为多分子聚集体,0.1 mol FeCl₃ 形成胶粒数远少于 0.1Nₐ(A错误)。
标准状况下 1 mol Ar 含 18 mol 质子(B正确)。
1 mol 丙三醇含 3 mol 羟基(C错误)。
CH₄ 与 Cl₂ 取代产物为混合物,CH₃Cl 分子数少于 1.0Nₐ(D错误)。
———
5
答案:C
解析:
螺(2,2)戊烷(C₅H₈)与环戊烯互为同分异构体(A正确)。
分子含4类氢原子,二氯代物超过2种(B正确)。
中心碳原子呈四面体构型,所有碳原子不共面(C错误)。
生成 1 mol C₅H₁₂ 需消耗 2 mol H₂(D正确)。
———
6
答案:B
解析:
第1页 | 共3页 W(F)、X(Na/Mg)、Y(Cl)、Z(Ca/K)。
X 单质(Na/Mg)常温为固体(A错误)。
Z 氢化物(CaH₂/KH)为离子化合物(B正确)。
Y、Z 化合物(CaCl₂/KCl)水溶液呈中性(C错误)。
F 无正价,Cl 最高+7价(D错误)。
———
7
答案:C
解析:
阴极反应:CO₂ + 2H⁺ + 2e⁻ → CO + H₂O(A正确)。
总反应:CO₂ + H₂S → CO + H₂O + S(B正确)。
石墨烯(阳极)电势高于 ZnO@石墨烯(阴极)(C错误)。
Fe³⁺/Fe²⁺ 需酸性环境防沉淀(D正确)。
———
8
答案及解析:
(1) 蒸馏水煮沸除氧;仪器 a 为分液漏斗。
(2)
① 离子方程式:Zn + 2Cr³⁺ → Zn²⁺ + 2Cr²⁺
② 氢气排除装置内空气,防 Cr²⁺ 氧化。
(3) 氢气压强使溶液流入 d;操作:冷却结晶、过滤。
(4) d 为敞开体系,可能氧化醋酸亚铬。
———
9
答案及解析:
(1) 2NaHSO₃ → Na₂S₂O₅ + H₂O
(2)
① pH=4.1 时溶液为 NaHSO₃。
② 加入 Na₂CO₃ 并通 SO₂ 可提高 NaHSO₃ 饱和度。
(3)
阳极反应:2H₂O - 4e⁻ → O₂↑ + 4H⁺
a 室生成 NaHSO₃,经结晶得产品。
(4)
滴定反应:S₂O₅²⁻ + 2I₂ + 3H₂O → 2SO₄²⁻ + 4I⁻ + 6H⁺
SO₂ 残留量计算:
0.050002×(0.01000×0.01000)×64=0.128 g\cdotpL−1
———
10
答案及解析:
(1) 氧化产物分子式:O₂
(2)
① H = [(-4.4)/2] - (-55.3) = +53.1 kJ·mol⁻¹
② t=62 min 时,p(N₂O₅) = 30.0 kPa,v = 6.0×10⁻² kPa·min⁻¹
△
③ 35 时 p∞ > 63.1 kPa(温度升高促进 N₂O₄ 解离,气体总量增加)。
℃
第2页 | 共3页④ 平衡常数 K_p = 13.4 kPa(计算基于 NO₂ 与 N₂O₄ 分压比)。
(3)
第一步逆反应速率 > 第二步反应速率(A正确)。
NO₂ 与 NO₃ 碰撞部分有效(C正确)。
———
11(物质结构)
答案及解析:
(1) 能量最低态:D;最高态:C
(2) Li⁺ 核电荷数大,离子半径小于 H⁻。
(3)
阴离子 [AlH₄]⁻ 为正四面体构型(sp³ 杂化)。
含离子键、σ键(AB正确)。
(4)
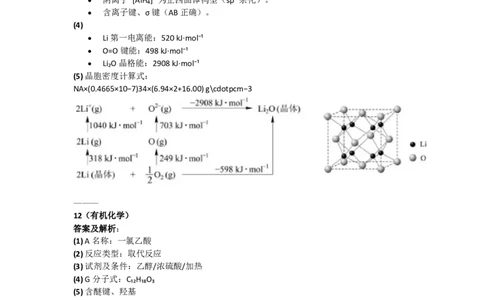
Li 第一电离能:520 kJ·mol⁻¹
O=O 键能:498 kJ·mol⁻¹
Li₂O 晶格能:2908 kJ·mol⁻¹
(5) 晶胞密度计算式:
NA×(0.4665×10−7)34×(6.94×2+16.00) g\cdotpcm−3
———
12(有机化学)
答案及解析:
(1) A 名称:一氯乙酸
(2) 反应类型:取代反应
(3) 试剂及条件:乙醇/浓硫酸/加热
(4) G 分子式:C₁₂H₁₈O₃
(5) 含醚键、羟基
(6) E 的同分异构体(酯类,核磁共振氢谱 1:1):
CHX3CHX2OOC−COOCHX2CHX3 CHX3CHX2OOC−COOCHX2CHX3
(7) 苯乙酸苄酯合成路线:
∣
苯甲醇HCl氯苄NaCN苯乙腈HX3OX+苯乙酸CHX3OH苯乙酸苄酯
———
第3页 | 共3页