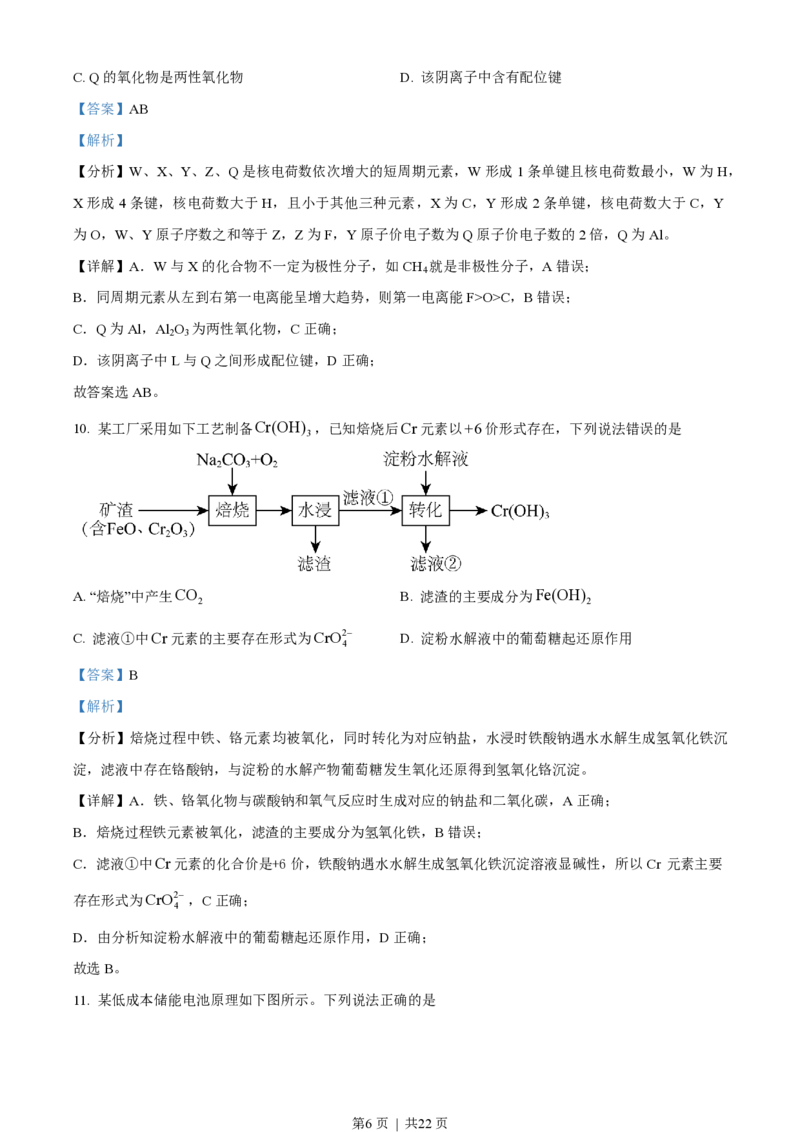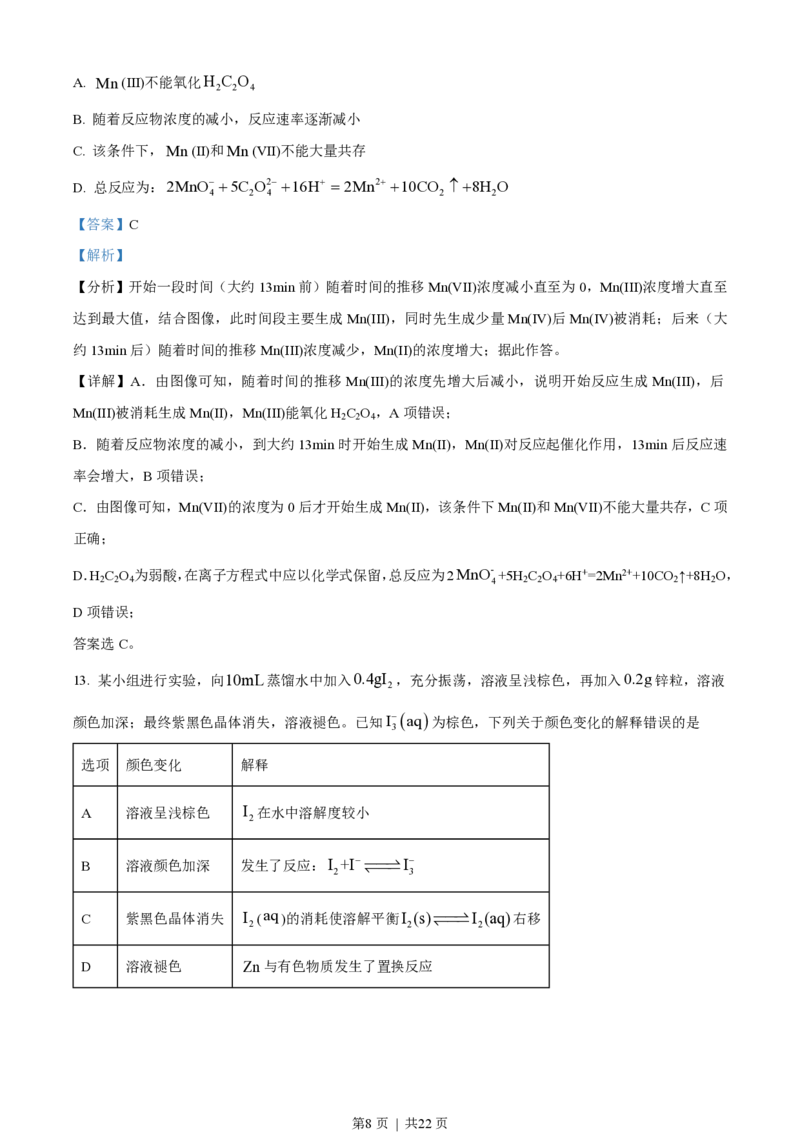文档内容
辽宁省 2023 年普通高等学校招生选择性考试(化学)
本试卷满分 100分,考试时间 75分钟。
可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 Na-23 S-32 Fe-56
一、选择题:本题共 15小题,每小题 3分,共 45分。在每小题给出的四个选项中,只有一
项符合题目要求。
的
1. 科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误 是
A. 利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
B. 发现了月壤中的“嫦娥石[(Ca Y)Fe(PO ) ]”:其成分属于无机盐
8 4 7
C. 研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D. 革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
【答案】A
【解析】
【详解】A.常见的脂肪酸有:硬脂酸(C H COOH)、油酸(C H COOH),二者相对分子质量虽大,但没
17 35 17 33
有达到高分子化合物的范畴,不属于有机高分子,A错误;
B.嫦娥石因其含有Y、Ca、Fe等元素,属于无机化合物,又因含有磷酸根,是无机盐,B正确;
C.电池是一种可以将其他能量转化为电能的装置,钙钛矿太阳能电池可以将太阳能转化为电能,C正确;
D.海水中含有大量的无机盐成分,可以将大多数物质腐蚀,而聚四氟乙烯塑料被称为塑料王,耐酸、耐碱,
不会被含水腐蚀,D正确;
故答案选A。
2. 下列化学用语或表述正确的是
A. BeCl 的空间结构:V形 B. P 中的共价键类型:非极性键
2 4
C. 基态Ni原子价电子排布式:3d10 D. 顺—2—丁烯的结构简式:
【答案】B
【解析】
【详解】A.BeCl 的中心原子为Be,根据VSEPR模型可以计算,BeCl 中不含有孤电子对,因此BeCl 为
2 2 2
直线型分子,A错误;
B.P 分子中相邻两P原子之间形成共价键,同种原子之间形成的共价键为非极性共价键,P 分子中的共价
4 4
键类型为非极性共价键,B正确;
第1页 | 共22页C.Ni原子的原子序数为28,其基态原子的价电子排布为3d84s2,C错误;
D.顺-2-丁烯的结构中两个甲基在双键的同一侧,其结构简式为 ,D错误;
故答案选B。
3. 下列有关物质的工业制备反应错误的是
点燃
A. 合成氨:N +3H ‡ˆ ˆˆ 高温ˆˆ 、ˆˆ 高ˆˆ 压ˆ†ˆˆ 2NH B. 制HCl:H +Cl 2HCl
2 2 催化剂 3 2 2
高温 电解
C. 制粗硅:SiO +2C Si+2CO D. 冶炼镁:2MgO(熔融) 2Mg+O ↑
2 2
【答案】D
【解析】
【详解】A.工业合成氨是利用氮气和氢气在催化剂的条件下反应生成的,反应方程式为N +3H ‡ˆ ˆˆ 高温ˆˆ 、ˆˆ 高ˆˆ 压ˆ†ˆˆ
2 2 催化剂
2NH ,A正确;
3
点燃
B.工业制氯化氢是利用氢气和氯气反应生成的,反应方程式为H +Cl 2HCl,B正确;
2 2
高温
C.工业制粗硅是将SiO 与C在高温下反应生成粗硅,反应方程式为SiO +2C Si+2CO,C正确;
2 2
电解
D.冶炼金属镁是电解熔融氯化镁,反应方程式为MgCl (熔融) Mg+Cl ↑,D错误;
2 2
故答案选D。
4. 下列鉴别或检验不能达到实验目的的是
A. 用石灰水鉴别Na CO 与NaHCO
2 3 3
B. 用KSCN溶液检验FeSO 是否变质
4
C. 用盐酸酸化的BaCl 溶液检验Na SO 是否被氧化
2 2 3
D. 加热条件下用银氨溶液检验乙醇中是否混有乙醛
【答案】A
【解析】
【详解】A.石灰水的主要成分为Ca(OH) 能与碳酸钠和碳酸氢钠反应生成碳酸钙,二者均生成白色沉淀,
2
不能达到鉴别的目的,A错误;
B.Fe2+变质后会生成Fe3+,可以利用KSCN溶液鉴别,现象为溶液变成血红色,可以达到检验的目的,B
第2页 | 共22页正确;
C.Na SO 被氧化后会变成Na SO ,加入盐酸酸化的BaCl 后可以产生白色沉淀,可以用来检验Na SO 是
2 3 2 4 2 2 3
否被氧化,C正确;
D.含有醛基的物质可以与银氨溶液反应生成银单质,可以用来检验乙醇中混油的乙醛,D正确;
故答案选A。
5. 我国古代四大发明之一黑火药的爆炸反应为:S+2KNO +3C=K S+N +3CO 。设N 为阿伏
3 2 2 2 A
加德罗常数的值,下列说法正确的是
A. 11.2LCO 含π键数目为N B. 每生成2.8gN 转移电子数目为N
2 A 2 A
C. 0.1molKNO 晶体中含离子数目为0.2N D. 1L0.1mol×L-1K S溶液中含S2-数目为0.1N
3 A 2 A
【答案】C
【解析】
【详解】A.CO 分子含有2个键,题中没有说是标况条件下,气体摩尔体积未知,无法计算键个
2
数,A项错误;
m 2.8
B.2.8gN 的物质的量n= = mol=0.1mol,1molN 生成转移的电子数为12N ,则0.1molN 转
2 M 28 2 A 2
移的电子数为1.2N ,B项错误;
A
C.0.1molKNO 晶体含有离子为K+、NO-,含有离子数目为0.2N ,C项正确;
3 3 A
D.因为S2-水解使溶液中S2-的数目小于0.1N ,D项错误;
A
答案选C。
6. 在光照下,螺呲喃发生开、闭环转换而变色,过程如下。下列关于开、闭环螺呲喃说法正确的是
A. 均有手性 B. 互为同分异构体
C. N原子杂化方式相同 D. 闭环螺吡喃亲水性更好
【答案】B
【解析】
【详解】A.手性是碳原子上连有四个不同的原子或原子团,因此闭环螺吡喃含有手性碳原子如图所示,
第3页 | 共22页,开环螺吡喃不含手性碳原子,故A错误;
B.根据它们的结构简式,分子式均为C H NO,它们结构不同,因此互为同分异构体,故B正确;
19 19
C.闭环螺吡喃中N原子杂化方式为sp3,开环螺吡喃中N原子杂化方式为sp2,故C错误;
D.开环螺吡喃中氧原子显负价,电子云密度大,容易与水分子形成分子间氢键,水溶性增大,因此开环
螺吡喃亲水性更好,故D错误;
答案为B。
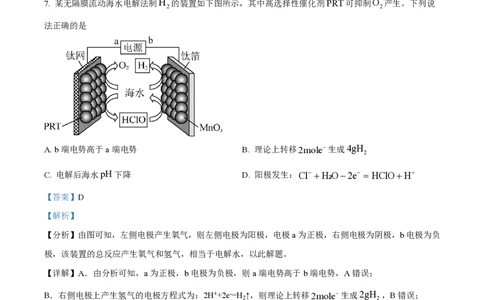
7. 某无隔膜流动海水电解法制H 的装置如下图所示,其中高选择性催化剂PRT可抑制O 产生。下列说
2 2
法正确的是
A. b端电势高于a端电势 B. 理论上转移2mole-生成4gH
2
C. 电解后海水pH下降 D. 阳极发生:Cl- +H₂O-2e- = HClO+H+
【答案】D
【解析】
【分析】由图可知,左侧电极产生氧气,则左侧电极为阳极,电极a为正极,右侧电极为阴极,b电极为负
极,该装置的总反应产生氧气和氢气,相当于电解水,以此解题。
【详解】A.由分析可知,a为正极,b电极为负极,则a端电势高于b端电势,A错误;
B.右侧电极上产生氢气的电极方程式为:2H++2e-=H ↑,则理论上转移2mole-生成2gH ,B错误;
2 2
C.由图可知,该装置的总反应为电解海水的装置,随着电解的进行,海水的浓度增大,但是其pH基本不
变,C错误;
D.由图可知,阳极上的电极反应为:Cl-+H₂O-2e-=HClO+H+,D正确;
故选D。
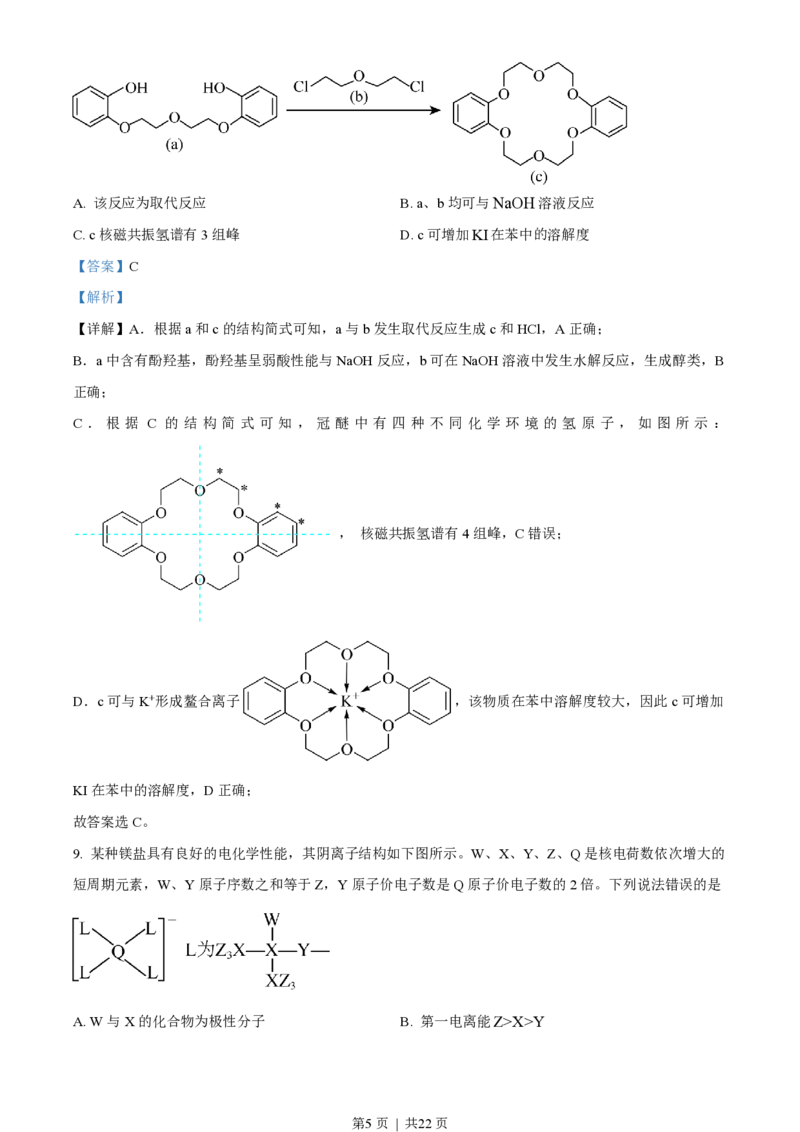
8. 冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别K+,其合成方法如下。下列说法错误的是
第4页 | 共22页A. 该反应为取代反应 B. a、b均可与NaOH溶液反应
C. c核磁共振氢谱有3组峰 D. c可增加KI在苯中的溶解度
【答案】C
【解析】
【详解】A.根据a和c的结构简式可知,a与b发生取代反应生成c和HCl,A正确;
B.a中含有酚羟基,酚羟基呈弱酸性能与NaOH反应,b可在NaOH溶液中发生水解反应,生成醇类,B
正确;
C . 根 据 C 的 结 构 简 式 可 知 , 冠 醚 中 有 四 种 不 同 化 学 环 境 的 氢 原 子 , 如 图 所 示 :
, 核磁共振氢谱有4组峰,C错误;
D.c可与K+形成鳌合离子 ,该物质在苯中溶解度较大,因此c可增加
KI在苯中的溶解度,D正确;
故答案选C。
9. 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q是核电荷数依次增大的
短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是
A. W与X的化合物为极性分子 B. 第一电离能Z>X>Y
第5页 | 共22页C. Q的氧化物是两性氧化物 D. 该阴离子中含有配位键
【答案】AB
【解析】
【分析】W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W形成1条单键且核电荷数最小,W为H,
X形成4条键,核电荷数大于H,且小于其他三种元素,X为C,Y形成2条单键,核电荷数大于C,Y
为O,W、Y原子序数之和等于Z,Z为F,Y原子价电子数为Q原子价电子数的2倍,Q为Al。
【详解】A.W与X的化合物不一定为极性分子,如CH 就是非极性分子,A错误;
4
B.同周期元素从左到右第一电离能呈增大趋势,则第一电离能F>O>C,B错误;
C.Q为Al,Al O 为两性氧化物,C正确;
2 3
D.该阴离子中L与Q之间形成配位键,D正确;
故答案选AB。
10. 某工厂采用如下工艺制备Cr(OH) ,已知焙烧后Cr元素以+6价形式存在,下列说法错误的是
3
A. “焙烧”中产生CO B. 滤渣的主要成分为Fe(OH)
2 2
C. 滤液①中Cr元素的主要存在形式为CrO2- D. 淀粉水解液中的葡萄糖起还原作用
4
【答案】B
【解析】
【分析】焙烧过程中铁、铬元素均被氧化,同时转化为对应钠盐,水浸时铁酸钠遇水水解生成氢氧化铁沉
淀,滤液中存在铬酸钠,与淀粉的水解产物葡萄糖发生氧化还原得到氢氧化铬沉淀。
【详解】A.铁、铬氧化物与碳酸钠和氧气反应时生成对应的钠盐和二氧化碳,A正确;
B.焙烧过程铁元素被氧化,滤渣的主要成分为氢氧化铁,B错误;
C.滤液①中Cr元素的化合价是+6价,铁酸钠遇水水解生成氢氧化铁沉淀溶液显碱性,所以Cr 元素主要
存在形式为CrO2-,C正确;
4
D.由分析知淀粉水解液中的葡萄糖起还原作用,D正确;
故选B。
11. 某低成本储能电池原理如下图所示。下列说法正确的是
第6页 | 共22页A. 放电时负极质量减小
B. 储能过程中电能转变为化学能
C. 放电时右侧H+通过质子交换膜移向左侧
D. 充电总反应:Pb+SO2- + 2Fe3+ = PbSO + 2Fe2+
4 4
【答案】B
【解析】
【分析】该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO ,则多孔碳电极为正极,正极
4
上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO 电极为阴极,PbSO
4 4
得电子生成Pb和硫酸。
【详解】A.放电时负极上Pb失电子结合硫酸根离子生成PbSO 附着在负极上,负极质量增大,A错误;
4
B.储能过程中,该装置为电解池,将电能转化为化学能,B正确;
C.放电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的H+通过质子交换膜移向右侧,C错
误;
D.充电时,总反应为PbSO +2Fe2+=Pb+SO2-+2Fe3+,D错误;
4 4
故答案选B。
12. 一定条件下,酸性KMnO 溶液与H C O 发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒
4 2 2 4
子的浓度随时间变化如下图所示。下列说法正确的是
第7页 | 共22页A. Mn(Ⅲ)不能氧化H C O
2 2 4
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
D. 总反应为:2MnO- +5C O2- +16H+ =2Mn2+ +10CO +8H O
4 2 4 2 2
【答案】C
【解析】
【分析】开始一段时间(大约13min前)随着时间的推移Mn(VII)浓度减小直至为0,Mn(III)浓度增大直至
达到最大值,结合图像,此时间段主要生成Mn(III),同时先生成少量Mn(IV)后Mn(IV)被消耗;后来(大
约13min后)随着时间的推移Mn(III)浓度减少,Mn(II)的浓度增大;据此作答。
【详解】A.由图像可知,随着时间的推移Mn(III)的浓度先增大后减小,说明开始反应生成Mn(III),后
Mn(III)被消耗生成Mn(II),Mn(III)能氧化H C O ,A项错误;
2 2 4
B.随着反应物浓度的减小,到大约13min时开始生成Mn(II),Mn(II)对反应起催化作用,13min后反应速
率会增大,B项错误;
C.由图像可知,Mn(VII)的浓度为0后才开始生成Mn(II),该条件下Mn(II)和Mn(VII)不能大量共存,C项
正确;
D.H C O 为弱酸,在离子方程式中应以化学式保留,总反应为2MnO- +5H C O +6H+=2Mn2++10CO ↑+8H O,
2 2 4 4 2 2 4 2 2
D项错误;
答案选C。
13. 某小组进行实验,向10mL蒸馏水中加入0.4gI ,充分振荡,溶液呈浅棕色,再加入0.2g锌粒,溶液
2
颜色加深;最终紫黑色晶体消失,溶液褪色。已知I-aq
为棕色,下列关于颜色变化的解释错误的是
3
选项 颜色变化 解释
A 溶液呈浅棕色 I 在水中溶解度较小
2
B 溶液颜色加深 发生了反应:I +I- ˆˆ†I-
2 ‡ˆˆ 3
C 紫黑色晶体消失 I ( aq )的消耗使溶解平衡I (s)ˆˆ†I (aq)右移
2 2 ‡ˆˆ 2
D 溶液褪色 Zn 与有色物质发生了置换反应
第8页 | 共22页A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.向10mL蒸馏水中加入0.4gI ,充分振荡,溶液呈浅棕色,说明I 的浓度较小,因为I 在水中
2 2 2
溶解度较小,A项正确;
B.已知I-(aq)为棕色,加入0.2g锌粒后,Zn与I 反应生成ZnI ,生成的I-与I 发生反应I-+I ⇌I-,生成I-
3 2 2 2 2 3 3
使溶液颜色加深,B项正确;
C.I 在水中存在溶解平衡I (s)⇌I (aq),Zn与I 反应生成的I-与I (aq)反应生成I-,I (aq)浓度减小,上述溶
2 2 2 2 2 3 2
解平衡向右移动,紫黑色晶体消失,C项正确;
D.最终溶液褪色是Zn与有色物质发生了化合反应,不是置换反应,D项错误;
答案选D。
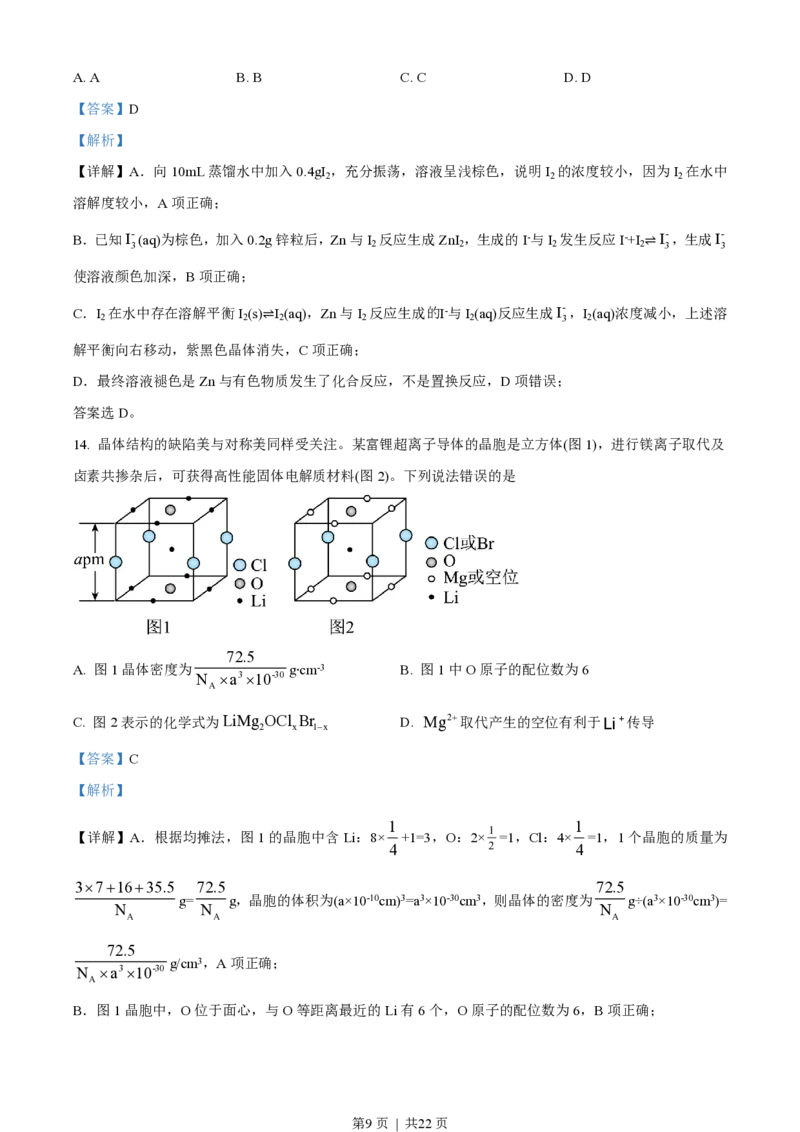
14. 晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及
卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
72.5
A. 图1晶体密度为 g∙cm-3 B. 图1中O原子的配位数为6
N ´a3´10-30
A
C. 图2表示的化学式为LiMg OCl Br D. Mg2+取代产生的空位有利于Li+传导
2 x 1-x
【答案】C
【解析】
1 1
1
【详解】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量为
4 2 4
3´7+16+35.5 72.5 72.5
g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-30cm3)=
N N N
A A A
72.5
g/cm3,A项正确;
N ´a3´10-30
A
B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B项正确;
第9页 | 共22页1 1
1
C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4× =1,Mg的个数小于
4 2 4
2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C项错误;
x 1-x
D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生的空位有利于Li+
的传导,D项正确;
答案选C。
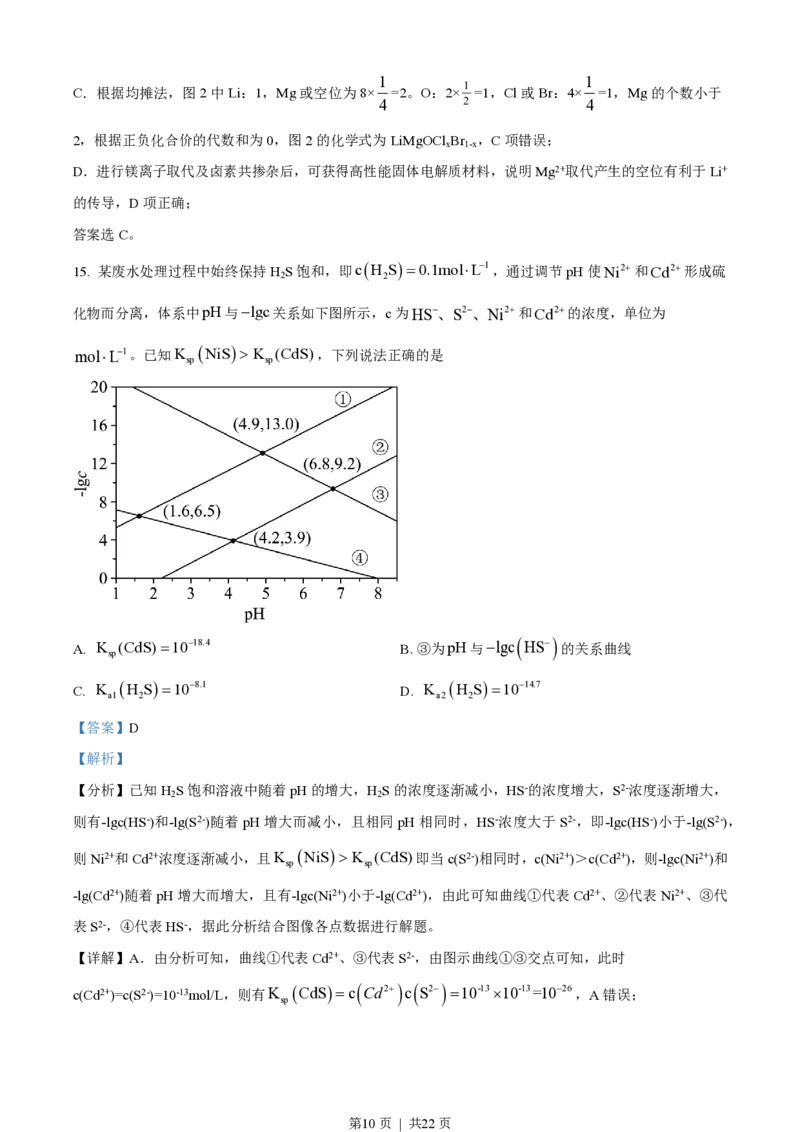
15. 某废水处理过程中始终保持H
S饱和,即cH S=0.1mol×L-1,通过调节pH使Ni2+和Cd2+形成硫
2 2
化物而分离,体系中pH与-lgc关系如下图所示,c为HS-、S2-、Ni2+和Cd2+的浓度,单位为
mol×L-1。已知K NiS> K (CdS),下列说法正确的是
sp sp
A. K (CdS)=10-18.4 B. ③为pH与-lgc HS- 的关系曲线
sp
C. K H S=10-8.1 D. K H S=10-14.7
a1 2 a2 2
【答案】D
【解析】
【分析】已知H S饱和溶液中随着pH的增大,H S的浓度逐渐减小,HS-的浓度增大,S2-浓度逐渐增大,
2 2
则有-lgc(HS-)和-lg(S2-)随着pH增大而减小,且相同pH相同时,HS-浓度大于S2-,即-lgc(HS-)小于-lg(S2-),
则Ni2+和Cd2+浓度逐渐减小,且K NiS> K (CdS)即当c(S2-)相同时,c(Ni2+)>c(Cd2+),则-lgc(Ni2+)和
sp sp
-lg(Cd2+)随着pH增大而增大,且有-lgc(Ni2+)小于-lg(Cd2+),由此可知曲线①代表Cd2+、②代表Ni2+、③代
表S2-,④代表HS-,据此分析结合图像各点数据进行解题。
【详解】A.由分析可知,曲线①代表Cd2+、③代表S2-,由图示曲线①③交点可知,此时
c(Cd2+)=c(S2-)=10-13mol/L,则有K CdS=c Cd2+ c S2- =10-13´10-13=10-26,A错误;
sp
第10页 | 共22页B.由分析可知,③为pH与-lgc
S2-
的关系曲线,B错误;
C.由分析可知,曲线④代表HS-,由图示曲线④两点坐标可知,此时c(H+)=10-1.6mol/L时,c(HS-)=10-
c
H+
c
HS-
10-1.6´10-6.5
6.5mol/L,K H S= = =10-7.1或者当c(H+)=10-4.2 mol/L时,c(HS-)=10-3.9
a1 2 cH S 0.1
2
c
H+
c
HS-
10-4.2´10-3.9
mol/L,K H S= = =10-7.1,C错误;
a1 2 cH S 0.1
2
c(H+)c(HS-) c(H+)c(S2-) c2(H+)c(S2-)
D.已知Ka Ka = × = ,由曲线③两点坐标可知,当c(H+)=10-4.9mol/L
1 2 c(H S) c(HS-) c(H S)
2 2
c2(H+)c(S2-)
时,c(S2-)=10-13mol/L,或者当c(H+)=10-6.8mol/L时,c(S2-)=10-9.2mol/L,故有Ka Ka = =
1 2
c(H S)
2
(10-4.9)2´10-13 (10-6.8)2´10-9.2
= =10-21.8,结合C项分析可知,Ka =10-7.1故有K H S=10-14.7,D正
1 a2 2
0.1 0.1
确;
故答案为:D。
二、非选择题:本题共 4小题,共 55分。
16. 某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+)。实现
镍、钴、镁元素的回收。
已知:
物质
FeOH CoOH NiOH MgOH
3 2 2 2
K 10-37.4 10-14.7 10-14.7 10-10.8
sp
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 H SO ,1molH SO 中
2 5 2 5
过氧键的数目为_______。
第11页 | 共22页(3)“氧化”中,用石灰乳调节pH=4,Mn2+被H SO 氧化为MnO ,该反应的离子方程式为
2 5 2
_______(H SO 的电离第一步完全,第二步微弱);滤渣的成分为MnO 、_______(填化学式)。
2 5 2
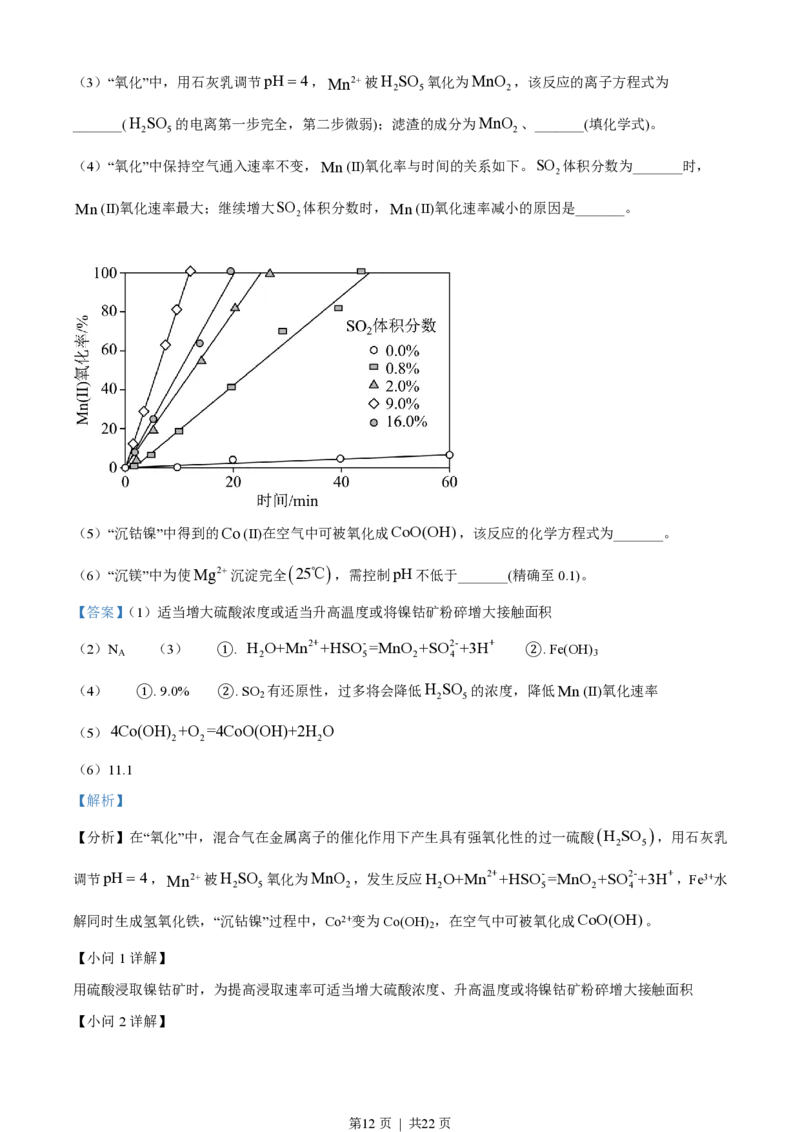
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。SO 体积分数为_______时,
2
Mn(Ⅱ)氧化速率最大;继续增大SO 体积分数时,Mn(Ⅱ)氧化速率减小的原因是_______。
2
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为_______。
(6)“沉镁”中为使Mg2+沉淀完全 25℃ ,需控制pH不低于_______(精确至0.1)。
【答案】(1)适当增大硫酸浓度或适当升高温度或将镍钴矿粉碎增大接触面积
(2)N (3) ①. H O+Mn2++HSO-=MnO +SO2-+3H+ ②. Fe(OH)
A 2 5 2 4 3
(4) ①. 9.0% ②. SO 有还原性,过多将会降低H SO 的浓度,降低Mn(Ⅱ)氧化速率
2 2 5
(5)4Co(OH) +O =4CoO(OH)+2H O
2 2 2
(6)11.1
【解析】
【分析】在“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 H SO ,用石灰乳
2 5
调节pH=4,Mn2+被H SO 氧化为MnO ,发生反应H O+Mn2++HSO-=MnO +SO2-+3H+,Fe3+水
2 5 2 2 5 2 4
解同时生成氢氧化铁,“沉钻镍”过程中,Co2+变为Co(OH) ,在空气中可被氧化成CoO(OH)。
2
【小问1详解】
用硫酸浸取镍钴矿时,为提高浸取速率可适当增大硫酸浓度、升高温度或将镍钴矿粉碎增大接触面积
【小问2详解】
第12页 | 共22页H SO 的结构简式为 ,所以1molH SO 中过氧键的数目为N
2 5 2 5 A
【小问3详解】
用石灰乳调节pH=4,Mn2+被H SO 氧化为MnO ,该反应的离子方程式为:
2 5 2
H O+Mn2++HSO-=MnO +SO2-+3H+;氢氧化铁的Ksp=10-37.4,当铁离子完全沉淀时,溶液中
2 5 2 4
c(Fe3+)=10-5mol/L,Ksp=c(OH-)3´c(Fe3+)=c(OH-)3´10-5=10-37.4,c(OH-)=10-10.8mol/L,根据Kw=10-
14,pH=3.2,此时溶液的pH=4,则铁离子完全水解,生成氢氧化铁沉淀,故滤渣还有氢氧化铁;
【小问4详解】
根据图示可知SO 体积分数为0.9%时,Mn(Ⅱ)氧化速率最大;继续增大SO 体积分数时,由于SO 有还
2 2 2
原性,过多将会降低H SO 的浓度,降低Mn(Ⅱ)氧化速率
2 5
【小问5详解】
“沉钻镍”中得到的Co(OH) ,在空气中可被氧化成CoO(OH),该反应的化学方程式为:
2
4Co(OH) +O =4CoO(OH)+2H O;
2 2 2
【小问6详解】
氢氧化镁的Ksp=10-10.8, 当镁离子完全沉淀时,c(Mg2+)=10-5mol/L,根据Ksp可计算c(OH-)=10-2.9mol/L,
根据Kw=10-14,c(H+)=10-11.1mol/L,所以溶液的pH=11.1;
17. 2—噻吩乙醇(M =128)是抗血栓药物氯吡格雷的重要中间体,其制备方法如下:
r
Ⅰ.制钠砂。向烧瓶中加入300mL液体A和4.60g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微
小钠珠出现。
Ⅱ.制噻吩钠。降温至10℃,加入25mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30min。
Ⅳ.水解。恢复室温,加入70mL水,搅拌30min;加盐酸调pH至4~6,继续反应2h,分液;用水洗
涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO ,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A
4
第13页 | 共22页后,得到产品17.92g。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择_______。
a.乙醇 b.水 c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是_______。
(3)步骤Ⅱ的化学方程式为_______。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是_______。
(5)步骤Ⅳ中用盐酸调节pH的目的是_______。
(6)下列仪器在步骤Ⅴ中无需使用的是_______(填名称):无水MgSO 的作用为_______。
4
(7)产品的产率为_______(用Na计算,精确至0.1%)。
【答案】(1)c (2): 中含有N原子,可以形成分子间氢键,氢键可以使熔沸点升高
(3)2 +2Na®2 +H
2
(4)将环氧乙烷溶液沿烧杯壁缓缓加入,此过程中不断用玻璃棒进行搅拌来散热
(5)将NaOH中和,使平衡正向移动,增大反应物的转化率
(6) ①. 球形冷凝管和分液漏斗 ②. 除去水
(7)70.0%
【解析】
【小问1详解】
步骤Ⅰ制钠砂过程中,液体A不能和Na反应,而乙醇、水和液氨都能和金属Na反应,故选c。
【小问2详解】
第14页 | 共22页噻吩沸点低于吡咯( )的原因是: 中含有N原子,可以形成分子间氢键,氢键可以使熔沸点
升高。
【小问3详解】
步骤Ⅱ中 和Na反应生成2-噻吩钠和H ,化学方程式为:2 +2Na®2
2
+H 。
2
【小问4详解】
步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是:将环氧乙烷溶液沿烧杯壁
缓缓加入,此过程中不断用玻璃棒进行搅拌来散热。
【小问5详解】
2-噻吩乙醇钠水解生成-噻吩乙醇的过程中有NaOH生成,用盐酸调节pH的目的是将NaOH中和,使平
衡正向移动,增大反应物的转化率。
【小问6详解】
步骤Ⅴ中的操作有过滤、蒸馏,蒸馏的过程中需要直形冷凝管不能用球形冷凝管,无需使用的是球形冷凝
管和分液漏斗;向有机相中加入无水MgSO 的作用是:除去水。
4
【小问7详解】
4.60g
步骤Ⅰ中向烧瓶中加入300mL液体A和4.60g金属钠,Na的物质的量为 =0.2mol,步骤Ⅱ中
23g/mol
Na完全反应,根据方程式可知,理论上可以生成0.2mol2-噻吩乙醇,产品的产率为
17.92g
´100%=70.0%。
0.2mol´128g/mol
18. 硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO ·5H O)取精华法”。借助现代仪器分析,该制备
4 2
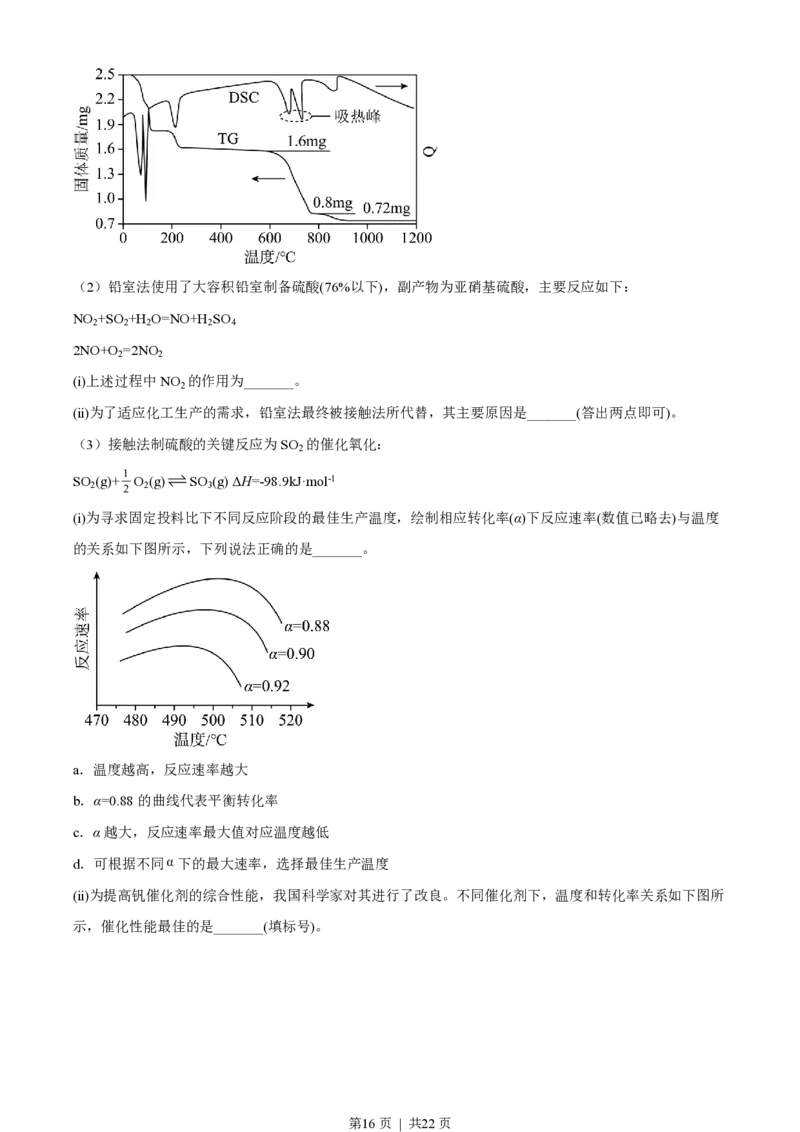
过程中CuSO ·5H O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所
4 2
示。700℃左右有两个吸热峰,则此时分解生成的氧化物有SO 、_______和_______(填化学式)。
2
第15页 | 共22页(2)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:
NO +SO +H O=NO+H SO
2 2 2 2 4
2NO+O =2NO
2 2
(ⅰ)上述过程中NO 的作用为_______。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是_______(答出两点即可)。
(3)接触法制硫酸的关键反应为SO 的催化氧化:
2
1
SO
2
(g)+
2
O
2
(g)SO
3
(g) ΔH=-98.9kJ·mol-1
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度
的关系如下图所示,下列说法正确的是_______。
a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
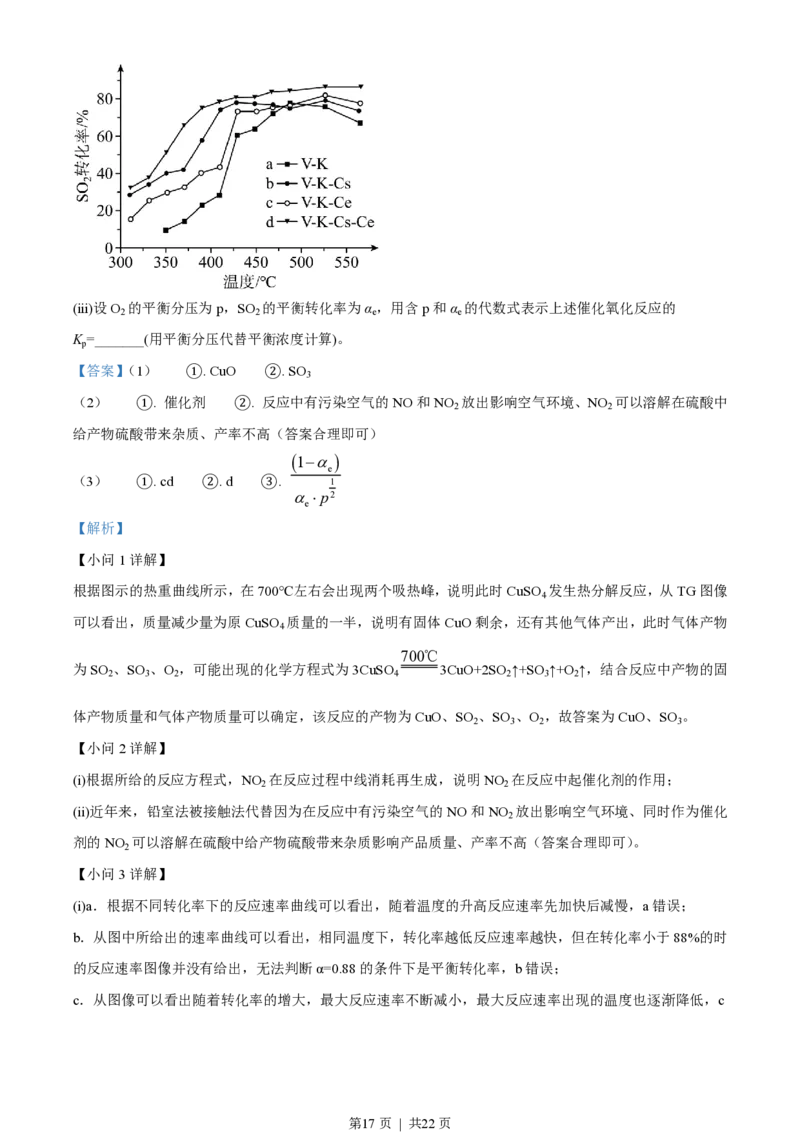
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所
示,催化性能最佳的是_______(填标号)。
第16页 | 共22页(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α ,用含p和α 的代数式表示上述催化氧化反应的
2 2 e e
K =_______(用平衡分压代替平衡浓度计算)。
p
【答案】(1) ①. CuO ②. SO
3
(2) ①. 催化剂 ②. 反应中有污染空气的NO和NO 放出影响空气环境、NO 可以溶解在硫酸中
2 2
给产物硫酸带来杂质、产率不高(答案合理即可)
1-a
e
(3) ①. cd ②. d ③. 1
a × p2
e
【解析】
【小问1详解】
根据图示的热重曲线所示,在700℃左右会出现两个吸热峰,说明此时CuSO 发生热分解反应,从TG图像
4
可以看出,质量减少量为原CuSO 质量的一半,说明有固体CuO剩余,还有其他气体产出,此时气体产物
4
700℃
为SO 、SO 、O ,可能出现的化学方程式为3CuSO 3CuO+2SO ↑+SO ↑+O ↑,结合反应中产物的固
2 3 2 4 2 3 2
体产物质量和气体产物质量可以确定,该反应的产物为CuO、SO 、SO 、O ,故答案为CuO、SO 。
2 3 2 3
【小问2详解】
(i)根据所给的反应方程式,NO 在反应过程中线消耗再生成,说明NO 在反应中起催化剂的作用;
2 2
(ii)近年来,铅室法被接触法代替因为在反应中有污染空气的NO和NO 放出影响空气环境、同时作为催化
2
剂的NO 可以溶解在硫酸中给产物硫酸带来杂质影响产品质量、产率不高(答案合理即可)。
2
【小问3详解】
(i)a.根据不同转化率下的反应速率曲线可以看出,随着温度的升高反应速率先加快后减慢,a错误;
b.从图中所给出的速率曲线可以看出,相同温度下,转化率越低反应速率越快,但在转化率小于88%的时
的反应速率图像并没有给出,无法判断α=0.88的条件下是平衡转化率,b错误;
c.从图像可以看出随着转化率的增大,最大反应速率不断减小,最大反应速率出现的温度也逐渐降低,c
第17页 | 共22页正确;
d.从图像可以看出随着转化率的增大,最大反应速率出现的温度也逐渐降低,这时可以根据不同转化率选
择合适的反应温度以减少能源的消耗,d正确;
故答案选cd;
(ii)为了提高催化剂的综合性能,科学家对催化剂进行了改良,从图中可以看出标号为d的催化剂V-K-Cs-Ce
对SO 的转化率最好,产率最佳,故答案选d;
2
n(SO )
3 p(总)
p(SO )
3
n(总)
(iii)利用分压代替浓度计算平衡常数,反应的平衡常数 K = 1 = =
p n(SO ) 1
p(SO
2
)p2(O
2
)
2 p(总)×p2(O )
n(总) 2
n(SO )
3
1 ;设 SO 初始量为 m mol,则平衡时 n(SO )=m·α ,n(SO )=m-m·α =m(1-α ),K =
2 2 e 3 e e p
n(SO )× p2(O )
2 2
m1-a 1-a 1-a
e e e
1 = 1 ,故答案为 1 。
m×a ×p2(O ) a × p2 a × p2
e 2 e e
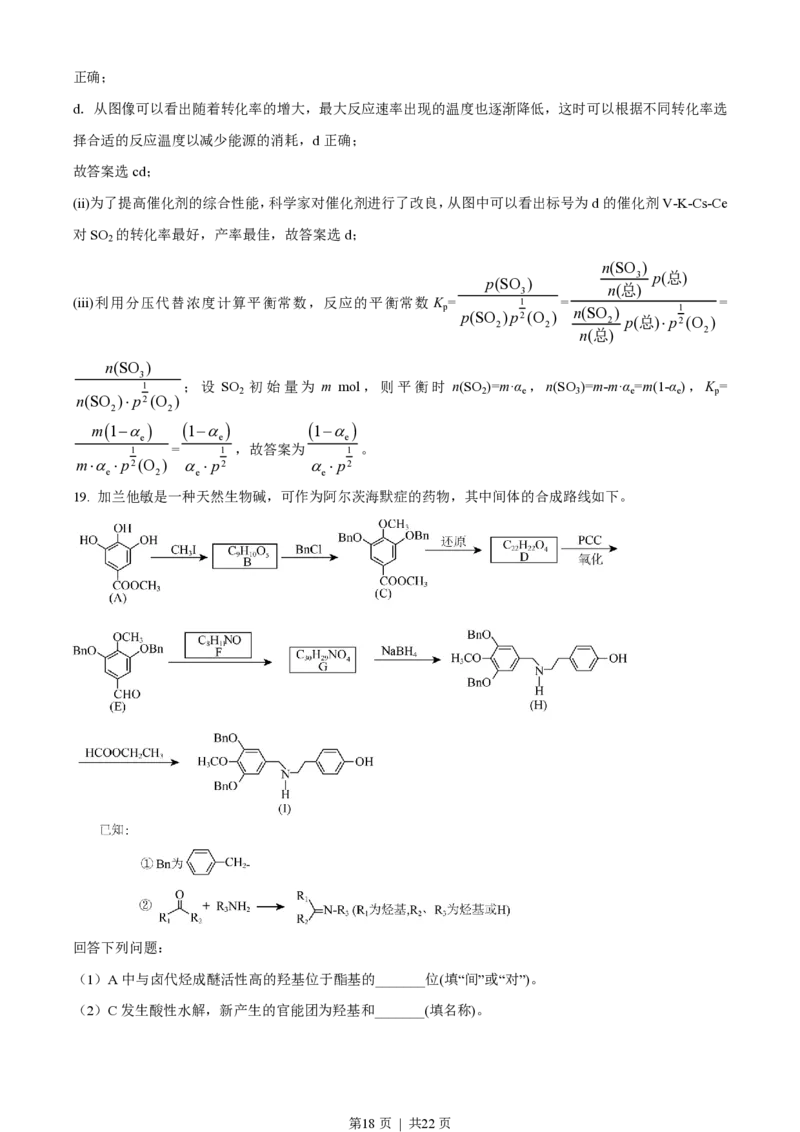
19. 加兰他敏是一种天然生物碱,可作为阿尔茨海默症的药物,其中间体的合成路线如下。
回答下列问题:
(1)A中与卤代烃成醚活性高的羟基位于酯基的_______位(填“间”或“对”)。
(2)C发生酸性水解,新产生的官能团为羟基和_______(填名称)。
第18页 | 共22页(3)用O 代替PCC完成D→E的转化,化学方程式为_______。
2
(4)F的同分异构体中,红外光谱显示有酚羟基、无N-H键的共有_______种。
(5)H→I的反应类型为_______。
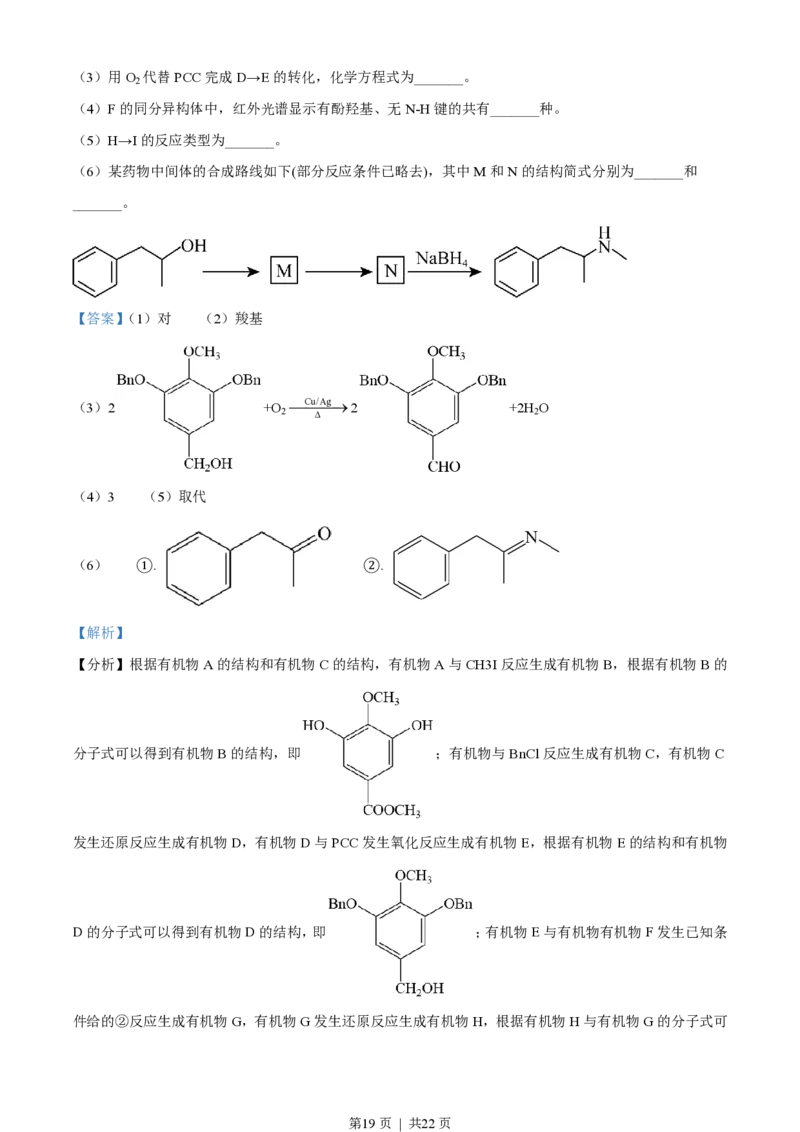
(6)某药物中间体的合成路线如下(部分反应条件已略去),其中M和N的结构简式分别为_______和
_______。
【答案】(1)对 (2)羧基
(3)2 +O ¾C¾u/A¾g®2 +2H O
2 D 2
(4)3 (5)取代
(6) ①. ②.
【解析】
【分析】根据有机物A的结构和有机物C的结构,有机物A与CH3I反应生成有机物B,根据有机物B的
分子式可以得到有机物B的结构,即 ;有机物与BnCl反应生成有机物C,有机物C
发生还原反应生成有机物D,有机物D与PCC发生氧化反应生成有机物E,根据有机物E的结构和有机物
D的分子式可以得到有机物D的结构,即 ;有机物E与有机物有机物F发生已知条
件给的②反应生成有机物G,有机物G发生还原反应生成有机物H,根据有机物H与有机物G的分子式可
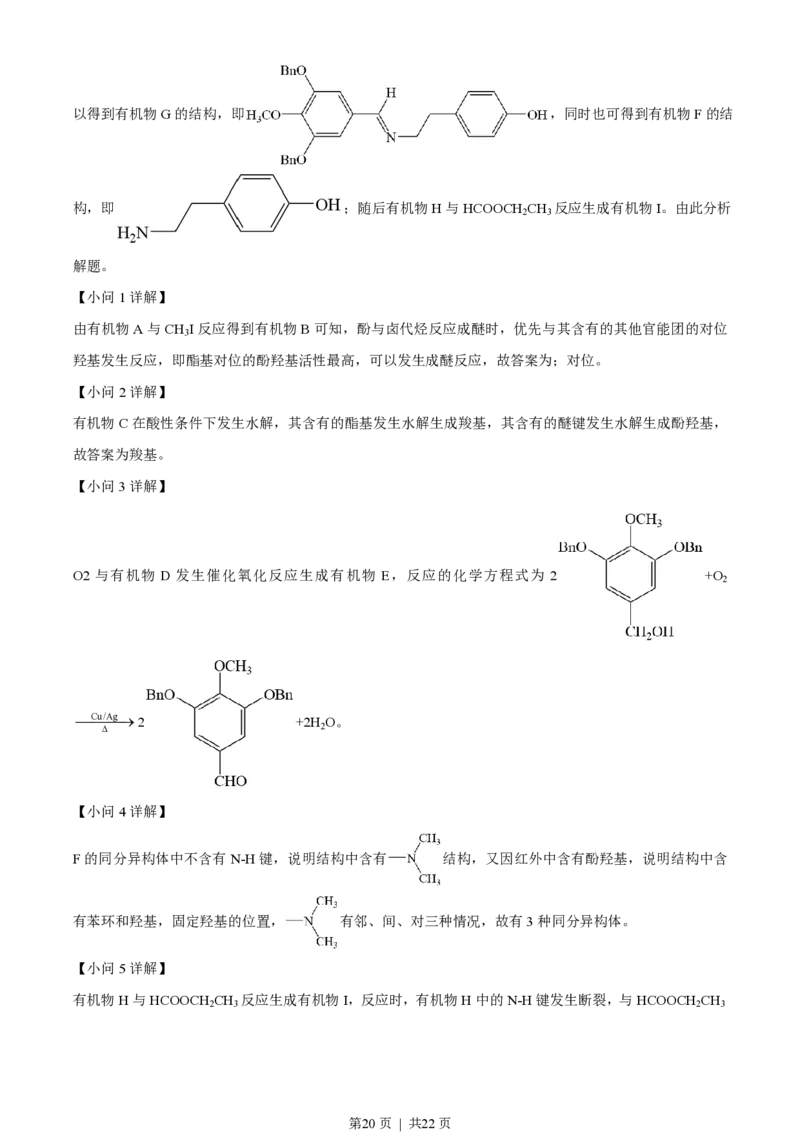
第19页 | 共22页以得到有机物G的结构,即 ,同时也可得到有机物F的结
构,即 ;随后有机物H与HCOOCH CH 反应生成有机物I。由此分析
2 3
解题。
【小问1详解】
由有机物A与CH I反应得到有机物B可知,酚与卤代烃反应成醚时,优先与其含有的其他官能团的对位
3
羟基发生反应,即酯基对位的酚羟基活性最高,可以发生成醚反应,故答案为;对位。
【小问2详解】
有机物C在酸性条件下发生水解,其含有的酯基发生水解生成羧基,其含有的醚键发生水解生成酚羟基,
故答案为羧基。
【小问3详解】
O2 与有机物 D 发生催化氧化反应生成有机物 E,反应的化学方程式为 2 +O
2
¾C¾u/A¾g®2 +2H O。
D 2
【小问4详解】
F的同分异构体中不含有N-H键,说明结构中含有 结构,又因红外中含有酚羟基,说明结构中含
有苯环和羟基,固定羟基的位置, 有邻、间、对三种情况,故有3种同分异构体。
【小问5详解】
有机物H与HCOOCH CH 反应生成有机物I,反应时,有机物H中的N-H键发生断裂,与HCOOCH CH
2 3 2 3
第20页 | 共22页中断裂的醛基结合,故反应类型为取代反应。
【小问6详解】
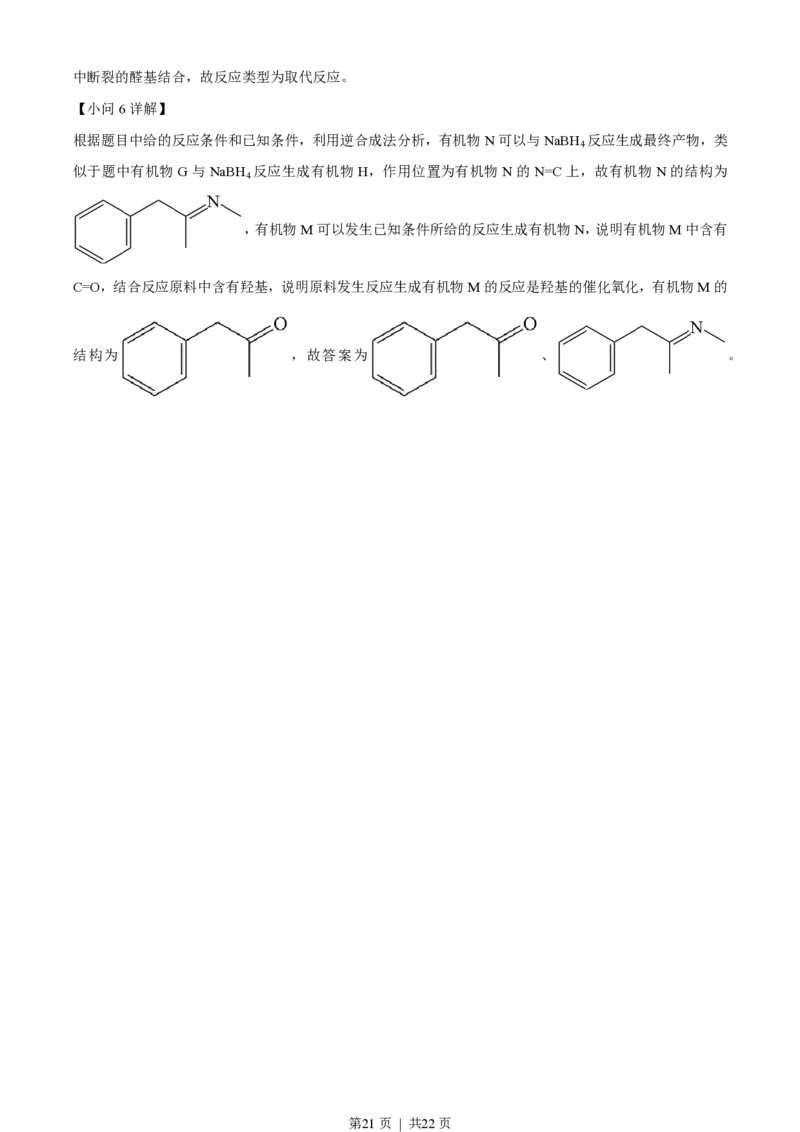
根据题目中给的反应条件和已知条件,利用逆合成法分析,有机物N可以与NaBH 反应生成最终产物,类
4
似于题中有机物G与NaBH 反应生成有机物H,作用位置为有机物N的N=C上,故有机物N的结构为
4
,有机物M可以发生已知条件所给的反应生成有机物N,说明有机物M中含有
C=O,结合反应原料中含有羟基,说明原料发生反应生成有机物M的反应是羟基的催化氧化,有机物M的
结构为 ,故答案为 、 。
第21页 | 共22页第22页 | 共22页