Nature子刊 | 碱基编辑器(ABE)体内应用的重大突破:ZSD小鼠模型的肝脏病理与代谢稳态重塑
点击蓝字

关注我们
Nature Biomedical Engineering 在线发表了一项关于体内碱基编辑(In vivo Base Editing)的重磅研究。来自 David R. Liu 团队与 Cathleen M. Lutz 团队的研究人员,成功利用腺嘌呤碱基编辑器(ABE),在齐薇格谱系障碍(Zellweger Spectrum Disorder, ZSD)的小鼠模型中,实现了对致病基因突变的精准修复。
这项研究不仅解决了长期以来ZSD缺乏根治性疗法的痛点,更重要的是,它通过详实的数据证明了:在疾病已发生的状态下,通过单次给药实现高效率、高安全性的体内基因修正,是可行的。

1. 研究背景:从“对症治疗”到“对因修正”
ZSD 是一种由于过氧化物酶体生物合成缺陷导致的常染色体隐性遗传病。其中,PEX1 基因的 p.G843D 突变(c.2528G>A)占据了约30%的等位基因突变频率。
-
病理机制: 该突变导致 PEX1 蛋白功能受损,进而引发过氧化物酶体无法组装,造成极长链脂肪酸(VLCFAs)和胆汁酸中间体的毒性堆积,最终导致严重的肝病和神经退行性病变。
-
现有局限: 目前的治疗手段(如胆酸补充)仅能缓解部分症状,无法修复根本的基因缺陷。
研究策略: 研究团队开发了针对该突变位点的 ABE 策略,旨在将错误的 A•T 碱基对直接修正为正确的 G•C 碱基对,从而恢复 PEX1 蛋白功能。
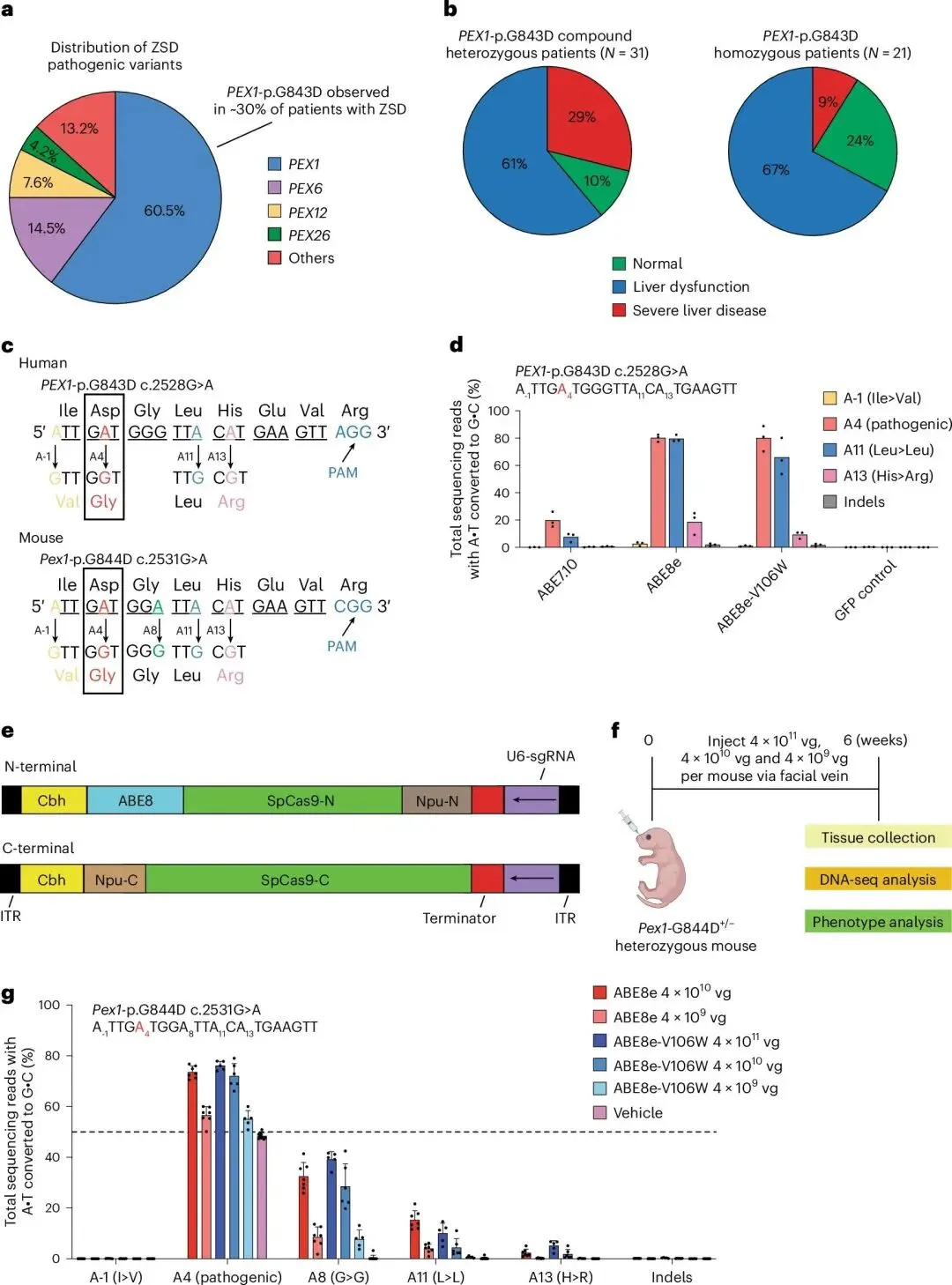
图 1:腺嘌呤碱基编辑策略校正培养的患者成纤维细胞中 PEX1-p.G843D 突变及杂合小鼠中 Pex1-p.G844D 突变的效果评估
2.核心数据:AAV 与 LNP 双平台验证
研究团队构建了携带人源化突变位点的小鼠模型(Pex1-p.G844D),并采用了两种主流的体内递送系统进行对比验证。
2.1 AAV9 递送平台(新生鼠与成年鼠)
通过静脉注射 AAV9 载体编码的 ABE8e-V106W(一种高保真变体),研究取得了令人瞩目的成效:
-
编辑效率: 在新生鼠(P1)和4周龄成年鼠中,肝脏的批量编辑效率(Bulk Editing)最高达到 60%。值得注意的是,即使在4周龄(相当于人类儿童期,此时肝脏病变已确立)给药,依然能实现高效的等位基因修正。
-
功能恢复:蛋白水平: 治疗组小鼠肝脏中过氧化物酶体膜蛋白 ABCD3 的表达量恢复至野生型水平,证明过氧化物酶体生物合成被重启。
代谢指标: 毒性代谢产物(如 C27-胆汁酸中间体、植烷酸、极长链脂肪酸)在血液和肝脏中的浓度显著下降,恢复至正常范围。
-
病理学: 肝脏脂肪变性、炎症和纤维化等组织病理学特征得到显著逆转,小鼠的生长曲线恢复正常。
-
安全性: 使用 ABE8e-V106W 变体有效降低了脱靶编辑(Off-target)和RNA脱靶效应。全基因组分析显示,其脱靶风险极低。
2.2 LNP 递送平台(非病毒递送)
为了探索更可控、可重复给药的临床路径,研究团队还使用了脂质纳米颗粒(LNP)递送 ABE8e-V106W 的 mRNA。
-
结果: 在4周龄小鼠中,LNP 递送实现了 27% 的肝脏编辑效率。
-
意义: 虽然效率略低于 AAV,但 LNP 展现出良好的耐受性,且由于 mRNA 的瞬时表达特性,进一步降低了长期脱靶风险。这为基因编辑疗法的临床应用提供了“病毒与非病毒”的双重选择。
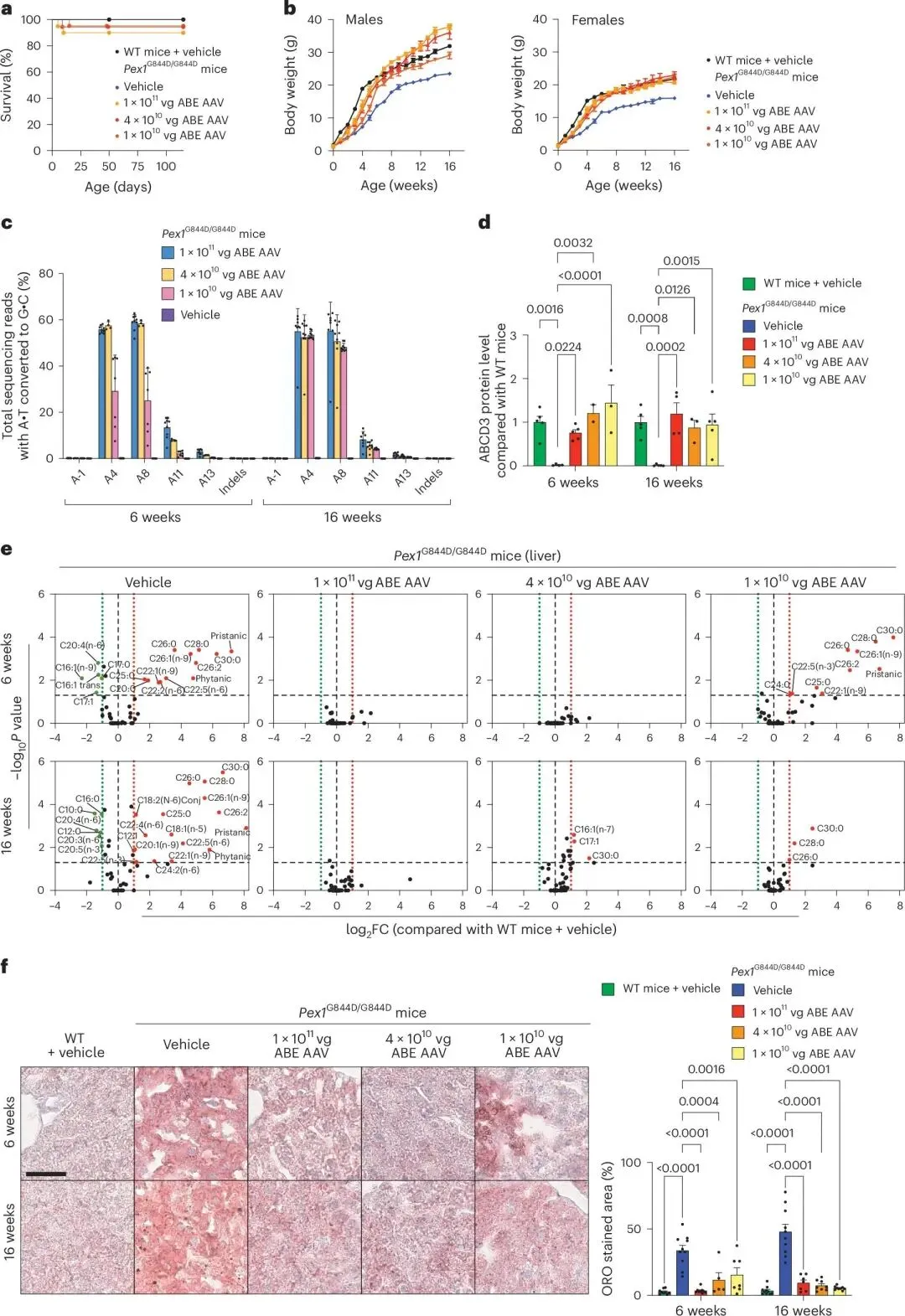
图 2:AAV9-ABE8e-V106W 治疗可挽救 Pex1G844D/G844D 新生小鼠的生长发育、过氧化物酶体功能及肝脂肪变性
3.技术亮点与行业启示
这项研究之所以被视为 2026 年基因治疗领域的标杆之作,主要基于以下三点核心价值:
(1)成年期干预的有效性:
传统的基因治疗往往强调“越早越好”。但该研究证明,即使在4周龄(成年期)小鼠中进行干预,依然能逆转已发生的肝脏纤维化和代谢紊乱。这意味着,该疗法有望覆盖到那些已经确诊的现症患者,而不仅仅是新生儿。
(2)高保真编辑器的临床验证:研究中使用的 ABE8e-V106W 是为了降低脱靶风险而进化的变体。在长达16周的观察期内,未发现明显的基因组不稳定性或异常的体重下降,这为该编辑器进入人体临床试验提供了强有力的安全性数据支持。
(3)多模态递送策略:
同时验证了 AAV(长效表达)和 LNP(瞬时表达)两种路径的成功,为不同病情阶段的患者提供了分层治疗的可能:对于需要长期稳定表达的严重患者可选用 AAV;对于需要短期干预或存在病毒中和抗体的患者,LNP 是极佳的替代方案。
结语
这项研究不仅是针对 ZSD 这一罕见病的突破,更是体内碱基编辑技术(In vivo Base Editing)成熟度的一次完美展示。
参考文献:
Gao, X.D., Presa, M., Duby, J.E. et al. In vivo base editing rescues liver pathophysiology and peroxisome dysfunction in a mouse model of Zellweger spectrum disorder. Nat. Biomed. Eng (2026). https://doi.org/10.1038/s41551-026-01651-5
基因编辑应用
Gene Editing Applications
基因编辑(gene editing),又称基因组编辑或基因组工程,通过对特定DNA片段进行敲除、插入等方式,实现对目标基因组区域的“任意编辑”,该技术被形象地称为“基因剪刀”。
基因编辑技术的发展历经了第一代的ZFNs(锌指核酸酶)技术到第二代的TALENs(转录激活因子效应物)技术,再到目前应用最广的CRISPR-Cas技术,并且该技术在2020年获诺贝尔化学奖。由于该技术具有合成简单、周期短、操作灵活、效率高等优点,现在备受人们关注。
诚如诺贝尔奖委员会的官方颁奖词所言:“借助(基因编辑)技术,研究人员可以非常精准地改变动物、植物、和微生物的DNA。CRISPR/cas9基因剪刀彻底改变了分子生命科学,为植物育种带来了新机遇,有望催生创新性癌症疗法,并可能使治愈遗传性疾病这一人类梦想美梦成真。”基因编辑技术在基因研究、基因治疗、基因调控和遗传改良等方面展示出了巨大的潜力,可广泛应用于抗体验证、靶点验证与确认、通路分析、疾病模型、生物标志物发现等领域。
“基因编辑应用”公众号专注基因编辑学术前沿,聚焦基因编辑最新研究成果,致力于分享基因编辑应用研究转化开发,发布基因编辑相关论文解读、政策研究、学术会议、临床转化及应用、行业热点等前沿资讯,为关注生命科学及基因编辑领域的科研单位与投资机构搭建交流合作的平台,定期开展基因编辑“线下投资路演”项目活动,举办基因编辑产业应用前沿高峰论坛,促进生命科学与基因编辑产业化落地与行业发展。

基因编辑·服务项目
基因敲除(KO)| 点突变(PM)
小片段敲入 | 大片段敲入(KI)
条件性基因敲除(CKO) | 类器官基因敲除
基因编辑细胞/微生物 | 基因敲入/敲除小鼠
更多科研请咨询:400-675-6758

商务合作、投稿请联系
微信号|bg-cas9
邮箱|3235735829qq.com
询洽热线 | 023-6531 6016
✦+版权声明
转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请联系我们及时更正、删除。
 夜雨聆风
夜雨聆风




