文档内容
2016年湖南省娄底市中考化学试卷
一、选择题(共15小题,每小题2分,满分30分)
1.(2分)成语是中华文化的瑰宝。下列成语涉及化学变化的是( )
A.聚沙成塔 B.死灰复燃 C.破釜沉舟 D.滴水成冰
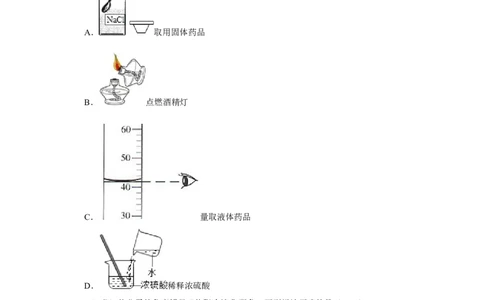
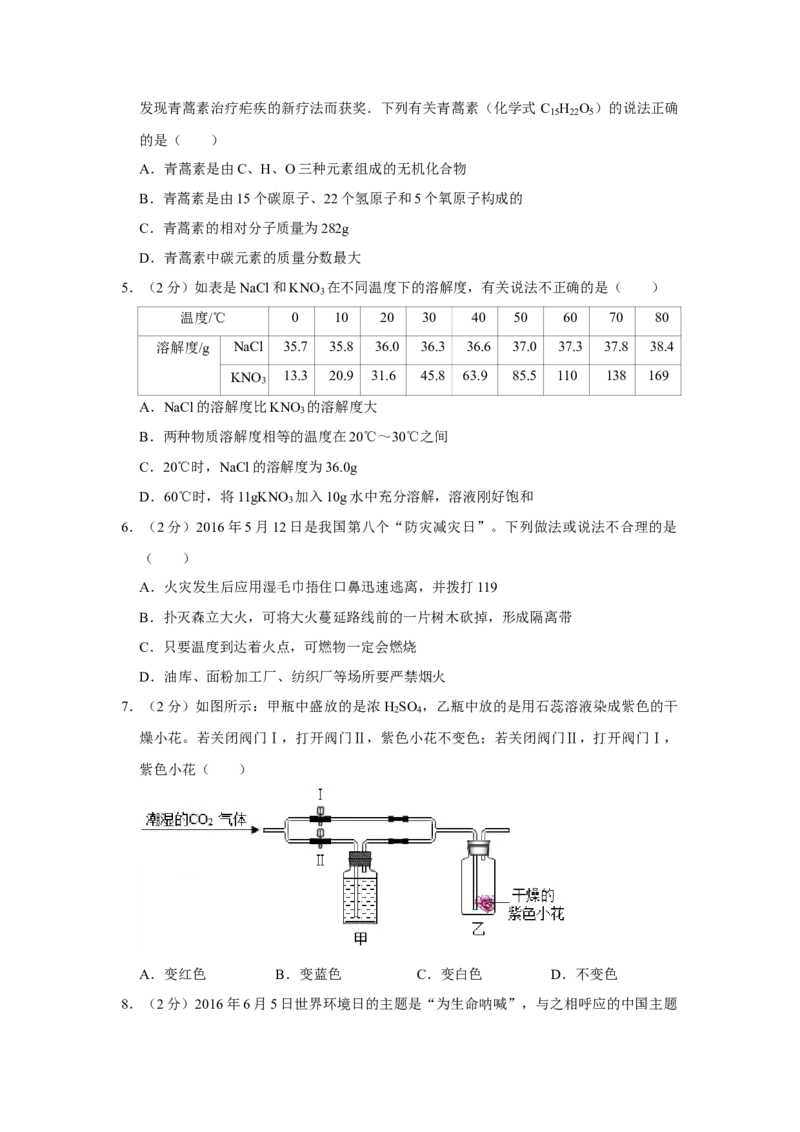
2.(2分)下列实验操作中正确的是( )
A. 取用固体药品
B. 点燃酒精灯
C. 量取液体药品
D. 稀释浓硫酸
3.(2分)从分子的角度解释“热胀冷缩'”现象,下列说法正确的是( )
A.分子遇热体积变大,遇冷体积变小
B.分子遇热间隔变大,遇冷间隔变小
C.分子遇热不断运动,遇冷静止不动
D.分子遇热数目增多,遇冷数目减少
4.(2分)2015年10月5日,瑞典卡罗琳医学院宣布将2015年诺贝尔生理学或医学奖授
予中国药学家屠呦呦等人,表彰他们在寄生虫疾病治疗研究方面取得的成就.屠呦呦因发现青蒿素治疗疟疾的新疗法而获奖.下列有关青蒿素(化学式 C H O )的说法正确
15 22 5
的是( )
A.青蒿素是由C、H、O三种元素组成的无机化合物
B.青蒿素是由15个碳原子、22个氢原子和5个氧原子构成的
C.青蒿素的相对分子质量为282g
D.青蒿素中碳元素的质量分数最大
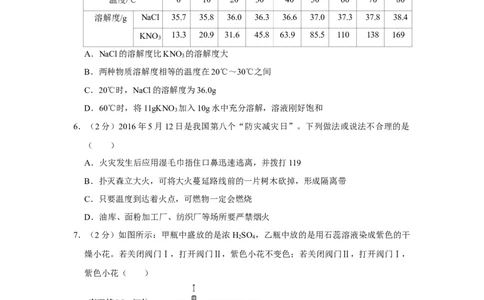
5.(2分)如表是NaCl和KNO 在不同温度下的溶解度,有关说法不正确的是( )
3
温度/℃ 0 10 20 30 40 50 60 70 80
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4
KNO 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169
3
A.NaCl的溶解度比KNO 的溶解度大
3
B.两种物质溶解度相等的温度在20℃~30℃之间
C.20℃时,NaCl的溶解度为36.0g
D.60℃时,将11gKNO 加入10g水中充分溶解,溶液刚好饱和
3
6.(2分)2016年5月12日是我国第八个“防灾减灾日”。下列做法或说法不合理的是
( )
A.火灾发生后应用湿毛巾捂住口鼻迅速逃离,并拨打119
B.扑灭森立大火,可将大火蔓延路线前的一片树木砍掉,形成隔离带
C.只要温度到达着火点,可燃物一定会燃烧
D.油库、面粉加工厂、纺织厂等场所要严禁烟火
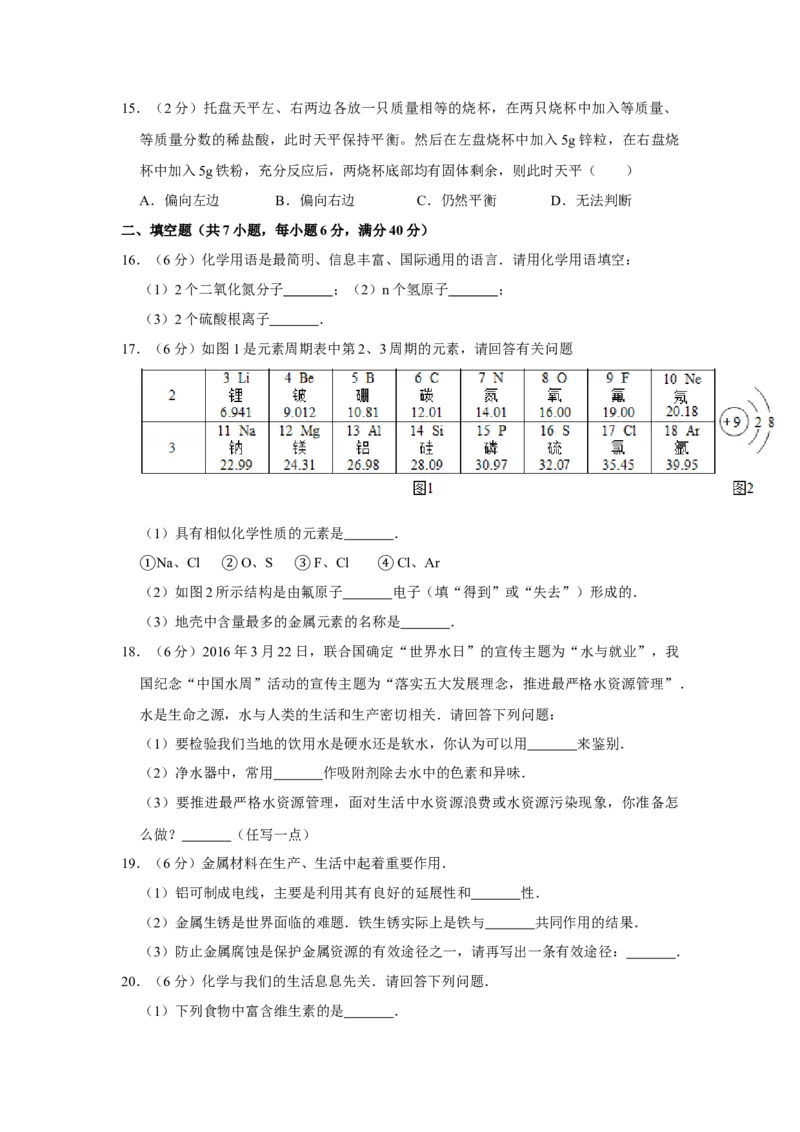
7.(2分)如图所示:甲瓶中盛放的是浓H SO ,乙瓶中放的是用石蕊溶液染成紫色的干
2 4
燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花不变色;若关闭阀门Ⅱ,打开阀门Ⅰ,
紫色小花( )
A.变红色 B.变蓝色 C.变白色 D.不变色
8.(2分)2016年6月5日世界环境日的主题是“为生命呐喊”,与之相呼应的中国主题为“改善环境质量,推动绿色发展”.下列说法错误的是( )
A.禁止使用含磷洗衣粉
B.禁止使用农药化肥
C.推广使用节能灯和太阳能路灯
D.尽量不使用一次性木筷
9.(2分)已知,结构相似,在分子组成上相差一个或若干个“CH ”原子团的物质互称
2
为同系物。如甲烷(CH )和乙烷(C H )互为同系物。则下列物质中与乙醇
4 2 6
(C H OH)互为同系物的是( )
2 5
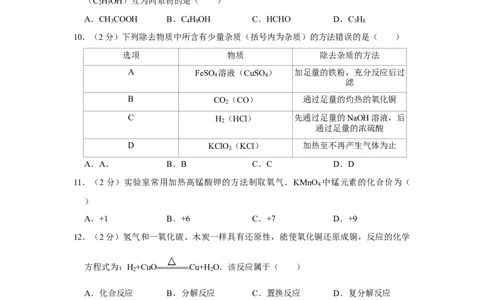
A.CH COOH B.C H OH C.HCHO D.C H
3 4 9 3 8
10.(2分)下列除去物质中所含有少量杂质(括号内为杂质)的方法错误的是( )
选项 物质 除去杂质的方法
A FeSO 溶液(CuSO ) 加足量的铁粉,充分反应后过
4 4
滤
B CO (CO) 通过足量的灼热的氧化铜
2
C H (HCl) 先通过足量的NaOH溶液,后
2
通过足量的浓硫酸
D KClO (KCl) 加热至不再产生气体为止
3
A.A、 B.B C.C D.D
11.(2分)实验室常用加热高锰酸钾的方法制取氧气.KMnO 中锰元素的化合价为(
4
)
A.+1 B.+6 C.+7 D.+9
12.(2分)氢气和一氧化碳、木炭一样具有还原性,能使氧化铜还原成铜,反应的化学
方程式为:H +CuO Cu+H O.该反应属于( )
2 2
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
13.(2分)“金银铜铁锡”俗称五金.在这五种金属中,金属活动性最强的是( )
A.金 B.银 C.铜 D.铁
14.(2分)分类是学习和研究化学的常用方法,下列分类不正确的是( )
A.碱:生石灰、熟石灰、烧碱
B.碳单质:金刚石、石墨、C
60
C.复合肥料:KNO 、NH H PO 、(NH ) HPO
3 4 2 4 4 2 4
D.化石燃料:煤、石油、天然气15.(2分)托盘天平左、右两边各放一只质量相等的烧杯,在两只烧杯中加入等质量、
等质量分数的稀盐酸,此时天平保持平衡。然后在左盘烧杯中加入5g锌粒,在右盘烧
杯中加入5g铁粉,充分反应后,两烧杯底部均有固体剩余,则此时天平( )
A.偏向左边 B.偏向右边 C.仍然平衡 D.无法判断
二、填空题(共7小题,每小题6分,满分40分)
16.(6分)化学用语是最简明、信息丰富、国际通用的语言.请用化学用语填空:
(1)2个二氧化氮分子 ;(2)n个氢原子 ;
(3)2个硫酸根离子 .
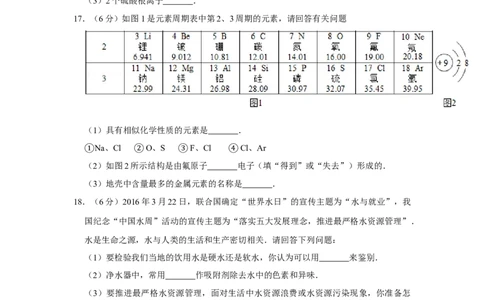
17.(6分)如图1是元素周期表中第2、3周期的元素,请回答有关问题
(1)具有相似化学性质的元素是 .
Na、Cl O、S F、Cl Cl、Ar
①(2)如图2所②示结构是由③氟原子 ④ 电子(填“得到”或“失去”)形成的.
(3)地壳中含量最多的金属元素的名称是 .
18.(6分)2016年3月22日,联合国确定“世界水日”的宣传主题为“水与就业”,我
国纪念“中国水周”活动的宣传主题为“落实五大发展理念,推进最严格水资源管理”.
水是生命之源,水与人类的生活和生产密切相关.请回答下列问题:
(1)要检验我们当地的饮用水是硬水还是软水,你认为可以用 来鉴别.
(2)净水器中,常用 作吸附剂除去水中的色素和异味.
(3)要推进最严格水资源管理,面对生活中水资源浪费或水资源污染现象,你准备怎
么做? (任写一点)
19.(6分)金属材料在生产、生活中起着重要作用.
(1)铝可制成电线,主要是利用其有良好的延展性和 性.
(2)金属生锈是世界面临的难题.铁生锈实际上是铁与 共同作用的结果.
(3)防止金属腐蚀是保护金属资源的有效途径之一,请再写出一条有效途径: .
20.(6分)化学与我们的生活息息先关.请回答下列问题.
(1)下列食物中富含维生素的是 .(2)联合国教科文组织认为中国铁锅是具有推广价值的一种烹饪工具,用铁锅做菜,
其优点是可以补充人体所需的微量元素.人体缺铁会引起 .
(3)三大合成材料指的是 、合成纤维、合成橡胶、合成材料废弃物的急剧增加
带来了环境问题,如“白色污染”等.
21.(2分)84消毒液是北京第一传染病医院(现北京地坛医院)于1984年研制的一种消
毒液.能迅速杀灭各种肝炎病毒,后广泛用于宾馆、旅游、医院、食品加工、家庭等的
卫生消毒,主要成分为次氯酸钠(NaClO),它不能与“洁厕灵”(主要成分是HCl)
混用,如果二者混用,会产生一种有毒气体氯气(Cl ),同时生成氯化钠和水.试写
2
出该反应的化学方程式: .
22.(8分)通过晾晒海水或者煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐.粗
盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等).工业上以粗
盐为原料制取精盐,其生产流程如图所示:
请回答下列问题:
(1)已知操作a、b、c中均含同一种操作,其名称是 .
(2)将足量稀盐酸加入溶液C中,反应的化学方程式为(任写一个) .
(3)在蒸发操作中,用玻璃棒搅拌的作用是 .
(4)如果称量Ⅰ中称得粗盐的质量为5g,称量Ⅱ中称得精盐的质量为5.1g,则下列分
析正确的是 .
A.精盐的产率一定为98.04%
B.精盐的产率一定为102%
C.蒸发操作中可能有水分没有蒸干
D.溶解操作中可能有粗盐没有溶解E.除杂过程中有NaCl生成.
三、解答题(共2小题,满分24分)
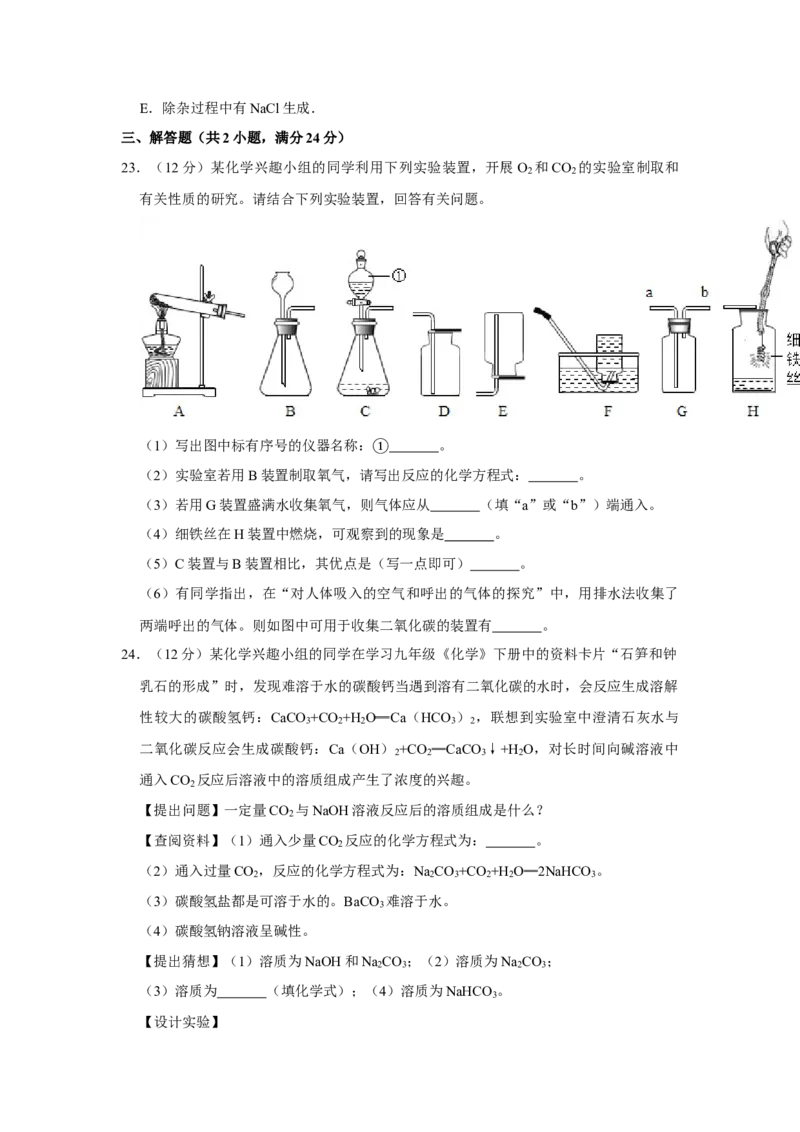
23.(12分)某化学兴趣小组的同学利用下列实验装置,开展O 和CO 的实验室制取和
2 2
有关性质的研究。请结合下列实验装置,回答有关问题。
(1)写出图中标有序号的仪器名称: 。
(2)实验室若用B装置制取氧气,请①写出反应的化学方程式: 。
(3)若用G装置盛满水收集氧气,则气体应从 (填“a”或“b”)端通入。
(4)细铁丝在H装置中燃烧,可观察到的现象是 。
(5)C装置与B装置相比,其优点是(写一点即可) 。
(6)有同学指出,在“对人体吸入的空气和呼出的气体的探究”中,用排水法收集了
两端呼出的气体。则如图中可用于收集二氧化碳的装置有 。
24.(12分)某化学兴趣小组的同学在学习九年级《化学》下册中的资料卡片“石笋和钟
乳石的形成”时,发现难溶于水的碳酸钙当遇到溶有二氧化碳的水时,会反应生成溶解
性较大的碳酸氢钙:CaCO +CO +H O═Ca(HCO ) ,联想到实验室中澄清石灰水与
3 2 2 3 2
二氧化碳反应会生成碳酸钙:Ca(OH) +CO ═CaCO ↓+H O,对长时间向碱溶液中
2 2 3 2
通入CO 反应后溶液中的溶质组成产生了浓度的兴趣。
2
【提出问题】一定量CO 与NaOH溶液反应后的溶质组成是什么?
2
【查阅资料】(1)通入少量CO 反应的化学方程式为: 。
2
(2)通入过量CO ,反应的化学方程式为:Na CO +CO +H O═2NaHCO 。
2 2 3 2 2 3
(3)碳酸氢盐都是可溶于水的。BaCO 难溶于水。
3
(4)碳酸氢钠溶液呈碱性。
【提出猜想】(1)溶质为NaOH和Na CO ;(2)溶质为Na CO ;
2 3 2 3
(3)溶质为 (填化学式);(4)溶质为NaHCO 。
3
【设计实验】实验步骤 实验现象 实验结论
(1)用玻璃棒蘸取反应后 pH=9 该溶液显碱性
溶液,滴在pH试纸上
(2)取反应后溶液少许于 有 猜想(4)不成立
试管中,向其中滴加过量的
生成
BaCl 溶液
2
(3)取步骤(2)中的上层 有气泡冒出 猜想(1)和(2)不成立
清液,滴入稀盐酸
【得出结论】猜想(3)成立。
【讨论交流】(1)有同学提出,实验步骤(1)是多余的。你认为该实验设计是否需要?
(填“需要”或“不需要”)。
(2)同学们又一次把目光投向了教材,发现遇热或压强变小时:Ca(HCO ) =
3 2
CaCO ↓+CO ↑+H O,纷纷提出,干粉灭火器中用NaHCO 灭火的反应原理与之相似,
3 2 2 3
试写出NaHCO 受热分解的化学方程式: 。
3
【反思应用】(1)同学们回忆起实验室检验二氧化碳的情景,心想:如果向澄清石灰
水中不断通入二氧化碳,会看到怎样的现象呢?请你描述一下: 。
(2)老师投影图片﹣新化县的梅山龙宫,冷水江市的波月洞,涟源市的藏经阁,双峰
县的药王洞…宛如人间仙境的美丽溶洞,竟然是文中两个简单的化学反应创造?!同学
们不禁对大自然的鬼斧神工咋不决口,纷纷表示“娄底那么大,我想去看看”。
四、解答题(共1小题,满分6分)
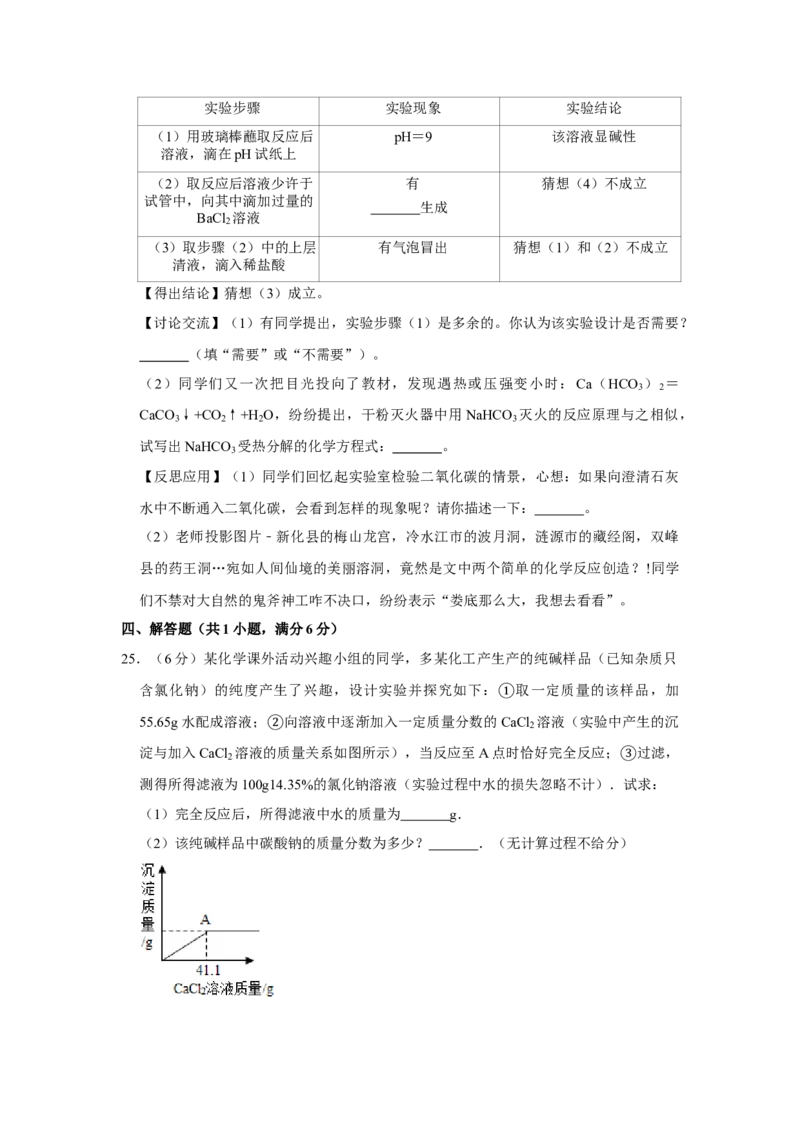
25.(6分)某化学课外活动兴趣小组的同学,多某化工产生产的纯碱样品(已知杂质只
含氯化钠)的纯度产生了兴趣,设计实验并探究如下: 取一定质量的该样品,加
55.65g水配成溶液; 向溶液中逐渐加入一定质量分数的①CaCl 溶液(实验中产生的沉
2
淀与加入CaCl 溶液的②质量关系如图所示),当反应至A点时恰好完全反应; 过滤,
2
测得所得滤液为100g14.35%的氯化钠溶液(实验过程中水的损失忽略不计).③试求:
(1)完全反应后,所得滤液中水的质量为 g.
(2)该纯碱样品中碳酸钠的质量分数为多少? .(无计算过程不给分)