文档内容
2017年四川省遂宁市中考化学试卷
一、选择题(本大题共7个小题,每小题3分,共21分.每小题只有一个选项符合
题意)
1.(3分)下列变化属于化学变化的是( )
A.试管破裂 B.酒精挥发 C.红磷燃烧 D.溶液稀释
2.(3分)下列实验操作正确的是( )
A.测定末知溶液的pH B.检査装置气密性C.检验CO D.称量食盐
2
3.(3分)香烟的烟雾中含有4000多种化学物质,其中大多数是有害物质,而危窨
较大的物质是一氧化碳、尼古丁(化学式为C H N )、焦油和重金属盐.下列关
10 14 2
于尼古丁的说法正确的是( )
A.尼古丁是由三种元素组成的混合物
B.尼古丁中碳元素、氢元素、氮元素的质量比为10:14:2
C.尼古丁由碳原子、氢原子、氮原子构成
D.尼古丁中氢元素的质量分数最小
4.(3分)下列说法正确的是( )
A.水电解过程中生成氢气和氧气的质量比为2:l
B.饱和溶液升温都能变为不饱和溶液
C.二氧化碳有毒,过多会导致温室效应
D.空气中含量最多的气体是氮气,它可用作食品包装的保护气
5.(3分)化学知识涉及衣、食、住、行各个领域,下列有关说法全部正确的一组是
( )
A.衣 1.鉴别羊毛制品和化纤制品可采用点燃闻气味的方法
2.衣服上的油污用汽油清洗是利用其乳化作用
B.食 1.蔬菜含维生素,种植时使用尿素[CO(NH ) ]属于有机氮肥
2 2
2.生火煮饭离不开氧气,是因为氧气具有可燃性
C.住 1.修建房屋使用的铝合金属于金属材料
第1页(共19页)2.能闻到新装修房屋里的异味,是因为分子在不断运动
D.行 1.汽车、自行车等车辆的金属表面喷漆主要目的是为了美观
2.活性炭包可用于吸附车内的异味
A.A B.B C.C D.D
6.(3分)要出去物质中所含的少量杂质,下列实验设计不合理的是( )
选项 物质 杂质 所选试剂或方法
A CaO CaCO 稀盐酸
3
B NaCl溶液 MgCl 适量NaOH溶液
2
C O 水蒸气 浓硫酸
2
D Cu粉 Fe粉 磁铁吸引
A.A B.B C.C D.D
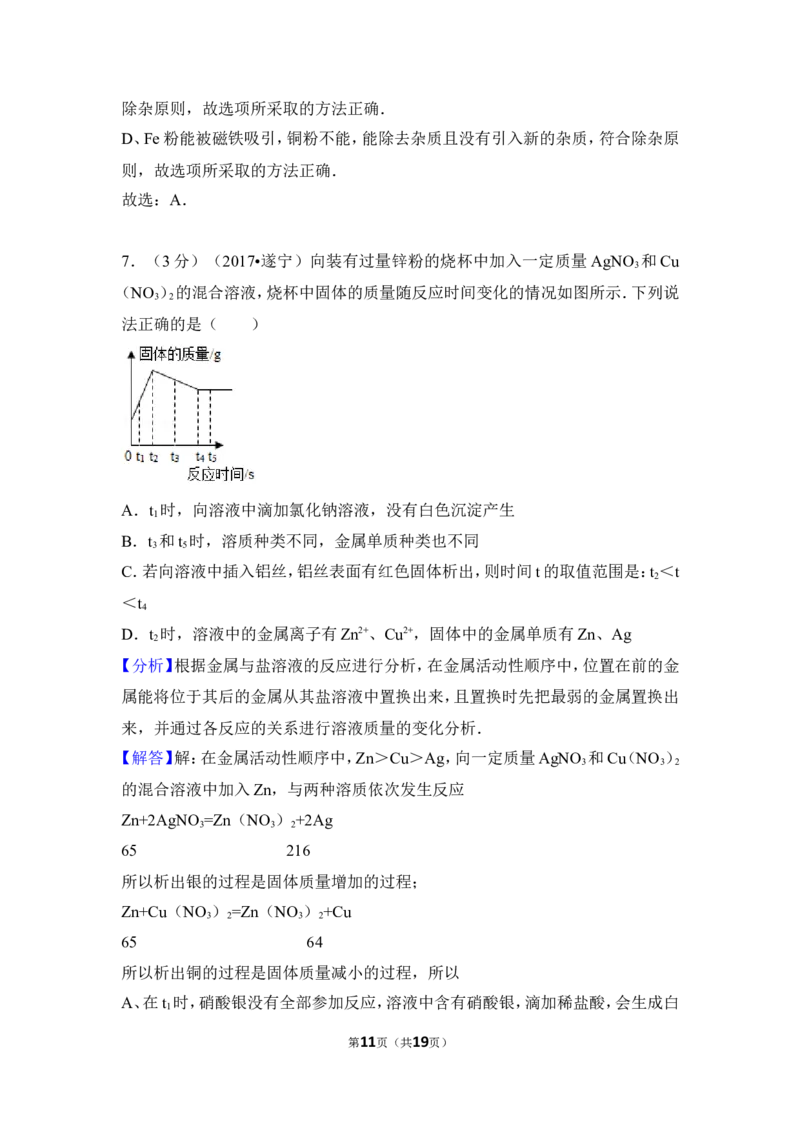
7.(3分)向装有过量锌粉的烧杯中加入一定质量AgNO 和Cu(NO )的混合溶
3 3 2
液,烧杯中固体的质量随反应时间变化的情况如图所示.下列说法正确的是(
)
A.t 时,向溶液中滴加氯化钠溶液,没有白色沉淀产生
1
B.t 和t 时,溶质种类不同,金属单质种类也不同
3 5
C.若向溶液中插入铝丝,铝丝表面有红色固体析出,则时间t的取值范围是:t <t
2
<t
4
D.t 时,溶液中的金属离子有Zn2+、Cu2+,固体中的金属单质有Zn、Ag
2
二、填空题(本大题共5小题,每空2分,共28分)
8.(4分)用化学用语回答:
(1 )能供给呼吸、支持燃烧的气体 .
(2)2个铁离子 .
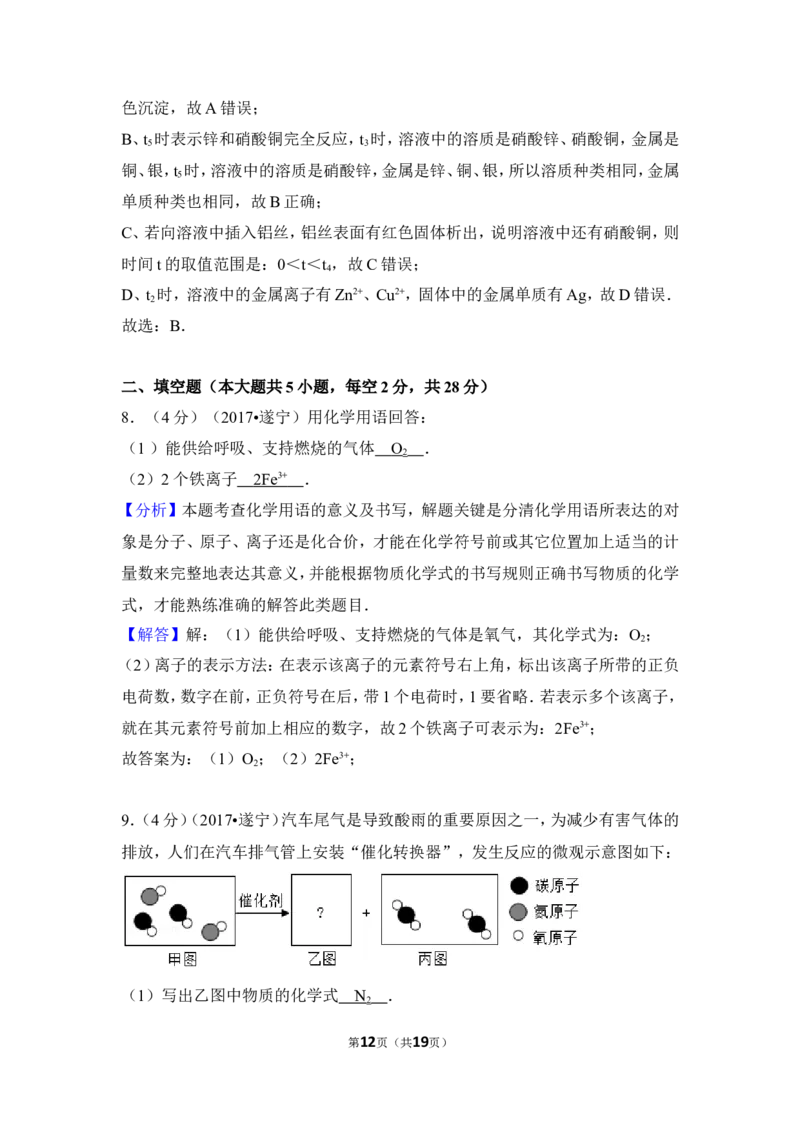
9.(4分)汽车尾气是导致酸雨的重要原因之一,为减少有害气体的排放,人们在
第2页(共19页)汽车排气管上安装“催化转换器”,发生反应的微观示意图如下:
(1)写出乙图中物质的化学式 .
(2)该反应中化合价有改变的两种元素是 (填元素符号).
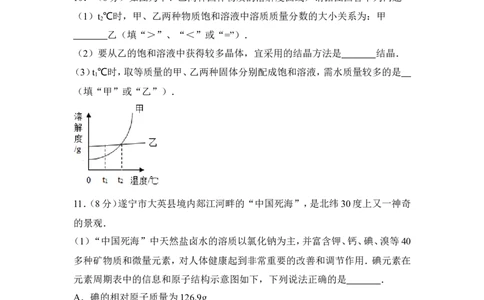
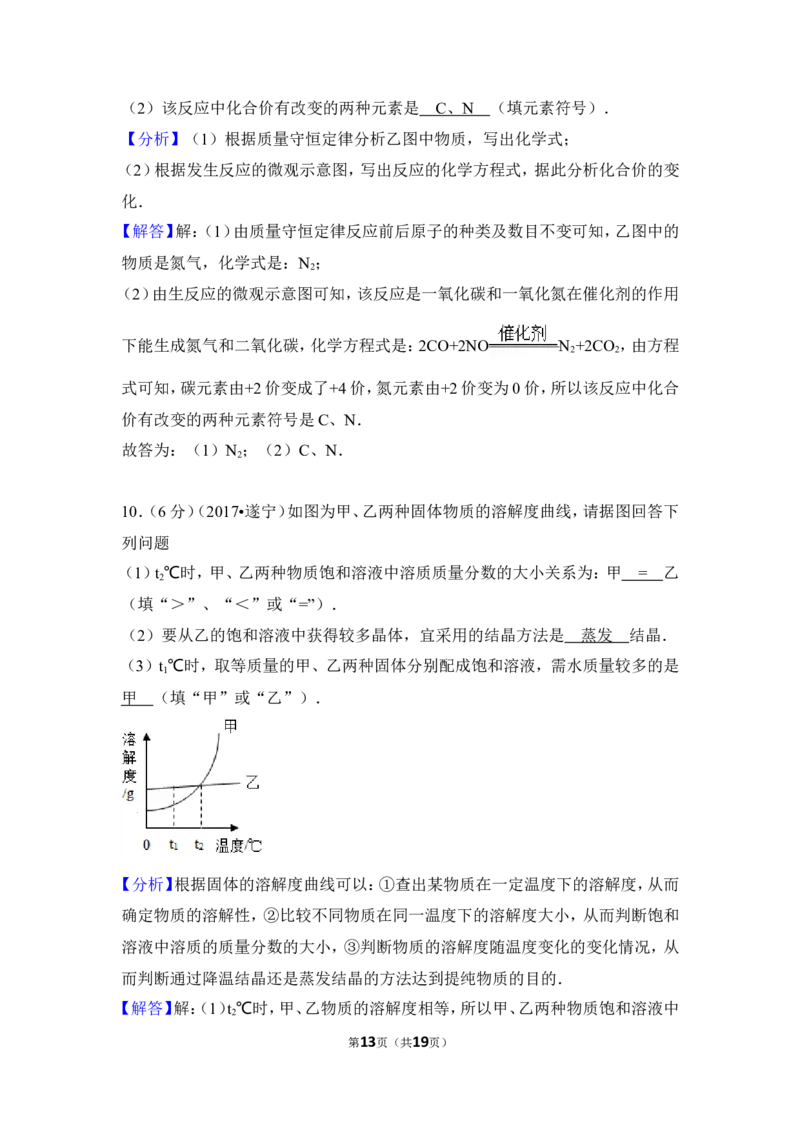
10.(6分)如图为甲、乙两种固体物质的溶解度曲线,请据图回答下列问题
(1)t ℃时,甲、乙两种物质饱和溶液中溶质质量分数的大小关系为:甲
2
乙(填“>”、“<”或“=”).
(2)要从乙的饱和溶液中获得较多晶体,宜采用的结晶方法是 结晶.
(3)t ℃时,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较多的是
1
(填“甲”或“乙”).
11.(8分)遂宁市大英县境内郯江河畔的“中国死海”,是北纬30度上又一神奇
的景观.
(1)“中国死海”中天然盐卤水的溶质以氯化钠为主,并富含钾、钙、碘、溴等40
多种矿物质和微量元素,对人体健康起到非常重要的改善和调节作用.碘元素在
元素周期表中的信息和原子结构示意图如下,下列说法正确的是 .
A.碘的相对原子质量为126.9g
B.人体缺碘易导致骨质疏松
C.碘在化学反应中形成的阴离子符号为I﹣
D.一个碘原子核内有53个中子
(2)“中国死海”的现代水上运动、休闲、度假、娱乐、保健等水文化旅游元素提
升了人们的生活品质,但也容易对郪江造成污染.请提出一条保护水资源的建议
.
第3页(共19页)(3)小西同学从郪江中取少量水样,观察到水样浑浊,有固体小颗粒.为除去这些
不溶性杂质,她应该采取实验操作的名称是 .
(4)浩瀚的海洋中蕴藏着丰富的资源,是巨大的天然宝库.从海水中提取溴,其中
一种方案涉及到的化学反应为:2NaBr+Cl =2NaCl+Br ,已知非金属单质也有类
2 2
似金属单质与盐溶液之间的反应规律,由此可判断Cl 、Br 的活动性顺序是:Cl
2 2 2
Br (填“>”、“<”或“=”).
2
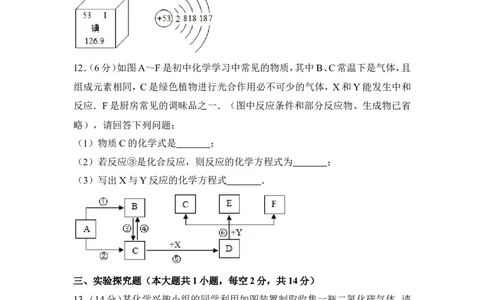
12.(6分)如图A~F是初中化学学习中常见的物质,其中B、C常温下是气体,且
组成元素相同,C是绿色植物进行光合作用必不可少的气体,X和Y能发生中和
反应.F是厨房常见的调昧品之一.(图中反应条件和部分反应物、生成物已省
略),请回答下列问题:
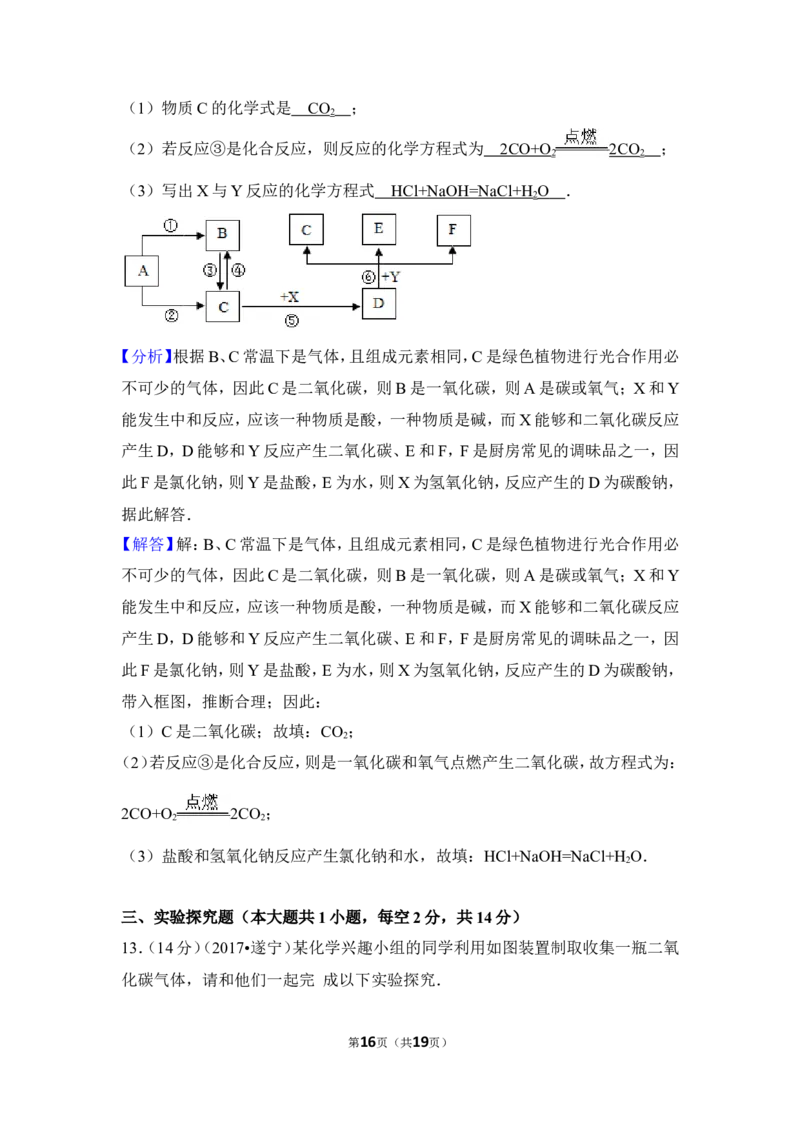
(1)物质C的化学式是 ;
(2)若反应③是化合反应,则反应的化学方程式为 ;
(3)写出X与Y反应的化学方程式 .
三、实验探究题(本大题共1小题,每空2分,共14分)
13.(14分)某化学兴趣小组的同学利用如图装置制取收集一瓶二氧化碳气体,请
和他们一起完 成以下实验探究.
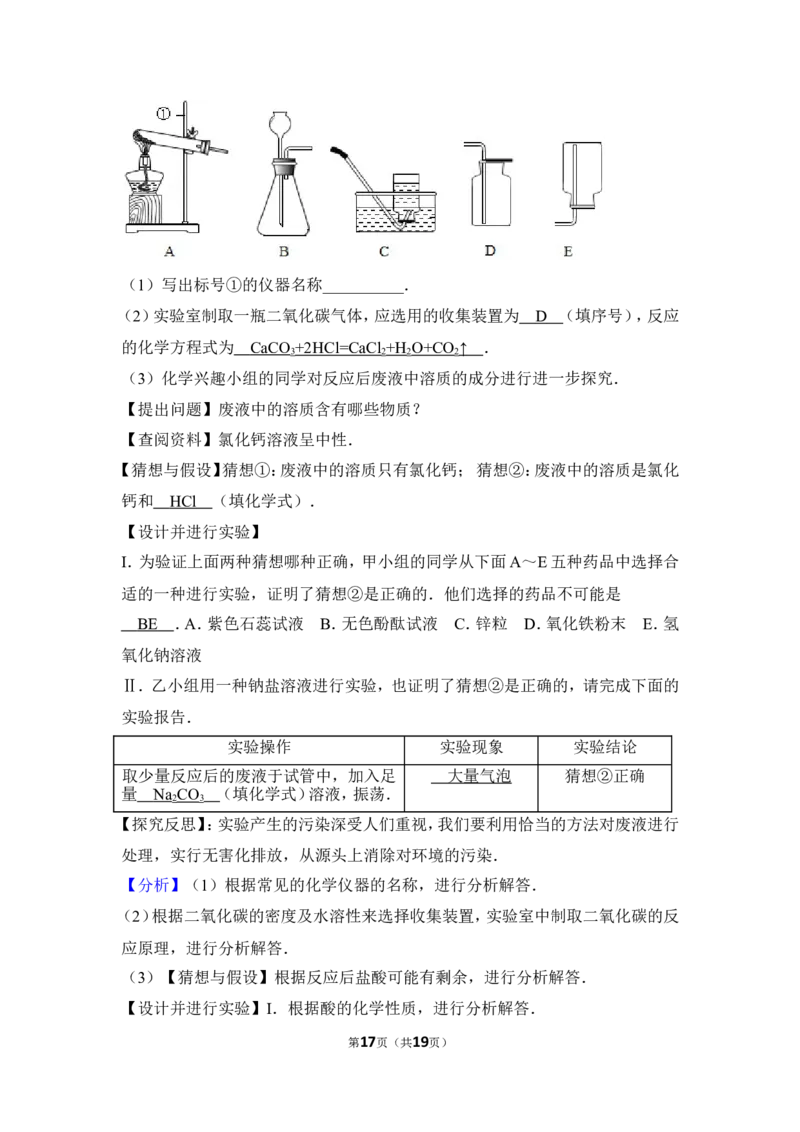
第4页(共19页)(1)写出标号①的仪器名称__________.
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为 (填序号),反应
的化学方程式为 .
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究.
【提出问题】废液中的溶质含有哪些物质?
【查阅资料】氯化钙溶液呈中性.
【猜想与假设】猜想①:废液中的溶质只有氯化钙; 猜想②:废液中的溶质是氯化
钙和 (填化学式).
【设计并进行实验】
I.为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合
适的一种进行实验,证明了猜想②是正确的.他们选择的药品不可能是
.A.紫色石蕊试液 B.无色酚酞试液 C.锌粒 D.氧化铁粉末 E.氢
氧化钠溶液
Ⅱ.乙小组用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的
实验报告.
实验操作 实验现象 实验结论
取少量反应后的废液于试管中,加入足 猜想②正确
量 (填化学式)溶液,振荡.
【探究反思】:实验产生的污染深受人们重视,我们要利用恰当的方法对废液进行
处理,实行无害化排放,从源头上消除对环境的污染.
四、计算题(本大题共1小题,共7分)
14.(7分)实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质量分数,兴
趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气体的质量
和反应时间关系如图.
(1)完全反应后,经过滤、烘干,得到固体的质量为
第5页(共19页)(不计操作过程中的损耗)
(2)产生气体的速度越来越慢的原因是 .
A.二氧化锰越来越少
B.过氧化氢溶液的溶质分数越来越小
D.温度越来越高
(3)计算所用过氧化氢溶液的溶质质量分数.(规范写出计算过程)
第6页(共19页)2017 年四川省遂宁市中考化学试卷
参考答案与试题解析
一、选择题(本大题共7个小题,每小题3分,共21分.每小题只有一个选项符合
题意)
1.(3分)(2017•遂宁)下列变化属于化学变化的是( )
A.试管破裂 B.酒精挥发 C.红磷燃烧 D.溶液稀释
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、试管破裂过程中只是形状发生改变,没有新物质生成,属于物理变
化.
B、酒精挥发过程中只是状态发生改变,没有新物质生成,属于物理变化.
C、红磷燃烧过程中有新物质五氧化二磷生成,属于化学变化.
D、溶液稀释过程中没有新物质生成,属于物理变化.
故选C.
2.(3分)(2017•遂宁)下列实验操作正确的是( )
A.测定末知溶液的pH B.检査装置气密性C.检验CO D.称量食盐
2
【分析】A、根据用pH试纸测定未知溶液的pH的方法进行分析判断.
B、根据检查装置气密性的方法进行分析判断.
C、根据二氧化碳气体的检验方法进行分析判断.
D、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
【解答】解:A、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸
取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能将pH
试纸伸入待测液中,以免污染待测液,图中所示操作错误.
第7页(共19页)B、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导
管口有气泡冒出,装置不漏气;图中所示操作正确.
C、检验是否是二氧化碳时,应用澄清的石灰水,不能使用燃着的木条,图中所示
操作错误.
D、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置
放反了,图中所示操作错误.
故选:B.
3.(3分)(2017•遂宁)香烟的烟雾中含有4000多种化学物质,其中大多数是有害
物质,而危窨较大的物质是一氧化碳、尼古丁(化学式为C H N )、焦油和重金
10 14 2
属盐.下列关于尼古丁的说法正确的是( )
A.尼古丁是由三种元素组成的混合物
B.尼古丁中碳元素、氢元素、氮元素的质量比为10:14:2
C.尼古丁由碳原子、氢原子、氮原子构成
D.尼古丁中氢元素的质量分数最小
【分析】A.根据物质的组成与分类来分析;
B.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分
析判断;
C.根据物质的构成来分析;
D.根据化合物中元素的质量比来分析.
【解答】解:A.尼古丁是由一种物质组成的,属于纯净物,故错误;
B.尼古丁中碳、氢、氮三种元素的质量比为(12×10):(1×14):(14×2)≠10:14:
2,故错误;
C.尼古丁是由尼古丁分子构成的,而不是由原子直接构成的,故错误;
D.尼古丁中碳、氢、氮三种元素的质量比为(12×10):(1×14):(14×2)=120:14:
28,可见其中氢元素的质量分数最小,故正确.
故选D.
4.(3分)(2017•遂宁)下列说法正确的是( )
A.水电解过程中生成氢气和氧气的质量比为2:l
第8页(共19页)B.饱和溶液升温都能变为不饱和溶液
C.二氧化碳有毒,过多会导致温室效应
D.空气中含量最多的气体是氮气,它可用作食品包装的保护气
【分析】A.水电解时所生成氢气和氧气的体积比为2:1,质量比是1:8.
B.对于溶解度随温度升高而增大的物质,升温可使饱和溶液变成不饱和溶液;对
于溶解度随温度升高而减小的物质,降温可使饱和溶液变成不饱和溶液.
C、根据二氧化碳没有毒性解答.
D.根据空气成分分析解答.
【解答】解:A.水电解时所生成氢气和氧气的体积比为2:1,质量比是1:8,故选
项错误;
B.对于溶解度随温度升高而增大的物质,升温可使饱和溶液变成不饱和溶液;对
于溶解度随温度升高而减小的物质,降温可使饱和溶液变成不饱和溶液;故选项
不对.
C、二氧化碳没有毒性,故错误.
D.空气中含量最多的气体是氮气,它化学性质稳定可用作食品包装的保护气,正
确;
5.(3分)(2017•遂宁)化学知识涉及衣、食、住、行各个领域,下列有关说法全部
正确的一组是( )
A 1.鉴别羊毛制品和化纤制品可采用点燃闻气
. 味的方法
衣
2.衣服上的油污用汽油清洗是利用其乳化作
用
B 1.蔬菜含维生素,种植时使用尿素[CO
. (NH ) ]属于有机氮肥
2 2
食
2.生火煮饭离不开氧气,是因为氧气具有可
燃性
C 1.修建房屋使用的铝合金属于金属材料
.
2.能闻到新装修房屋里的异味,是因为分子
住
在不断运动
D 1.汽车、自行车等车辆的金属表面喷漆主要
. 目的是为了美观
行
第9页(共19页)2.活性炭包可用于吸附车内的异味
A.A B.B C.C D.D
【分析】根据物质的性质结合物质与衣食住行的关系进行分析解答即可.
【解答】解:A、1.羊毛的成分是蛋白质,灼烧有烧焦羽毛的气味,而化纤制品灼烧
没有烧焦羽毛的气味,故鉴别羊毛制品和化纤制品可采用点燃闻气味的方法,正
确;2.衣服上的油污用汽油清洗是利用其溶解作用,错误;
B、1.蔬菜含维生素,种植时使用尿素[CO(NH )]属于有机氮肥,正确;2.生火煮
2 2
饭离不开氧气,是因为氧气具有助燃性,不是可燃性,错误;
C、1.修建房屋使用的铝合金属于金属材料,正确;2.能闻到新装修房屋里的异味,
是因为分子在不断运动,正确;
D、1.汽车、自行车等车辆的金属表面喷漆主要目的是为了防止锈蚀,错误;2.活
性炭具有吸附性,故活性炭包可用于吸附车内的异味,正确;
故选C.
6.(3分)(2017•遂宁)要出去物质中所含的少量杂质,下列实验设计不合理的是
( )
选项 物质 杂质 所选试剂或方法
A CaO CaCO 稀盐酸
3
B NaCl溶液 MgCl 适量NaOH溶液
2
C O 水蒸气 浓硫酸
2
D Cu粉 Fe粉 磁铁吸引
A.A B.B C.C D.D
【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提
纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:
①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质
【解答】解:A、CaO和CaCO 均能与稀盐酸反应,不但能把杂质除去,也会把原物
3
质除去,不符合除杂原则,故选项所采取的方法错误.
B、MgCl 能与适量NaOH溶液反应生成氢氧化镁沉淀和氯化钠,能除去杂质且没
2
有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、浓硫酸具有吸水性,且不与氧气反应,能除去杂质且没有引入新的杂质,符合
第10页(共19页)除杂原则,故选项所采取的方法正确.
D、Fe粉能被磁铁吸引,铜粉不能,能除去杂质且没有引入新的杂质,符合除杂原
则,故选项所采取的方法正确.
故选:A.
7.(3分)(2017•遂宁)向装有过量锌粉的烧杯中加入一定质量 AgNO 和Cu
3
(NO )的混合溶液,烧杯中固体的质量随反应时间变化的情况如图所示.下列说
3 2
法正确的是( )
A.t 时,向溶液中滴加氯化钠溶液,没有白色沉淀产生
1
B.t 和t 时,溶质种类不同,金属单质种类也不同
3 5
C.若向溶液中插入铝丝,铝丝表面有红色固体析出,则时间t的取值范围是:t <t
2
<t
4
D.t 时,溶液中的金属离子有Zn2+、Cu2+,固体中的金属单质有Zn、Ag
2
【分析】根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金
属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出
来,并通过各反应的关系进行溶液质量的变化分析.
【解答】解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO 和Cu(NO )
3 3 2
的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO =Zn(NO ) +2Ag
3 3 2
65 216
所以析出银的过程是固体质量增加的过程;
Zn+Cu(NO ) =Zn(NO ) +Cu
3 2 3 2
65 64
所以析出铜的过程是固体质量减小的过程,所以
A、在t 时,硝酸银没有全部参加反应,溶液中含有硝酸银,滴加稀盐酸,会生成白
1
第11页(共19页)色沉淀,故A错误;
B、t 时表示锌和硝酸铜完全反应,t 时,溶液中的溶质是硝酸锌、硝酸铜,金属是
5 3
铜、银,t 时,溶液中的溶质是硝酸锌,金属是锌、铜、银,所以溶质种类相同,金属
5
单质种类也相同,故B正确;
C、若向溶液中插入铝丝,铝丝表面有红色固体析出,说明溶液中还有硝酸铜,则
时间t的取值范围是:0<t<t ,故C错误;
4
D、t 时,溶液中的金属离子有Zn2+、Cu2+,固体中的金属单质有Ag,故D错误.
2
故选:B.
二、填空题(本大题共5小题,每空2分,共28分)
8.(4分)(2017•遂宁)用化学用语回答:
(1 )能供给呼吸、支持燃烧的气体 O .
2
(2)2个铁离子 2F e 3 + .
【分析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对
象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计
量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学
式,才能熟练准确的解答此类题目.
【解答】解:(1)能供给呼吸、支持燃烧的气体是氧气,其化学式为:O ;
2
(2)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负
电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,
就在其元素符号前加上相应的数字,故2个铁离子可表示为:2Fe3+;
故答案为:(1)O ;(2)2Fe3+;
2
9.(4分)(2017•遂宁)汽车尾气是导致酸雨的重要原因之一,为减少有害气体的
排放,人们在汽车排气管上安装“催化转换器”,发生反应的微观示意图如下:
(1)写出乙图中物质的化学式 N .
2
第12页(共19页)(2)该反应中化合价有改变的两种元素是 C 、 N (填元素符号).
【分析】(1)根据质量守恒定律分析乙图中物质,写出化学式;
(2)根据发生反应的微观示意图,写出反应的化学方程式,据此分析化合价的变
化.
【解答】解:(1)由质量守恒定律反应前后原子的种类及数目不变可知,乙图中的
物质是氮气,化学式是:N ;
2
(2)由生反应的微观示意图可知,该反应是一氧化碳和一氧化氮在催化剂的作用
下能生成氮气和二氧化碳,化学方程式是:2CO+2NO N +2CO ,由方程
2 2
式可知,碳元素由+2价变成了+4价,氮元素由+2价变为0价,所以该反应中化合
价有改变的两种元素符号是C、N.
故答为:(1)N ;(2)C、N.
2
10.(6分)(2017•遂宁)如图为甲、乙两种固体物质的溶解度曲线,请据图回答下
列问题
(1)t ℃时,甲、乙两种物质饱和溶液中溶质质量分数的大小关系为:甲 = 乙
2
(填“>”、“<”或“=”).
(2)要从乙的饱和溶液中获得较多晶体,宜采用的结晶方法是 蒸发 结晶.
(3)t ℃时,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较多的是
1
甲 (填“甲”或“乙”).
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而
确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和
溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从
而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
【解答】解:(1)t ℃时,甲、乙物质的溶解度相等,所以甲、乙两种物质饱和溶液中
2
第13页(共19页)溶质质量分数的大小关系为:甲=乙;
(2)乙物质的溶解度受温度变化影响较小,所以要从乙的饱和溶液中获得较多晶
体,宜采用的结晶方法是蒸发结晶;
(3)t ℃时,乙物质的溶解度大于甲物质的溶解度,所以取等质量的甲、乙两种固
1
体分别配成饱和溶液,需水质量较多的是甲.
故答案为:(1)=;
(2)蒸发;
(3)甲.
11.(8分)(2017•遂宁)遂宁市大英县境内郯江河畔的“中国死海”,是北纬30
度上又一神奇的景观.
(1)“中国死海”中天然盐卤水的溶质以氯化钠为主,并富含钾、钙、碘、溴等40
多种矿物质和微量元素,对人体健康起到非常重要的改善和调节作用.碘元素在
元素周期表中的信息和原子结构示意图如下,下列说法正确的是 C .
A.碘的相对原子质量为126.9g
B.人体缺碘易导致骨质疏松
C.碘在化学反应中形成的阴离子符号为I﹣
D.一个碘原子核内有53个中子
(2)“中国死海”的现代水上运动、休闲、度假、娱乐、保健等水文化旅游元素提
升了人们的生活品质,但也容易对郪江造成污染.请提出一条保护水资源的建议
工业废水经过处理后再排放 .
(3)小西同学从郪江中取少量水样,观察到水样浑浊,有固体小颗粒.为除去这些
不溶性杂质,她应该采取实验操作的名称是 过滤 .
(4)浩瀚的海洋中蕴藏着丰富的资源,是巨大的天然宝库.从海水中提取溴,其中
一种方案涉及到的化学反应为:2NaBr+Cl =2NaCl+Br ,已知非金属单质也有类
2 2
似金属单质与盐溶液之间的反应规律,由此可判断Cl 、Br 的活动性顺序是:Cl
2 2 2
> Br (填“>”、“<”或“=”).
2
第14页(共19页)【分析】(1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;
字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相
对原子质量;原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,
弧线上的数字表示该层上的电子数;进行分析判断即可;
(2)根据防治水污染的方法以及节约用水的方法进行解答;
(3)根据分离混合物的方法来分析;
(4)根据非金属与盐溶液之间的反应规律,比较非金属的活泼性.
【解答】解:(1)A.由元素周期表的信息可知,碘的相对原子质量为126.9,单位不
是“g”而是“1”,通常省略,故错误;
B.人体缺碘易导致甲状腺肿大,故错误;
C.由碘原子结构示意图可知,其最外层电子数为7,所以在化学反应中易得到1
个电子而形成带有1个单位负电荷的碘离子﹣﹣I﹣,故正确;
D.由元素周期表的信息可知,碘的原子序数为53,即原子核内质子数为53,而不
是中子数,故错误.
故选C.
(2)保护水资源可以从防治水污染的方法以及节约用水的方法考虑.防治水污染
的方法:工业废水经过处理后再排放;节约用水的方法:使用节水器具例如节水
马桶;故填:工业废水经过处理后再排放(答案合理即可);
(3)除去水中的不溶性杂质可以采用过滤的方法,故填:过滤;
(4)由题意可知,非金属单质也具有类似金属与盐溶液之间的反应规律.由
2NaBr+Cl =2NaCl+Br ,说明了Cl 的活动性大于Br 活动性;故填:>.
2 2 2 2
12.(6分)(2017•遂宁)如图A~F是初中化学学习中常见的物质,其中B、C常温
下是气体,且组成元素相同,C是绿色植物进行光合作用必不可少的气体,X和Y
能发生中和反应.F是厨房常见的调昧品之一.(图中反应条件和部分反应物、生
成物已省略),请回答下列问题:
第15页(共19页)(1)物质C的化学式是 CO ;
2
(2)若反应③是化合反应,则反应的化学方程式为 2CO+O 2CO ;
2 2
(3)写出X与Y反应的化学方程式 HCl+NaOH=NaCl+H O .
2
【分析】根据B、C常温下是气体,且组成元素相同,C是绿色植物进行光合作用必
不可少的气体,因此C是二氧化碳,则B是一氧化碳,则A是碳或氧气;X和Y
能发生中和反应,应该一种物质是酸,一种物质是碱,而X能够和二氧化碳反应
产生D,D能够和Y反应产生二氧化碳、E和F,F是厨房常见的调昧品之一,因
此F是氯化钠,则Y是盐酸,E为水,则X为氢氧化钠,反应产生的D为碳酸钠,
据此解答.
【解答】解:B、C常温下是气体,且组成元素相同,C是绿色植物进行光合作用必
不可少的气体,因此C是二氧化碳,则B是一氧化碳,则A是碳或氧气;X和Y
能发生中和反应,应该一种物质是酸,一种物质是碱,而X能够和二氧化碳反应
产生D,D能够和Y反应产生二氧化碳、E和F,F是厨房常见的调昧品之一,因
此F是氯化钠,则Y是盐酸,E为水,则X为氢氧化钠,反应产生的D为碳酸钠,
带入框图,推断合理;因此:
(1)C是二氧化碳;故填:CO ;
2
(2)若反应③是化合反应,则是一氧化碳和氧气点燃产生二氧化碳,故方程式为:
2CO+O 2CO ;
2 2
(3)盐酸和氢氧化钠反应产生氯化钠和水,故填:HCl+NaOH=NaCl+H O.
2
三、实验探究题(本大题共1小题,每空2分,共14分)
13.(14分)(2017•遂宁)某化学兴趣小组的同学利用如图装置制取收集一瓶二氧
化碳气体,请和他们一起完 成以下实验探究.
第16页(共19页)(1)写出标号①的仪器名称__________.
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为 D (填序号),反应
的化学方程式为 CaCO +2HCl=CaCl +H O+CO ↑ .
3 2 2 2
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究.
【提出问题】废液中的溶质含有哪些物质?
【查阅资料】氯化钙溶液呈中性.
【猜想与假设】猜想①:废液中的溶质只有氯化钙; 猜想②:废液中的溶质是氯化
钙和 HC l (填化学式).
【设计并进行实验】
I.为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合
适的一种进行实验,证明了猜想②是正确的.他们选择的药品不可能是
BE .A.紫色石蕊试液 B.无色酚酞试液 C.锌粒 D.氧化铁粉末 E.氢
氧化钠溶液
Ⅱ.乙小组用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的
实验报告.
实验操作 实验现象 实验结论
取少量反应后的废液于试管中,加入足 大量气泡 猜想②正确
量 N a CO (填化学式)溶液,振荡.
2 3
【探究反思】:实验产生的污染深受人们重视,我们要利用恰当的方法对废液进行
处理,实行无害化排放,从源头上消除对环境的污染.
【分析】(1)根据常见的化学仪器的名称,进行分析解答.
(2)根据二氧化碳的密度及水溶性来选择收集装置,实验室中制取二氧化碳的反
应原理,进行分析解答.
(3)【猜想与假设】根据反应后盐酸可能有剩余,进行分析解答.
【设计并进行实验】I.根据酸的化学性质,进行分析解答.
第17页(共19页)Ⅱ.根据稀盐酸能与碳酸钠等盐溶液反应生成二氧化碳气体,进行分析解答.
【解答】解:(1)标号①的仪器名称是铁架台.
(2)二氧化碳密度比空气大,能溶于水,应用向上排空气法收集,应选用的收集装
置为D.实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于
固 液 常 温 型 , 同 时 生 成 氯 化 钙 、 水 , 反 应 的 化 学 方 程 式 是 :
CaCO +2HCl=CaCl +H O+CO ↑.
3 2 2 2
(3)【猜想与假设】反应后盐酸可能有剩余,废液中的溶质是氯化钙和HCl.
【设计并进行实验】I.酸使紫色石蕊溶液变红色,不能使无色酚酞溶液变色;稀盐
酸能与锌粒反应生成氢气,能与氧化铁粉末反应生成氯化铁和水,会观察到红棕
色粉末逐渐溶解,溶液变黄色;稀盐酸与氢氧化钠溶液反应生成氯化钠和水,但
无聂鑫变化,故选择的药品不可能是BE.
Ⅱ.稀盐酸能与碳酸钠等盐溶液反应生成二氧化碳气体,取少量反应后的废液于
试管中,加入足量Na CO 溶液溶液,振荡,产生大量气泡,说明由盐酸存在,即猜
2 3
想②正确.
故答案为:(1)铁架台;(2)D;CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
(3)【猜想与假设】HCl;
【设计并进行实验】I.BE;Ⅱ.Na CO ;大量气泡.
2 3
四、计算题(本大题共1小题,共7分)
14.(7分)(2017•遂宁)实验室有一瓶失去标签的过氧化氢溶液,为测定其溶质质
量分数,兴趣小组同学取l00g该溶液与1g二氧化锰混合,使其充分反应,产生气
体的质量和反应时间关系如图.
(1)完全反应后,经过滤、烘干,得到固体的质量为 1 g
(不计操作过程中的损耗)
(2)产生气体的速度越来越慢的原因是 B .
A.二氧化锰越来越少
B.过氧化氢溶液的溶质分数越来越小
D.温度越来越高
(3)计算所用过氧化氢溶液的溶质质量分数.(规范写出计算过程)
第18页(共19页)【分析】(1)根据催化剂的特点分析;
(2)根据影响反应进行的因素分析;
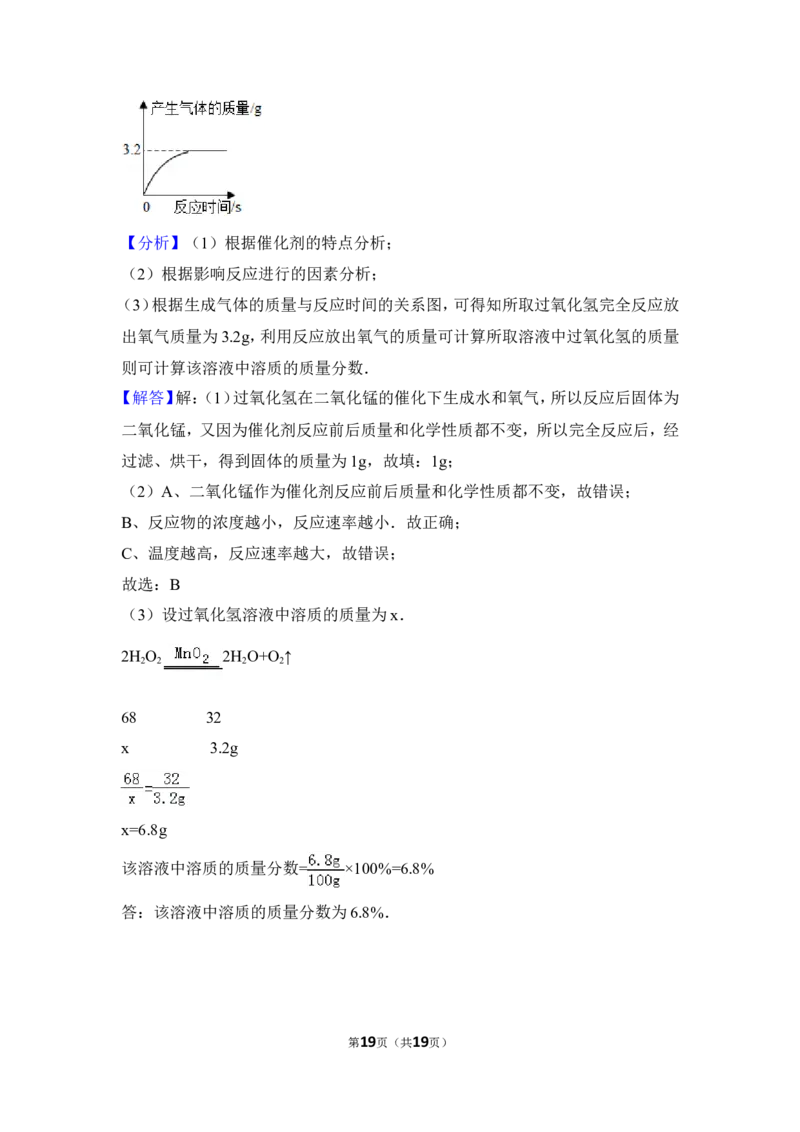
(3)根据生成气体的质量与反应时间的关系图,可得知所取过氧化氢完全反应放
出氧气质量为3.2g,利用反应放出氧气的质量可计算所取溶液中过氧化氢的质量
则可计算该溶液中溶质的质量分数.
【解答】解:(1)过氧化氢在二氧化锰的催化下生成水和氧气,所以反应后固体为
二氧化锰,又因为催化剂反应前后质量和化学性质都不变,所以完全反应后,经
过滤、烘干,得到固体的质量为1g,故填:1g;
(2)A、二氧化锰作为催化剂反应前后质量和化学性质都不变,故错误;
B、反应物的浓度越小,反应速率越小.故正确;
C、温度越高,反应速率越大,故错误;
故选:B
(3)设过氧化氢溶液中溶质的质量为x.
2H O 2H O+O ↑
2 2 2 2
68 32
x 3.2g
x=6.8g
该溶液中溶质的质量分数= ×100%=6.8%
答:该溶液中溶质的质量分数为6.8%.
第19页(共19页)