文档内容
2026届“皖南八校”高三第二次大联考
化 学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答
题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
獉獉獉獉獉獉獉獉獉獉獉獉獉 獉獉獉獉 獉獉獉獉獉獉獉獉
3.本卷命题范围:必修第一、二册、选择性必修1、选择性必修2。
可能用到的相对原子质量:H1 Li7 C12 N14 O16 Al27 S32 Cl35.5 K39
Fe56 Cu64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.一般情况下物质的性质决定用途。下列有关说法错误的是
A.宋代名画《千里江山图》中使用了氧化铁作红色颜料
B.AlO 熔点高,可用于制造耐火材料
2 3
C.石墨烯能导电,在新能源电池中得到广泛应用
D.亚硝酸钠具有酸性,可用作食品防腐剂
2.我国著名化学家付鹰说,“化学是实验的科学,只有实验才是最高法庭”。下列有关实验的说法
正确的是
A.NO 与Br(g)均为红棕色气体,可用湿润的淀粉KI试纸鉴别
2 2
B.阳离子交换膜法电解饱和食盐水可制备较纯净的烧碱
C.银氨溶液配制完成后,装入棕色试剂瓶,长期保存以备使用
D.皮肤溅上酸液后,先用大量水冲洗,然后涂上稀NaCO 溶液
2 3
3.我国正在大力推广美好乡村建设,下列有关化学与生活的说法合理的是
选项 化学知识 劳动生活
A 铝有强还原性 可用于制作门窗框架
B NaCO 可与酸反应产生CO 用小苏打作发泡剂烘焙面包
2 3 2
C 茄子中含有易被空气氧化的物质 切开的茄子放置后切面变色
D 沥青属于天然高分子材料 村村通工程中使用沥青铺设乡村公路
4.某有机物的结构如图所示,已知丙烷可表示为 。下列有关该物质的说法错 COOH
误的是
師師
A.分子式为C H O 帨帨
10 14 3
B.能发生氧化反应、加聚反应和取代反应 OH
C.该分子能被催化氧化生成含醛基的有机物
D.该分子中所有碳原子不可能共面
5.不同卤素原子之间相互形成的化合物称为卤素互化物。卤素互化物BrF 与水反应的化学方
3
程式为3BrF+5H O9HF+Br+HBrO +O ↑,但纯的三氟化溴能发生类似水的自耦
3 2 2 3 2
电离(H O+H O幑幐H O++OH-)而具有一定的导电性。下列说法正确的是
2 2 3
A.氧化剂是BrF,还原剂是 H O和BrF
3 2 3
B.已知 HBrO 的酸性大于 HCO ,因此溴元素的非金属性比碳元素强
3 2 3
4
C.若有1molH O参加反应,被水还原的BrF 为 mol
2 3 5
D.三氟化溴的自耦电离:2BrF 幑幐BrF-+BrF+
3 2 4
【“皖八”高三二联·化学 第 1页(共6页) W】
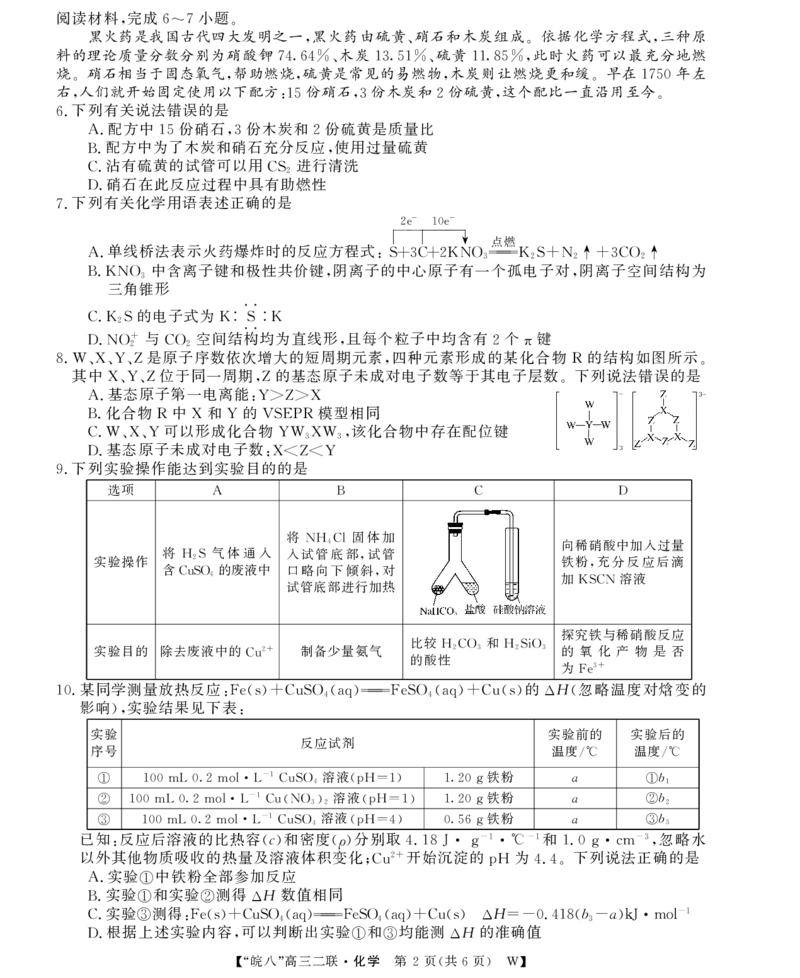
书书书阅读材料,完成6~7小题。
黑火药是我国古代四大发明之一,黑火药由硫黄、硝石和木炭组成。依据化学方程式,三种原
料的理论质量分数分别为硝酸钾7464%、木炭1351%、硫黄1185%,此时火药可以最充分地燃
烧。硝石相当于固态氧气,帮助燃烧,硫黄是常见的易燃物,木炭则让燃烧更和缓。早在1750年左
右,人们就开始固定使用以下配方:15份硝石,3份木炭和2份硫黄,这个配比一直沿用至今。
6.下列有关说法错误的是
A.配方中15份硝石,3份木炭和2份硫黄是质量比
B.配方中为了木炭和硝石充分反应,使用过量硫黄
C.沾有硫黄的试管可以用CS 进行清洗
2
D.硝石在此反应过程中具有助燃性
7.下列有关化学用语表述正确的是
2e- 1 0e -
↓↓
点燃
A.单线桥法表示火药爆炸时的反应方程式:S+3C+2KNO KS+N ↑+3CO ↑
3 2 2 2
B.KNO 中含离子键和极性共价键,阴离子的中心原子有一个孤电子对,阴离子空间结构为
3
三角锥形
··
C.KS的电子式为K· S·K
2 · ·
··
D.NO+ 与CO 空间结构均为直线形,且每个粒子中均含有2个π键
2 2
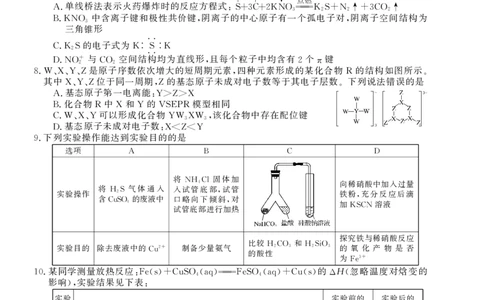
8.W、X、Y、Z是原子序数依次增大的短周期元素,四种元素形成的某化合物R的结构如图所示。
其中X、Y、Z位于同一周期,Z的基态原子未成对电子数等于其电子层数。下列说法错误的是
A.基态原子第一电离能:Y>Z>X
B.化合物R中X和Y的VSEPR模型相同
C.W、X、Y可以形成化合物YW XW ,该化合物中存在配位键
3 3
D.基态原子未成对电子数:X<Z<Y
9.下列实验操作能达到实验目的的是
选项 A B C D
将 NHCl固体加
4 向稀硝酸中加入过量
将 HS气体通入 入试管底部,试管
实验操作 2 铁粉,充分反应后滴
含CuSO 的废液中 口略向下倾斜,对
4 加KSCN溶液
试管底部进行加热
探究铁与稀硝酸反应
比较HCO 和HSiO
实验目的 除去废液中的Cu2+ 制备少量氨气 2 3 2 3 的 氧 化 产 物 是 否
的酸性
为Fe3+
10.某同学测量放热反应:Fe(s)+CuSO (aq)FeSO (aq)+Cu(s)的ΔH(忽略温度对焓变的
4 4
影响),实验结果见下表:
实验 实验前的 实验后的
反应试剂
序号 温度/℃ 温度/℃
① 100mL02mol·L-1CuSO
4
溶液(pH=1) 120g铁粉 a ①b
1
② 100mL02mol·L-1Cu(NO )溶液(pH=1) 120g铁粉 a ②b
3 2 2
③ 100mL02mol·L-1CuSO 溶液(pH=4) 056g铁粉 a ③b
4 3
已知:反应后溶液的比热容(c)和密度(
ρ
)分别取4.18J·g-1·℃-1和1.0g·cm-3,忽略水
以外其他物质吸收的热量及溶液体积变化;Cu2+开始沉淀的pH为4.4。下列说法正确的是
A.实验①中铁粉全部参加反应
B.实验①和实验②测得ΔH数值相同
C.实验③测得:Fe(s)+CuSO(aq)FeSO(aq)+Cu(s) ΔH=-0.418(b-a)kJ·mol-1
4 4 3
D.根据上述实验内容,可以判断出实验①和③均能测ΔH的准确值
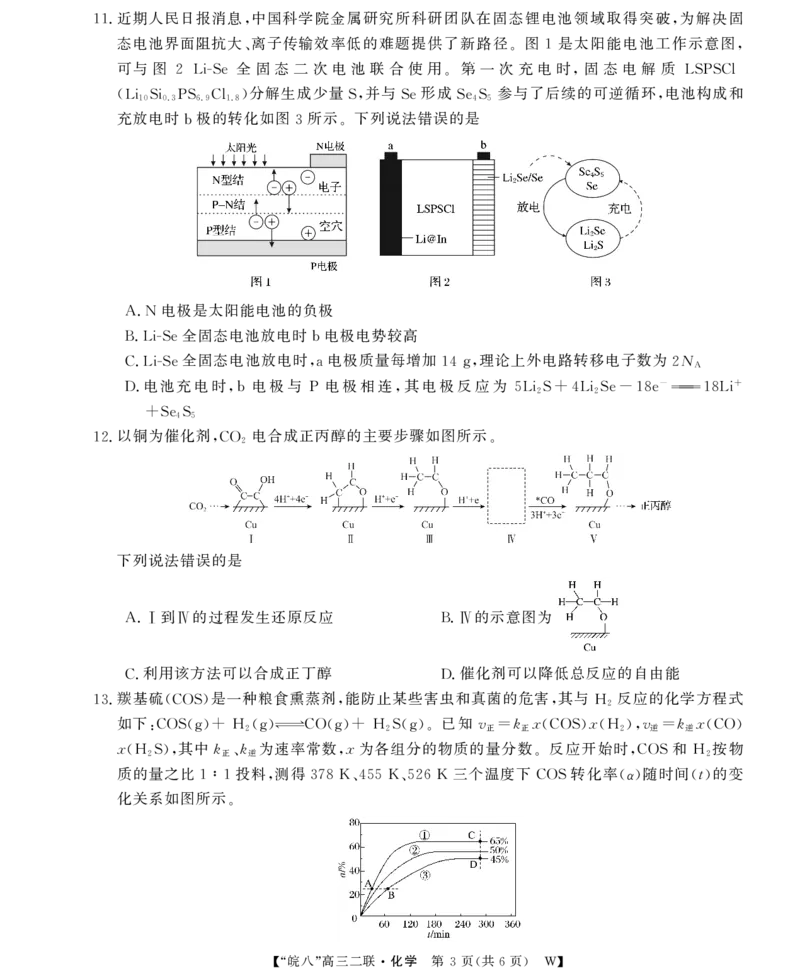
【“皖八”高三二联·化学 第 2页(共6页) W】11.近期人民日报消息,中国科学院金属研究所科研团队在固态锂电池领域取得突破,为解决固
态电池界面阻抗大、离子传输效率低的难题提供了新路径。图1是太阳能电池工作示意图,
可与 图 2 LiSe 全 固 态 二 次 电 池 联 合 使 用。第 一 次 充 电 时,固 态 电 解 质 LSPSCl
(LiSi PS Cl )分解生成少量S,并与Se形成SeS 参与了后续的可逆循环,电池构成和
10 0.3 6.9 1.8 4 5
充放电时b极的转化如图3所示。下列说法错误的是
A.N电极是太阳能电池的负极
B.LiSe全固态电池放电时b电极电势较高
C.LiSe全固态电池放电时,a电极质量每增加14g,理论上外电路转移电子数为2N
A
D.电池充电时,b电极与 P 电极相连,其电极反应为5LiS+4LiSe-18e- 18Li+
2 2
+SeS
4 5
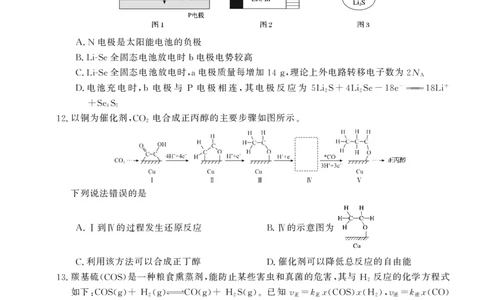
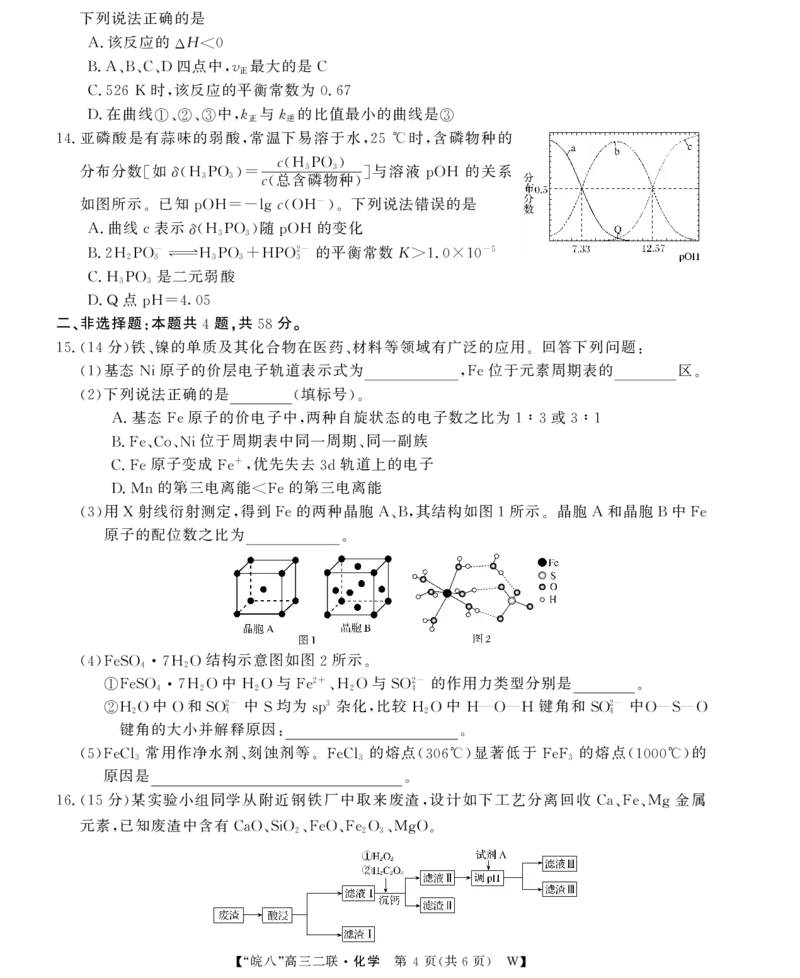
12.以铜为催化剂,CO 电合成正丙醇的主要步骤如图所示。
2
下列说法错误的是
A.Ⅰ到Ⅳ的过程发生还原反应 B.Ⅳ的示意图为
C.利用该方法可以合成正丁醇 D.催化剂可以降低总反应的自由能
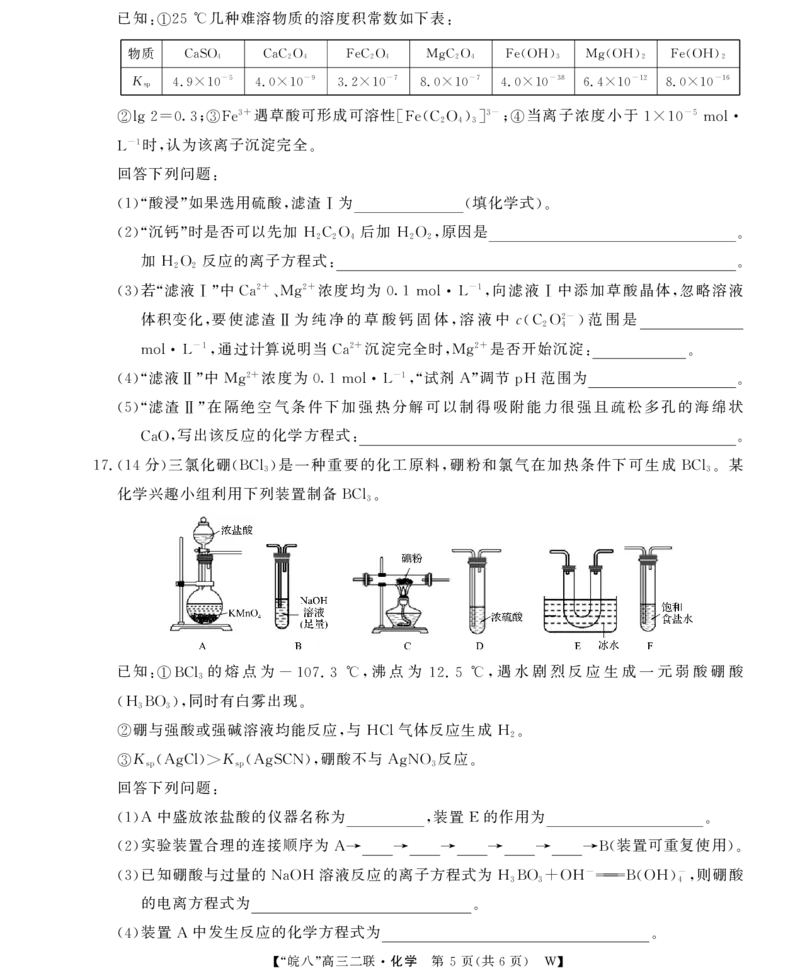
13.羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害,其与 H 反应的化学方程式
2
如下:COS(g)+ H (g)幑幐CO(g)+ HS(g)。已知v =kx(COS)x(H ),v =kx(CO)
2 2 正 正 2 逆 逆
x(HS),其中k 、k 为速率常数,x为各组分的物质的量分数。反应开始时,COS和 H 按物
2 正 逆 2
质的量之比1∶1投料,测得378K、455K、526K三个温度下COS转化率(α)随时间(t)的变
化关系如图所示。
【“皖八”高三二联·化学 第 3页(共6页) W】下列说法正确的是
A.该反应的ΔH<0
B.A、B、C、D四点中,v 最大的是C
正
C.526K时,该反应的平衡常数为0.67
D.在曲线①、②、③中,k 与k 的比值最小的曲线是③
正 逆
14.亚磷酸是有蒜味的弱酸,常温下易溶于水,25℃时,含磷物种的
c(HPO )
分布分数[如δ(HPO )= 3 3 ]与溶液pOH 的关系
3 3 c(总含磷物种)
如图所示。已知pOH=-lgc(OH-)。下列说法错误的是
A.曲线c表示δ(HPO )随pOH的变化
3 3
B.2HPO- 幑幐HPO +HPO2- 的平衡常数K>1.0×10-5
2 3 3 3 3
C.HPO 是二元弱酸
3 3
D.Q点pH=405
二、非选择题:本题共4题,共58分。
15.(14分)铁、镍的单质及其化合物在医药、材料等领域有广泛的应用。回答下列问题:
(1)基态Ni原子的价层电子轨道表示式为 ,Fe位于元素周期表的 区。
(2)下列说法正确的是 (填标号)。
A.基态Fe原子的价电子中,两种自旋状态的电子数之比为1∶3或3∶1
B.Fe、Co、Ni位于周期表中同一周期、同一副族
C.Fe原子变成Fe+,优先失去3d轨道上的电子
D.Mn的第三电离能<Fe的第三电离能
(3)用X射线衍射测定,得到Fe的两种晶胞A、B,其结构如图1所示。晶胞A和晶胞B中Fe
原子的配位数之比为 。
(4)FeSO ·7H O结构示意图如图2所示。
4 2
①FeSO ·7H O中 H O与Fe2+、H O与SO2- 的作用力类型分别是 。
4 2 2 2 4
②HO中O和SO2- 中S均为sp3 杂化,比较 HO中 H—O—H键角和SO2- 中O—S—O
2 4 2 4
键角的大小并解释原因: 。
(5)FeCl 常用作净水剂、刻蚀剂等。FeCl 的熔点(306℃)显著低于FeF 的熔点(1000℃)的
3 3 3
原因是 。
16.(15分)某实验小组同学从附近钢铁厂中取来废渣,设计如下工艺分离回收Ca、Fe、Mg金属
元素,已知废渣中含有CaO、SiO 、FeO、FeO 、MgO。
2 2 3
【“皖八”高三二联·化学 第 4页(共6页) W】已知:①25℃几种难溶物质的溶度积常数如下表:
物质 CaSO
4
CaC
2
O
4
FeC
2
O
4
MgC
2
O
4
Fe(OH)
3
Mg(OH)
2
Fe(OH)
2
K
sp
4.9×10-5 4.0×10-9 3.2×10-7 8.0×10-7 4.0×10-38 6.4×10-12 8.0×10-16
②lg2=03;③Fe3+遇草酸可形成可溶性[Fe(CO )]3-;④当离子浓度小于1×10-5mol·
2 4 3
L-1时,认为该离子沉淀完全。
回答下列问题:
(1)“酸浸”如果选用硫酸,滤渣Ⅰ为 (填化学式)。
(2)“沉钙”时是否可以先加 HCO 后加 H O ,原因是 。
2 2 4 2 2
加 H O 反应的离子方程式: 。
2 2
(3)若“滤液Ⅰ”中Ca2+、Mg2+浓度均为01mol·L-1,向滤液Ⅰ中添加草酸晶体,忽略溶液
体积变化,要使滤渣Ⅱ为纯净的草酸钙固体,溶液中c(CO2-)范围是
2 4
mol·L-1,通过计算说明当Ca2+沉淀完全时,Mg2+是否开始沉淀: 。
(4)“滤液Ⅱ”中 Mg2+浓度为01mol·L-1,“试剂A”调节pH范围为 。
(5)“滤渣Ⅱ”在隔绝空气条件下加强热分解可以制得吸附能力很强且疏松多孔的海绵状
CaO,写出该反应的化学方程式: 。
17.(14分)三氯化硼(BCl)是一种重要的化工原料,硼粉和氯气在加热条件下可生成BCl。某
3 3
化学兴趣小组利用下列装置制备BCl。
3
已知:①BCl的熔点为-107.3 ℃,沸点为12.5 ℃,遇水剧烈反应生成一元弱酸硼酸
3
(HBO ),同时有白雾出现。
3 3
②硼与强酸或强碱溶液均能反应,与 HCl气体反应生成 H 。
2
③K (AgCl)>K (AgSCN),硼酸不与AgNO 反应。
sp sp 3
回答下列问题:
(1)A中盛放浓盐酸的仪器名称为 ,装置E的作用为 。
(2)实验装置合理的连接顺序为A→ → → → → →B(装置可重复使用)。
(3)已知硼酸与过量的NaOH溶液反应的离子方程式为 HBO +OH-B(OH)-,则硼酸
3 3 4
的电离方程式为 。
(4)装置A中发生反应的化学方程式为 。
【“皖八”高三二联·化学 第 5页(共6页) W】(5)测定产品中氯元素的含量:准确称取3.5g产品,配制成250mL溶液,量取10.00mL于锥
形瓶中,加入22.20mL0.2000mol·L-1AgNO 溶液,使Cl-完全沉淀,再加少许硝基苯
3
用力振荡;以Fe(NO )为指示剂,用0.2000mol·L-1KSCN标准溶液滴定过量的 Ag+
3 3
(Ag++SCN-AgSCN↓),三次平行实验数据如下:
KSCN标准溶液
实验编号 待测液体积/mL
滴定前读数/mL 滴定后读数/mL
① 10.00 0.40 10.41
② 10.00 0.10 10.80
③ 10.00 0.00 9.99
①达到滴定终点时的现象为 。
②产品中氯元素的质量分数为 %(保留三位有效数字)。
18.(15分)MgCO 的热分解与CuS催化的CH 重整结合,可生产高纯度合成气,有利于实现碳
3 x 4
中和。主要反应如下:
反应Ⅰ:MgCO (s)MgO(s)+CO (g) ΔH =+101kJ·mol-1
3 2 1
反应Ⅱ:CH (g)+CO (g)幑幐2H (g)+2CO(g) ΔH =+247kJ·mol-1
4 2 2 2
反应Ⅲ:H (g)+CO (g)幑幐H O(g)+CO(g) ΔH =+41kJ·mol-1
2 2 2 3
回答下列问题:
(1)反应Ⅱ在 (填“高温”“低温”或“任意温度”)下能自发进行。
(2)MgCO (s)+H (g)幑幐MgO(s)+H O(g)+CO(g) ΔH= 。
3 2 2
(3)CuS晶胞中S2-的位置如图1所示,Cu2+位于S2-所构成的正四面体中心,CuS的晶胞
x x
参数为apm,阿伏加德罗常数为N 。x=1或2时,两者晶胞正视图都如图2所示,若x
A
=1时,两个Cu2+最近距离为 ,若晶胞的密度为 ρg·cm-3时,x= 。
(4)向恒容密闭容器中加入1.0molMgCO 、1.0molCH 和3.0molAr,初始压强为80kPa,
3 4
发生上述反应Ⅰ、Ⅱ、Ⅲ,平衡时体系中各物质的物质的量和 MgCO 的转化率随温度变化
3
如图3所示。
①600℃之后,随着温度的升高,H 的物质的量减少的原因是 。
2
②600℃时CH 转化率为 ,反应Ⅱ的K = kPa2。
4 p
【“皖八”高三二联·化学 第 6页(共6页) W】