文档内容
武汉二中 2025 届高三年级高考模拟考试
化学试卷
命题学校:武汉二中
考试时间:2025年5月22日下午:14:30-15:45 试卷满分100分
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Cu 64
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1. 化学是社会发展的基础,下列说法正确的是
A.合成纤维是以石油、天然气和煤为原料制成的
B.添加纳米银颗粒的抗菌材料:纳米银颗粒具有强氧化性
C.稀土元素是指镧系金属元素,在钢中添加稀土元素可以增加钢的塑性、韧性等
D.量子通信材料螺旋碳纳米管与石墨烯互为同分异构体
2.下列化学用语表示不正确的是
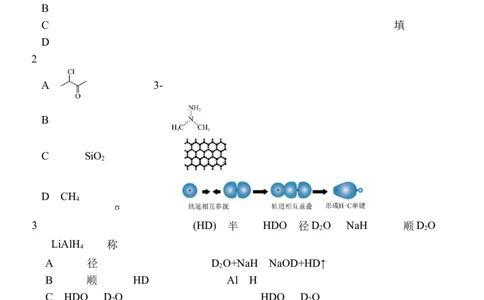
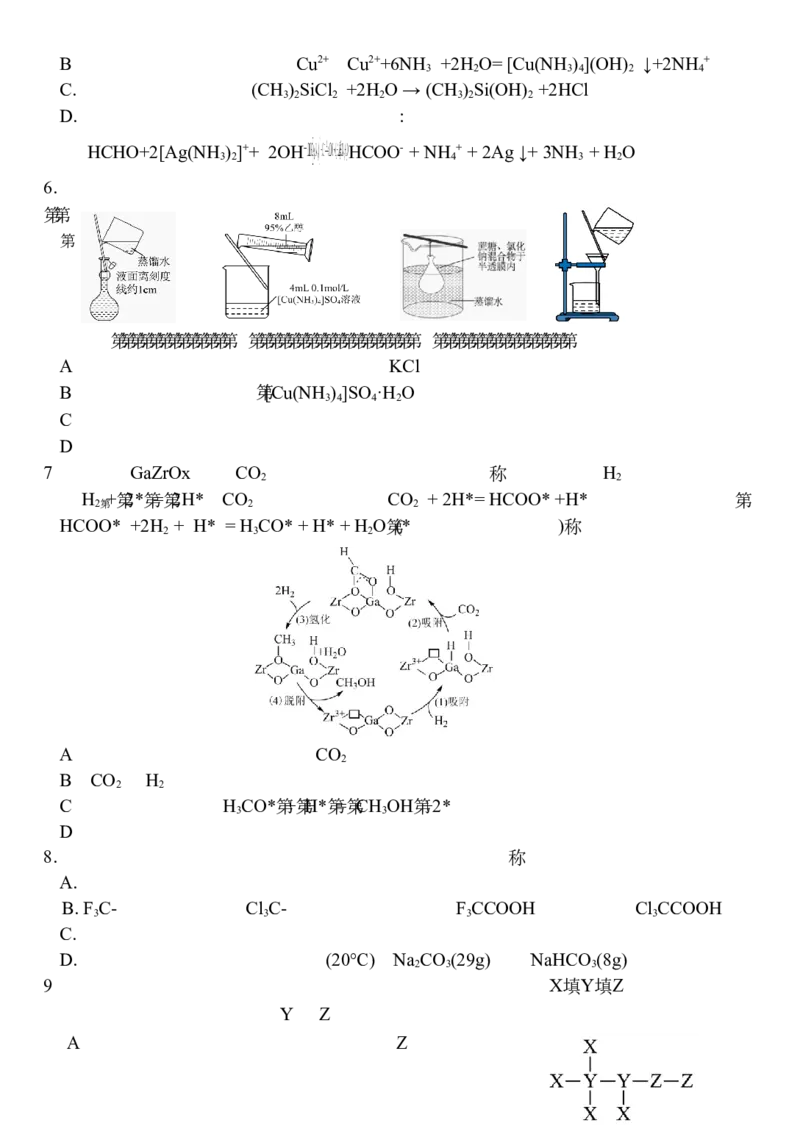
A. 的系统命名:3-氯丁酮
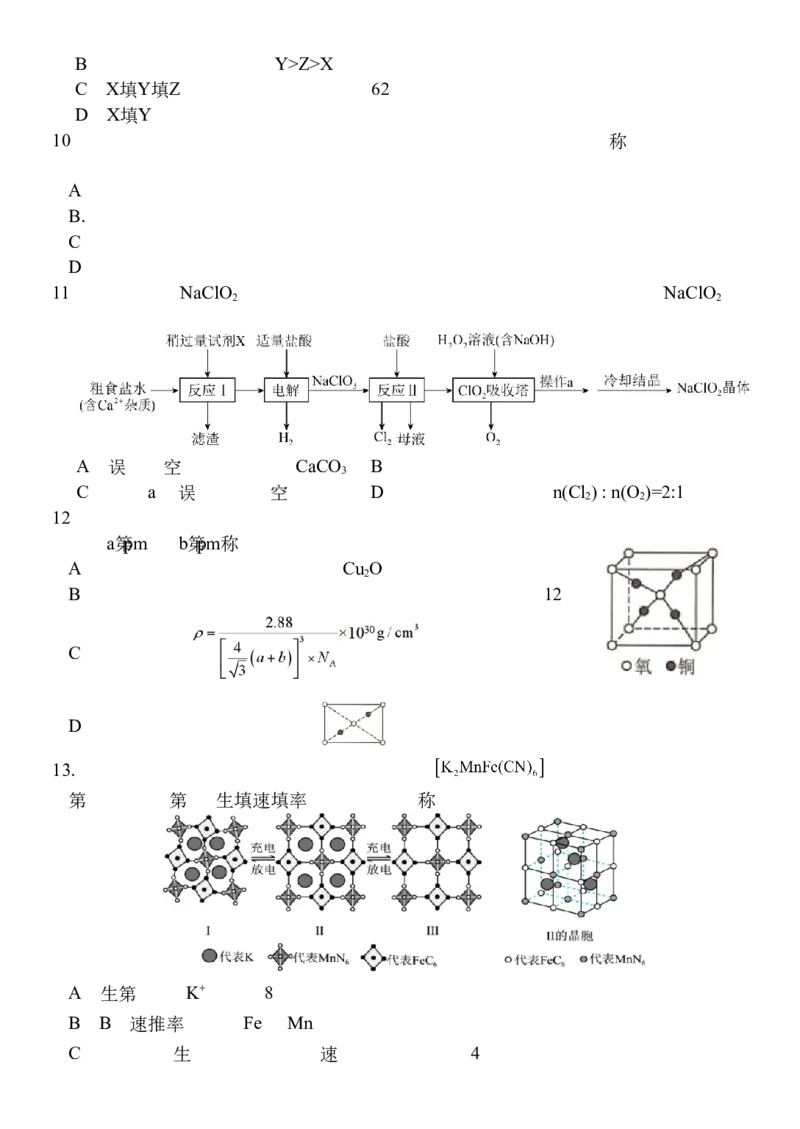
B.偏二甲肼的结构简式:
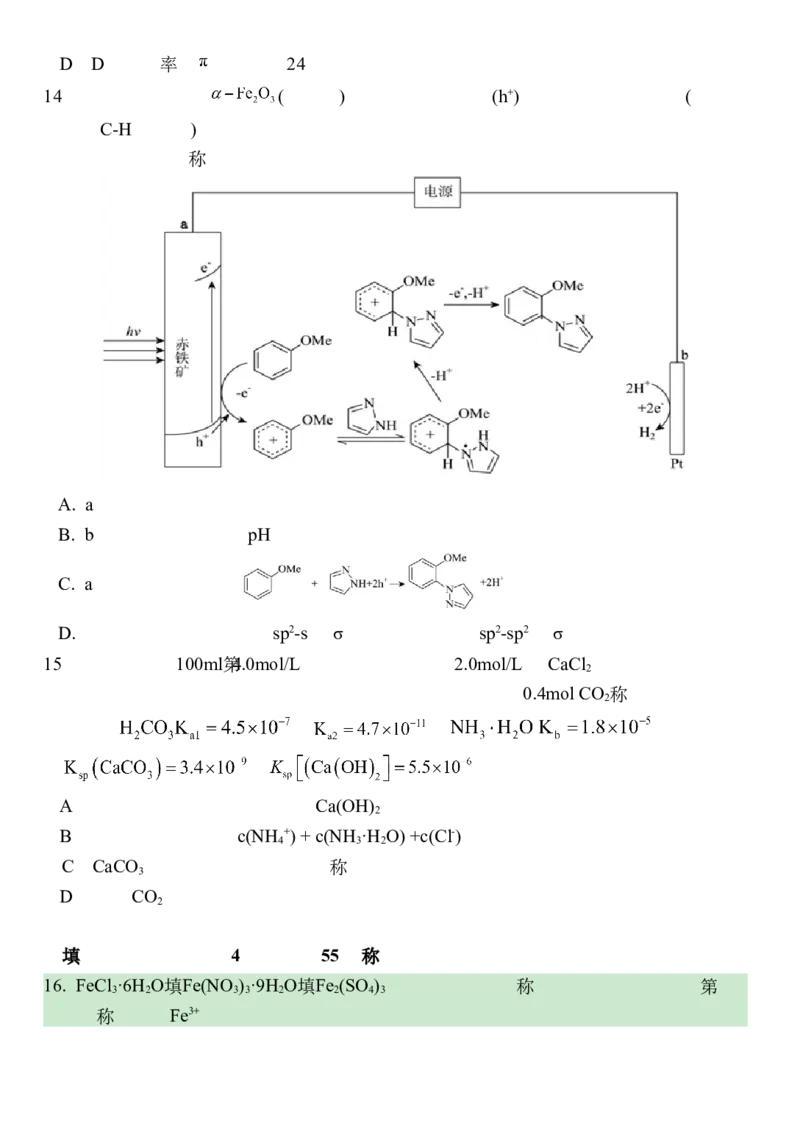
C.晶体SiO 的微观投影图:
2
D.CH 分子中 键的形成:
4
3.下列三种方法均可得到氘化氢(HD):①电解HDO;②D O与NaH反应;③D O与
2 2
LiAlH 反应。下列说法不正确的是
4
A.方法②中反应的化学方程式为D O+NaH=NaOD+HD↑
2
B.方法③能得到HD,说明电负性:Al<H
C.HDO和D O均为极性分子,质量相同的HDO和D O所含质子数相同
2 2
D.方法②得到的产品纯度比方法①的高
4.化合物 是合成某种抗真菌药药物的中间体,下列说法不正确的是
A.X分子中所有碳原子可能共平面 B.Y分子存在对映异构现象
C.1mol Z最多能与3mol NaOH反应 D.Y、Z可用溴的CCl 溶液鉴别
4
5. 下列离子方程式正确的是
A.碱性CH OH--O 燃料电池的总反应:2CH OH + 3O = 2CO + 4H O
3 2 3 2 2 2B.若向溶液中通入氨气除去Cu2+:Cu2++6NH +2H O= [Cu(NH ) ](OH) ↓+2NH +
3 2 3 4 2 4
C. 硅橡胶单体的制备:(CH ) SiCl +2H O → (CH ) Si(OH) +2HCl
3 2 2 2 3 2 2
D. 甲醛溶液中加入足量的银氨溶液并加热:
HCHO+2[Ag(NH ) ]++ 2OH- HCOO- + NH + + 2Ag ↓+ 3NH + H O
3 2 4 3 2
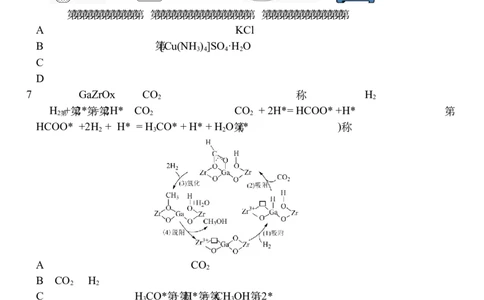
6. 用下列装置进行相应实验,操作规范且能达到实验目的的是
甲 乙 丙 丁
A.装置甲用于配制一定物质的量浓度的KCl溶液
B.装置乙用于制备晶体 [Cu(NH ) ]SO ·H O
3 4 4 2
C.装置丙用于分离蔗糖与氯化钠的混合溶液
D.装置丁用于从浑浊的苯酚水溶液中分离苯酚
7.催化剂GaZrOx催化CO 加氢制甲醇的机理如图所示。已知:图中H 吸附过程表示
2 2
为H + 2* = 2H*;CO 吸附过程表示为CO + 2H*= HCOO* +H*;氢化过程表示为
2 2 2
HCOO* +2H + H* = H CO* + H* + H O (*为催化剂活性位点)。下列说法错误的是
2 3 2
A.氧空位浓度高,有利于增强CO 的吸附能力
2
B.CO 和H 的活化位点是不相同的
2 2
C.脱附过程表示为H CO* + H* = CH OH +2*
3 3
D.降低氢化过程的活化能,一定能有效加快甲醇的生成速率
8. 从微观视角探析物质结构及性质是学习化学的有效方法。下列说法正确的是
A. 乙醚是非极性分子,乙醇是极性分子,因此乙醚在水中的溶解度比乙醇小
B. F C-是吸电子基团,Cl C-是推电子基团,因此F CCOOH的酸性强于Cl CCOOH
3 3 3 3
C. 原子的能级是量子化的,因此原子光谱是不连续的线状谱线
D. 阴离子电荷不同,因此溶解度(20℃):Na CO (29g)大于NaHCO (8g)
2 3 3
9.一种二元活性自由基(单电子未标出)的结构如下图所示,X、Y、Z为原子序数依
次增大的短周期主族元素,Y和Z可形成两种常见化合物,下列说法不正确的是
A.该自由基的两个活性中心分别在两个Z原子上B.原子半径大小顺序为Y>Z>X
C.X、Y、Z可形成相对分子质量为62的化合物
D.X、Y形成的化合物可既含有极性键又含有非极性键
10.化学仿生学是用化学方法在分子水平上模拟生物体功能的一门科学。下列说法错误的
是
A.模仿叶绿体分解水的功能开发的光催化剂能将光能转化为化学能
B. 模仿生物细胞膜制成的海水淡化反渗透膜属于功能高分子材料
C.模仿壁虎足的结构制成的仿生胶带能与被黏着物之间形成化学键
D.模仿荷叶表面微观结构和蜡质层制成的自清洁涂层需选用疏水材料
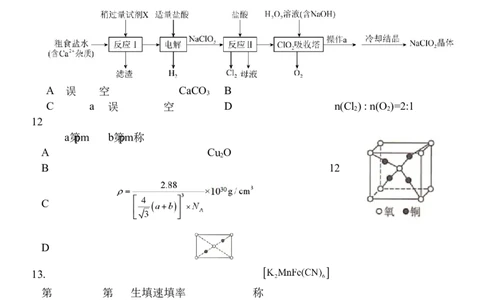
11.亚氯酸钠(NaClO ,受热易分解)是一种重要的含氯消毒剂,一种制备NaClO 的
2 2
工艺流程如图所示,下列说法错误的是
A.“滤渣”的主要成分为CaCO B.流程中两处盐酸的作用不同
3
C.操作a为“减压蒸发” D.理论上,该流程中n(Cl ) : n(O )=2:1
2 2
12.铜和氧形成的一种离子化合物的晶体结构如图所示,设阳离子和阴离子的半径分别
为a pm 和b pm。下列相关说法正确的是
A.该化合物的分子式可以表示为Cu O
2
B.晶体中每个阳离子周围紧邻且距离相等的阳离子个数为12 个
C.晶体的密度
D.晶胞沿面对角线的剖面图为
13. 一种钾离子电池正极材料钾锰铁基普鲁士白 充电或放电时变化如
下图所示, 其中Ⅰ、Ⅱ、Ⅲ为晶胞俯视图。下列说法中错误的是
A.Ⅰ 晶胞中K+数目为8
B.B.Ⅱ→Ⅲ过程中Fe或Mn的价态升高
C.每个晶胞Ⅰ完全转化为晶胞Ⅱ,转移电子数为4D.D.晶胞Ⅲ中 键数目为24
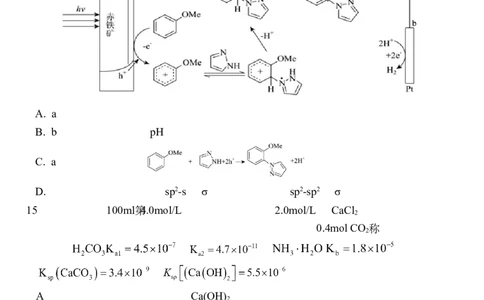
14.在光照条件下, (赤铁矿)材料中的光生空穴(h+)可氧化富电子的芳烃(使苯环
上的C-H键胺化)形成相应的阳离子自由基物种,生成物进一步与吡唑反应得到偶联
产物,机理如图。下列叙述正确的是
A. a电极为正极
B. b极附近电解质溶液pH降低
C. a极的电极反应式为
D. 上述总反应中,只断裂sp2-s型σ键,同时只形成sp2-sp2型σ键
15.常温下,将100ml 4.0mol/L的氨水滴入等体积2.0mol/L的CaCl 溶液中后,未见明
2
显现象,振荡,出现白色浑浊;再向混合体系中缓慢通入0.4mol CO 。
2
已知: , ; ;
, ,下列说法正确的是
A.滴入氨水后,振荡后,没有Ca(OH) 沉淀生成
2
B.滴入氨水过程中:c(NH +) + c(NH ·H O) +c(Cl-) 不变
4 3 2
C.CaCO 固体易溶于碳酸溶液中。
3
D.通入CO 过程中,水的电离程度不断减小
2
二、非选择题:本题共4小题,共55分。
16. FeCl ·6H O、Fe(NO ) ·9H O、Fe (SO ) 均为重要的铁盐。某学习小组展开如下
3 2 3 3 2 2 4 3
探究。已知:Fe3+的配离子在溶液中呈现颜色情况如下表所示:[Fe(H O) ]3+ [Fe(H O) (OH)]2+ [FeCl ]- [Fe(C H O) ]3-
2 6 2 5 4 6 5 6
淡紫色(稀溶液时为无
颜色 黄色 亮黄色 紫色
色)
请回答下列问题:
(1)实验室若要用FeCl ·6H O配制100ml 0.200mol/L的FeCl 溶液,下列仪器中不需
3 2 3
要使用的是 (填仪器名称)。
(2)向盛有0.2g铜片的试管中加入5ml 0.5 mol/L 的Fe (SO ) 溶液,铜片部分溶解,
2 4 3
溶液变为蓝色,则发生反应的离子方程式为 。
(3)淡紫色的Fe(NO ) ·9H O晶体溶于水后依次加入硝酸和NaCl,溶液颜色出现下列
3 3 2
变 化:
①溶液Ⅰ为黄色的原因是 。
②溶液Ⅲ又变为亮黄色的原因是 (用离子方程式表示)。
(4)查阅资料:Fe3+ + 6C H OH [Fe(C H O) ]3- + 6H+。取FeCl 溶液和苯酚溶液,进
6 5 6 5 6 3
行如下实验,溶液颜色出现下列变化:
随着NaOH溶液的滴加,紫色溶液先变深,后变浅的主要原因是 (不考虑
体积影响)。
(5)查阅资料:Fe3+ 能与银反应:Fe3+ +Ag Ag+ + Fe2+且该反应为可逆反应。据此
设计如下实验方案,溶解银镜实验后的Ag:
实验ⅰ:向有银镜的试管中加入0.2mol/L的Fe(NO ) 溶液(pH=2),银镜慢慢消失,溶
3 3
液变澄清;实验ⅱ:向有银镜的试管中加入0.2mol/L的FeCl 溶液(pH=2),银镜快速溶解,反应
3
后溶液中有明显灰色沉淀。
①经小组讨论认为,实验ⅰ不能证明Fe3+能与银反应,其原因为 。
②推测实验ⅱ比实验ⅰ银镜溶解快的可能原因: 。
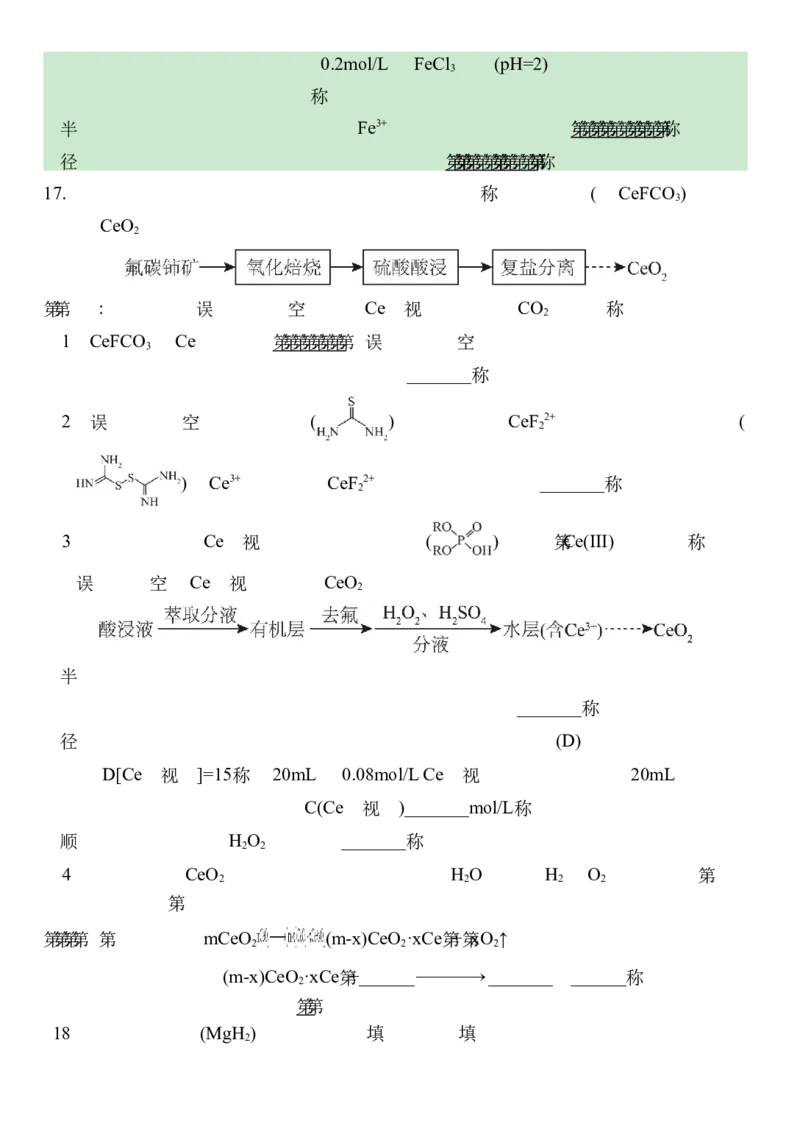
17. 稀土元素已成为发展尖端科学技术不可缺少的材料。以氟碳铈矿(含CeFCO )为原料
3
制备CeO 的工艺流程可表示为
2
已知:氟碳铈矿在“氧化焙烧”中生成Ce(Ⅳ)化合物和CO 等气体。
2
(1)CeFCO 中Ce的化合价 ,“氧化焙烧”冷却后往往不需要机械加工粉碎
3
成颗粒,就能与硫酸充分反应,其原因是_______。
(2)“复盐分离”时先加入硫脲( )还原酸浸液中CeF 2+等离子,生成二硫甲脒(
2
)和Ce3+ ,硫脲和CeF 2+反应的离子方程式为_______。
2
(3)在硫酸介质中Ce(Ⅳ)可被磷酸二异辛酯( )萃取, Ce(III)不被萃取。萃取
“酸浸液”中Ce(Ⅳ),制取CeO 的流程如下:
2
①磷酸二异辛酯在煤油中通过氢键形成对称的环状二聚体,较大的烃基会使与之连接
的氧原子难以形成氢键,该环状二聚体结构式可表示为_______。
②被萃取物在有机层和水层中的物质的量浓度之比称为分配比(D),本题实验条件
下D[Ce(Ⅳ)]=15。向20mL含0.08mol/L Ce(Ⅳ)的酸浸液中加入20mL萃取剂
充分振荡,静置后,水层中C(Ce(Ⅳ))_______mol/L。
③反萃取时有机层加H O 的作用是_______。
2 2
(4)科学家利用CeO 作催化剂在太阳能作用下将H O转化成H 和O ,该反应分
2 2 2 2
两步进行,
第 一步反应为mCeO (m-x)CeO ·xCe + xO ↑
2 2 2
则第二步反应为:(m-x)CeO ·xCe +______ _______+______。
2
将该反应方程式补充完整:
18.镁基储氢材料(MgH )因其储氢量大、资源丰富、成本低而被认为是最具应用前景
2的金属储氢材料之一。
(1)镁基储氢材料水解反应可制氢:
①
②
则 。
(2)一定质量的MgH (s)在pH=7时发生水解反应,生成氢气的体积V(单位: )与时
2
间t(单位:s)的关系式为V=1.25t - 40 (t>32)。
①用氢气的体积变化表示前5min 的反应速率为 。
②MgH 在MgCl 溶液中的产氢速率快于纯水,其原因是 (已知该现象只与
2 2
Mg2+ 有关)。
(3)已知Mg与H 在一定条件下发生反应: 可制备镁基储氢材
2
料。
①若反应达平衡后,再加入等物质的量的Mg和MgH ,平衡 (填“正
2
向”、“逆向”或“不”)移动。
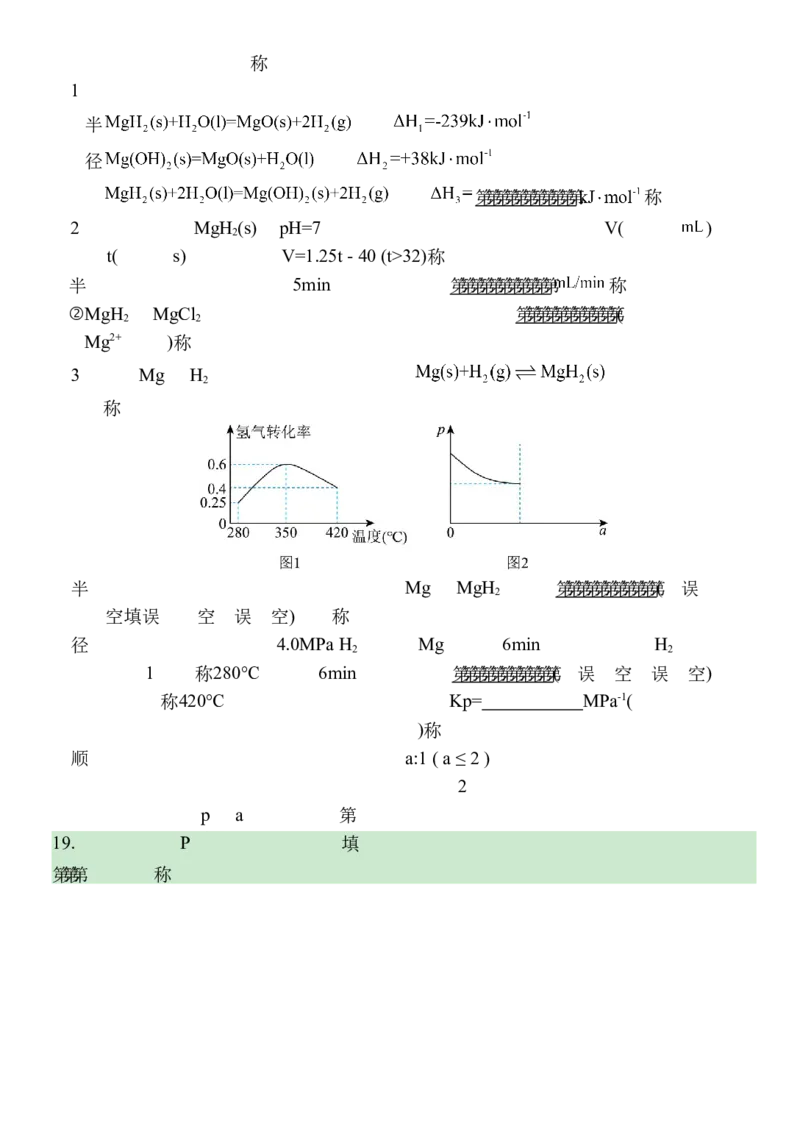
②在恒容密闭容器中加入4.0MPa H 及足量Mg,反应6min,不同温度下H 的转化率
2 2
如上图1所示。280℃下反应6min时,该反应 (填“是”或“否”)达到
平衡状态。420℃时,该反应的压强平衡常数Kp= MPa-1(以平衡分压代
替物质的量浓度计算,保留两位有效数字)。
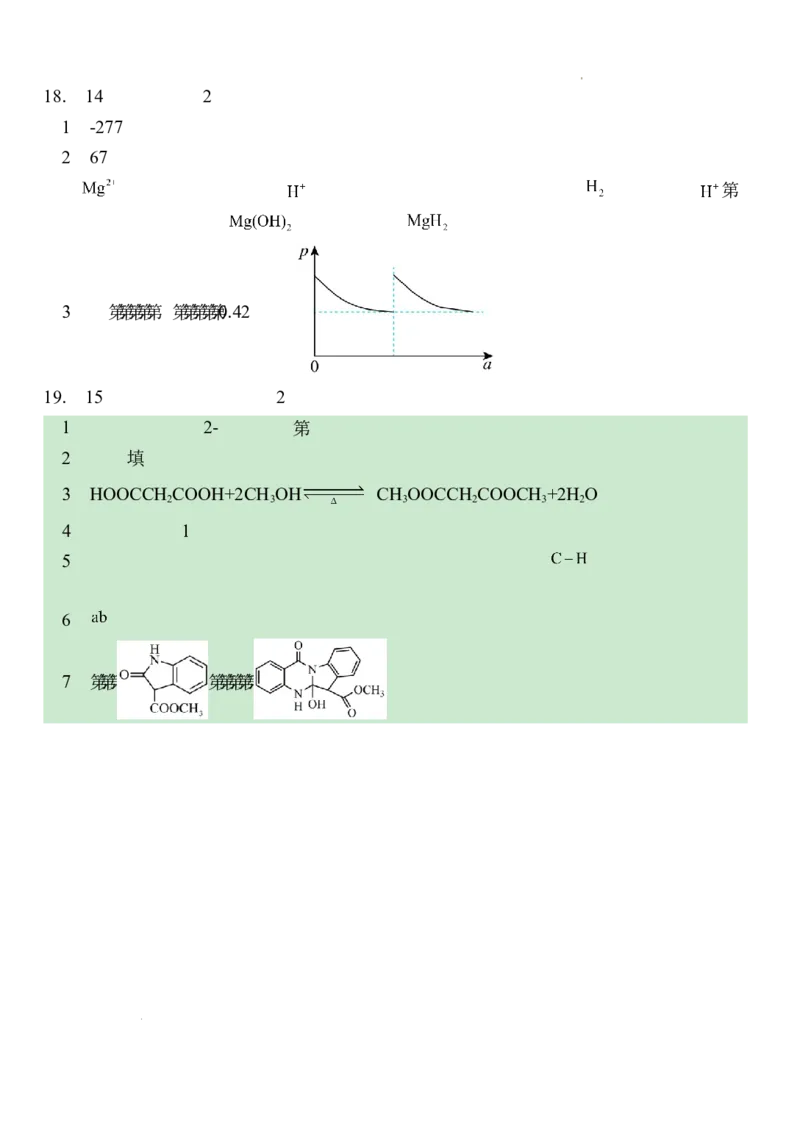
③假设制得储氢材料中氢镁原子个数比为a:1 ( a ≤ 2 ),该反应在恒温密闭容器中达到
平衡后,缩小容器体积为原来的一半,在上图2中画出从改变条件到建立平衡的过
程中气体压强p与a的变化曲线
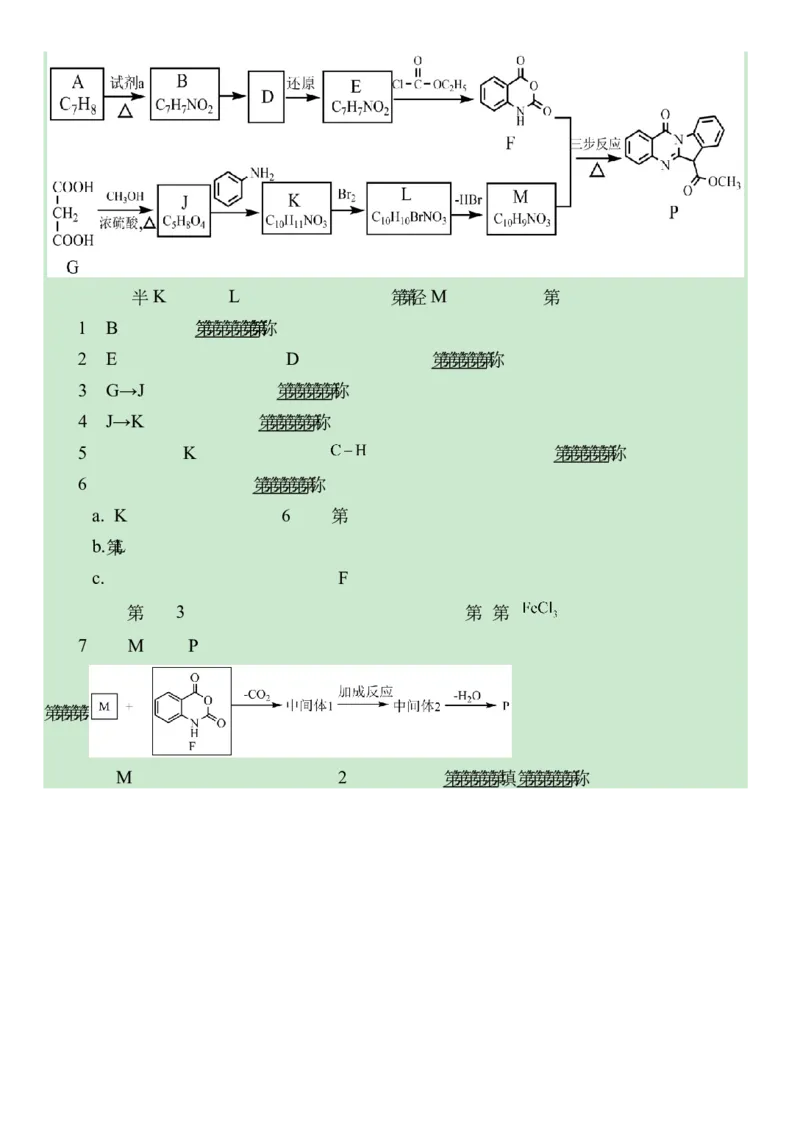
19. 有机化合物P是一种具有抗肿瘤、抗菌等多种药理活性的色胺酮类衍生物,合成
路线如图。已知:①K转化为L的反应为取代反应 ②M含有五元环
(1)B的名称是 。
(2)E既有酸性又有碱性,D含有的官能团是 。
(3)G→J的化学方程式是 。
(4)J→K的反应类型是 。
(5)溴单质与K中苯环侧链上的 发生取代反应的原因是 。
(6)下列说法正确的是 。
a. K的核磁共振氢谱有6组峰
b. L可发生水解反应
c. 不存在同时满足下列条件的F的同分异构体:
ⅰ 含有3种官能团(其中一种为碳碳三键) ⅱ 遇 溶液显紫色
(7)由M生成P经三步反应过程:
写出M(含有五元环)与中间体2的结构简式 、 。武汉二中 2025 届高三年级高考模拟考试
化学试卷参考答案
一、选择题(每小题只有1个正确答案,每小题3分,共45分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 A D C C C B D C A C D B D C B
二、非选择题(共55分)
16.(13分)(除标注外每空2分)
(1)碱式滴定管(1分)
(2)
(3)部分 水解生成 (合理即可)
(4) 随着NaOH溶液的滴入,开始时中和溶液中的H+,平衡向右移动;随着pH增
大,与Fe3+生成Fe(OH) ,平衡向左移动(合理即可)
3
(5) 0.2mol/L Fe(NO ) 溶液(pH=2)中含有的稀硝酸也能溶解银
3 3
Ag+结合Cl- 生成AgCl,有利于反应 正向移动,从而加快
Ag的溶解
17. (13分)(除标注外每空2分)
(1)+3 (1分)
氟碳铈矿在焙烧过程中产生CO 气体时固体变疏松
2
(2)2
(3) ① ② 0.005
③将四价铈还原为三价铈,使其进入水层
(4)
学科网(北京)股份有限公司18.(14分)(每空2分)
(1)-277
(2)67
水解使溶液呈酸性, 浓度增大,增强了氧化性,加快了 生成速率;
能溶解表面沉积的 保护层,促进 与水接触,提高了水解速率
(3)不 否 0.42
19.(15分)(除标注外每空2分)
(1)邻硝基甲苯或2-硝基甲苯
(2)硝基、羧基
(3)HOOCCH COOH+2CH OH CH OOCCH COOCH +2H O
2 3 3 2 3 2
(4)取代反应(1分)
(5)受两侧羰基的(吸电子)作用影响,使相连的碳原子上的 的极性增强,易断
裂
(6)
(7)
学科网(北京)股份有限公司