文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【黑吉辽版】
可能用到的相对原子质量:H-1、Li-7、N-14、O-16、S-32、Cu-64、Co-59、In-115
一、选择题:本题共 15 小题,每小题 3 分,共 45 分。每小题只有一个选项符合题目要求。
1.我国是文明古国,文化底蕴深厚。下列与化学有关的说法正确的是( )
A.潮州木雕历史悠久,始于唐代,盛于明清,木雕的主要成分是蛋白质
B.指南针的发明可以追溯到战国时期,制造指南针的磁性物质是Fe O
2 3
C.贾湖遗址出土了大量炭化稻米,是世界水稻文明的源头之一,可利用12C测定年代
6
D.洛阳杜康酒起源于黄帝时期,谷物酿酒过程涉及氧化还原反应
2.化学用语可以表达化学过程,下列化学用语的表达错误的是( )
A.H 分子中s—sσ键与HCl分子中s—pσ键的电子云图形对称性相同
2
B.NH 的VSEPR模型:
3
C.MgCl 的形成过程:
2
D.己二酸与丁二醇制备聚酯类合成树脂:nHOOCCH COOHnHOCH CH CH CH OH
2 4 2 2 2 2
‡ˆ ˆˆ 催化ˆˆ 剂ˆˆ†ˆ (n1)H O
△ 2
3.下列气体的制备方法错误的是( )
A.制备Cl :漂白粉与浓盐酸在常温下反应
2
B.制备 HBr:浓磷酸与NaBr在加热条件下反应
C.制备SO :Na SO 与98%的浓硫酸在加热条件下反应
2 2 3
D.制备NO :Cu与浓硝酸在常温下反应
2
4.下列物质的鉴别方法(必要时可加热)错误的是( )
A.鉴别植物油、汽油、甘油:滴加NaOH溶液
B.鉴别苯、乙醇、四氯化碳:燃烧
C.鉴别浓度均为0.1molL1的NaCl、NaNO 、KNO 溶液:测定溶液pH
2 3
D.鉴别CuO、MnO 和Fe粉三种固体:滴加浓盐酸
2
5.氯气溶于水可以发生反应Cl H O‡ˆ ˆˆ†ˆ HClHClO。设N 为阿伏加德罗常数的值,下列
2 2 A
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
说法正确的是( )
A.11.2LCl 含有N 个Cl原子
2 A
B.0.1 mol HClO溶于水,溶液中含有0.1N 个ClO
A
C.若反应消耗1molCl ,则转移N 个电子
2 A
D.若所得溶液pH=3,则溶液中含有103N 个H
A
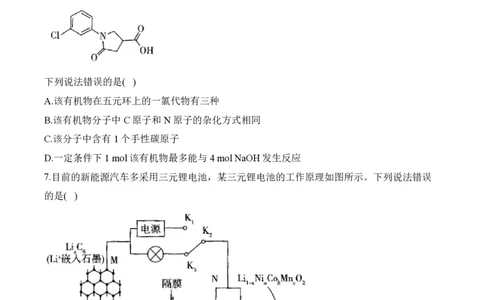
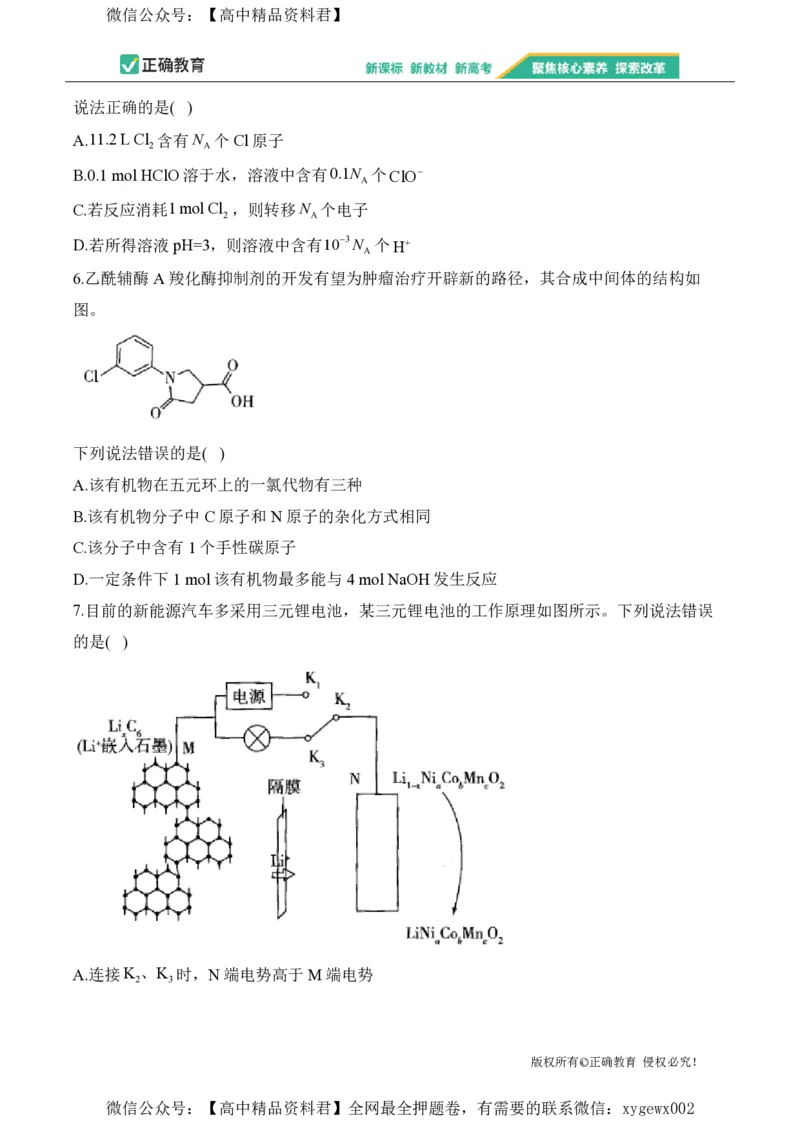
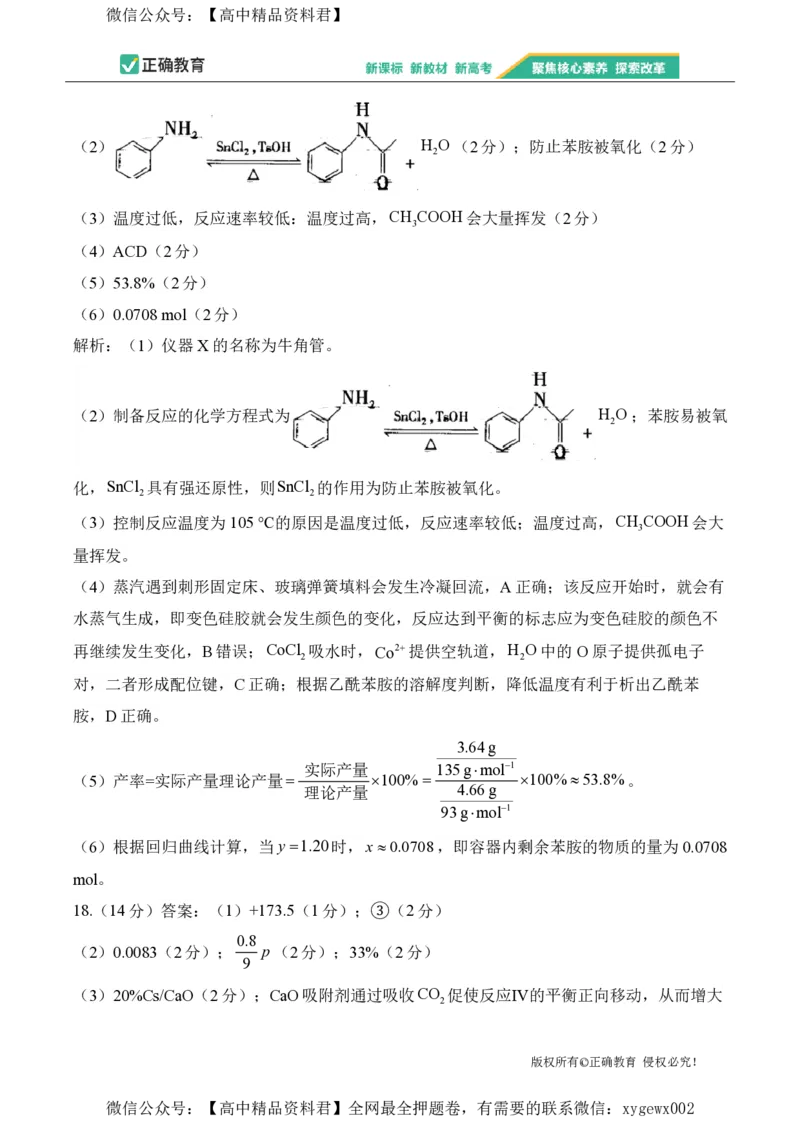
6.乙酰辅酶A羧化酶抑制剂的开发有望为肿瘤治疗开辟新的路径,其合成中间体的结构如
图。
下列说法错误的是( )
A.该有机物在五元环上的一氯代物有三种
B.该有机物分子中C原子和N原子的杂化方式相同
C.该分子中含有1个手性碳原子
D.一定条件下1 mol该有机物最多能与4 mol NaOH发生反应
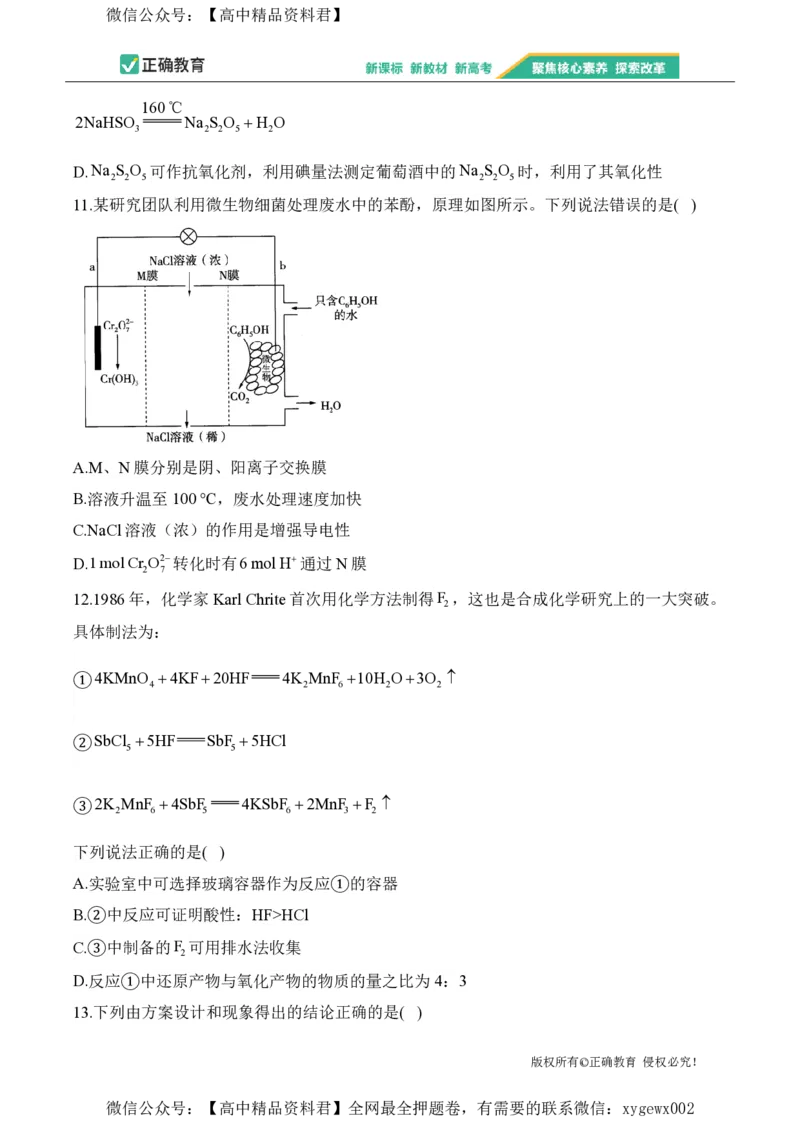
7.目前的新能源汽车多采用三元锂电池,某三元锂电池的工作原理如图所示。下列说法错误
的是( )
A.连接K 、K 时,N端电势高于M端电势
2 3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
B.连接K、K 时,N极的电极反应式为LiNi Co Mn O xe Li Ni Co Mn O xLi
1 2 a b c 2 1x a b c 2
C.放电时,电子流向:M极→用电器→N极→电解质溶液→M极
D.当外电路通过0.1 mol电子时,通过隔膜的Li的质量为 0.7 g
8.香豆素是一种重要的香料,常用作定香剂、脱臭剂,其合成原理如下:
下列说法错误的是( )
A.有机物M存在顺反异构体
B.1 mol香豆素最多可与5molH 加成
2
C.上述涉及物质中,有4种能与NaOH溶液反应
D.水杨醛的芳香族酯类同分异构体能发生银镜反应
9.W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X、Y与Z分别位于同一周期
且相邻,这4种元素位于3个主族,W与Z的最外层电子数之和等于X与Y的最外层电子数
之和,W、X、Z的单质在常温下均为气态。下列说法正确的是( )
A.第一电离能:X>W>Y
B.简单气态氢化物沸点:W>X
C.X与Z形成的一种化合物可作为自来水的消毒剂
D.W、Y、Z的最高价氧化物对应的水化物中,W的酸性最强
10.工业上以锅炉烟气(SO 、NH 、N 、CO 等)与纯碱为原料制备亚硫酸氢钠(NaHSO )
2 3 2 2 3
与焦亚硫酸钠(Na S O )的主要流程如图示。下列说法错误的是( )
2 2 5
A.SO 使品红溶液褪色,溶液受热后可复原,使高锰酸钾溶液褪色,加热该溶液不可复原
2
B.NH 与水分子间可以形成氢键而极易溶于水,实验室制备NH 不能用CaCl 干燥
3 3 2
C.产品 1、2分别为NaHSO、Na S O ,160 ℃脱水的化学方程式为
3 2 2 5
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
160℃
2NaHSO Na S O H O
3 2 2 5 2
D.Na S O 可作抗氧化剂,利用碘量法测定葡萄酒中的Na S O 时,利用了其氧化性
2 2 5 2 2 5
11.某研究团队利用微生物细菌处理废水中的苯酚,原理如图所示。下列说法错误的是( )
A.M、N膜分别是阴、阳离子交换膜
B.溶液升温至100 ℃,废水处理速度加快
C.NaCl溶液(浓)的作用是增强导电性
D.1molCr O2转化时有6molH通过N膜
2 7
12.1986年,化学家Karl Chrite首次用化学方法制得F ,这也是合成化学研究上的一大突破。
2
具体制法为:
①4KMnO 4KF20HF 4K MnF 10H O3O
4 2 6 2 2
②SbCl 5HF SbF 5HCl
5 5
③2K MnF 4SbF 4KSbF 2MnF F
2 6 5 6 3 2
下列说法正确的是( )
A.实验室中可选择玻璃容器作为反应①的容器
B.②中反应可证明酸性:HF>HCl
C.③中制备的F 可用排水法收集
2
D.反应①中还原产物与氧化产物的物质的量之比为 4:3
13.下列由方案设计和现象得出的结论正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
方案设计 现象 结论
将浓硫酸和CaF 在铅皿中混合
2
A 有白雾出现 挥发性:H SO HF
2 4
并加热
向浑浊鸡蛋清中滴加稀 NaCl 氯化钠不能使蛋白质发生
B 液体变澄清
溶液 盐析
先有沉淀生成,
C 向硫酸铜溶液中滴加足量氨水 NH H O是强碱
3 2
后沉淀溶解
该浓度的NaHCO 溶液中
既有白色沉淀生
3
向某浓度的NaHCO 溶液中加 成,又能产生使 存在程度较大的自耦电
3
D
入少量CaCl 溶液 澄清石灰水变浑 离:
2
浊的气体 2HCO CO2 H CO
3 3 2 3
A.A B.B C.C D.D
14.Cu、In与S形成的一种化合物晶体是半导体材料,其四方晶系的晶胞如图(b2a),晶
胞棱边夹角均为90°。设阿伏加德罗常数的值为N ,下列说法正确的是( )
A
A.晶胞中2和3位置的Cu与1位置的In距离相等
B.S处于两个Cu和两个In原子围成的正四面体的中心
C.该化合物的化学式为CuInS
4
42431021
D.该晶体的密度为 gcm3
a2bN
A
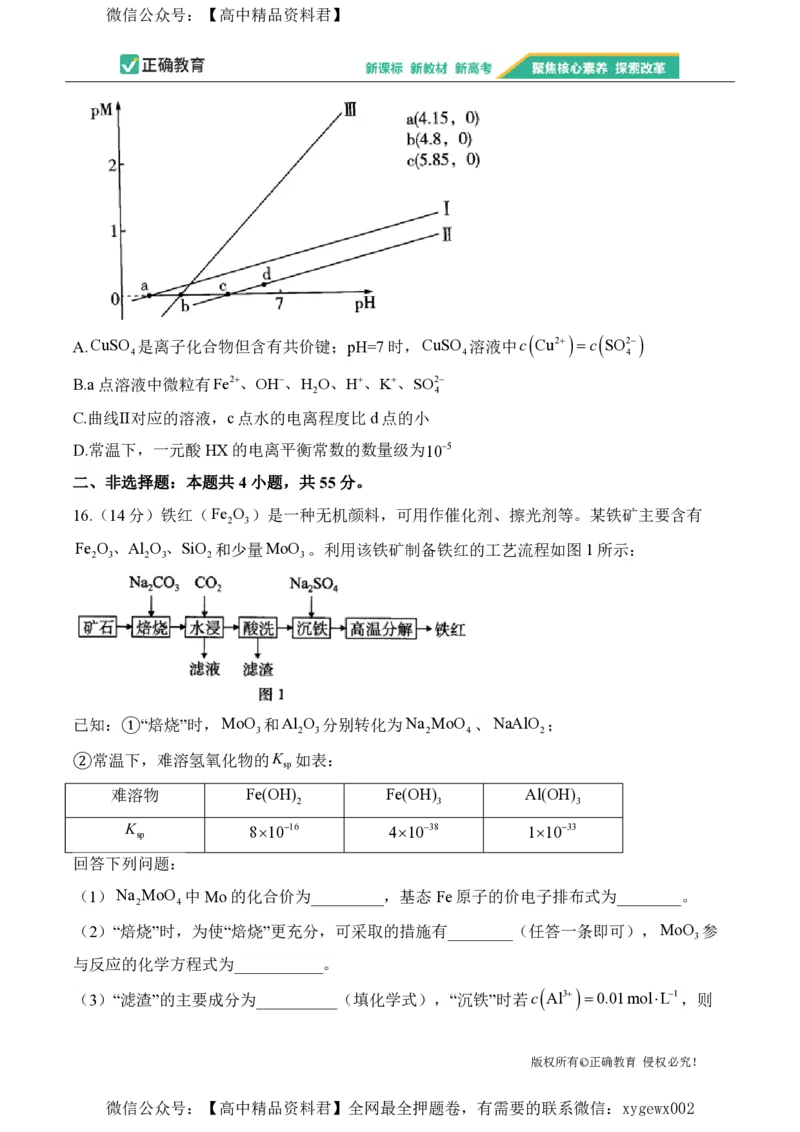
15.常温下,分别向一元酸HX溶液、CuSO 溶液、FeSO 溶液中滴加KOH溶液,pM随pH
4 4
c(HX)
的变化关系如图所示。已知:pM表示lg
c
X
或lgc Cu2 或lgc Fe2 ,K
sp
Cu(OH)
2
1019.7,K Fe(OH) 1016.3。下列说法正确的是( )
sp 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.CuSO 是离子化合物但含有共价键;pH=7时,CuSO 溶液中c
Cu2
c
SO2
4 4 4
B.a点溶液中微粒有Fe2、OH、H O、H、K、SO2
2 4
C.曲线Ⅱ对应的溶液,c点水的电离程度比d点的小
D.常温下,一元酸HX的电离平衡常数的数量级为105
二、非选择题:本题共 4 小题,共 55 分。
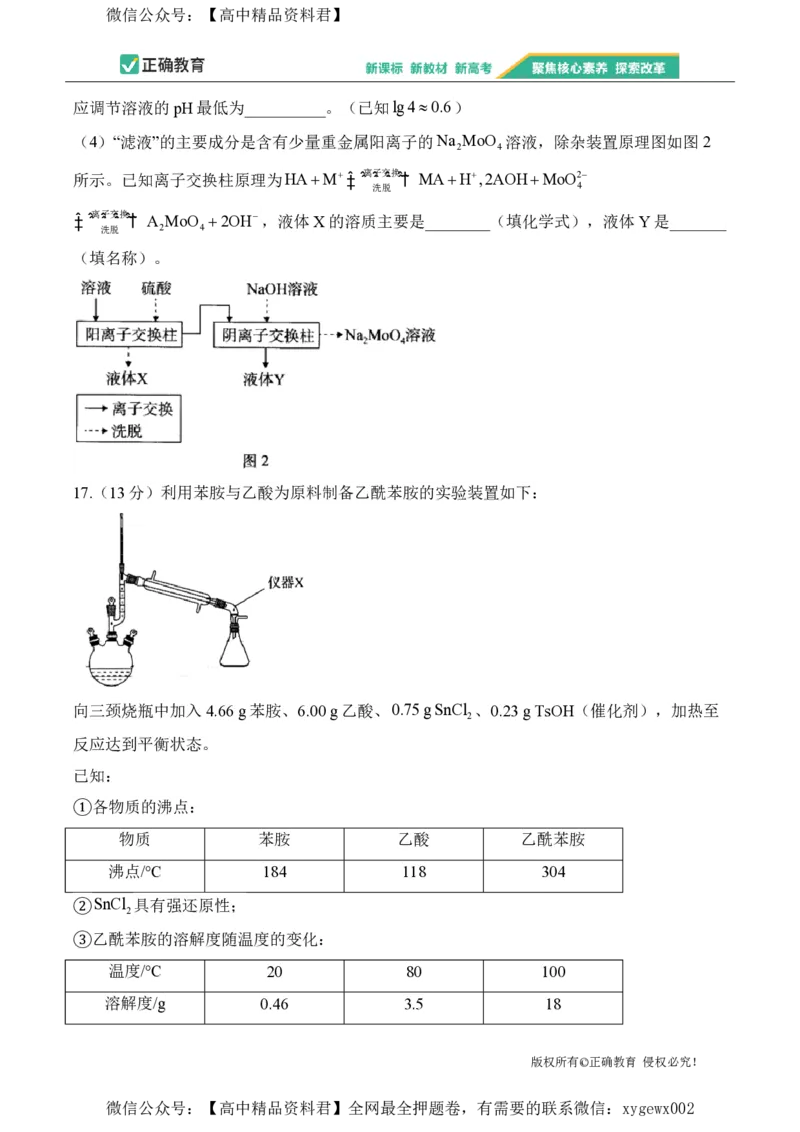
16.(14分)铁红(Fe O )是一种无机颜料,可用作催化剂、擦光剂等。某铁矿主要含有
2 3
Fe O、Al O、SiO 和少量MoO 。利用该铁矿制备铁红的工艺流程如图1所示:
2 3 2 3 2 3
已知:①“焙烧”时,MoO 和Al O 分别转化为Na MoO 、NaAlO ;
3 2 3 2 4 2
②常温下,难溶氢氧化物的K 如表:
sp
难溶物 Fe(OH) Fe(OH) Al(OH)
2 3 3
K 81016 41038 11033
sp
回答下列问题:
(1)Na MoO 中Mo的化合价为_________,基态 Fe原子的价电子排布式为________。
2 4
(2)“焙烧”时,为使“焙烧”更充分,可采取的措施有________(任答一条即可),MoO 参
3
与反应的化学方程式为___________。
(3)“滤渣”的主要成分为__________(填化学式),“沉铁”时若c Al3 0.01molL1,则
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
应调节溶液的pH最低为__________。(已知lg40.6)
(4)“滤液”的主要成分是含有少量重金属阳离子的Na MoO 溶液,除杂装置原理图如图2
2 4
所示。已知离子交换柱原理为HAM‡ˆ ˆˆ 离子ˆˆ 交ˆˆ 换ˆˆ†ˆ MAH,2AOHMoO2
洗脱 4
‡ˆ ˆˆ 离子ˆˆ 交ˆˆ 换ˆˆ†ˆ A MoO 2OH,液体X的溶质主要是________(填化学式),液体Y是_______
洗脱 2 4
(填名称)。
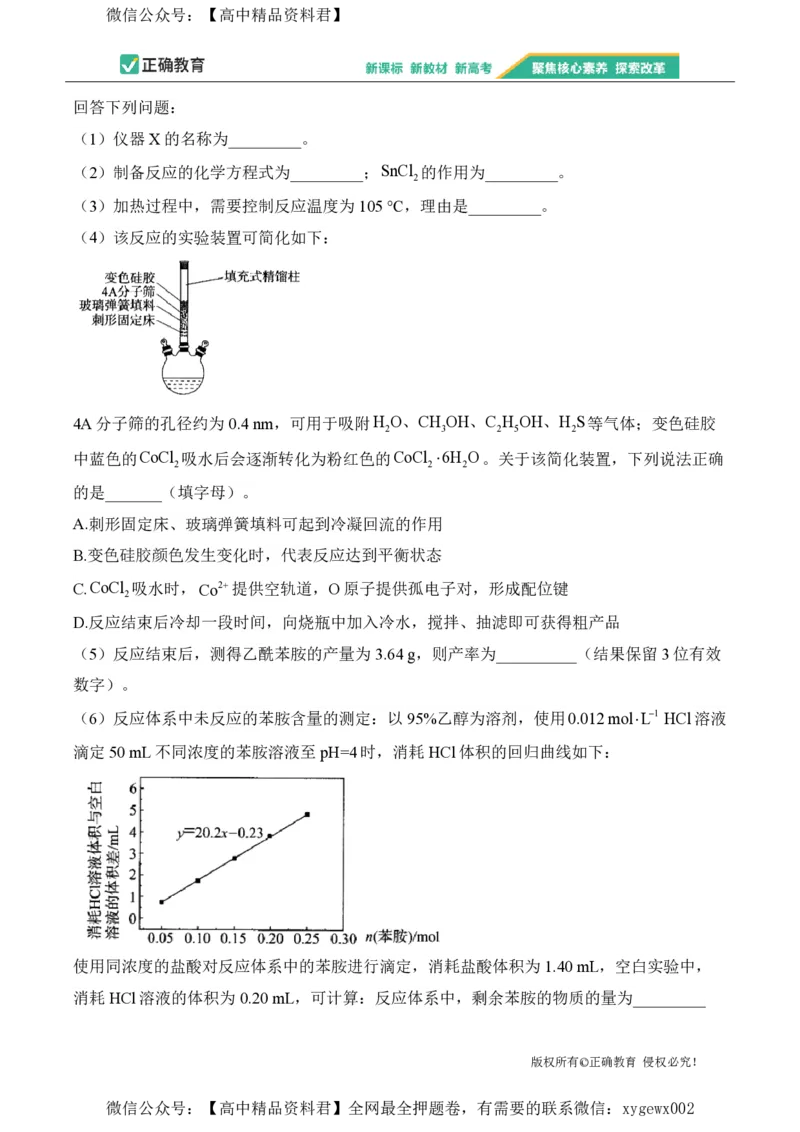
17.(13分)利用苯胺与乙酸为原料制备乙酰苯胺的实验装置如下:
向三颈烧瓶中加入4.66 g苯胺、6.00 g乙酸、0.75gSnCl 、0.23 g TsOH(催化剂),加热至
2
反应达到平衡状态。
已知:
①各物质的沸点:
物质 苯胺 乙酸 乙酰苯胺
沸点/℃ 184 118 304
②SnCl 具有强还原性;
2
③乙酰苯胺的溶解度随温度的变化:
温度/℃ 20 80 100
溶解度/g 0.46 3.5 18
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
回答下列问题:
(1)仪器X的名称为_________。
(2)制备反应的化学方程式为_________;SnCl 的作用为_________。
2
(3)加热过程中,需要控制反应温度为105 ℃,理由是_________。
(4)该反应的实验装置可简化如下:
4A分子筛的孔径约为0.4 nm,可用于吸附H O、CH OH、C H OH、H S等气体;变色硅胶
2 3 2 5 2
中蓝色的CoCl 吸水后会逐渐转化为粉红色的CoCl 6H O。关于该简化装置,下列说法正确
2 2 2
的是_______(填字母)。
A.刺形固定床、玻璃弹簧填料可起到冷凝回流的作用
B.变色硅胶颜色发生变化时,代表反应达到平衡状态
C.CoCl 吸水时,Co2提供空轨道,O原子提供孤电子对,形成配位键
2
D.反应结束后冷却一段时间,向烧瓶中加入冷水,搅拌、抽滤即可获得粗产品
(5)反应结束后,测得乙酰苯胺的产量为3.64 g,则产率为__________(结果保留3位有效
数字)。
(6)反应体系中未反应的苯胺含量的测定:以95%乙醇为溶剂,使用0.012molL1 HCl溶液
滴定50 mL不同浓度的苯胺溶液至pH=4时,消耗HCl体积的回归曲线如下:
使用同浓度的盐酸对反应体系中的苯胺进行滴定,消耗盐酸体积为1.40 mL,空白实验中,
消耗HCl溶液的体积为0.20 mL,可计算:反应体系中,剩余苯胺的物质的量为_________
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(结果保留3位有效数字)。
18.(14分)乙醇水蒸气重整制H 的热化学方程式为
2
C H OH(g)3H O(g) 2CO (g)6H (g) H ,其化学过程可以表述为一系列基元反应,
2 5 2 2 2
结合反应间联系进一步整理可以得到如下的四个主反应:
反应Ⅰ:C H OH(g) C H O(g)H (g) H 68.9kJmol1
2 5 2 4 2 1
反应Ⅱ:C H O(g) CH (g)CO(g) H 19.1kJmol1
2 4 4 2
反应Ⅲ:CH (g)H O(g)‡ˆ ˆˆ†ˆ CO(g)3H (g) H 206.1kJmol1
4 2 2 3
反应Ⅳ:CO(g)H O(g)‡ˆ ˆˆ†ˆ CO (g)H (g) H 41.2kJmol1
2 2 2 4
(1)根据题干,H ____________kJmol1,平衡时CO的选择性随温度的变化应是图1
n (CO)
中曲线_____________(填序号)[已知:CO的选择性 生成 100%]
n CO n (CO)
生成 2 生成
(2)为研究上述反应体系中的平衡关系,向某恒温恒容反应容器中按n
nC H OH:nH O1:8投料,初始压强为 pkPa。充分反应后,将混合气体干燥处理,测
2 5 2
得H 占混合气体(干燥后)总体积的50%,CO 占10%,则反应Ⅲ的平衡常数K
2 2 x
x3H x(CO)
__________[K 为用摩尔分数表示的平衡常数,K 2 ,x表示该物质占气体
x x xCH xH O
4 2
的物质的量分数],到达平衡时体系中CO的分压为_________kPa,H 的产率为
2
____________(保留2位有效数字)。
(3)一定温度下,加入吸附剂可以改变氢气产率。图2为几种改性CO吸附剂增重量随时间
变化曲线,其中提高氢气产率最大的吸附剂为___________________,原因是
________________________。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
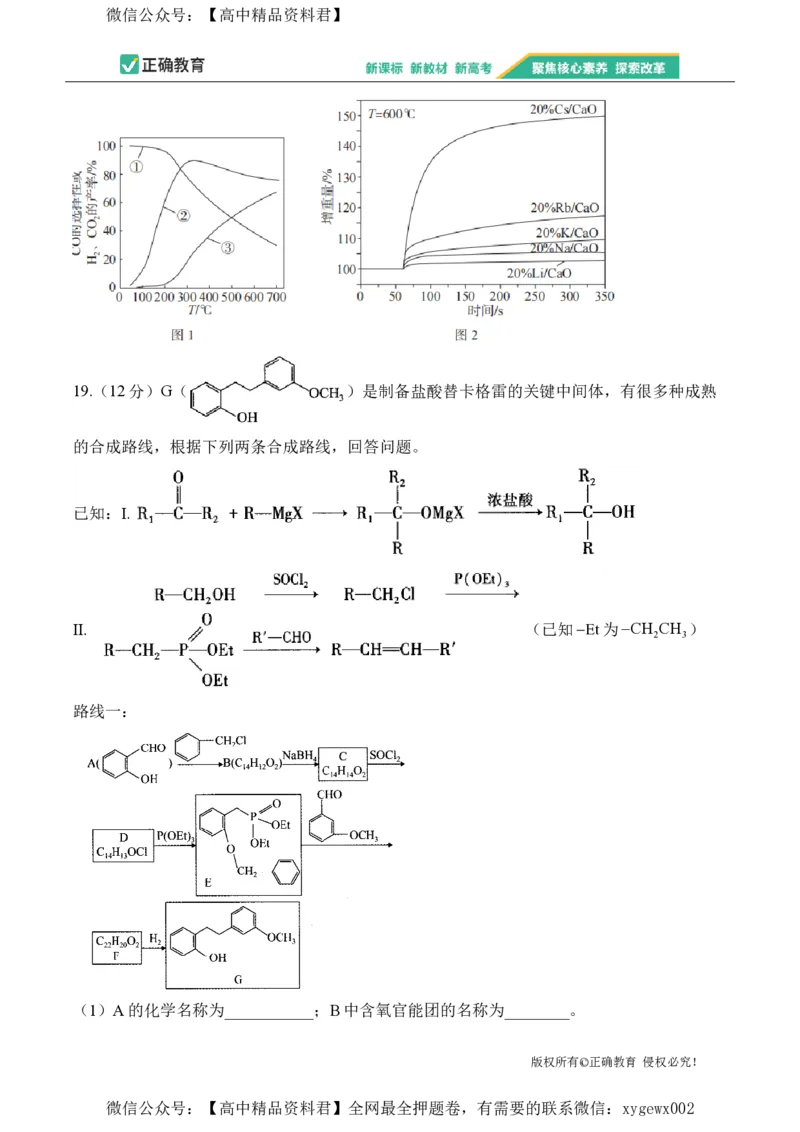
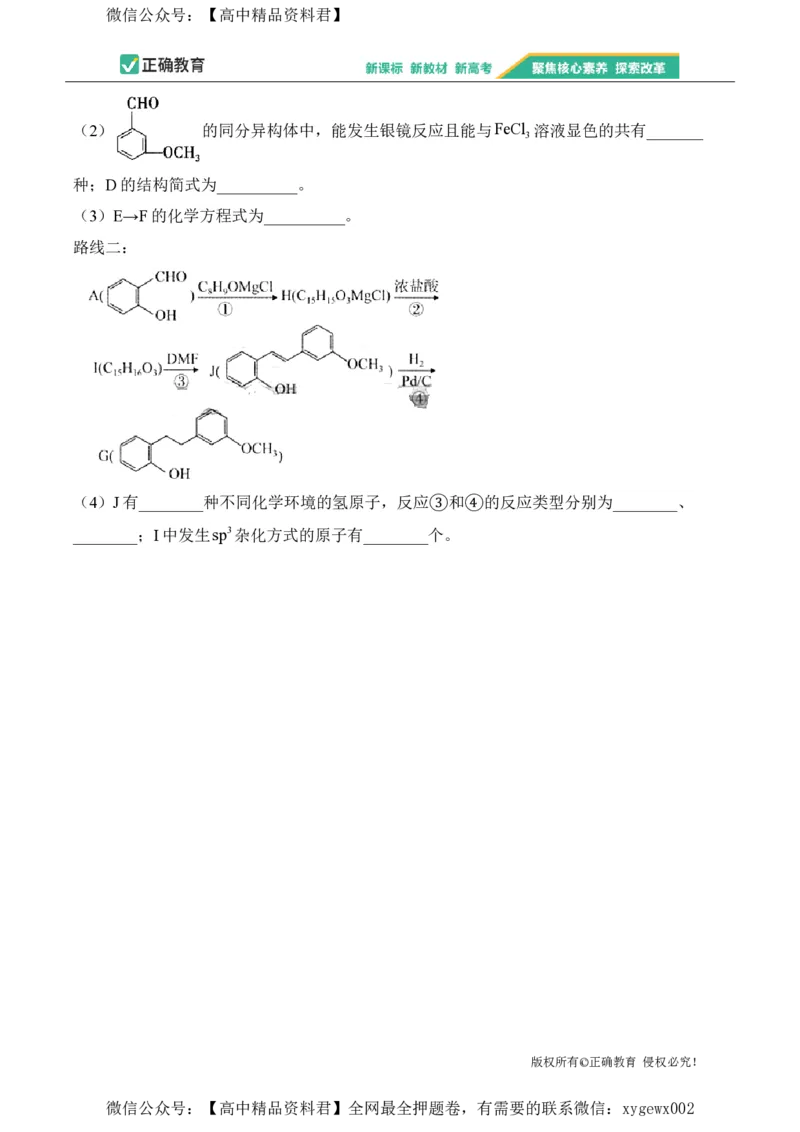
19.(12分)G( )是制备盐酸替卡格雷的关键中间体,有很多种成熟
的合成路线,根据下列两条合成路线,回答问题。
已知:Ⅰ.
Ⅱ. (已知Et为CH CH )
2 3
路线一:
(1)A的化学名称为___________;B中含氧官能团的名称为________。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2) 的同分异构体中,能发生银镜反应且能与FeCl 溶液显色的共有_______
3
种;D的结构简式为__________。
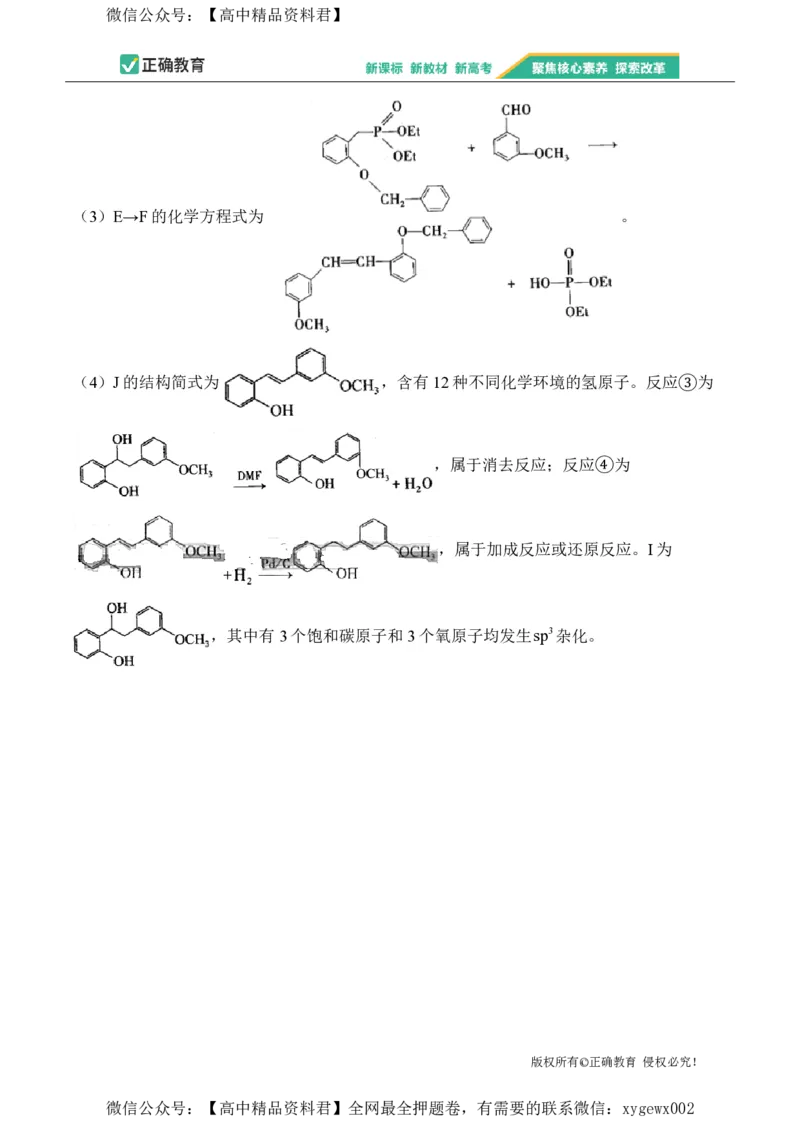
(3)E→F的化学方程式为__________。
路线二:
(4)J有________种不同化学环境的氢原子,反应③和④的反应类型分别为________、
________;I中发生sp3杂化方式的原子有________个。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:D
解析:木雕的主要成分为纤维素,A错误;制造指南针的磁性物质是Fe O ,B错误;利用
3 4
14C可以测定年代,C错误;谷物在酿酒过程中,淀粉水解生成葡萄糖,葡萄糖在酒化酶的作
6
用下发生氧化还原反应C H O 酒化酶2C H OH2CO ,D正确。
6 12 6 2 5 2
2.答案:D
解析:H 分子中s—sσ键与 HCl分子中s—pσ键的电子云图形都是轴对称的,A正确;NH
2 3
513
中N的孤电子对数为 1,σ键电子对数为3,价层电子对数为4,故VSEPR模型为
2
四面体形,B正确;MgCl 的形成过程为Mg原子失去电子,形成Mg2,氯原子得到电子,
2
形成Cl, Mg2与Cl通过离子键结合形成MgCl ,C正确;用化学方程式表示己二酸催化
2
剂与丁二醇制备聚酯类合成树脂:nHOOCCH COOHnHOCH CH CH CH OH ‡ˆ ˆˆ 催化ˆˆ 剂ˆˆ†ˆ
2 4 2 2 2 2 △
(2n1)H O,D错误。
2
3.答案:C
解析:漂白粉与浓盐酸在不加热的条件下可用于制备少量Cl ,A正确;浓磷酸的沸点高于
2
HBr的,可利用难挥发性酸制备易挥发性酸的原理制备 HBr,B正确;实验室制备SO 时,
2
如果选择98%的浓硫酸[提示:98%的浓硫酸中H SO 主要以分子形式存在],会因氢离子浓度
2 4
过小导致反应速率过慢,故实验室通常选用70%的浓硫酸,C错误;Cu浓硝酸可在常温下反
应制备NO ,D正确。
2
4.答案:C
解析:植物油不溶于水,在碱性条件加热会发生水解反应且液体互溶;汽油不溶于水,与
NaOH溶液混合后分层,且汽油在上层;甘油易溶于水,与 NaOH不反应现象不同,可鉴
别,A正确。乙醇燃烧产生淡蓝色火焰,苯燃烧火焰明亮并伴有黑烟,四氯化碳不能燃烧,
现象不同,能鉴别,B正确。NaCl和KNO 溶液均呈中性,无法鉴别二者,C错误。各取少
3
量固体粉末,加入过量浓盐酸,无气体产生,溶液呈绿色的为CuO[提示:生成的CuCl 溶液
2
呈绿色];加热产生刺激性气味的气体,溶液呈棕黄色,无沉淀生成的为MnO [点拨:
2
△
MnO 4HCl(浓) MnCl Cl 2H O];产生无色气体的为Fe粉,现象各不相同,可
2 2 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
以鉴别,D正确。
5.答案:C
解析:没有说明氯气所处的状态,不能计算出Cl 中含有的Cl原子数目,A错误;HClO属于
2
弱电解质,不能完全电离,B错误;根据反应原理,可以得出每消耗1molCl ,反应转移N
2 A
个电子,C正确;没有给出具体的溶液体积,溶液中H个数难以得出,D错误。
6.答案:B
解析:
7.答案:C
解析:第一步:原理分析。连接K 、K 时,装置为原电池,M极为负极,N极为正极;连接
2 3
K、K 时,装置为电解池,M极为阴极,N极为阳极。放电时总反应为
1 3
Li Ni Co Mn O Li C LiNi Co Mn O 6C(石墨),逆过程是充电时的总反应。第
1x a b c 2 x 6 a b c 2
二步:各电极反应式判断。装置为原电池时,正极反应式为
Li Ni Co Mn O xLi xe LiNi Co Mn O (逆过程为充电时的阳极反应式),负极
1x a b c 2 a b c 2
反应式为Li C xe xLi 6C(逆过程为充电时的阴极反应式)。第三步:逐项分析判
x 6
断。连接K 、K ,装置为原电池,M极为负极,N极为正极,正极(N极)电势高于负极
2 3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(M极)电势,A正确;由上述分析知,B正确;电子不能通过电解质溶液,电解质溶液中
离子的定向移动形成电流,C错误;当外电路通过0.1 mol电子时,通过隔膜的Li的物质的
量为0.1 mol,其质量为0.1mol7gmol1 0.7g,D正确。
8.答案:B
解析:有机物存在顺反异构体一般满足的条件为含有碳碳双键、双键所连碳原子上均连两个
不同的原子或基团。有机物M分子中含有碳碳双键,且碳碳双键两端的碳原子上各连 2个不
同的原子或基团,故M存在顺反异构体,A项不符合题意;酯基中的碳氧双键不能与H 加
2
成,1 mol香豆素最多可与4molH 加成,B项符合题意;除乙酸钠和水外,另外4种物质均
2
能与NaOH溶液反应,C项不符合题意;水杨醛的芳香族酯类同分异构体是甲酸苯酯,能发
生银镜反应,D项不符合题意。
9.答案:C
解析:第一电离能:N>O>S,A错误;常温下,H O是液态,NH 是气态,H O的沸点高于
2 3 2
NH 的,B错误;HNO、H SO 和HClO 均为强酸,HClO 的酸性最强,D错误。
3 3 2 4 4 4
10.答案:D
解析:二氧化硫使高锰酸钾溶液褪色是因为发生氧化还原反应而褪色,颜色不可复原,SO
2
使品红溶液褪色是因为生成不稳定的无色物质,加热后溶液由无色变为红色,A正确;氨与
水分子间可以形成氢键,极易溶于水,氨气会和氯化钙反应生成CaCl 8NH ,不能用氯化钙
2 3
干燥,B正确;由图解可知,C正确;Na S O 中硫元素化合价为+4,类比SO 中硫元素的价
2 2 5 2
态可知其具有还原性,可作抗氧化剂,碘量法测定Na S O 时利用其还原性,离子方程式为
2 2 5
S O2 2I 3H O 2SO2 4I 6H,D错误。
2 5 2 2 4
11.答案:B
解析:M、N膜分别是阴、阳离子交换膜,A正确;溶液升温至 100 ℃,会使微生物蛋白质
变性,微生物失活,废水处理速度减慢,B错误;NaCl溶液(浓)的作用是增强导电性,C
正确;根据电路中通过的电荷量处处相等知,1molCr O2转化时有6mole转移,则有
2 7
6molH自右向左通过N膜,D正确。
12.答案:D
解析:玻璃容器的主要成分为SiO ,HF能和SiO 反应,所以不能选择玻璃容器作为反应①
2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
的容器,A错误;HF为弱酸、HCl为强酸,B错误;F 和H O反应生成HF和O ,所以F 不
2 2 2 2
能采用排水法收集,C错误;反应①中KMnO 既是氧化剂又是还原剂,根据还原产物
4
(K MnF )和氧化产物(O )的计量数之比可得,还原产物与氧化产物的物质的量之比为
2 6 2
4:3,D正确。
13.答案:D
解析:可利用高沸点难挥发的硫酸制备低沸点的HF,化学方程式为
加热
CaF H SO 浓 CaSO 2HF,A错误;稀NaCl溶液能促进蛋白质的溶解,但浓
2 2 4 4
NaCl溶液可使蛋白质发生盐析,B错误;硫酸铜与氨水反应先生成Cu(OH) 沉淀,后沉淀溶
2
解生成配合物CuNH 2 ,不能说明NH H O是强碱,C错误;由现象可知,该浓度
3 4 3 2
NaHCO 溶液中存在不少CO2和H CO ,说明该浓度的NaHCO 溶液中存在程度较大的自耦
3 3 2 3 3
电离:2HCO CO2 H CO ,D正确。
3 3 2 3
14.答案:D
解析:因b2a,故晶胞中2和3位置的Cu与1位置的In距离不相等,A错误;b2a,S
处于两个Cu和两个In原子围成的四面体的中心,但不是正四面体的中心,B错误;根据均
1 1
摊法,每个晶胞中Cu的个数是 8(顶角) 4(面上)+1(体心)=4,In的个数是
8 2
1 1
4(棱上) 6(面上)=4,S的个数是8(体内),故该化合物的化学式为CuInS ,
4 2 2
C错误;该晶体的密度为
V
m
(
(
晶
晶
胞
胞
)
)
a10
4
7
2
2
b
4
3
107N
gcm3 4
a
24
2b
3
N
1021 gcm3,D正
A A
确。
15.答案:D
解析:CuSO 中既有离子键又有共价键,共价键来自硫酸根离子;pH=7时,CuSO 溶液中
4 4
存在电荷守恒2c
Cu2
c
K
c
H
2c
SO2
c
OH
,又c
H
c
OH
,则可知
4
2c
Cu2
c
K
2c
SO2
,A错误。a点溶液的pH=4.l5,
4
pM 0,c OH 109.85 molL1,c2 OH 1019.7 mol2L2,则曲线Ⅰ表示lgc Cu2 与pH
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
c(HX)
的关系,同理可得曲线Ⅱ表示lgc Fe2 与pH的关系,曲线Ⅲ表示lg
c
X
与pH的关系,
B错误。FeSO 水解溶液显酸性,促进水的电离,随着KOH的加入,对水的电离的促进程度
4
减小,故c点水的电离程度比 d点的大,C错误。根据 b点坐标(4.8,0)来算,
c(HX) c H c X
lg
c
X 0,则c(HX)c X ,K
a
c(HX)
c H 104.8,K
a
的数量级为105,
D正确。
16.(13分)答案:(1)+6(1分);3d64s2(1分)
(2)将原料粉碎(或少量多次添加Na CO ,答案合理焙烧即可);(1分)
2 3
焙烧
MoO Na CO Na MoO CO (2分)
3 2 3 2 4 2
(3)H SiO (2分);3.2(2分)
2 3
(4)Na SO (2分);水(2分)
2 4
解析:(1)Na MoO 中Na为+1价,O为-2价,由化合物中各元素正、负化合价代数和为
2 4
0,可推知Mo的化合价为+6。Fe为26号元素,基态 Fe原子的价电子排布式为3d64s2。
(2)为使“焙烧”更充分,可将原料粉碎,也可以少量多次添加Na CO 等;“焙烧”时,
2 3
焙烧
MoO 转化为Na MoO ,该反应的化学方程式为MoO Na CO Na MoO CO 。
3 2 4 3 2 3 2 4 2
(3)由流程分析可知,“滤渣”的主要成分为H SiO 。Fe3完全沉淀时,溶液中
2 3
c OH 3 41038 molL1,则pOHlg 3 41011 11 1 lg410.8,所以pH3.2,此
105 3
时c Al3 0.01molL1,则c Al3 c3 OH 41035 K Al(OH) ,说明Fe3沉淀完全
sp 3
时,Al3尚未开始沉淀,则“沉铁”时溶液的pH最低为3.2。
(4)由题图2可知,Na MoO 与硫酸发生阳离子交换得到硫酸钠和H MoO ,H MoO 与氢
2 4 2 4 2 4
氧化钠发生阴离子交换得到Na MoO 和水,则液体X的溶质主要是Na SO ,液体Y是水。
2 4 2 4
17.(13分)答案:(1)牛角管(1分)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2) H O(2分);防止苯胺被氧化(2分)
2
(3)温度过低,反应速率较低:温度过高,CH COOH会大量挥发(2分)
3
(4)ACD(2分)
(5)53.8%(2分)
(6)0.0708 mol(2分)
解析:(1)仪器X的名称为牛角管。
(2)制备反应的化学方程式为 H O;苯胺易被氧
2
化,SnCl 具有强还原性,则SnCl 的作用为防止苯胺被氧化。
2 2
(3)控制反应温度为105 ℃的原因是温度过低,反应速率较低;温度过高,CH COOH会大
3
量挥发。
(4)蒸汽遇到刺形固定床、玻璃弹簧填料会发生冷凝回流,A正确;该反应开始时,就会有
水蒸气生成,即变色硅胶就会发生颜色的变化,反应达到平衡的标志应为变色硅胶的颜色不
再继续发生变化,B错误;CoCl 吸水时,Co2提供空轨道,H O中的O原子提供孤电子
2 2
对,二者形成配位键,C正确;根据乙酰苯胺的溶解度判断,降低温度有利于析出乙酰苯
胺,D正确。
3.64g
实际产量 135gmol1
(5)产率=实际产量理论产量 100% 100%53.8%。
理论产量 4.66g
93gmol1
(6)根据回归曲线计算,当y 1.20时,x0.0708,即容器内剩余苯胺的物质的量为0.0708
mol。
18.(14分)答案:(1)+173.5(1分);③(2分)
0.8
(2)0.0083(2分); p(2分);33%(2分)
9
(3)20%Cs/CaO(2分);CaO吸附剂通过吸收CO 促使反应Ⅳ的平衡正向移动,从而增大
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
氢气的产率,20%Cs/CaO增重量最大,吸收CO 最多,提高氢气产率的效果最好(合理即
2
可)(3分)
解析:(1)根据盖斯定律可知,ΔH ΔH ΔH ΔH 2ΔH 173.5kJmol1。反应Ⅲ的
1 2 3 4
ΔH 0,温度升高,平衡正向移动,反应Ⅳ的ΔH 0,温度升高,平衡逆向移动,故温度
3 4
升高,反应Ⅲ、Ⅳ的平衡移动均会使 CO的选择性增大,虽然温度升高,反应Ⅱ平衡逆向移
动,会使CO选择性减小,但是反应Ⅱ热效应较小,所以总的来说,升温时 CO选择性增大,
所以题图1中曲线③代表CO的选择性随温度的变化。
(2)根据题目信息,反应Ⅰ、Ⅱ能进行到底,反应Ⅲ、Ⅳ为可逆反应,设投料时
nC H OHamol,则nH O8a mol,反应Ⅲ生成氢气3xmol,反应Ⅳ生成氢气
2 5 2
y mol,根据反应Ⅲ、Ⅳ列出“三段式”:
CH (g)H O(g)‡ˆ ˆˆ†ˆ CO(g)3H (g)
4 2 2
起始量/mol a 8a a a
转化量/mol x x x 3x
平衡量/mol ax 8ax ax a3x
CO(g)H O(g)‡ˆ ˆˆ†ˆ CO (g)H (g)
2 2 2
起始量/mol ax 8ax 0 a3x
转化量/mol y y y y
平衡量/mol ax y 8ax y y a3x y
充分反应后,H 占混合气体(除水干燥后)总体积的50%,CO 占10%,混合气体(除水干
2 2
燥后)的总物质的量n(3a3x y)mol,可得关系式:
(a3x y)mol y mol
100%50%, 100%10%,解得x0.2a,y 0.4a,所以
(3a3x y)mol (3a3x y)mol
平衡时nH O7.4a mol,nH 2a mol,nCO
2 2 2
0.4a mol,n(CO)0.8a mol,nCH 0.8a mol,平衡时体系内气体总物质的量为11.4a mol,
4
7.4 2
各组分的物质的量分数分别为xH O ,xH ,
2 11.4 2 11.4
0.4 0.8 0.8
xCO ,x(CO) ,xCH ,则反应Ⅲ的平衡常数
2 11.4 11.4 4 11.4
x3H x(CO)
K 2 0.0083。根据反应前后体系总物质的量的变化,可以得出反应后体系
x xCH xH O
4 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
11.4 0.8
总压强为 pkPa,则平衡时CO的分压为 p kPa。氢气的理论产量为6amol,实际产
9 9
量为2amol,故H 的产率约为33%。
2
(3)CaO吸附剂通过吸收CO 促使反应Ⅳ的平衡正向移动,从而增大氢气的产率,由题图2
2
可知,20%Cs/CaO增重量最大,吸收CO 最多,提高氢气产率的效果最好。
2
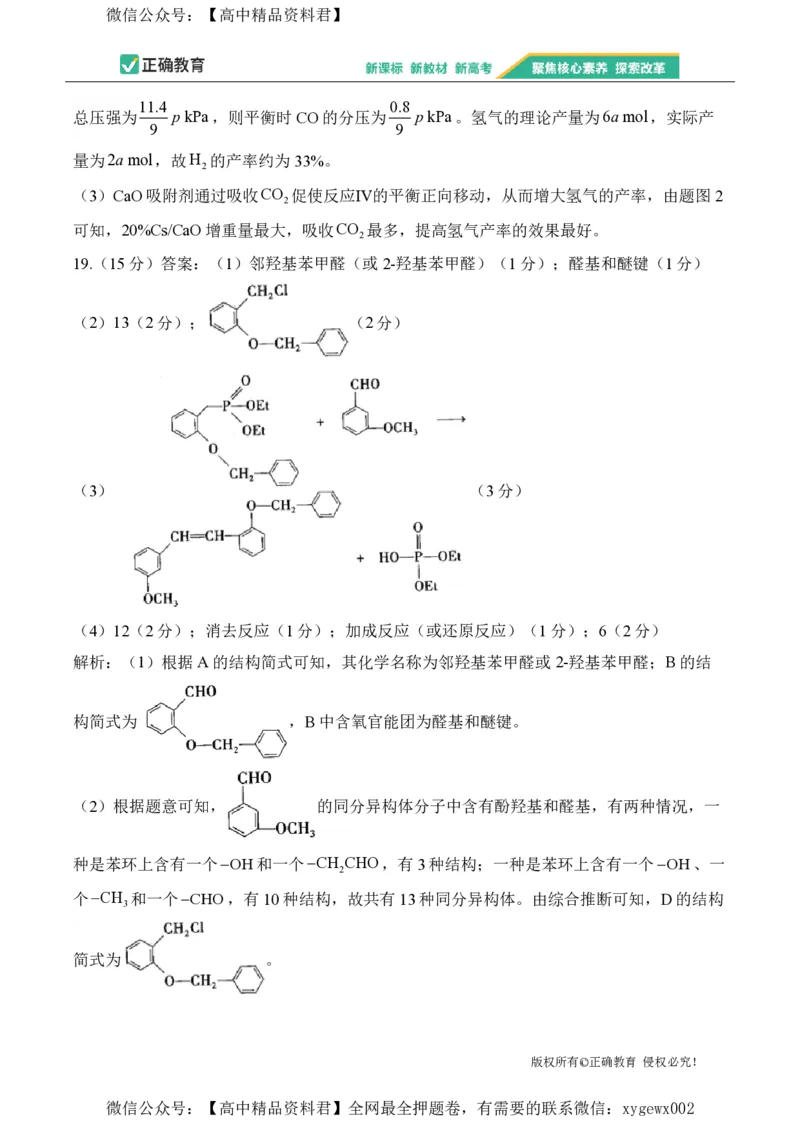
19.(15分)答案:(1)邻羟基苯甲醛(或2-羟基苯甲醛)(1分);醛基和醚键(1分)
(2)13(2分); (2分)
(3) (3分)
(4)12(2分);消去反应(1分);加成反应(或还原反应)(1分);6(2分)
解析:(1)根据A的结构简式可知,其化学名称为邻羟基苯甲醛或 2-羟基苯甲醛;B的结
构简式为 ,B中含氧官能团为醛基和醚键。
(2)根据题意可知, 的同分异构体分子中含有酚羟基和醛基,有两种情况,一
种是苯环上含有一个OH和一个CH CHO,有3种结构;一种是苯环上含有一个OH、一
2
个CH 和一个CHO,有10种结构,故共有13种同分异构体。由综合推断可知,D的结构
3
简式为 。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(3)E→F的化学方程式为 。
(4)J的结构简式为 ,含有 12种不同化学环境的氢原子。反应③为
,属于消去反应;反应④为
,属于加成反应或还原反应。I为
,其中有3个饱和碳原子和3个氧原子均发生sp3杂化。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002