文档内容
连城一中2025-2026学年暑期月考
高三化学试卷
考试时间:75分钟 满分:100分
原子量:H-1 C-12 N-14 O-16 Na-23 K-39 Cl-35.5
一、选择题(共14小题,每题只有一个选项符合要求,每小题3分,共42分)
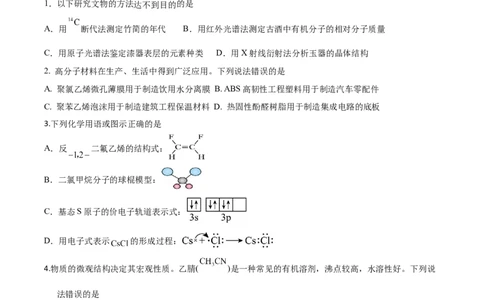
1.以下研究文物的方法达不到目的的是
A.用 断代法测定竹简的年代 B.用红外光谱法测定古酒中有机分子的相对分子质量
C.用原子光谱法鉴定漆器表层的元素种类 D.用X射线衍射法分析玉器的晶体结构
2. 高分子材料在生产、生活中得到广泛应用。下列说法错误的是
A. 聚氯乙烯微孔薄膜用于制造饮用水分离膜 B. ABS高韧性工程塑料用于制造汽车零配件
C. 聚苯乙烯泡沫用于制造建筑工程保温材料 D. 热固性酚醛树脂用于制造集成电路的底板
3.下列化学用语或图示正确的是
A.反 二氟乙烯的结构式:
B.二氯甲烷分子的球棍模型:
C.基态S原子的价电子轨道表示式:
D.用电子式表示 的形成过程:
4.物质的微观结构决定其宏观性质。乙腈( )是一种常见的有机溶剂,沸点较高,水溶性好。下列说
法错误的是
A.乙腈的电子式: B.乙腈可发生加成反应
C.乙腈的沸点高于与其分子量相近的丙炔 D.乙腈分子中所有原子均在同一平面
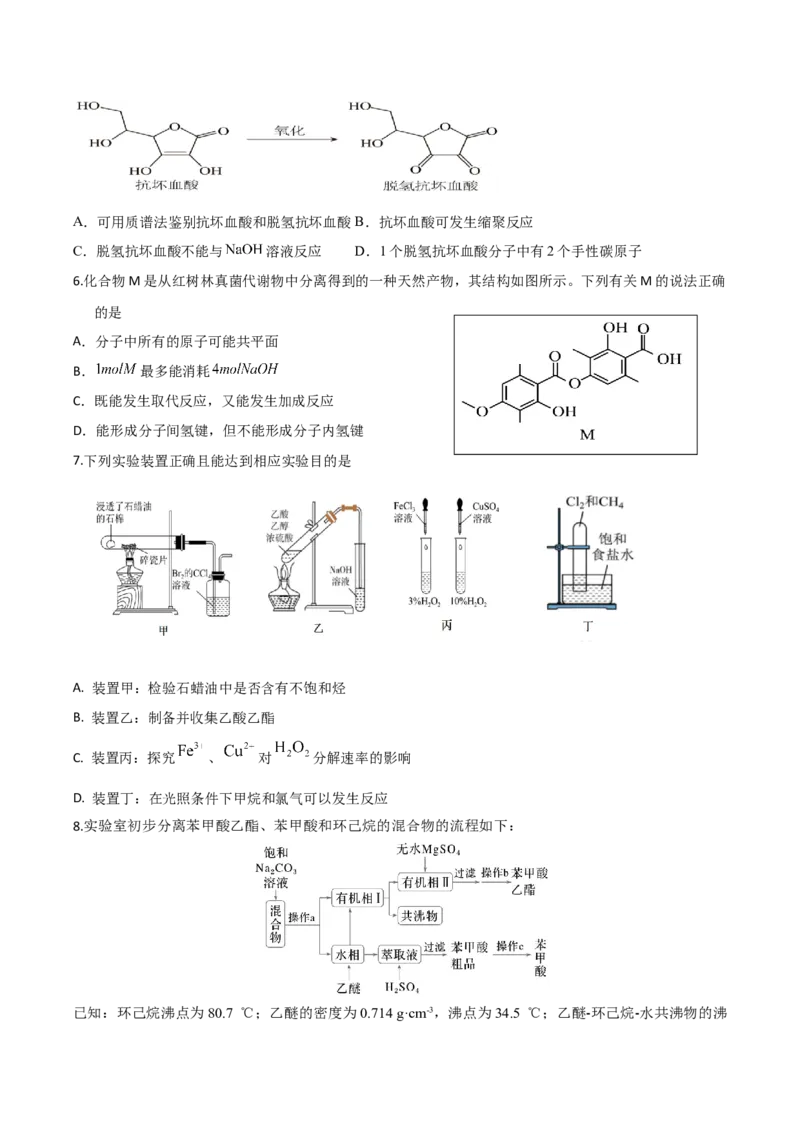
5.抗坏血酸(维生素C)是常用的抗氧化剂。下列说法错误的是A.可用质谱法鉴别抗坏血酸和脱氢抗坏血酸B.抗坏血酸可发生缩聚反应
C.脱氢抗坏血酸不能与 溶液反应 D.1个脱氢抗坏血酸分子中有2个手性碳原子
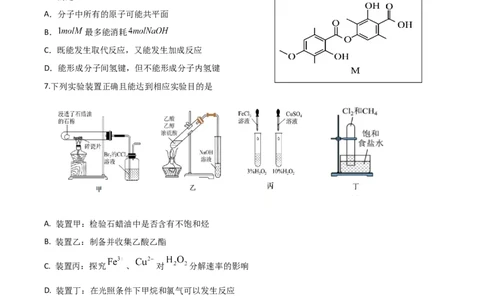
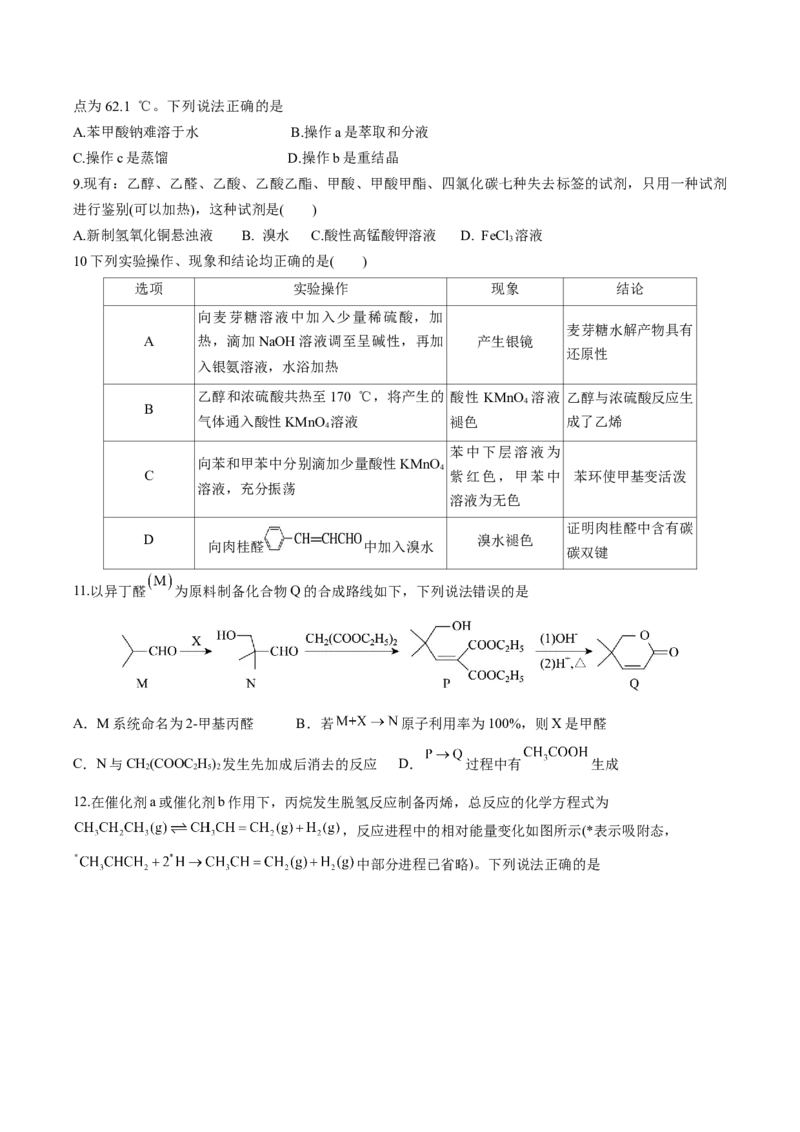
6.化合物M是从红树林真菌代谢物中分离得到的一种天然产物,其结构如图所示。下列有关M的说法正确
的是
A.分子中所有的原子可能共平面
B. 最多能消耗
C.既能发生取代反应,又能发生加成反应
D.能形成分子间氢键,但不能形成分子内氢键
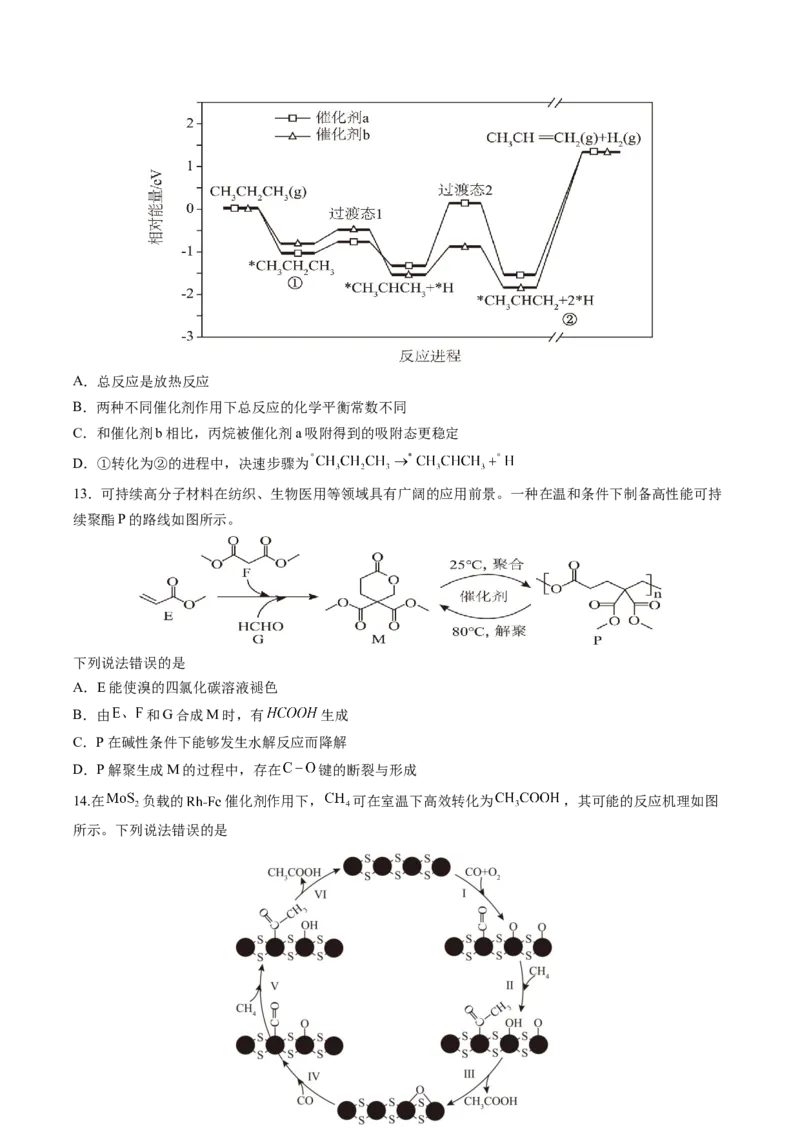
7.下列实验装置正确且能达到相应实验目的是
A. 装置甲:检验石蜡油中是否含有不饱和烃
B. 装置乙:制备并收集乙酸乙酯
C. 装置丙:探究 、 对 分解速率的影响
D. 装置丁:在光照条件下甲烷和氯气可以发生反应
8.实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的混合物的流程如下:
已知:环己烷沸点为80.7 ℃;乙醚的密度为0.714 g·cm-3,沸点为34.5 ℃;乙醚
⁃
环己烷
⁃
水共沸物的沸点为62.1 ℃。下列说法正确的是
A.苯甲酸钠难溶于水 B.操作a是萃取和分液
C.操作c是蒸馏 D.操作b是重结晶
9.现有:乙醇、乙醛、乙酸、乙酸乙酯、甲酸、甲酸甲酯、四氯化碳七种失去标签的试剂,只用一种试剂
进行鉴别(可以加热),这种试剂是( )
A.新制氢氧化铜悬浊液 B. 溴水 C.酸性高锰酸钾溶液 D. FeCl 溶液
3
10下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
向麦芽糖溶液中加入少量稀硫酸,加
麦芽糖水解产物具有
A 热,滴加NaOH溶液调至呈碱性,再加 产生银镜
还原性
入银氨溶液,水浴加热
乙醇和浓硫酸共热至170 ℃,将产生的 酸性 KMnO 溶液 乙醇与浓硫酸反应生
4
B
气体通入酸性KMnO 溶液 褪色 成了乙烯
4
苯中下层溶液为
向苯和甲苯中分别滴加少量酸性KMnO
4
C 紫红色,甲苯中 苯环使甲基变活泼
溶液,充分振荡
溶液为无色
证明肉桂醛中含有碳
D 溴水褪色
向肉桂醛 中加入溴水
碳双键
11.以异丁醛 为原料制备化合物Q的合成路线如下,下列说法错误的是
A.M系统命名为2-甲基丙醛 B.若 原子利用率为100%,则X是甲醛
C.N与CH(COOC H) 发生先加成后消去的反应 D. 过程中有 生成
2 2 5 2
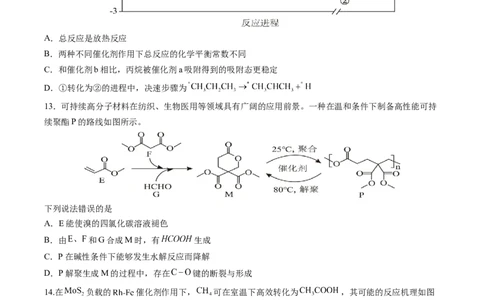
12.在催化剂a或催化剂b作用下,丙烷发生脱氢反应制备丙烯,总反应的化学方程式为
,反应进程中的相对能量变化如图所示(*表示吸附态,
中部分进程已省略)。下列说法正确的是A.总反应是放热反应
B.两种不同催化剂作用下总反应的化学平衡常数不同
C.和催化剂b相比,丙烷被催化剂a吸附得到的吸附态更稳定
D.①转化为②的进程中,决速步骤为
13.可持续高分子材料在纺织、生物医用等领域具有广阔的应用前景。一种在温和条件下制备高性能可持
续聚酯P的路线如图所示。
下列说法错误的是
A.E能使溴的四氯化碳溶液褪色
B.由 和G合成M时,有 生成
C.P在碱性条件下能够发生水解反应而降解
D.P解聚生成M的过程中,存在 键的断裂与形成
14.在 负载的 催化剂作用下, 可在室温下高效转化为 ,其可能的反应机理如图
所示。下列说法错误的是A.该反应的原子利用率为 B.若以 为原料,用 吸收产物可得到
C.反应过程中, 和 的化合价均发生变化 D.每消耗 可生成
二、非选择题(共4大题。共58分)
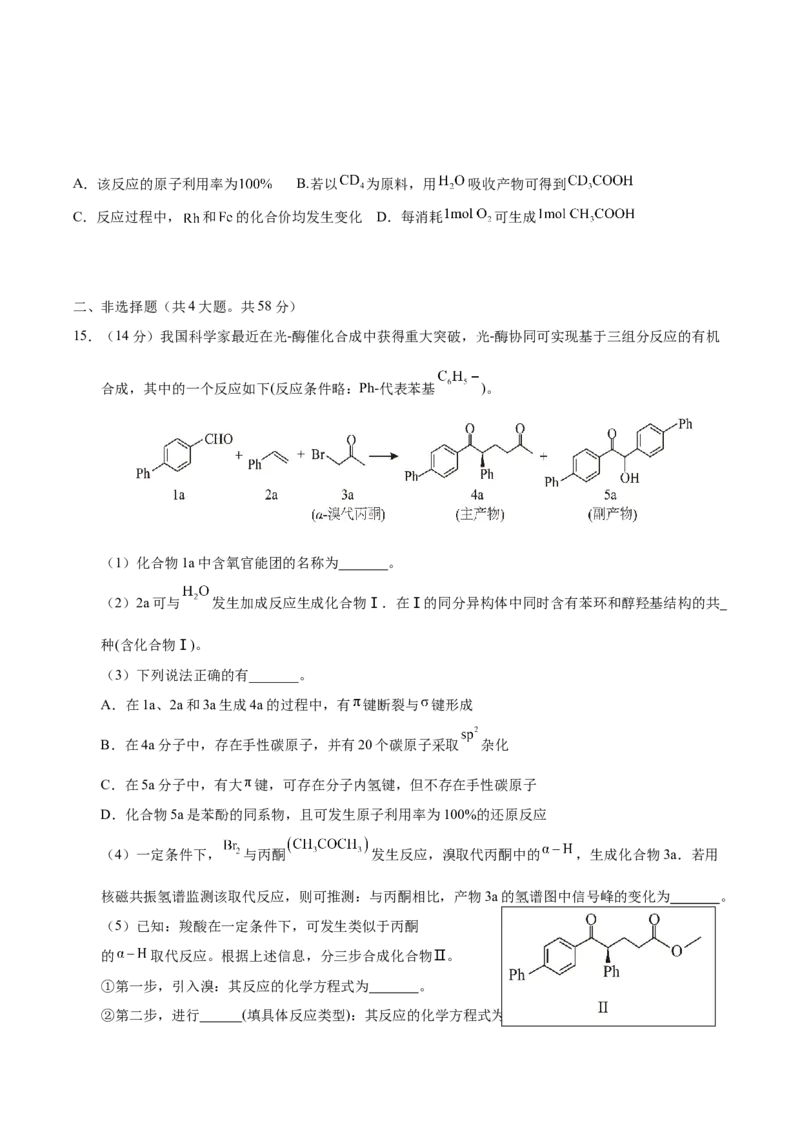
15.(14分)我国科学家最近在光-酶催化合成中获得重大突破,光-酶协同可实现基于三组分反应的有机
合成,其中的一个反应如下(反应条件略:Ph-代表苯基 )。
(1)化合物1a中含氧官能团的名称为 。
(2)2a可与 发生加成反应生成化合物Ⅰ.在Ⅰ的同分异构体中同时含有苯环和醇羟基结构的共
种(含化合物Ⅰ)。
(3)下列说法正确的有_______。
A.在1a、2a和3a生成4a的过程中,有 键断裂与 键形成
B.在4a分子中,存在手性碳原子,并有20个碳原子采取 杂化
C.在5a分子中,有大 键,可存在分子内氢键,但不存在手性碳原子
D.化合物5a是苯酚的同系物,且可发生原子利用率为100%的还原反应
(4)一定条件下, 与丙酮 发生反应,溴取代丙酮中的 ,生成化合物3a.若用
核磁共振氢谱监测该取代反应,则可推测:与丙酮相比,产物3a的氢谱图中信号峰的变化为 。
(5)已知:羧酸在一定条件下,可发生类似于丙酮
的 取代反应。根据上述信息,分三步合成化合物Ⅱ。
①第一步,引入溴:其反应的化学方程式为 。
②第二步,进行 (填具体反应类型):其反应的化学方程式为 (注明反应条件)。③第三步,合成Ⅱ:②中得到的含溴有机物与1a、2a反应。
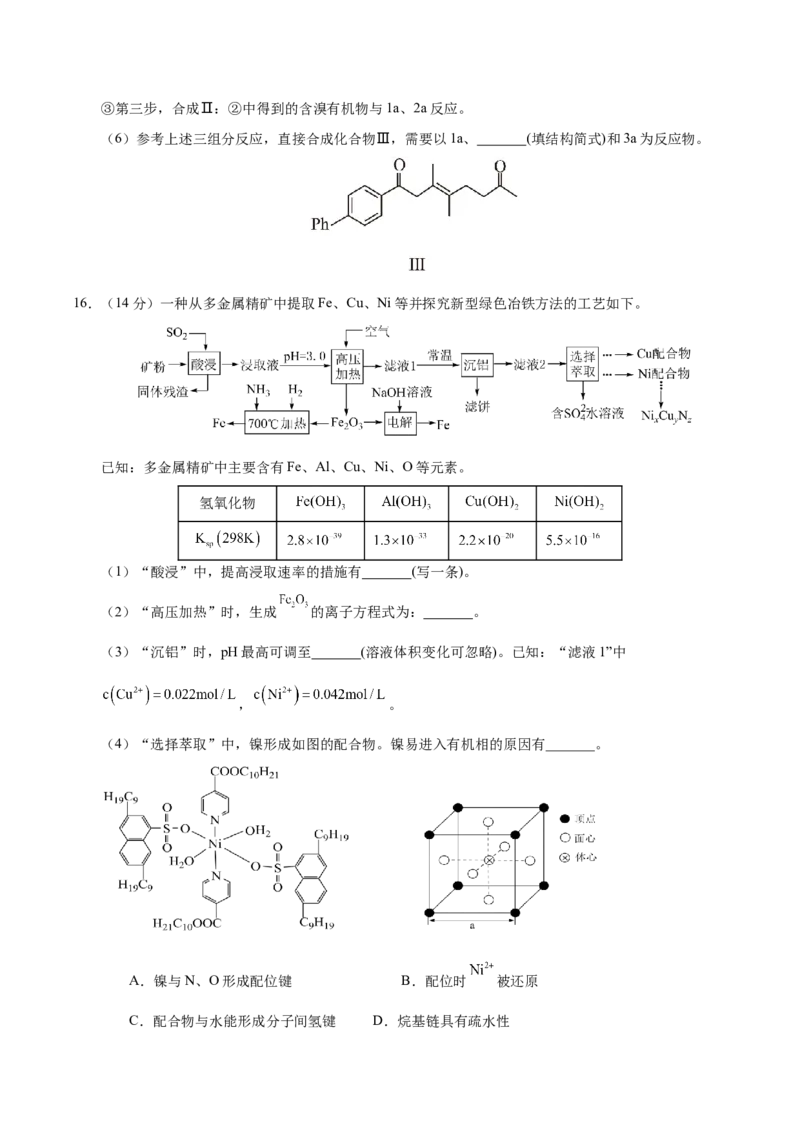
(6)参考上述三组分反应,直接合成化合物Ⅲ,需要以1a、 (填结构简式)和3a为反应物。
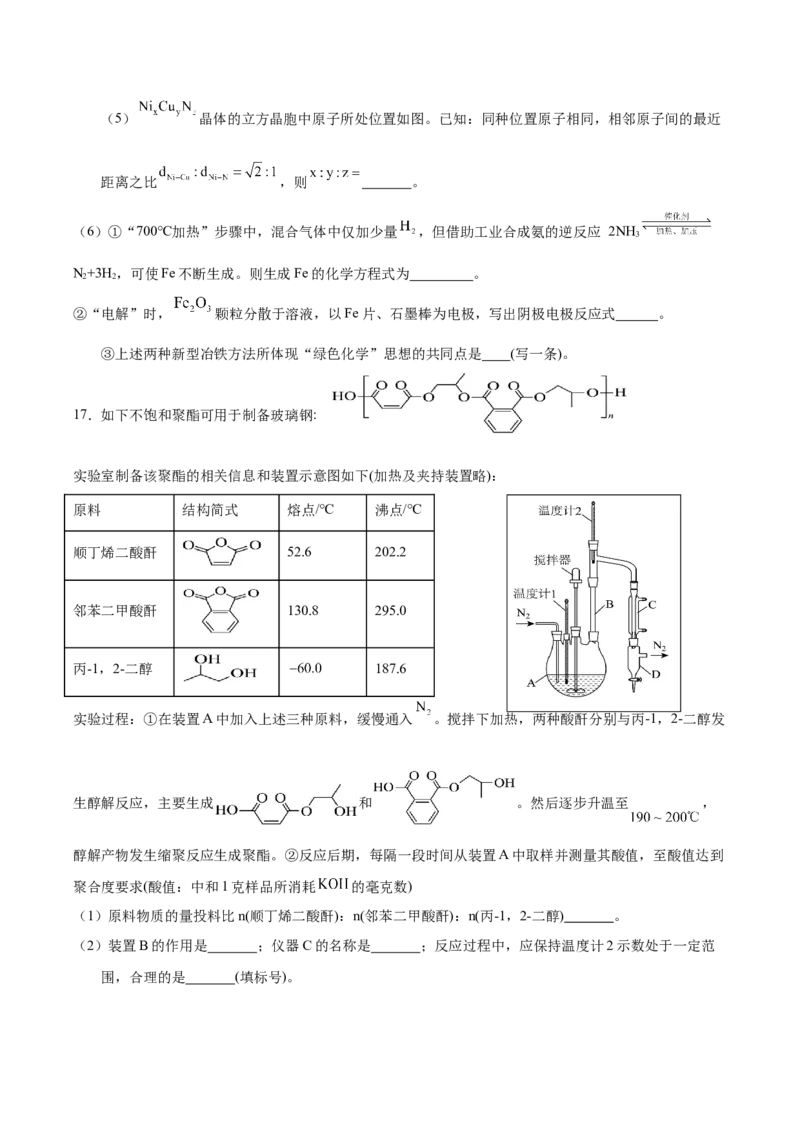
16.(14分)一种从多金属精矿中提取Fe、Cu、Ni等并探究新型绿色冶铁方法的工艺如下。
已知:多金属精矿中主要含有Fe、Al、Cu、Ni、O等元素。
氢氧化物
(1)“酸浸”中,提高浸取速率的措施有 (写一条)。
(2)“高压加热”时,生成 的离子方程式为: 。
(3)“沉铝”时,pH最高可调至 (溶液体积变化可忽略)。已知:“滤液1”中
, 。
(4)“选择萃取”中,镍形成如图的配合物。镍易进入有机相的原因有_______。
A.镍与N、O形成配位键 B.配位时 被还原
C.配合物与水能形成分子间氢键 D.烷基链具有疏水性(5) 晶体的立方晶胞中原子所处位置如图。已知:同种位置原子相同,相邻原子间的最近
距离之比 ,则 。
(6)①“700℃加热”步骤中,混合气体中仅加少量 ,但借助工业合成氨的逆反应 2NH
3
N+3H ,可使Fe不断生成。则生成Fe的化学方程式为 。
2 2
②“电解”时, 颗粒分散于溶液,以Fe片、石墨棒为电极,写出阴极电极反应式 。
③上述两种新型冶铁方法所体现“绿色化学”思想的共同点是 (写一条)。
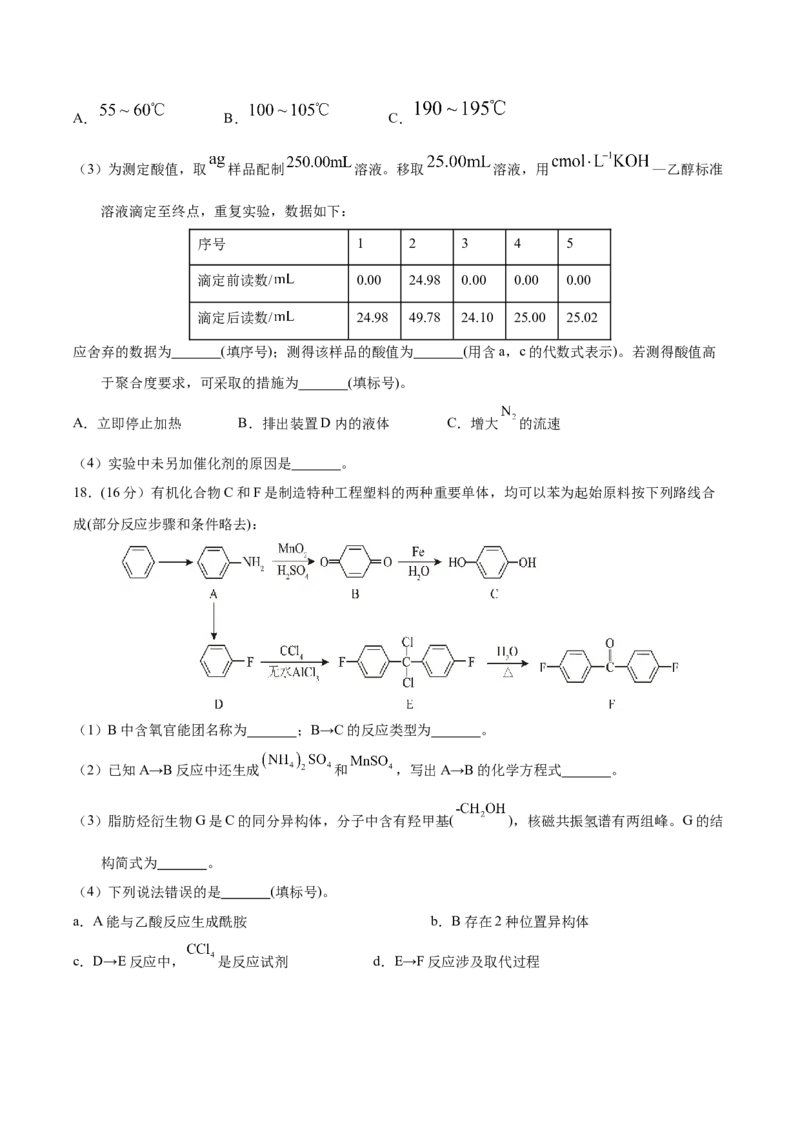
17.如下不饱和聚酯可用于制备玻璃钢:
实验室制备该聚酯的相关信息和装置示意图如下(加热及夹持装置略):
原料 结构简式 熔点/℃ 沸点/℃
顺丁烯二酸酐 52.6 202.2
邻苯二甲酸酐 130.8 295.0
丙-1,2-二醇 187.6
实验过程:①在装置A中加入上述三种原料,缓慢通入 。搅拌下加热,两种酸酐分别与丙-1,2-二醇发
生醇解反应,主要生成 和 。然后逐步升温至 ,
醇解产物发生缩聚反应生成聚酯。②反应后期,每隔一段时间从装置A中取样并测量其酸值,至酸值达到
聚合度要求(酸值:中和1克样品所消耗 的毫克数)
(1)原料物质的量投料比n(顺丁烯二酸酐):n(邻苯二甲酸酐):n(丙-1,2-二醇) 。
(2)装置B的作用是 ;仪器C的名称是 ;反应过程中,应保持温度计2示数处于一定范
围,合理的是 (填标号)。A. B. C.
(3)为测定酸值,取 样品配制 溶液。移取 溶液,用 —乙醇标准
溶液滴定至终点,重复实验,数据如下:
序号 1 2 3 4 5
滴定前读数/ 0.00 24.98 0.00 0.00 0.00
滴定后读数/ 24.98 49.78 24.10 25.00 25.02
应舍弃的数据为 (填序号);测得该样品的酸值为 (用含a,c的代数式表示)。若测得酸值高
于聚合度要求,可采取的措施为 (填标号)。
A.立即停止加热 B.排出装置D内的液体 C.增大 的流速
(4)实验中未另加催化剂的原因是 。
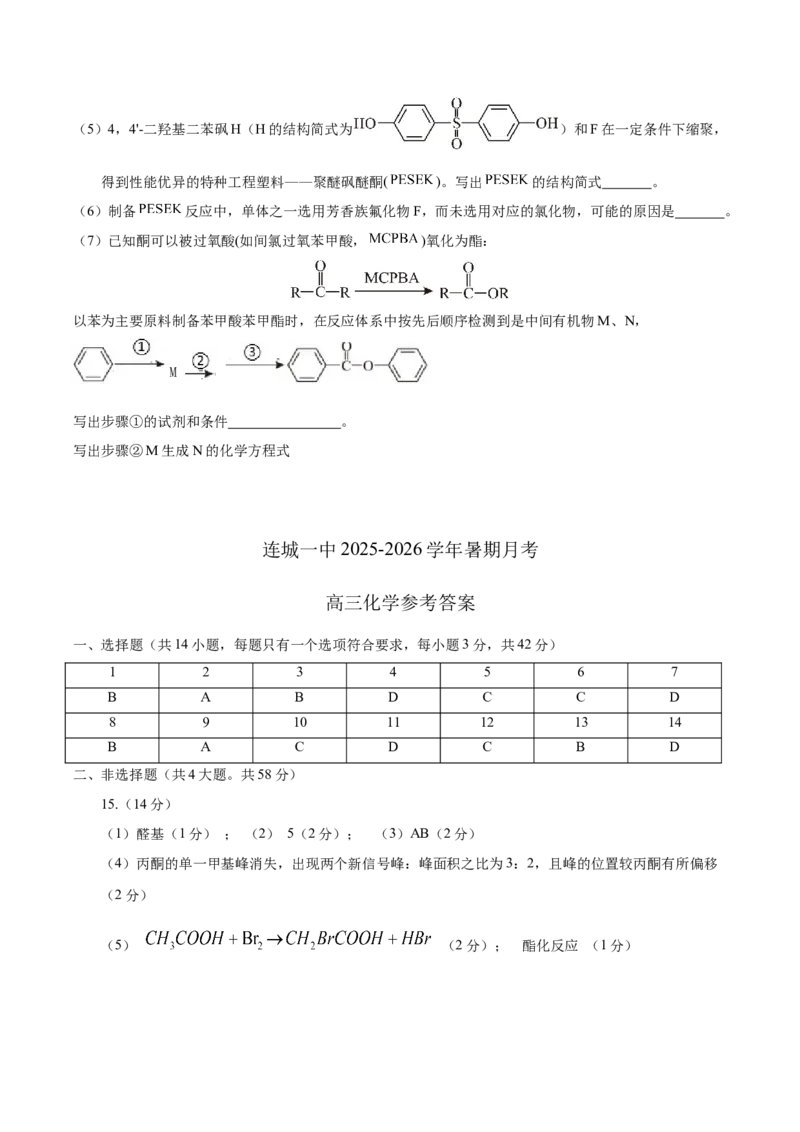
18.(16分)有机化合物C和F是制造特种工程塑料的两种重要单体,均可以苯为起始原料按下列路线合
成(部分反应步骤和条件略去):
(1)B中含氧官能团名称为 ;B→C的反应类型为 。
(2)已知A→B反应中还生成 和 ,写出A→B的化学方程式 。
(3)脂肪烃衍生物G是C的同分异构体,分子中含有羟甲基( ),核磁共振氢谱有两组峰。G的结
构简式为 。
(4)下列说法错误的是 (填标号)。
a.A能与乙酸反应生成酰胺 b.B存在2种位置异构体
c.D→E反应中, 是反应试剂 d.E→F反应涉及取代过程(5)4,4'-二羟基二苯砜H(H的结构简式为 )和F在一定条件下缩聚,
得到性能优异的特种工程塑料——聚醚砜醚酮( )。写出 的结构简式 。
(6)制备 反应中,单体之一选用芳香族氟化物F,而未选用对应的氯化物,可能的原因是 。
(7)已知酮可以被过氧酸(如间氯过氧苯甲酸, )氧化为酯:
以苯为主要原料制备苯甲酸苯甲酯时,在反应体系中按先后顺序检测到是中间有机物M、N,
M N
写出步骤①的试剂和条件 。
写出步骤②M生成N的化学方程式
连城一中2025-2026学年暑期月考
高三化学参考答案
一、选择题(共14小题,每题只有一个选项符合要求,每小题3分,共42分)
1 2 3 4 5 6 7
B A B D C C D
8 9 10 11 12 13 14
B A C D C B D
二、非选择题(共4大题。共58分)
15.(14分)
(1)醛基(1分) ; (2) 5(2分); (3)AB(2分)
(4)丙酮的单一甲基峰消失,出现两个新信号峰:峰面积之比为3:2,且峰的位置较丙酮有所偏移
(2分)
(5) (2分); 酯化反应 (1分)(2分)
(6) (2分)
16. (14分)
(1)搅拌、粉碎多金属精矿、提高酸浸温度等(1分)
(2)4Fe2++O +4H O 2Fe O↓+8H+(2分)
2 2 2 3
(3)5(2分) ; (4)AD(2分) ;(5) 3:1:1 (2分)
(6) ① Fe O+3H 2Fe+3H O (2分)
2 3 2 2
②Fe O+6e-+3H O=2Fe+6OH- (2分) ③ 没有污染物产生(1分)
2 3 2
17(14分)
(1)1:1:2(2分)
(2) 导气,同时将顺丁烯二酸酐、苯二甲酸酐、丙-1,2-二醇以及醇解反应的产物冷凝回流到装置A中,
但是不会将水蒸气冷凝 (2分);
直形冷凝管(1分) ; B(1分)
(3) 2、3(2分); (2分); C(2分)
(4)酸酐本身就能催化成酯反应(酰基化反应),且可以与水反应,促进缩聚反应正向进行(2分)
18(16分)
(1) (酮)羰基(1分) 还原反应(1分)
(2) ;(2
分)
(3) (2分)
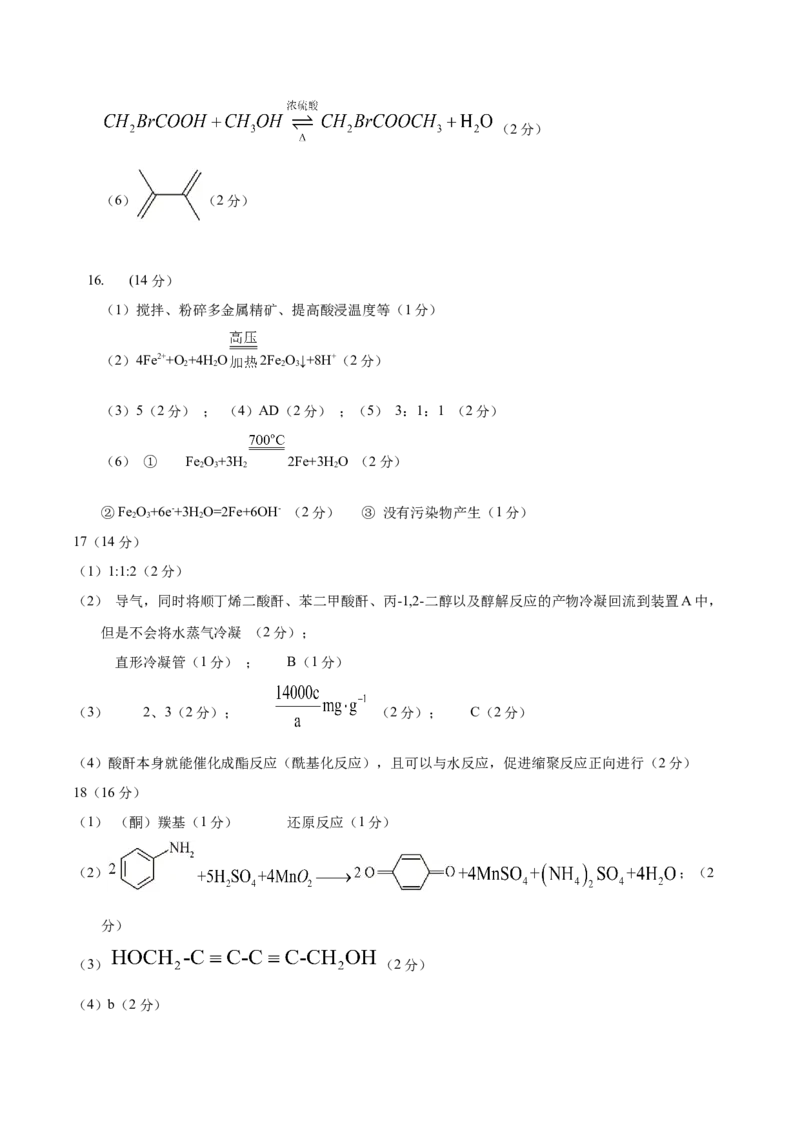
(4)b(2分)(5) (2分)
(6)电负性:F>Cl,C-F键极性更大,易断裂,容易与H发生缩聚反应
(2分)
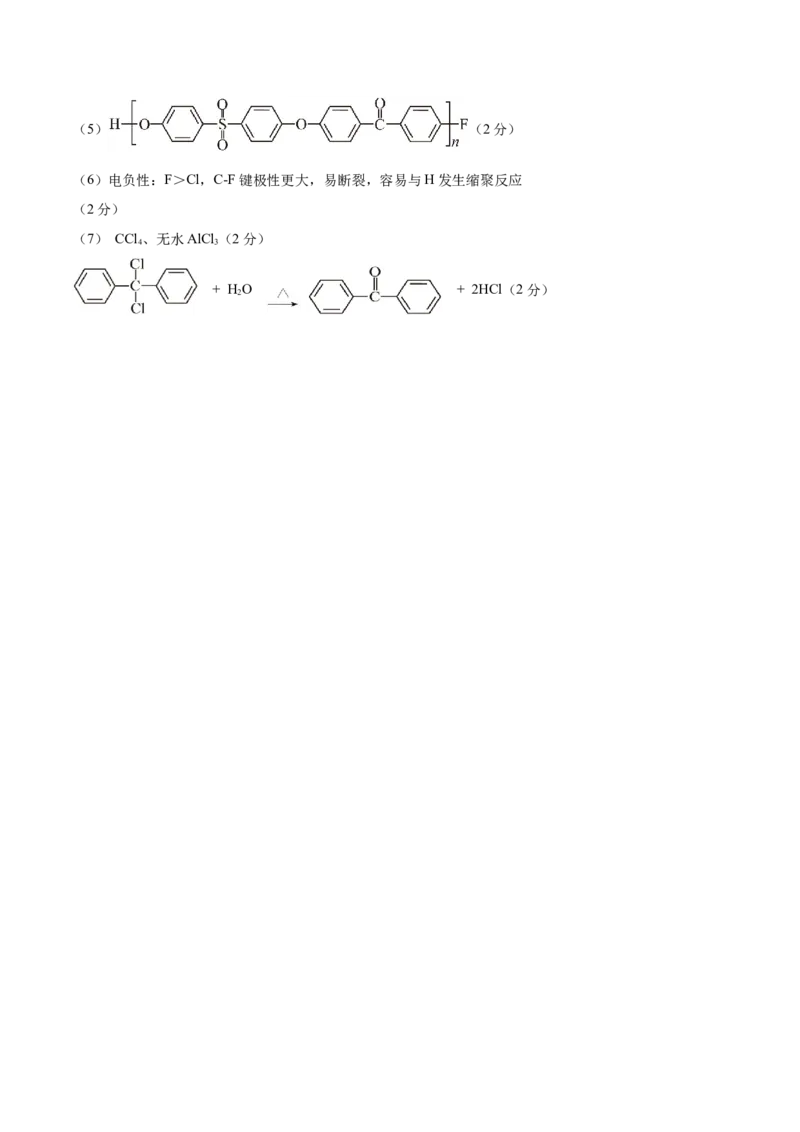
(7) CCl 、无水AlCl (2分)
4 3
+ HO + 2HCl(2分)
2