文档内容
专题87 实验设计与评价——装置图型
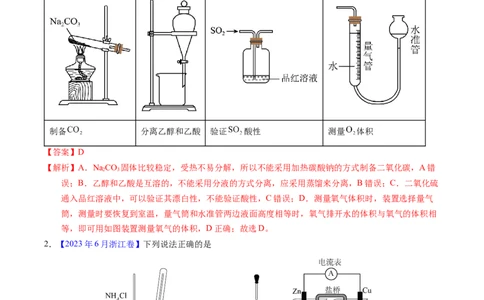
1.【2023年全国乙卷】下列装置可以用于相应实验的是
A B C D
制备 分离乙醇和乙酸 验证 酸性 测量 体积
【答案】D
【解析】A.NaCO 固体比较稳定,受热不易分解,所以不能采用加热碳酸钠的方式制备二氧化碳,A错
2 3
误;B.乙醇和乙酸是互溶的,不能采用分液的方式分离,应采用蒸馏来分离,B错误;C.二氧化硫
通入品红溶液中,可以验证其漂白性,不能验证酸性,C错误;D.测量氧气体积时,装置选择量气
筒,测量时要恢复到室温,量气筒和水准管两边液面高度相等时,氧气排开水的体积与氧气的体积相
等,即可用如图装置测量氧气的体积,D正确;故选D。
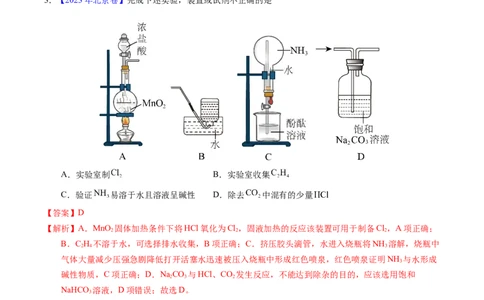
2.【2023年6月浙江卷】下列说法正确的是
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大D.图④装置盐桥中阳离子向 溶液中迁移
【答案】C
【解析】A.氯化铵受热分解生成氨气和氯化氢,遇冷又化合生成氯化铵,则直接加热氯化铵无法制得氨
气,实验室用加热氯化铵和氢氧化钙固体的方法制备氨气,故A错误;B.高锰酸钾溶液具有强氧化
性,会腐蚀橡胶管,所以高锰酸钾溶液应盛放在酸式滴定管在,不能盛放在碱式滴定管中,故B错误;
C.配制一定物质的量浓度的溶液时,俯视刻度线定容会使溶液的体积偏小,导致所配溶液浓度偏大,
故C正确;D.由图可知,锌铜原电池中,锌电极为原电池的负极,铜为正极,盐桥中阳离子向硫酸
铜溶液中迁移,故D错误;故选C。
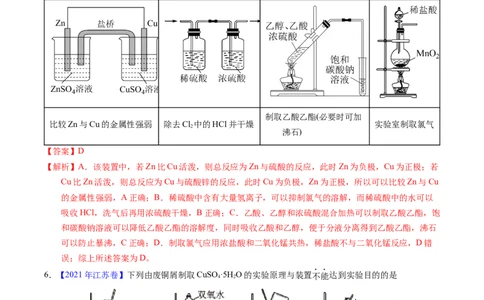
3.【2023年北京卷】完成下述实验,装置或试剂不正确的是
A.实验室制 B.实验室收集
C.验证 易溶于水且溶液呈碱性 D.除去 中混有的少量
【答案】D
【解析】A.MnO 固体加热条件下将HCl氧化为Cl,固液加热的反应该装置可用于制备Cl,A项正确;
2 2 2
B.C H 不溶于水,可选择排水收集,B项正确;C.挤压胶头滴管,水进入烧瓶将NH 溶解,烧瓶中
2 4 3
气体大量减少压强急剧降低打开活塞水迅速被压入烧瓶中形成红色喷泉,红色喷泉证明NH 与水形成
3
碱性物质,C项正确;D.NaCO 与HCl、CO 发生反应,不能达到除杂的目的,应该选用饱和
2 3 2
NaHCO 溶液,D项错误;故选D。
3
4.【2022年湖北卷】下列实验装置(部分夹持装置略)或现象错误的是
A.滴入酚酞溶液 B.吸氧腐蚀 C.钠的燃烧 D.石蜡油的热分解【答案】C
【解析】A.碳酸钠和碳酸氢钠都会因水解而使溶液显碱性,碳酸钠的碱性强于碳酸氢钠,滴入酚酞溶液
后,碳酸钠溶液呈现红色,碳酸氢钠的溶液呈现浅红色,A正确;B.食盐水为中性,铁钉发生吸氧
腐蚀,试管中的气体减少,导管口形成一段水柱,B正确;C.钠燃烧温度在400℃以上,玻璃表面皿
不耐高温,故钠燃烧通常载体为坩埚或者燃烧匙,C错误;D.石蜡油发生热分解,产生不饱和烃,
不饱和烃与溴发生加成反应,使试管中溴的四氯化碳溶液褪色,D正确;故答案选C。
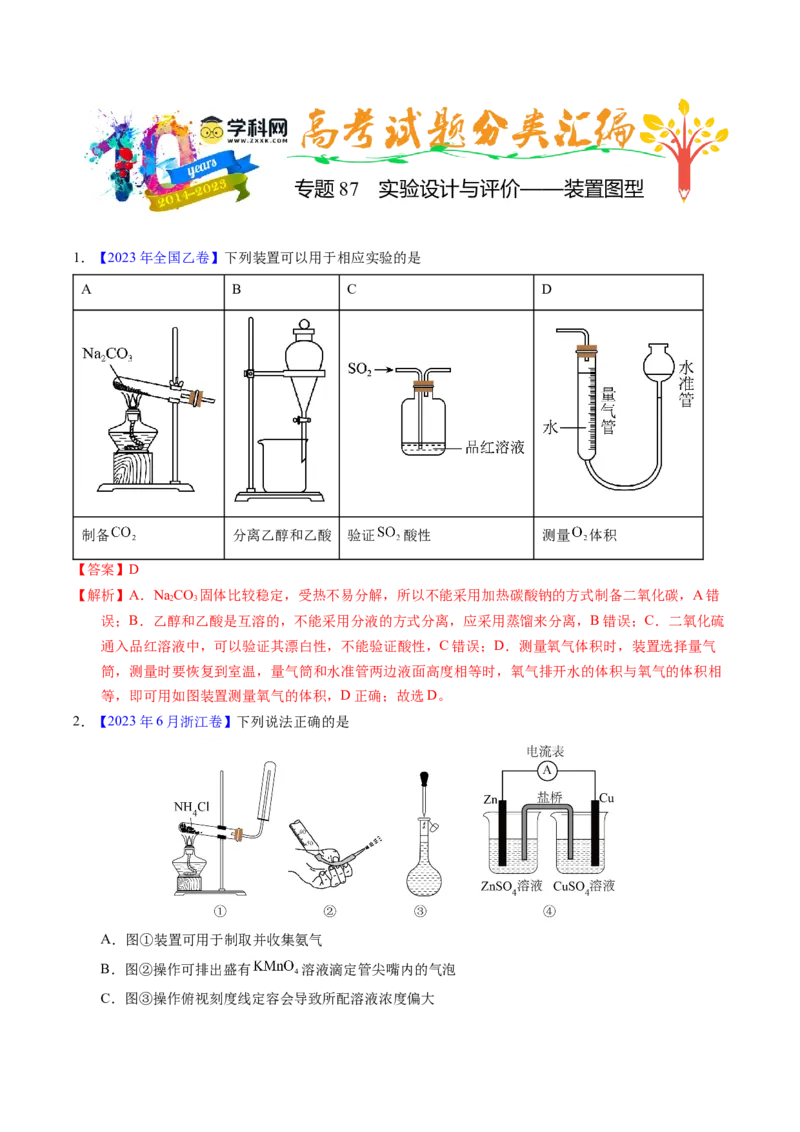
5.(2021·福建真题)利用下列装置和试剂进行实验,不能达到实验目的的是
A B C D
制取乙酸乙酯(必要时可加
比较Zn与Cu的金属性强弱 除去Cl 中的HCl并干燥 实验室制取氯气
2
沸石)
【答案】D
【解析】A.该装置中,若Zn比Cu活泼,则总反应为Zn与硫酸的反应,此时Zn为负极,Cu为正极;若
Cu比Zn活泼,则总反应为Cu与硫酸锌的反应,此时Cu为负极,Zn为正极,所以可以比较Zn与Cu
的金属性强弱,A正确;B.稀硫酸中含有大量氢离子,可以抑制氯气的溶解,而稀硫酸中的水可以
吸收HCl,洗气后再用浓硫酸干燥,B正确;C.乙酸、乙醇和浓硫酸混合加热可以制取乙酸乙酯,饱
和碳酸钠溶液可以降低乙酸乙酯的溶解度,同时吸收乙酸和乙醇,便于分液分离得到乙酸乙酯,沸石
可以防止暴沸,C正确;D.制取氯气应用浓盐酸和二氧化锰共热,稀盐酸不与二氧化锰反应,D错
误;综上所述答案为D。
6.【2021年江苏卷】下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2
A.用装置甲除去废铜屑表面的油污 B.用装置乙在加热的条件下溶解废铜屑
C.用装置丙过滤得到CuSO 溶液 D.用装置丁蒸干溶液获得CuSO ·5H O
4 4 2
【答案】D【解析】A.碳酸钠溶液显碱性,在加热的条件下可以除去铜屑表面的油污,A正确;B.在酸性条件下,
铜与双氧水发生氧化反应得到硫酸铜,B正确;C.装置丙为过滤装置,过滤可以除去难溶杂质,得
到硫酸铜溶液,C正确;D.用装置丁蒸干溶液得到硫酸铜固体,而不是CuSO ·5H O,D错误;答案
4 2
选D。
7.(2021·全国乙卷真题)在实验室采用如图装置制备气体,合理的是
化学试剂 制备的气体
A
B (浓)
C
D (浓)
【答案】C
【解析】由实验装置图可知,制备气体的装置为固固加热装置,收集气体的装置为向上排空气法,说明该
气体的密度大于空气的密度; A.氨气的密度比空气小,不能用向上排空法收集,故A错误;B.二
氧化锰与浓盐酸共热制备氯气为固液加热反应,需要选用固液加热装置,不能选用固固加热装置,故
B错误;C.二氧化锰和氯酸钾共热制备氧气为固固加热的反应,能选用固固加热装置,氧气的密度
大于空气,可选用向上排空气法收集,故C正确;D.氯化钠与浓硫酸共热制备为固液加热反应,需
要选用固液加热装置,不能选用固固加热装置,故D错误;故选C。
8.(2019·北京高考真题)探究草酸(HC O)性质,进行如下实验。(已知:室温下,0.1 mol·L−1
2 2 4
HC O 的pH=1.3)
2 2 4
实验 装置 试剂a 现象
① Ca(OH) 溶液(含酚酞) 溶液褪色,产生白色沉淀
2
② 少量NaHCO 溶液 产生气泡
3
③ 酸性KMnO 溶液 紫色溶液褪色
4
④ C HOH和浓硫酸 加热后产生有香味物质
2 5
由上述实验所得草酸性质所对应的方程式不正确的是
A.HC O 有酸性,Ca(OH) + H C O CaC O↓+2H O
2 2 4 2 2 2 4 2 4 2
B.酸性:HC O> H CO,NaHCO + H C O NaHC O+CO ↑+H O
2 2 4 2 3 3 2 2 4 2 4 2 2
C.HC O 具有还原性,2 +5 +16H+ 2Mn2++10CO ↑+ 8H O
2 2 4 2 2D.HC O 可发生酯化反应,HOOCCOOH+2C HOH C HOOCCOOC H+2H O
2 2 4 2 5 2 5 2 5 2
【答案】C
【解析】草酸(又称乙二酸)为一种二元弱酸,具有酸的通性,因此能发生中和反应,具有还原性,因为
乙二酸中含有羧基因此能发生酯化反应,据此解题;A.HC O 为二元弱酸,能与氢氧化钙溶液发生
2 2 4
中和反应,生成白色沉淀草酸钙和水,因此含酚酞的氢氧化钙溶液碱性逐渐减弱,溶液红色退去,正
确;B.产生气泡证明有CO 产生,因此可证明酸性HC O>HCO,反应方程式为:
2 2 2 4 2 3
HC O+2NaHCO=Na C O+2CO +2H O 或,H C O+NaHCO=NaHC O+2CO +2H O,正确;C.0.1
2 2 4 3 2 2 4 2 2 2 2 4 3 2 4 2 2
mol·L−1 HC O 的pH=1.3,说明草酸为弱酸,故在其参与的离子方程式中要写其化学式,不能用草酸根
2 2 4
表示,不正确;D.草酸(又称乙二酸),其中含有羧基,因此其能发生酯化反应,反应方程式正确,
正确;本题选不正确的,应选C。
9.(2019·天津高考真题)下列实验操作或装置能达到目的的是( )
A B C D
配制一定浓度的 证明乙炔可使溴水褪
混合浓硫酸和乙醇 收集 气体
溶液 色
【答案】B
【解析】A、乙醇的密度小于浓硫酸,混合时应将浓硫酸沿烧杯壁倒入乙醇中,边倒边搅拌,若顺序相反
则容易引起液体飞溅,不能达到目的;B、容量瓶上的刻度与凹液面的最低处相切,胶头滴管垂直位
于容量瓶的正上方,能达到目的;C、二氧化氮的密度大于空气,集气瓶中的导气管应长进短出,不
能达到目的;D、乙炔中的HS等杂质也能使溴水褪色,应先通过一个盛碱液的洗气瓶将杂质除去,
2
不能达到目的;故选B。
10.(2017·全国高考真题)实验室用H 还原WO 制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,
2 3
与酸反应产生还原性的硫化氢气体;焦性没食子酸溶液用于吸收少量氧气)。下列说法正确的是
A.①、②、③中依次盛装KMnO 溶液、浓HSO 、焦性没食子酸溶液
4 2 4B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
【答案】B
【解析】H 还原WO 制备金属W,装置Q用于制备氢气;A.气体从焦性没食子酸溶液中逸出,得到的氢
2 3
气混有水蒸气,应最后通过浓硫酸干燥,错误;B.点燃酒精灯进行加热前,应检验氢气的纯度,以
避免不纯的氢气发生爆炸,可点燃气体,通过声音判断气体纯度,声音越尖锐,氢气的纯度越低,正
确;C.实验结束后应先停止加热再停止通入氢气,使W处在氢气的氛围中冷却,以避免W被重新氧
化,错误;D.二氧化锰与浓盐酸需在加热条件下反应,而启普发生器不能加热,错误。答案选B。
11.(2014·上海高考真题)如图是模拟“侯氏制碱法”制取NaHCO 的部分装置。下列操作正确的是( )
3
A.a通入CO,然后b通入NH ,c中放碱石灰
2 3
B.b通入NH ,然后a通入CO,c中放碱石灰
3 2
C.a通入NH ,然后b通入CO,c中放蘸稀硫酸的脱脂棉
3 2
D.b通入CO,然后a通入NH ,c中放蘸稀硫酸的脱脂棉
2 3
【答案】C
【解析】由于CO 在水中的溶解度比较小,而NH 极易溶于水,所以在实验中要先通入溶解度较大的
2 3
NH ,再通入CO;由于NH 极易溶于水,在溶于水时极易发生倒吸现象,所以通入NH 的导气管的
3 2 3 3
末端不能伸入到溶液中,即a先通入NH ,然后b通入CO,A、B、D选项均错误;因为NH 是碱性
3 2 3
气体,所以过量的NH 要用稀硫酸来吸收,选项C合理;故合理答案是C。
3
12.(2013·北京高考真题)用下图所示装置检验乙烯时不需要除杂的是( )
选项 乙烯的制备 试剂X 试剂Y
A CHCHBr与NaOH乙醇溶液共热 HO KMnO 酸性溶液
3 2 2 4B CHCHBr与NaOH乙醇溶液共热 HO Br 的CCl 溶液
3 2 2 2 4
C C HOH与浓HSO 加热至170 ℃ NaOH溶液 KMnO 酸性溶液
2 5 2 4 4
D C HOH与浓HSO 加热至170 ℃ NaOH溶液 Br 的CCl 溶液
2 5 2 4 2 4
【答案】B
【解析】A.发生消去反应生成乙烯,乙醇受热会挥发,水吸收乙醇,乙醇能被高锰酸钾氧化,则需要加
水除杂,否则干扰乙烯的检验,不选;B.发生消去反应生成乙烯,乙醇与Br 的CCl 溶液不反应,
2 4
乙烯与Br 的CCl 溶液反应,则不需要除杂,不影响乙烯检验,选;C.发生消去反应生成乙烯,
2 4
NaOH溶液吸收乙醇,以及副反应生成的SO ,乙醇和SO 能被高锰酸钾氧化,则需要NaOH溶液除
2 2
杂,否则干扰乙烯的检验,不选;D.发生消去反应生成乙烯,乙醇与溴水不反应,但可能混有
SO ,SO 、乙烯均与溴水发生反应,则需要除杂,否则可干扰乙烯检验,不选;故选B。
2 2
13.(2014·北京高考真题)用下图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反
应发生的是( )
①中实验 ②中现象
A 铁粉与水蒸气加热 肥皂水冒泡
B 加热NH Cl和Ca(OH) 混合物 酚酞溶液变红
4 2
C NaHCO 固体受热分解 澄清石灰水变浑浊
3
D 石蜡油在碎瓷片上受热分解 Br 的CCl 溶液褪色
2 4
【答案】A
【解析】A.加热过程中的热空气、铁和水蒸气反应生成的氢气都能使肥皂水冒泡,所以肥皂水冒泡该反
应不一定发生,错误;B.NH
4
Cl+Ca(OH)
2
NH
3
↑+CaCl
2
+H
2
O、NH
3
+H
2
O⇌NH
3
.H
2
O⇌NH
4
+
+OH﹣,氨水溶液呈碱性,所以能使酚酞试液变红色,正确;C.2NaHCO
3
NaCO+CO ↑+H O,二氧化碳能使澄清石灰水变浑浊,如果②中澄清石灰水变浑浊,则①中一定发生
2 3 2 2
反应,正确;D.溴的四氯化碳褪色说明有不饱和烃生成,所以①中一定发生化学反应,正确;故选
A。
14.(2012·北京高考真题)用右图所示装置进行下列实验,实验结果与预测的现象不一致的是
①中的物质 ②中的物质 预测①中现象
A 淀粉碘化钾溶液 浓硝酸 无明显现象
B 酚酞溶液 浓盐酸 无明显现象C 氯化铝溶液 浓氨水 有白色沉淀
D 湿润红纸条 饱和氯水 红纸条褪色
【答案】A
【解析】A.硝酸具有挥发性,挥发出的硝酸进入淀粉KI溶液,硝酸具有强氧化性,可以将KI氧化为
I,I 遇淀粉变蓝色,错误;B.浓盐酸具有挥发性,挥发出的HCl进入酚酞溶液,酚酞溶液在酸性条
2 2
件下不变色,正确;C.浓氨水具有挥发性,挥发出的氨气溶于氯化铝溶液,一水合氨与氯化铝反应
生成氢氧化铝白色沉淀,正确;D.饱和氯水挥发出氯气,氯气与湿润红纸条接触,氯气水反应生成
HClO,HClO具有漂白性,使湿润红纸条褪色,正确;故答案为A。
15.(2014·全国高考真题)利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 ① ② ③ 实验结论 实验装置
AgNO 与AgCl的溶
3
A 稀硫酸 NaS Ksp(AgCl)>Ksp(Ag S)
2 2
液
B 浓硫酸 蔗糖 溴水 浓硫酸具有脱水性、氧化性
SO 与可溶性钡盐均可以生成白色
2
C 稀盐酸 NaSO Ba(NO ) 溶液
2 3 3 2
沉淀
D 浓硝酸 NaCO NaSiO 溶液 酸性:硝酸>碳酸>硅酸
2 3 2 3
【答案】B
【解析】A.稀硫酸与硫化钠反应生成硫化氢气体,由于③中含有硝酸银,通入HS一定生成硫化银沉淀,
2
不能确定硫化银一定是由氯化银转化的,也就不能比较溶度积大小,A错误;B.浓硫酸将蔗糖脱水
炭化,进而碳被氧化,生成CO、SO 和HO,SO 能使溴水褪色,B正确;C.二氧化硫溶液呈酸性,
2 2 2 2
酸性条件下,硝酸根离子具有强氧化性,可氧化二氧化硫生成硫酸根离子,可生成沉淀,但二氧化硫
通入氯化钡溶液中则没有沉淀生成,C错误;D.强酸能与弱酸盐反应生成弱酸,根据强酸制取弱酸
判断酸性强弱,浓硝酸和碳酸钠反应生成二氧化碳,二氧化碳、水和硅酸钠反应生成难溶性硅酸,但
硝酸具有挥发性,生成的CO 中含有硝酸,硝酸也与硅酸钠反应产生硅酸沉淀,不能实现实验目的,
2
D错误;答案选B。
16.(2015·全国高考真题)用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符
的是
选项 ①中物质 ②中物质 预测②中的现象
A. 稀盐酸 碳酸钠与氢氧化钠的混 立即产生气泡合溶液
B. 浓硝酸 用砂纸打磨过的铝条 产生红棕色气体
C. 氯化铝溶液 浓氢氧化钠溶液 产生大量白色沉淀
D. 草酸溶液 高锰酸钾酸性溶液 溶液逐渐褪色
【答案】D
【解析】A、氢氧化钠是强碱,碳酸钠是盐,因此盐酸首先中和氢氧化钠,然后再与碳酸钠反应生成碳酸
氢钠和氯化钠,最后盐酸与碳酸氢钠反应放出CO,不会立即产生气泡,A错误;B、常温下铝在浓
2
硝酸中钝化,反应很快停止,看不到红棕色NO 气体,B错误;C、氢氧化钠溶液开始是过量的,滴
2
入氯化铝生成偏铝酸钠,没有白色沉淀,当氢氧化钠完全消耗后,再滴入氯化铝,铝离子与偏铝酸根
离子反应生成白色沉淀氢氧化铝,C错误;D、草酸具有还原性,酸性高锰酸钾溶液具有强氧化性,
能被酸性高锰酸钾溶液氧化,因此草酸能使酸性高锰酸钾溶液褪色,D正确;答案选D。