文档内容
重庆市七校联盟 2025 年秋期第一次适应性考试
化 学 试 题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3 考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H-1 C-12 N-14 O-16 I-127 Pb-207
一、单选题:本题共14小题,每小题3分,共42分。
1.化学与生产、生活、环境、社会发展等关系密切。下列说法不正确的是( )
A.植物油催化加氢可制肥皂
B.臭氧、二氧化氯可作为新的自来水消毒剂
C.用FeCl 溶液作为“腐蚀液”去除覆铜板上不需要的铜
3
D.苯甲酸及其钠盐可用作食品防腐剂
2.神舟十八号载人飞船顺利升空并进入空间站。下列说法所涉及的化学知识,不正确的是( )
A.神舟十八号载人飞船外壳采用的高温陶瓷材料氮化硅属于共价晶体
B.出舱活动所穿舱外服的主要材料聚氨酯属于有机合成高分子材料
C.火箭使用的燃料偏二甲肼[(CH ) NNH ]属于烃类物质
3 2 2
D.空间站的能量主要来自柔性太阳能电池翼,其工作原理是将太阳能转化为电能
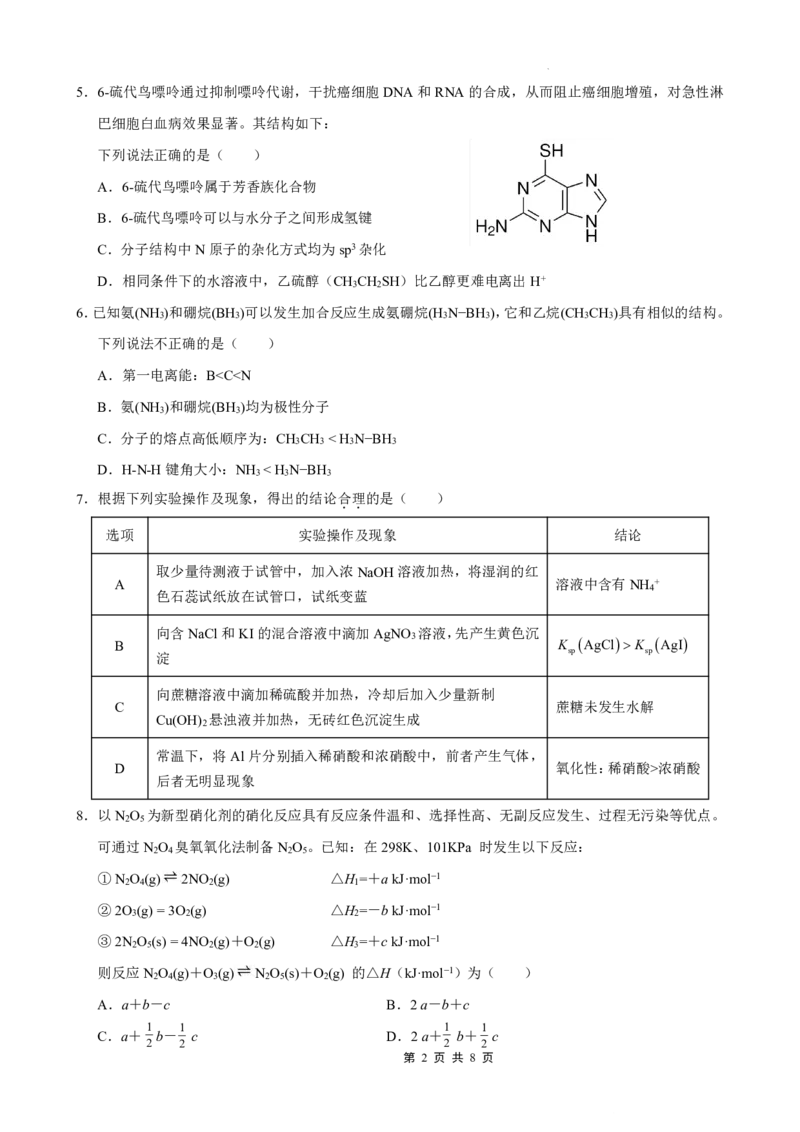
3.下列制备实验中,实验装置及操作均正确的是( )
A.用高锰酸钾标准溶液滴定草酸溶液 B.除去CO 中的少量HCl C.溶液转移 D.中和热测定
2
4.下列离子方程式不正确的是( )
A.纯碱溶液可用于去油污的原因:CO2-+H O HCO-+OH−
3 2 3
B.工业废水中的Pb2+用FeS去除:Pb2++S2−=PbS↓
C.用NaOH溶液吸收NO 气体:2NO +2OH−=NO-+NO-+H O
2 2 3 2 2
D.用丙烯腈电合成己二腈,在阴极发生的电极反应:2CH =CHCN+2H++2e−=NC(CH ) CN
2 2 4
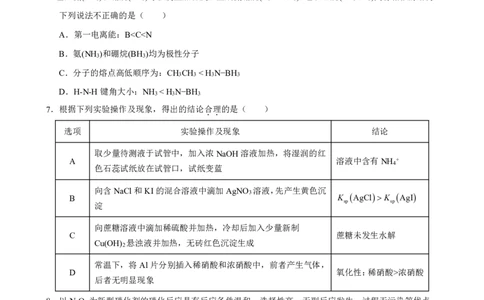
第 1 页 共 8 页5.6-硫代鸟嘌呤通过抑制嘌呤代谢,干扰癌细胞DNA和RNA的合成,从而阻止癌细胞增殖,对急性淋
巴细胞白血病效果显著。其结构如下:
下列说法正确的是( )
A.6-硫代鸟嘌呤属于芳香族化合物
B.6-硫代鸟嘌呤可以与水分子之间形成氢键
C.分子结构中N原子的杂化方式均为sp3杂化
D.相同条件下的水溶液中,乙硫醇(CH CH SH)比乙醇更难电离出H+
3 2
6.已知氨(NH )和硼烷(BH )可以发生加合反应生成氨硼烷(H N−BH ),它和乙烷(CH CH )具有相似的结构。
3 3 3 3 3 3
下列说法不正确的是( )
A.第一电离能:B浓硝酸
后者无明显现象
8.以N O 为新型硝化剂的硝化反应具有反应条件温和、选择性高、无副反应发生、过程无污染等优点。
2 5
可通过N O 臭氧氧化法制备N O 。已知:在298K、101KPa 时发生以下反应:
2 4 2 5
①N O (g) 2NO (g) △H =+akJ·mol−1
2 4 2 1
②2O (g)=3O (g) △H =-bkJ·mol−1
3 2 2
③2N O (s)=4NO (g)+O (g) △H =+ckJ·mol−1
2 5 2 2 3
则反应N O (g)+O (g) N O (s)+O (g) 的△H(kJ·mol−1)为( )
2 4 3 2 5 2
A.a+b-c B.2a-b+c
1 1 1 1
C.a+ b- c D.2a+ b+ c
2 2 2 2
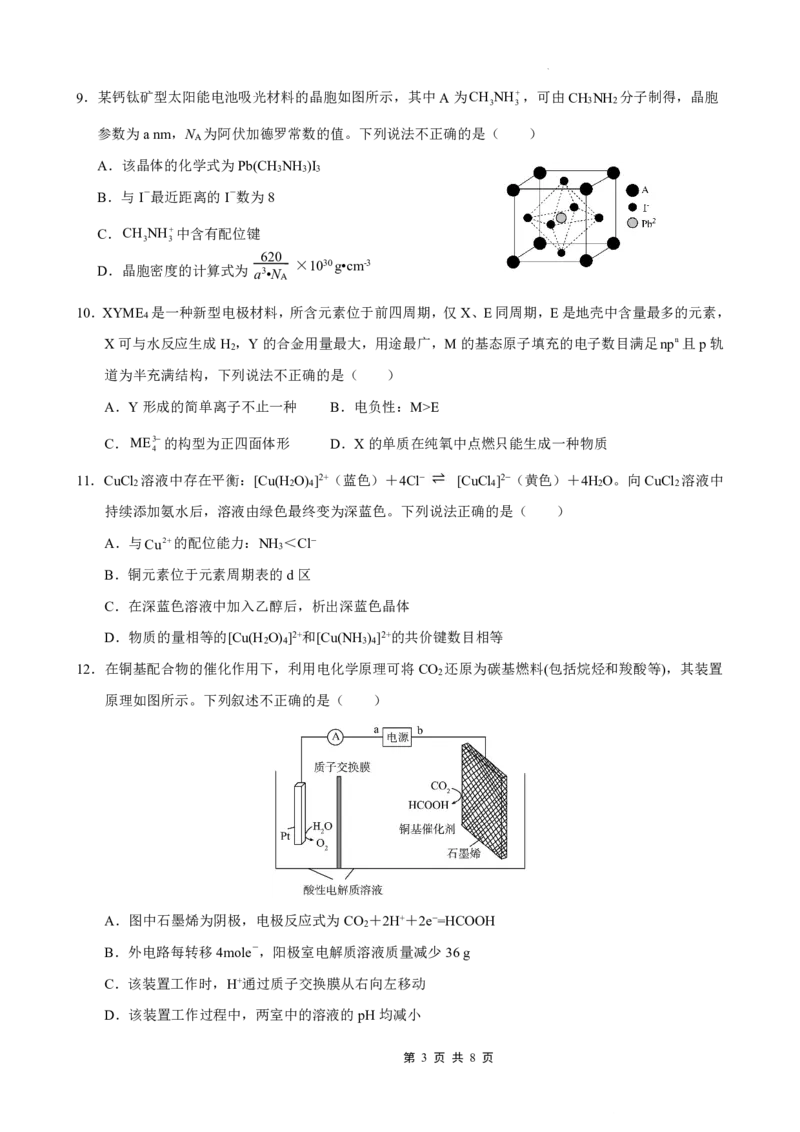
第 2 页 共 8 页9.某钙钛矿型太阳能电池吸光材料的晶胞如图所示,其中A为CH NH,可由CH NH 分子制得,晶胞
3 3 3 2
参数为anm,N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.该晶体的化学式为Pb(CH NH )I
3 3 3
B.与I-最近距离的I-数为8
C.CH NH中含有配位键
3 3
620
D.晶胞密度的计算式为
a3•N
×1030g•cm-3
A
10.XYME 是一种新型电极材料,所含元素位于前四周期,仅X、E同周期,E是地壳中含量最多的元素,
4
X可与水反应生成H ,Y的合金用量最大,用途最广,M的基态原子填充的电子数目满足npn且p轨
2
道为半充满结构,下列说法不正确的是( )
A.Y形成的简单离子不止一种 B.电负性:M>E
C.ME3的构型为正四面体形 D.X的单质在纯氧中点燃只能生成一种物质
4
11.CuCl 溶液中存在平衡:[Cu(H O) ]2+(蓝色)+4Cl− [CuCl ]2−(黄色)+4H O。向CuCl 溶液中
2 2 4 4 2 2
持续添加氨水后,溶液由绿色最终变为深蓝色。下列说法正确的是( )
A.与Cu2的配位能力:NH
3
<Cl−
B.铜元素位于元素周期表的d区
C.在深蓝色溶液中加入乙醇后,析出深蓝色晶体
D.物质的量相等的[Cu(H O) ]2+和[Cu(NH ) ]2+的共价键数目相等
2 4 3 4
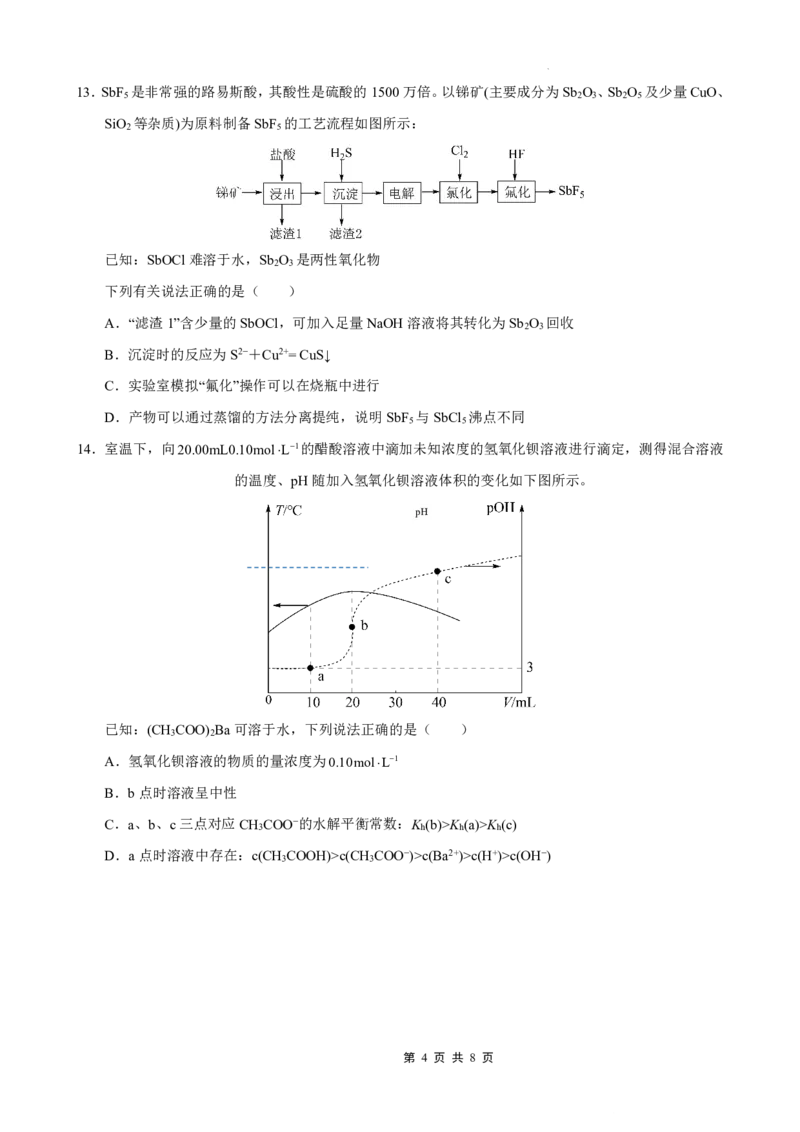
12.在铜基配合物的催化作用下,利用电化学原理可将CO 还原为碳基燃料(包括烷烃和羧酸等),其装置
2
原理如图所示。下列叙述不正确的是( )
A.图中石墨烯为阴极,电极反应式为CO +2H++2e−=HCOOH
2
B.外电路每转移4mole-,阳极室电解质溶液质量减少36g
C.该装置工作时,H+通过质子交换膜从右向左移动
D.该装置工作过程中,两室中的溶液的pH均减小
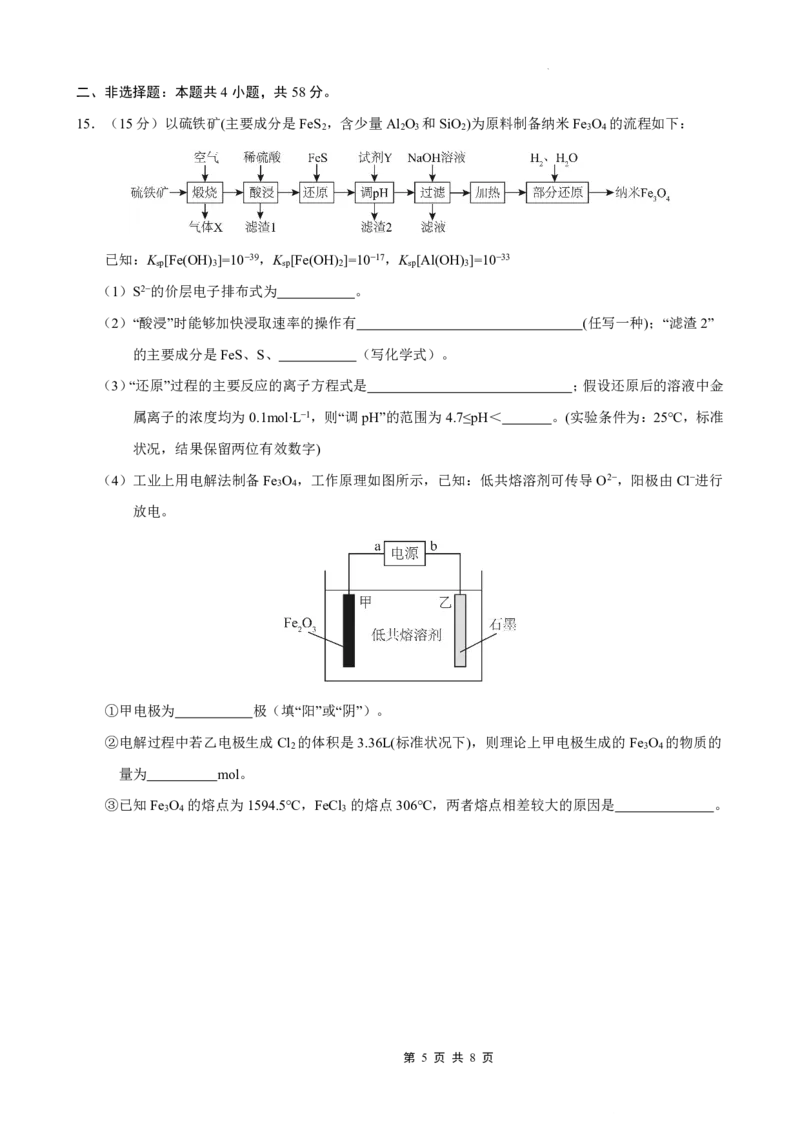
第 3 页 共 8 页13.SbF 是非常强的路易斯酸,其酸性是硫酸的1500万倍。以锑矿(主要成分为Sb O 、Sb O 及少量CuO、
5 2 3 2 5
SiO 等杂质)为原料制备SbF 的工艺流程如图所示:
2 5
已知:SbOCl难溶于水,Sb O 是两性氧化物
2 3
下列有关说法正确的是( )
A.“滤渣1”含少量的SbOCl,可加入足量NaOH溶液将其转化为Sb O 回收
2 3
B.沉淀时的反应为S2−+Cu2+=CuS↓
C.实验室模拟“氟化”操作可以在烧瓶中进行
D.产物可以通过蒸馏的方法分离提纯,说明SbF 与SbCl 沸点不同
5 5
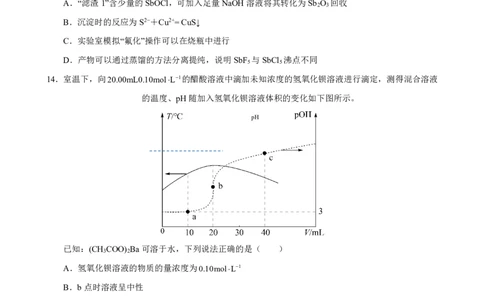
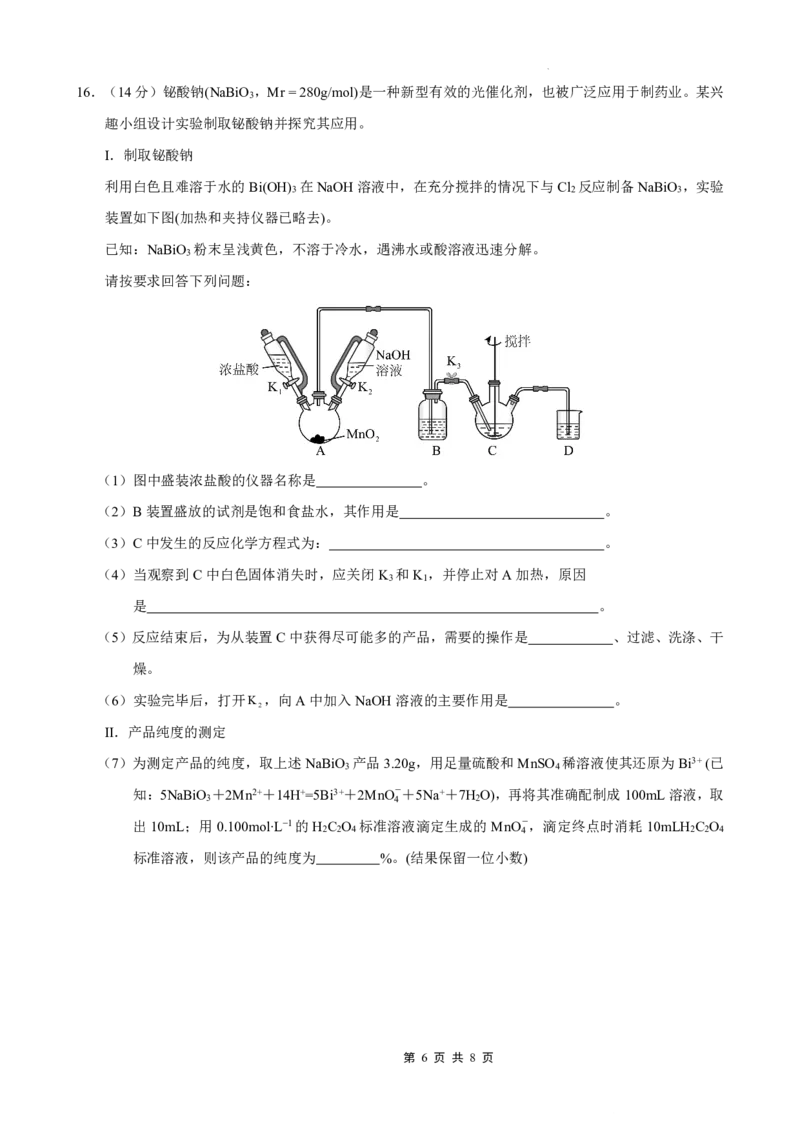
14.室温下,向20.00mL0.10molL1的醋酸溶液中滴加未知浓度的氢氧化钡溶液进行滴定,测得混合溶液
的温度、pH随加入氢氧化钡溶液体积的变化如下图所示。
pH
已知:(CH COO) Ba可溶于水,下列说法正确的是( )
3 2
A.氢氧化钡溶液的物质的量浓度为0.10molL1
B.b点时溶液呈中性
C.a、b、c三点对应CH COO−的水解平衡常数:K (b)>K (a)>K (c)
3 h h h
D.a点时溶液中存在:c(CH COOH)>c(CH COO−)>c(Ba2+)>c(H+)>c(OH−)
3 3
第 4 页 共 8 页二、非选择题:本题共4小题,共58分。
15.(15分)以硫铁矿(主要成分是FeS ,含少量Al O 和SiO )为原料制备纳米Fe O 的流程如下:
2 2 3 2 3 4
已知:K [Fe(OH) ]=10−39,K [Fe(OH) ]=10−17,K [Al(OH) ]=10−33
sp 3 sp 2 sp 3
(1)S2−的价层电子排布式为 。
(2)“酸浸”时能够加快浸取速率的操作有 (任写一种);“滤渣2”
的主要成分是FeS、S、 (写化学式)。
(3)“还原”过程的主要反应的离子方程式是 ;假设还原后的溶液中金
属离子的浓度均为0.1mol∙L−1,则“调pH”的范围为4.7≤pH< 。(实验条件为:25℃,标准
状况,结果保留两位有效数字)
(4)工业上用电解法制备Fe O ,工作原理如图所示,已知:低共熔溶剂可传导O2−,阳极由Cl−进行
3 4
放电。
①甲电极为 极(填“阳”或“阴”)。
②电解过程中若乙电极生成Cl 的体积是3.36L(标准状况下),则理论上甲电极生成的Fe O 的物质的
2 3 4
量为 mol。
③已知Fe O 的熔点为1594.5℃,FeCl 的熔点306℃,两者熔点相差较大的原因是 。
3 4 3
第 5 页 共 8 页16.(14分)铋酸钠(NaBiO ,Mr=280g/mol)是一种新型有效的光催化剂,也被广泛应用于制药业。某兴
3
趣小组设计实验制取铋酸钠并探究其应用。
Ⅰ.制取铋酸钠
利用白色且难溶于水的Bi(OH) 在NaOH溶液中,在充分搅拌的情况下与Cl 反应制备NaBiO ,实验
3 2 3
装置如下图(加热和夹持仪器已略去)。
已知:NaBiO 粉末呈浅黄色,不溶于冷水,遇沸水或酸溶液迅速分解。
3
请按要求回答下列问题:
(1)图中盛装浓盐酸的仪器名称是 。
(2)B装置盛放的试剂是饱和食盐水,其作用是 。
(3)C中发生的反应化学方程式为: 。
(4)当观察到C中白色固体消失时,应关闭K 和K ,并停止对A加热,原因
3 1
是 。
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是 、过滤、洗涤、干
燥。
(6)实验完毕后,打开K ,向A中加入NaOH溶液的主要作用是 。
2
Ⅱ.产品纯度的测定
(7)为测定产品的纯度,取上述NaBiO 产品3.20g,用足量硫酸和MnSO 稀溶液使其还原为Bi3+(已
3 4
知:5NaBiO +2Mn2++14H+=5Bi3++2MnO-+5Na++7H O),再将其准确配制成100mL溶液,取
3 4 2
出10mL;用0.100mol∙L−1的H C O 标准溶液滴定生成的MnO-,滴定终点时消耗10mLH C O
2 2 4 4 2 2 4
标准溶液,则该产品的纯度为 %。(结果保留一位小数)
第 6 页 共 8 页17.(15分)乙炔(C H )、乙烯和乙烷是重要的基础化工原料,在生产、生活中有广泛应用。回答问题:
2 2
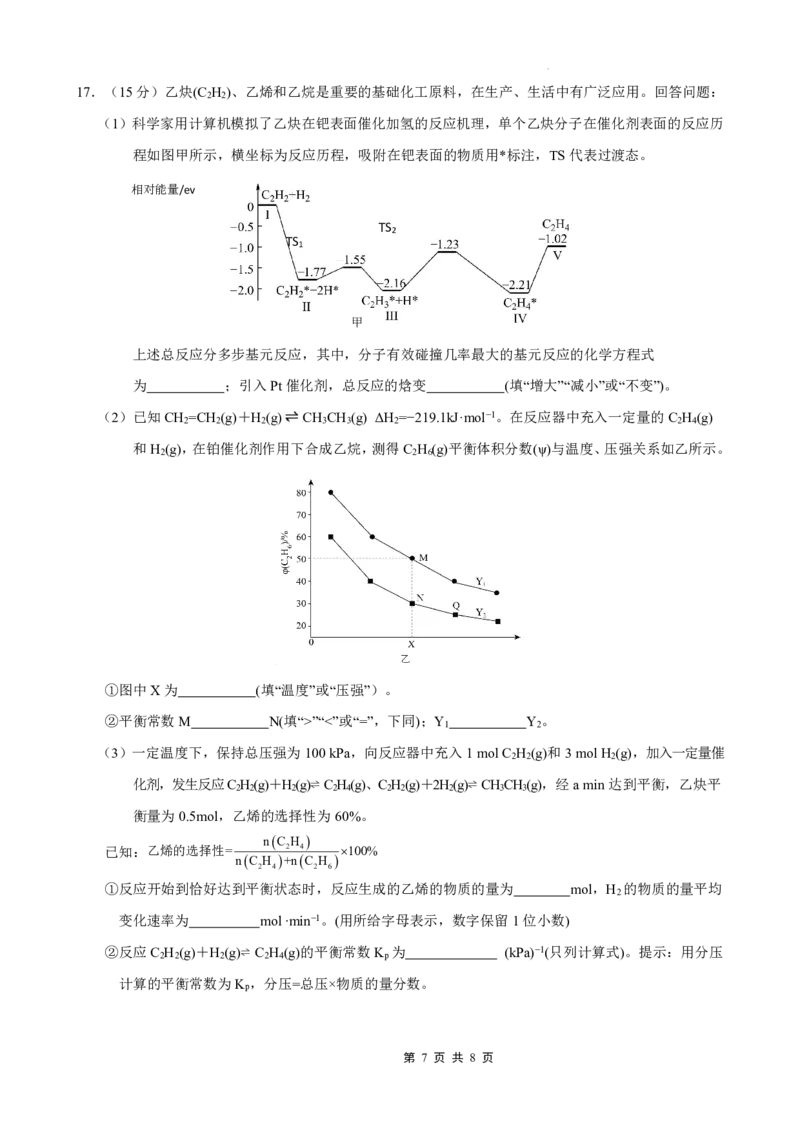
(1)科学家用计算机模拟了乙炔在钯表面催化加氢的反应机理,单个乙炔分子在催化剂表面的反应历
程如图甲所示,横坐标为反应历程,吸附在钯表面的物质用*标注,TS代表过渡态。
相对能量/ev
TS
2
TS
1
甲
上述总反应分多步基元反应,其中,分子有效碰撞几率最大的基元反应的化学方程式
为 ;引入Pt催化剂,总反应的焓变 (填“增大”“减小”或“不变”)。
(2)已知CH =CH (g)+H (g) CH CH (g) ΔH =−219.1kJ·mol−1。在反应器中充入一定量的C H (g)
2 2 2 3 3 2 2 4
和H (g),在铂催化剂作用下合成乙烷,测得C H (g)平衡体积分数(ψ)与温度、压强关系如乙所示。
2 2 6
①图中X为 (填“温度”或“压强”)。
②平衡常数M N(填“>”“<”或“=”,下同);Y Y 。
1 2
(3)一定温度下,保持总压强为100kPa,向反应器中充入1molC H (g)和3molH (g),加入一定量催
2 2 2
化剂,发生反应CH(g)+H(g)⇌ CH(g)、CH(g)+2H(g)⇌ CHCH(g),经amin达到平衡,乙炔平
2 2 2 2 4 2 2 2 3 3
衡量为0.5mol,乙烯的选择性为60%。
nC H
已知:乙烯的选择性= 2 4 100%
nC H +nC H
2 4 2 6
①反应开始到恰好达到平衡状态时,反应生成的乙烯的物质的量为 mol,H 的物质的量平均
2
变化速率为 mol∙min−1。(用所给字母表示,数字保留1位小数)
②反应C H (g)+H (g)⇌ C H (g)的平衡常数K 为 (kPa)−1(只列计算式)。提示:用分压
2 2 2 2 4 p
计算的平衡常数为K ,分压=总压×物质的量分数。
p
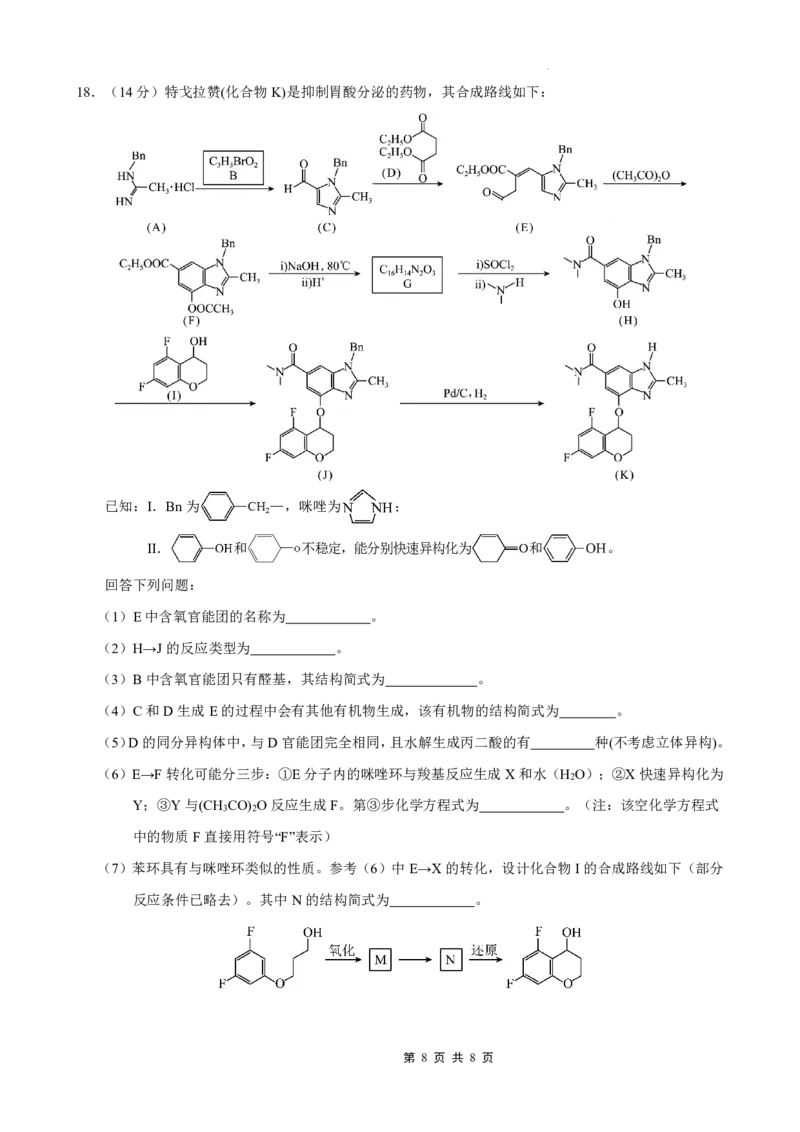
第 7 页 共 8 页18.(14分)特戈拉赞(化合物K)是抑制胃酸分泌的药物,其合成路线如下:
已知:Ⅰ.Bn为 ,咪唑为 ;
Ⅱ. 和 不稳定,能分别快速异构化为 和 。
回答下列问题:
(1)E中含氧官能团的名称为 。
(2)H→J的反应类型为 。
(3)B中含氧官能团只有醛基,其结构简式为 。
(4)C和D生成E的过程中会有其他有机物生成,该有机物的结构简式为 。
(5)D的同分异构体中,与D官能团完全相同,且水解生成丙二酸的有 种(不考虑立体异构)。
(6)E→F转化可能分三步:①E分子内的咪唑环与羧基反应生成X和水(H O);②X快速异构化为
2
Y;③Y与(CH CO) O反应生成F。第③步化学方程式为 。(注:该空化学方程式
3 2
中的物质F直接用符号“F”表示)
(7)苯环具有与咪唑环类似的性质。参考(6)中E→X的转化,设计化合物I的合成路线如下(部分
反应条件已略去)。其中N的结构简式为 。
第 8 页 共 8 页