文档内容
高三化学第一次半月考试题
一、单选题(本大题共13小题,1-5每题4分,6-13每题5分共60.0分)
1. 通常超市里 商品在摆放到货架前会先进行分类,因此我们在超市能迅速找到所需商品。下列关
于物质的分类组合正确的是
选项 物质 类别
A 钠、液氯、铁、冰水混合物 纯净物
B 碘伏、生石灰、青铜、空气 混合物
C H SO 、HClO 、稀盐酸、NaCl溶液 电解质
2 4 4
D 纯碱、NaOH、N H 、KOH 碱
3
A. A B. B C. C D. D
2. 已知:①Al(OH) 固体的 熔点为300℃;②无水AlCl 晶体易升华;③熔融状态的HgCl 不
3 3 2
能导电,稀溶液具有弱的导电能力且可作为手术刀的消毒液,下列关于Al(OH) 、AlCl 和HgCl 的
3 3 2
说法正确的是
A. 均为弱电解质 B. 均为离子化合物
C. HgCl 的水溶液导电能力很弱,说明其难溶于水
2
D. HgCl 2 在水中的电离方程式可能是 HgCl 2 ⇀HgCl++Cl−
↽
3. 下列离子方程式正确的是
A. 澄清石灰水与过量CO 反应:CO +Ca2++2OH−=CaCO ↓+H O
2 2 3 2
B. Fe2+与H O 在酸性溶液中的反应:2Fe2++H O =2Fe3++2H O+2H+
2 2 2 2 2
Δ
C. 向沸水中滴加饱和的FeCl 溶液制备Fe(OH) 胶体:Fe3++3H O ̲(cid:19) Fe(OH) (胶体)+3H+
3 3 2 ̲(cid:19) 3
D. 向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO−+OH−=CaCO ↓+H O
3 3 2
学科网(北京)股份有限公司4. N 为阿伏加德罗常数的值,下列说法不正确的是
A
A. 常温常压下,22.4LCO 气体中含有的氧原子数小于2N
2 A
B. 6gSiO 中含有的Si−O键的数目为0.4N
2 A
C. 78gNa O 中含有的离子总数为3 N❑
2 2 A
D. 50mL12mol·L−1盐酸与足量MnO 共热,转移的电子数为0.3 N❑
2 A
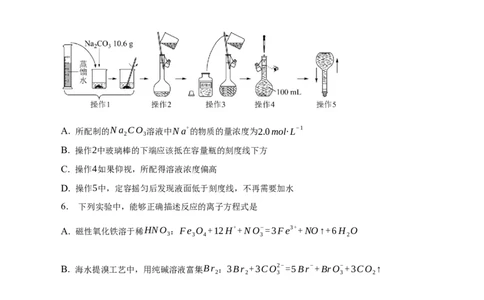
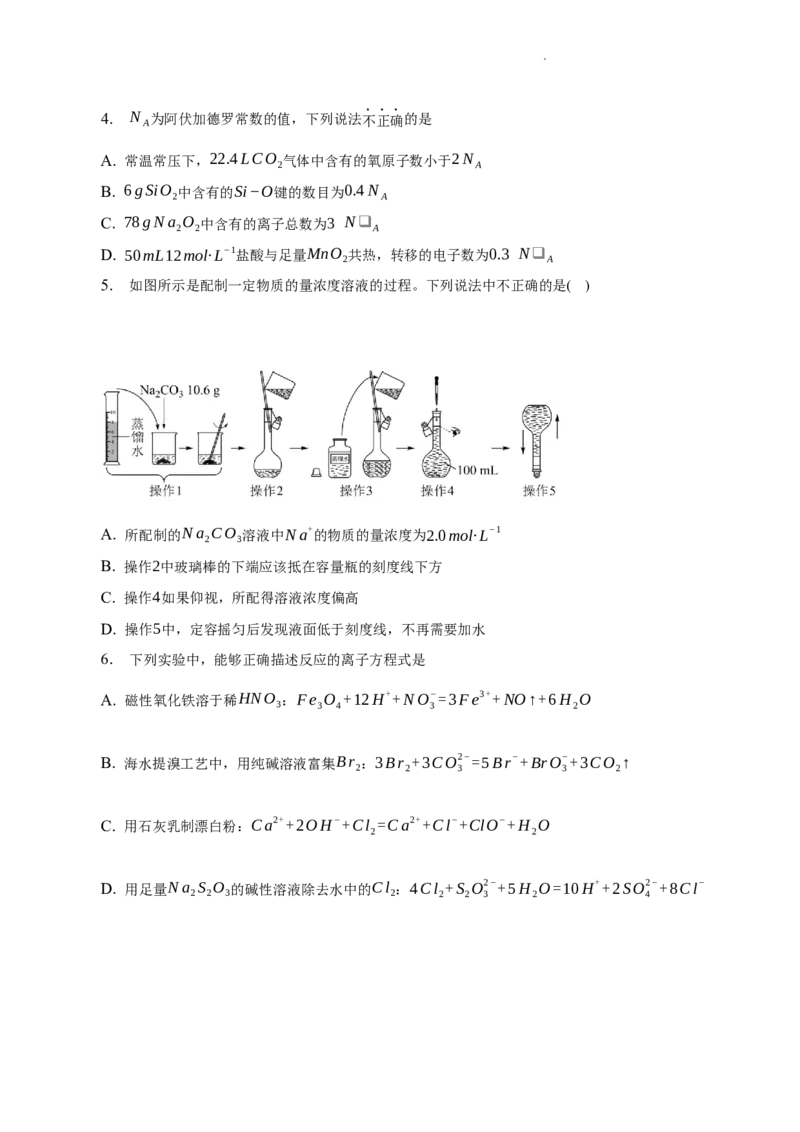
5. 如图所示是配制一定物质的量浓度溶液的过程。下列说法中不正确的是( )
A. 所配制的Na CO 溶液中Na+的物质的量浓度为2.0mol·L−1
2 3
B. 操作2中玻璃棒的下端应该抵在容量瓶的刻度线下方
C. 操作4如果仰视,所配得溶液浓度偏高
D. 操作5中,定容摇匀后发现液面低于刻度线,不再需要加水
6. 下列实验中,能够正确描述反应的离子方程式是
A. 磁性氧化铁溶于稀HNO :Fe O +12H++NO−=3Fe3++NO↑+6H O
3 3 4 3 2
B. 海水提溴工艺中,用纯碱溶液富集Br :3Br +3CO2−=5Br−+BrO−+3CO ↑
2 2 3 3 2
C. 用石灰乳制漂白粉:Ca2++2OH−+Cl =Ca2++Cl−+ClO−+H O
2 2
D. 用足量Na S O 的碱性溶液除去水中的Cl :4Cl +S O2−+5H O=10H++2SO2−+8Cl−
2 2 3 2 2 2 3 2 4
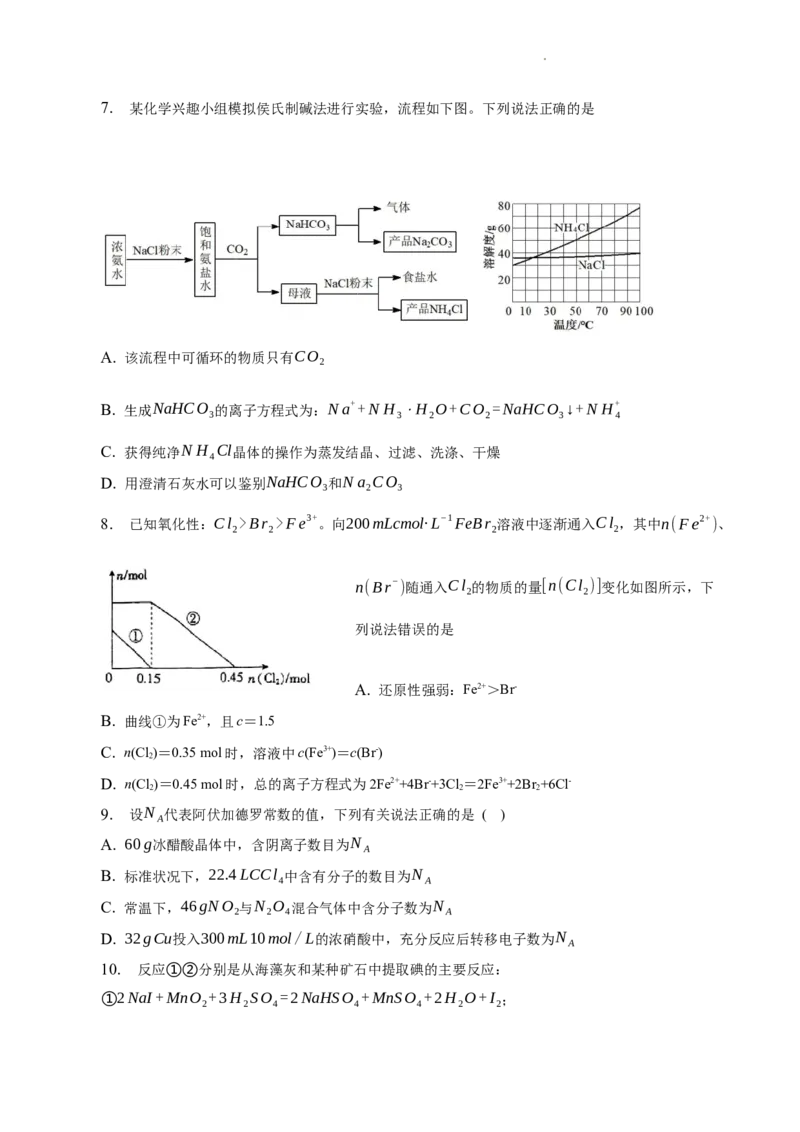
学科网(北京)股份有限公司7. 某化学兴趣小组模拟侯氏制碱法进行实验,流程如下图。下列说法正确的是
A. 该流程中可循环的物质只有CO
2
B. 生成NaHCO 的离子方程式为:Na++N H ⋅H O+CO =NaHCO ↓+N H+
3 3 2 2 3 4
C. 获得纯净N H Cl晶体的操作为蒸发结晶、过滤、洗涤、干燥
4
D. 用澄清石灰水可以鉴别NaHCO 和Na CO
3 2 3
8. 已知氧化性:Cl >Br >Fe3+ 。向200mLcmol·L−1FeBr 溶液中逐渐通入Cl ,其中n(Fe2+ )、
2 2 2 2
n(Br− )随通入Cl 的物质的量[n(Cl )]变化如图所示,下
2 2
列说法错误的是
A. 还原性强弱:Fe2+>Br-
B. 曲线①为Fe2+,且c=1.5
C. n(Cl )=0.35 mol时,溶液中c(Fe3+)=c(Br-)
2
D. n(Cl )=0.45 mol时,总的离子方程式为2Fe2++4Br-+3Cl=2Fe3++2Br +6Cl-
2 2 2
9. 设N 代表阿伏加德罗常数的值,下列有关说法正确的是 ( )
A
A. 60g冰醋酸晶体中,含阴离子数目为N
A
B. 标准状况下,22.4LCCl 中含有分子的数目为N
4 A
C. 常温下,46gNO 与N O 混合气体中含分子数为N
2 2 4 A
D. 32gCu投入300mL10mol/L的浓硝酸中,充分反应后转移电子数为N
A
10. 反应①②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO +3H SO =2NaHSO +MnSO +2H O+I ;
2 2 4 4 4 2 2
学科网(北京)股份有限公司②2NaIO +5NaHSO =2Na SO +3NaHSO +H O+I 。下列说法正确的是 ( )
3 3 2 4 4 2 2
A. 两个反应中硫元素均被氧化
B. 碘元素在反应①中被还原,在反应②中被氧化
C. 氧化性:MnO >SO 2−>IO −>I
2 4 3 2
D. 反应①②中生成等量的I 时,转移电子数之比为1:5
2
11. 用N 表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A
A. 1molFe与1molCl 充分反应生成FeCl 时,转移电子数为3N
2 3 A
B. 标准状况下,22.4L乙烷中所含的极性共价键数目为7N
A
C. 1mol羟基与17gN H 所含电子数之比为9∶10
3
D. 一定温度下1L0.5mol·L−1N H Cl溶液与2L0.25mol·L−1N H Cl溶液含N H+ 的物质的量相同
4 4 4
12. 为预防新型冠状病毒肺炎,某同学购买了一瓶84消毒液,其包装说明如图所示。
基本信息:含质量分数为25%的NaClO、1000mL、密度
1.19g⋅cm−3
使用方法:稀释100倍后使用
注意事项:密封保存,易吸收空气中的CO 、H O而变质
2 2
根据图中信息和相关知识判断,下列分析不正确的是 ( )
A. 从物质分类的角度看84消毒液的有效成分NaClO属于强电解质
B. 84消毒液在空气中敞口放置一段时间后浓度会变小
C. 该84消毒液中NaClO的物质的量浓度约为0.4mol⋅L−1
D. 用容量瓶配制上述84消毒液时,定容时俯视刻度线,所得溶液浓度会偏大
13. 常温下,下列各组离子一定能在指定溶液中大量共存的是
A. 在中性溶液中:Na+、Ba2+、SO2− 、Cl—
4
B. 与Al反应能放出H 的溶液中:Fe2+、K+、NO− 、SO2−
2 3 4
学科网(北京)股份有限公司K
C. W =1×10−13mol·L−1 的溶液中:N H+ 、Na+、Cl−、NO−
c(H+
)
4 3
D. 水电离的c(H+ )=1×10−13mol·L−1的溶液中:K+、Na+、AlO− 、CO2−
2 3
二、填空题(本大题共1小题,每空4分共16.0分)
14. 计算(1)15.6gNa X中含有0.4molNa+,则X的相对原子质量为_______。
2
(2)标准状况下,44.8L氯气通入足量NaOH溶液中,转移的电子数目为_______。
(3)标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为7.6g,则混合气体中甲烷的物质的
量为_______ 。
(4)测定Na CO 样品(含氯化钠杂质)中Na CO 的质量分数:称取mg样品放入烧杯内加水溶解,
2 3 2 3
加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na CO 的
2 3
质量分数为_______。
三、实验题(本大题共1小题,每空3分共24.0分)
15. 【任务一】某小组研究Na CO 和NaHCO 的性质,实验如下:
2 3 3
现象
序号 操作
Na CO NaHCO
2 3 3
在两支试管中加入1gNa CO 或 温度由17.6℃变为23.2℃温度由17.6℃变为17.2℃
2 3
① 1NaHCO 固体,再加入5mL水,;放置至室温时,试管内无;放置至室温时,试管内有少
3
振荡;将温度计分别插入其中 固体 量固体残留
室温时,分别向①所得溶液中滴入
② 溶液变红 溶液微红
2滴酚酞溶液
(1)室温下,Na CO 的溶解度大于NaHCO 的实验证据是
2 3 3
______________________________________________________________________________。
(2)该实验不能说明Na CO 溶液的碱性强于NaHCO 溶液,理由是
2 3 3
______________________________________________________________________________。
【任务二】为进一步探究Na CO 和NaHCO 的性质,利用传感器继续做如下实验:
2 3 3
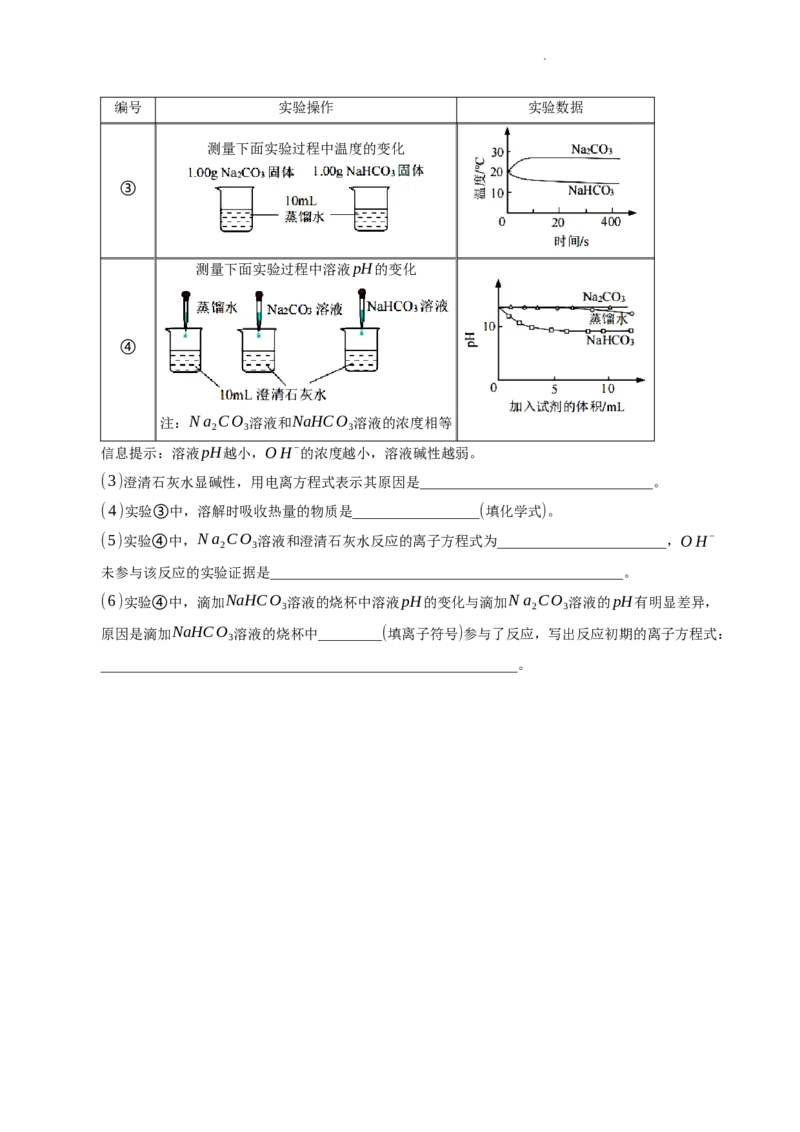
学科网(北京)股份有限公司编号 实验操作 实验数据
测量下面实验过程中温度的变化
③
测量下面实验过程中溶液pH的变化
④
注:Na CO 溶液和NaHCO 溶液的浓度相等
2 3 3
信息提示:溶液pH越小,OH−的浓度越小,溶液碱性越弱。
(3)澄清石灰水显碱性,用电离方程式表示其原因是_________________________________。
(4)实验③中,溶解时吸收热量的物质是__________________(填化学式)。
(5)实验④中,Na CO 溶液和澄清石灰水反应的离子方程式为________________________,OH−
2 3
未参与该反应的实验证据是__________________________________________________。
(6)实验④中,滴加NaHCO 溶液的烧杯中溶液pH的变化与滴加Na CO 溶液的pH有明显差异,
3 2 3
原因是滴加NaHCO 溶液的烧杯中_________(填离子符号)参与了反应,写出反应初期的离子方程式:
3
___________________________________________________________。
学科网(北京)股份有限公司