文档内容
滴定法的应用
1.(3分)利用K Cr O 滴定亚铁离子,来测定FeCl ·4H O晶体纯度。准确称取a g重结晶后的FeCl ·4H O晶
2 2 7 2 2 2 2
体,溶于酸中并定容至100 mL。移取三份25.00 mL溶液,滴加几滴指示剂,用c mol·L-1K Cr O 标准溶液
2 2 7
滴定至终点,半分钟内不恢复原色,消耗K Cr O 标准溶液平均体积为V mL(此时Cl-不被氧化)
2 2 7
[M(FeCl ·4H O)=199 g·mol-1]。
2 2
计算FeCl ·4H O晶体的纯度为 %(用含a、c、V的最简代数式表示)。
2 2
2.(6分)三甲基镓[Ga(CH ) ]是一种重要的半导体材料前驱体。已知[Ga(CH ) ]与盐酸反应生成甲烷,某实验
3 3 3 3
小组用下列方法测定Ga(CH ) 产品的纯度。
3 3
取m g Ga(CH ) 样品于锥形瓶中,加入V mL c mol·L-1盐酸,至不再产生气泡,加入2滴甲基橙,用c
3 3 1
mol·L-1NaOH溶液滴定剩余盐酸,消耗NaOH溶液的体积为V mL,则Ga(CH ) 的质量分数为 (用
1 3 3
含m、V、V 、c、c 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
1 1
(填“偏高”“偏低”或“无影响”)。
3.(8分)硫酸四氨合铜晶体{[Cu(NH ) ]SO ∙H O}在工业上用途广泛,常温下该物质在空气中不稳定,受热
3 4 4 2
时易发生分解。晶体中氨含量的测定方法如下:
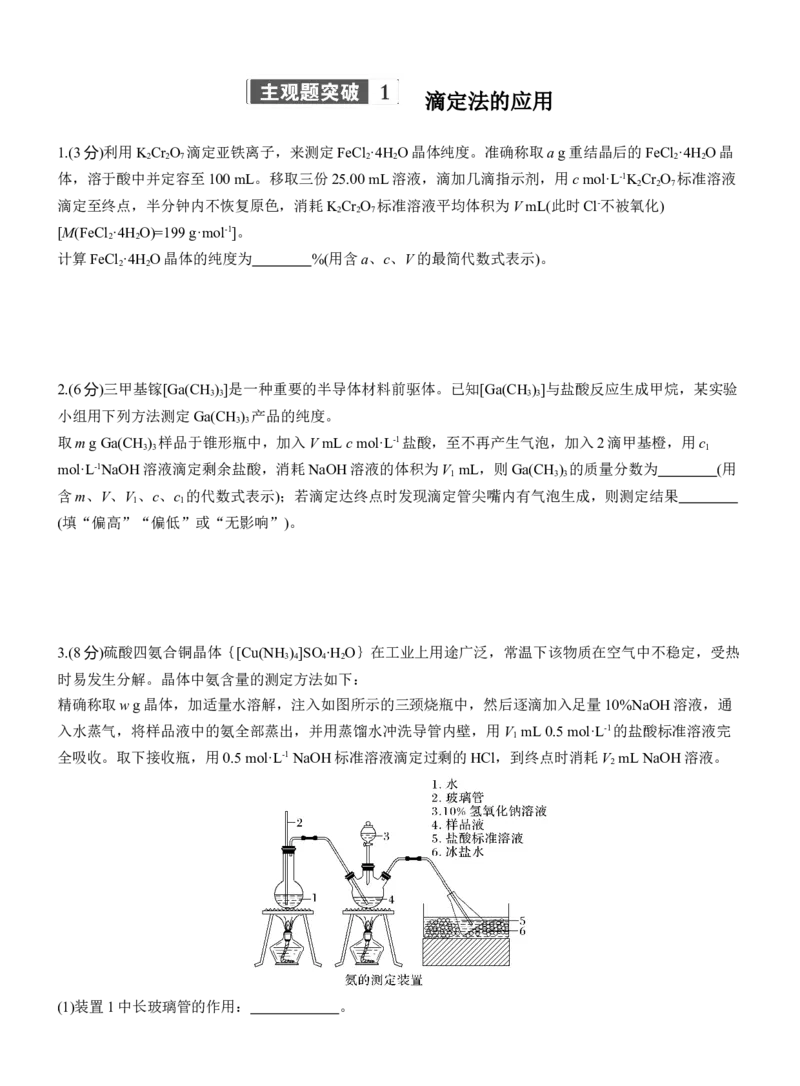
精确称取w g晶体,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入足量10%NaOH溶液,通
入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V mL 0.5 mol·L-1的盐酸标准溶液完
1
全吸收。取下接收瓶,用0.5 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V mL NaOH溶液。
2
(1)装置1中长玻璃管的作用: 。(2)为了减少误差,用NaOH标准溶液滴定过剩的HCl溶液时最好使用 (填“酚酞”或
“甲基橙”)作指示剂。
(3)样品中氨的质量分数为 (用含w、V 、V 的代数式表示)。
1 2
(4)下列实验操作可能使氨含量的测定结果偏高的是 (填字母)。
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.将样品液中的氨全部蒸出后,未用蒸馏水冲洗导管内壁
D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁
4.(6分)亚硝酰硫酸(NOSO H)主要用于重氮化反应。某实验小组用下列方法测定亚硝酰硫酸(NOSO H)的纯
4 4
度。准确称取1.380 g产品放入250 mL的碘量瓶中,加入60.00 mL 0.100 0 mol·L-1的KMnO 标准溶液和10
4
mL 25% H SO 溶液,然后摇匀。用0.250 0 mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00
2 4
mL。已知:2KMnO +5NOSO H+2H O===K SO +2MnSO +5HNO +2H SO 。
4 4 2 2 4 4 3 2 4
(1)写出Na C O 溶液与酸性KMnO 溶液反应的离子方程式: 。
2 2 4 4
(2)滴定终点时的现象为 。
(3)亚硝酰硫酸的纯度= [精确到0.1%,M(NOSO H)=127 g·mol-1]。
4
5.(9分)测定过硫酸钠(Na S O )产品纯度:称取0.250 0 g样品,用蒸馏水溶解,加入过量KI,充分反应后,
2 2 8
再滴加几滴指示剂,用0.100 0 mol·L-1Na S O 标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为
2 2 3
19.50 mL(已知:I +2S O2- ===S O2- +2I-)。
2 2 3 4 6
(1)选用的指示剂是 ,达到滴定终点的现象是 。
(2)样品的纯度为 %。
6.(9分)过氧乙酸(含有少量H O 杂质)的含量测定流程如图。
2 2
取样―→H SO 酸化―→KMnO 溶液除H O ―→―→
2 4 4 2 2
(1)判断H O 恰好除尽的实验现象是 。
2 2
(2)过氧乙酸被Fe2+还原,还原产物之一为乙酸,其离子方程式为 。(3)若样品体积为V mL,加入c mol·L-1 FeSO 溶液V mL,消耗c mol·L-1 K Cr O 溶液V mL。则过氧乙酸
0 1 4 1 2 2 2 7 2
的含量为 g·L-1。
7.(6分)沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-的浓度,可用标准AgNO 溶液滴
3
定待测液。已知:
物质 AgCl AgI AgCN Ag CrO AgSCN
2 4
颜色 白 黄 白 砖红 白
K 1.8×10-10 8.3×10-17 1.2×10-16 3.5×10-11 1.0×10-12
sp
(1)滴定时可选为滴定指示剂的是 (填字母)。
A.NaCl溶液 B.K CrO 溶液
2 4
C.KI溶液 D.NaCN溶液
(2)如何确定该滴定过程的终点: 。
8.(3分)已知:ClNO与H O反应生成HNO 和HCl。通过以下实验测定ClNO样品的纯度。取m g ClNO样
2 2
品溶于水,配制成250 mL溶液,取出25.00 mL样品于锥形瓶中,以K CrO 溶液作为指示剂,用 c mol·L-1
2 4
AgNO 标准溶液滴定至终点,消耗标准溶液的体积为20.00 mL。亚硝酰氯(ClNO)的质量分数为 。
3
[已知:Ag CrO 为砖红色固体;K (AgCl)=1.8×10-10,K (Ag CrO )=3.5×10-11]
2 4 sp sp 2 4答案精析
477.6cV
1.
a
解析 K Cr O 与亚铁离子反应的离子方程式为6Fe2++Cr
O2-
+14H+===6Fe3++2Cr3++7H O,消耗Cr
O2-
的物
2 2 7 2 7 2 2 7
质的量为cV×10-3 mol,消耗Fe2+的物质的量为6cV×10-3 mol,则a g样品中含有Fe2+的物质的量为2.4cV×10-
2.4cV ×10-2×199 477.6cV
2 mol,FeCl ·4H O晶体的纯度为 ×100%= %。
2 2 a a
11.5×(cV -c V )
2. 1 1 % 偏高
3m
解析 NaOH与HCl按物质的量比1∶1反应,与Ga(CH ) 反应的n(HCl)=(cV-c V )×10-3 mol,盐酸与
3 3 1 1
1 (cV -c V )×10-3
Ga(CH ) 的反应为Ga(CH ) +3HCl===GaCl +3CH ↑,样品中n[Ga(CH ) ]= n(HCl)= 1 1
3 3 3 3 3 4 3 3 3 3
(cV -c V )×10-3 0.115×(cV -c V )
mol,样品中m[Ga(CH ) ]= 1 1 mol×115 g·mol-1= 1 1 g,则Ga(CH ) 的质量
3 3 3 3 3 3
0.115×(cV -c V ) 11.5×(cV -c V )
分数为 1 1 ×100%= 1 1 %;若滴定达终点时发现滴定管尖嘴内有气泡生成,
3m 3m
测定的NaOH溶液体积偏小,与Ga(CH ) 反应的盐酸物质的量偏多,Ga(CH ) 的质量偏多,则测定结果偏
3 3 3 3
高。
3.(1)平衡气压,防止堵塞和倒吸 (2)甲基橙
0.85(V -V )
(3) 1 2 % (4)BD
w
解析 (2)由于NaOH标准溶液滴定的是NH Cl和过剩的HCl的混合溶液,滴入NaOH标准溶液的目的是将
4
过剩的盐酸中和,滴定终点为酸性溶液(因为含有NH Cl),所以选择甲基橙作指示剂误差更小。(3)根据关
4
0.85(V -V )
系式NH ~HCl可知,n(NH )=n(HCl)=0.5×10-3(V -V ) mol,则样品中氨的质量分数为 1 2 %。(4)滴
3 3 1 2 w
定时未用NaOH标准溶液润洗滴定管,则相当于稀释了NaOH溶液,V 偏大,氨含量偏低,A项错误;读
2
数时,滴定前平视,滴定后俯视,则V 偏小,氨含量偏高,B项正确;将样品液中的氨全部蒸出后,未用
2
蒸馏水冲洗导管内壁,则部分氨损失,滴定时消耗NaOH溶液的体积偏大,即V 偏大,氨含量偏低,C项
2
错误;未用蒸馏水冲洗插入接收瓶中的导管外壁,则盐酸有损失,导致消耗的NaOH溶液的体积偏小,即
V 偏小,氨含量偏高,D项正确。
2
4.(1)2MnO- +5C O2- +16H+===2Mn2++10CO ↑+8H O (2)滴入最后半滴草酸溶液,溶液恰好由紫红色变为
4 2 4 2 2
无色,且半分钟内不变色 (3)92.0%2
解析
(3)根据关系式:2MnO-
~5C
O2-
,与NOSO H反应的高锰酸钾的物质的量为0.100 0×0.06 mol-
4 2 4 4 5
5
×0.25×0.02 mol=0.004 mol,根据关系式:2KMnO ~5NOSO H,可得NOSO H的物质的量为0.004 mol×
4 4 4 2
0.01mol×127 g·mol-1
=0.01 mol,亚硝酰硫酸的纯度= ×100%≈92.0%。
1.380 g
5.(1)淀粉溶液 滴入最后半滴标准溶液,溶液的蓝色褪去,且半分钟内不恢复蓝色 (2)92.82
解析 (2)Na S O 作氧化剂,与KI反应的离子方程式为S
O2- +2I-===2SO2-
+I ,I 与Na S O 反应的离子方
2 2 8 2 8 4 2 2 2 2 3
程式为I +2S
O2-
===S
O2-
+2I-,可得关系式:Na S O ~I ~2Na S O ,n(Na S O )=0.100 0 mol·L-1×19.50×10-3
2 2 3 4 6 2 2 8 2 2 2 3 2 2 3
1
L=1.95×10-3 mol,则n(Na S O )= n(Na S O )=9.75×10-4 mol,m(Na S O )=9.75×10-4 mol×238 g·mol-1=0.232
2 2 8 2 2 2 3 2 2 8
0.232 05 g
05 g,则该样品的纯度为 ×100%=92.82%。
0.250 0 g
6.(1)当滴入最后半滴高锰酸钾溶液时,溶液由无色变为浅红色,且半分钟内不褪色 (2)CH COOOH+2Fe2+
3
38(c V -6c V )
+2H+===CH COOH+2Fe3++H O (3) 1 1 2 2
3 2 V
0
解析 (1)高锰酸钾溶液为紫红色,过氧化氢没除尽之前,加高锰酸钾,溶液紫红色会褪去,若过氧化氢恰
好除尽,再滴入高锰酸钾溶液,溶液将变为浅红色。(3)Fe2+总物质的量为c V ×10-3 mol,
1 1
n(K Cr O )=c V ×10-3 mol。根据得失电子守恒有:K Cr O ~2Cr3+~6e-~6Fe2+~6Fe3+,即每1 mol K Cr O 与6
2 2 7 2 2 2 2 7 2 2 7
mol Fe2+恰好完全反应,所以与c V ×10-3 mol K Cr O 反应的Fe2+的物质的量为6c V ×10-3 mol,则与过氧乙
2 2 2 2 7 2 2
酸反应的Fe2+的物质的量为c V ×10-3 mol-6c V ×10-3 mol,根据CH COOOH+2Fe2++2H+===CH COOH+2Fe3+
1 1 2 2 3 3
+H O可得,CH COOOH的物质的量为
2 3
c V ×10-3mol-6c V ×10-3mol c V ×10-3mol-6c V ×10-3mol
1 1 2 2 ,CH COOOH的质量为 1 1 2 2 ×76
3
2 2
38(c V ×10-3-6c V ×10-3 ) g
1 1 2 2
g·mol-1=38(c V ×10-3-6c V ×10-3) g,则过氧乙酸的含量为 =
1 1 2 2 V ×10-3L
0
38(c V -6c V )
1 1 2 2 g·L-1。
V
0
7.(1)B (2)当滴入最后半滴标准液时,出现浅红色沉淀,且半分钟内沉淀颜色不改变
解析 (1)指示剂选择原则为颜色变化明显、溶解度微大于AgSCN,根据表中数据可知选K CrO 溶液作为
2 4
指示剂。
1 310c
8. %
m
解析 根据ClNO~HCl~AgNO 关系式,得到25.00 mL样品溶液中n(ClNO)=n(AgNO )=c mol·L-1×0.02
3 3
250 mL
0.02cmol× ×65.5 g·mol-1 1 310c
L=0.02c mol,亚硝酰氯(ClNO)的质量分数为 25.00 mL ×100%= %。
m
mg