文档内容
化学综合实验
考向一 以无机物制备为主线的综合实验
1.有气体参与的物质制备综合题考向分析
2.物质制备型实验题的思维方法
1.[2023·河北,15(1)(2)(3)(4)(5)]配合物Na [Co(NO ) ](M=404 g·mol-1)在分析化学中用于K+的鉴定,其制
3 2 6
备装置示意图(夹持装置等略)如图,步骤如下:
①向三颈烧瓶中加入15.0 g NaNO 和15.0 mL热蒸馏水,搅拌溶解。
2②磁力搅拌下加入5.0 g Co(NO ) ·6H O,从仪器a加入50%醋酸7.0 mL。冷却至室温后,再从仪器b缓
3 2 2
慢滴入30%双氧水8.0 mL。待反应结束,滤去固体。
③在滤液中加入95%乙醇,静置40分钟。固液分离后,依次用乙醇、乙醚洗涤固体产品,称重。
已知:ⅰ.乙醇、乙醚的沸点分别是78.5 ℃、34.5 ℃;
ⅱ.NaNO 的溶解度数据如下表。
2
温度/℃ 20 30 40 50
溶解度/(g/
84.5 91.6 98.4 104.1
100 g H O)
2
回答下列问题:
(1)仪器a的名称是 ,使用前应 。
(2)Na [Co(NO ) ]中钴的化合价是 ,制备该配合物的化学方程式为 。
3 2 6
(3)步骤①中,用热蒸馏水的目的是 。
(4)步骤③中,用乙醚洗涤固体产品的作用是 。
(5)已知:2K++Na++[Co(NO ) ]3- K Na[Co(NO ) ]↓(亮黄色),足量KCl与1.010 g产品反应生
2 6 2 2 6
成0.872 g亮黄色沉淀,产品纯度为 %。
答案 (1)分液漏斗 检漏 (2)+3
12NaNO +2Co(NO ) +H O +2CH COOH===2Na [Co(NO ) ]+4NaNO +2CH COONa+2H O
2 3 2 2 2 3 3 2 6 3 3 2
(3)增加NaNO 的溶解度 (4)加速产品干燥 (5)80
2
解析 (5)已知:2K++Na++[Co(NO ) ]3- K Na[Co(NO ) ]↓(亮黄色),足量KCl与1.010 g产品反
2 6 2 2 6
0.872
应生成0.872 g亮黄色沉淀,则n(K Na[Co(NO ) ])=n(Na [Co(NO ) ])= mol=0.002 mol,
2 2 6 3 2 6 436
0.808
m(Na [Co(NO ) ])=0.002 mol×404 g·mol-1=0.808 g,产品纯度为 ×100%=80%。
3 2 6 1.010
考向二 以有机物制备、提取、纯化为主线的综合实验
解有机物制备类实验题的思维模型
分析制备流程(1)有机化合物易挥发,反应中通常采用冷凝回流装置,以减少有机物
的挥发,提高原料的利用率和产物的产率;
依据有机反应特 (2)有机反应通常都是可逆反应,且易发生副反应,因此常使价格较低
点作答 的反应物过量,以提高另一反应物的转化率和产物的产率,同时在实
验中需要控制反应条件,以减少副反应的发生;
(3)根据产品与杂质的性质差异,选择合适的分离、提纯方法
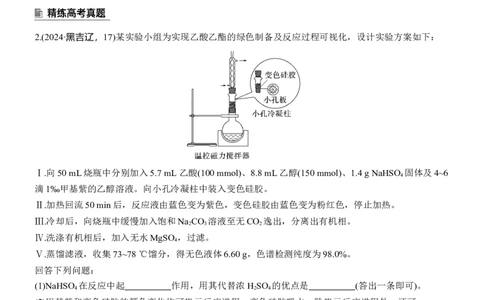
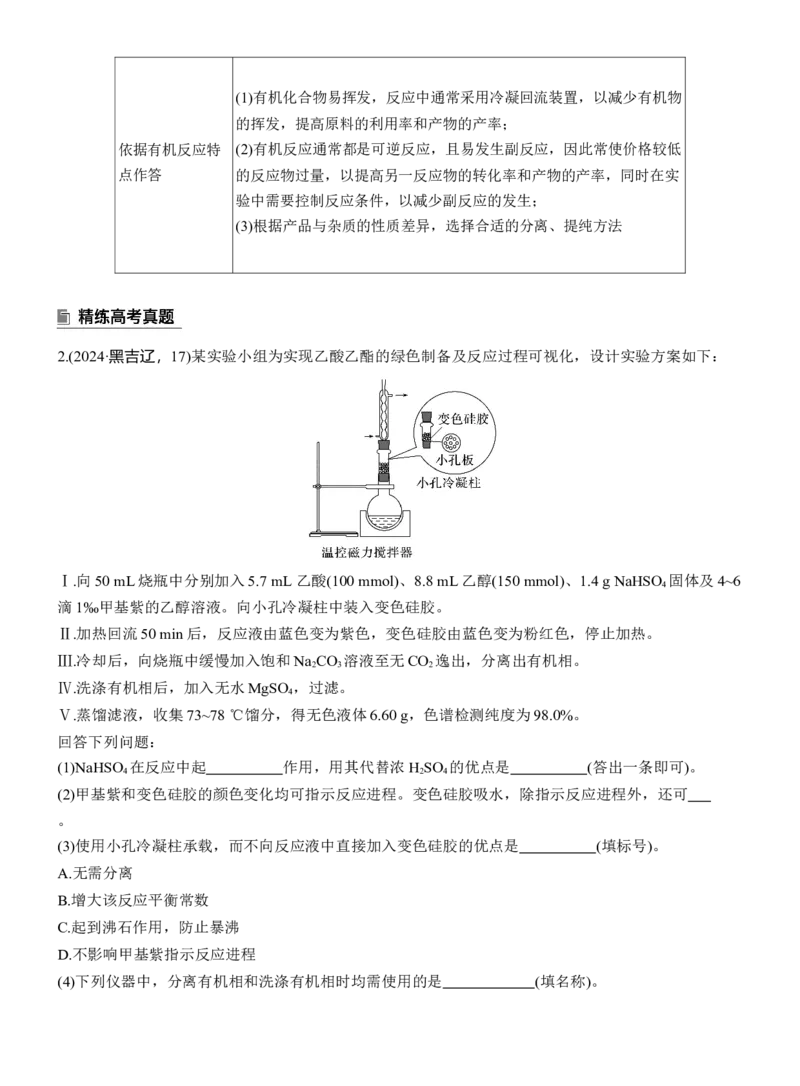
2.(2024·黑吉辽,17)某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验方案如下:
Ⅰ.向50 mL烧瓶中分别加入5.7 mL 乙酸(100 mmol)、8.8 mL乙醇(150 mmol)、1.4 g NaHSO 固体及4~6
4
滴1‰甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
Ⅱ.加热回流50 min后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。
Ⅲ.冷却后,向烧瓶中缓慢加入饱和Na CO 溶液至无CO 逸出,分离出有机相。
2 3 2
Ⅳ.洗涤有机相后,加入无水MgSO ,过滤。
4
Ⅴ.蒸馏滤液,收集73~78 ℃馏分,得无色液体6.60 g,色谱检测纯度为98.0%。
回答下列问题:
(1)NaHSO 在反应中起 作用,用其代替浓H SO 的优点是 (答出一条即可)。
4 2 4
(2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可
。
(3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是 (填标号)。
A.无需分离
B.增大该反应平衡常数
C.起到沸石作用,防止暴沸
D.不影响甲基紫指示反应进程
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是 (填名称)。(5)该实验乙酸乙酯的产率为 (精确至0.1%)。
(6)若改用C H 18 OH作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为
2 5
(精确至1)。
答案 (1)催化剂 无有毒气体二氧化硫产生 (2)吸收生成的水,使平衡正向移动,提高乙酸乙酯的产率
(3)AD (4)分液漏斗 (5)73.5% (6)90
解析 (1)乙酸、乙醇中加浓硫酸制乙酸乙酯时,浓硫酸的作用是催化剂和吸水剂,故本实验NaHSO 在反
4
应中起催化剂作用;浓硫酸还具有强氧化性和脱水性,用浓H SO 时可能发生副反应,且浓硫酸的还原产
2 4
物二氧化硫为有毒气体,用NaHSO 代替浓H SO 的优点是副产物少,可绿色制备乙酸乙酯,无有毒气体
4 2 4
二氧化硫产生。(3)若向反应液中直接加入变色硅胶,反应后需要过滤出硅胶,而使用小孔冷凝柱承载则无
需分离,故A正确;平衡常数只与温度有关,使用小孔冷凝柱承载不能增大该反应平衡常数,故B错误;
小孔冷凝柱承载并没有投入溶液中,不能起到沸石作用,不能防止暴沸,故C错误;由题中“反应液由蓝
色变为紫色,变色硅胶由蓝色变为粉红色”可知,若向反应液中直接加入变色硅胶,则变色硅胶由蓝色变
为粉红色,会影响观察反应液由蓝色变为紫色,使用小孔冷凝柱承载不影响甲基紫指示反应进程,故D正
确。(5)由反应CH COOH+CH CH OH CH COOCH CH +H O可知,100 mmol乙酸与150 mmol乙
3 3 2 3 2 3 2
醇反应时,乙醇过量,理论上可获得的乙酸乙酯的质量为0.1 mol×88 g·mol-1=8.8 g,该实验乙酸乙酯的产
6.60 g×98.0%
率为 ×100%=73.5%。(6)若改用C H 18 OH作为反应物进行反应:CH COOH+CH CH 18 OH
8.8 g 2 5 3 3 2
CH CO18OCH CH +H O,生成的乙酸乙酯的摩尔质量为90 g·mol-1,所以质谱检测目标产物分子
3 2 3 2
离子峰的质荷比数值应为90。
考向三 以物质性质探究为主的综合实验
1.研究物质性质的基本方法和程序
注意事项:(1)若探究影响物质性质的因素,首先应确定变量,其次是“定多变一”,即其他因素不变,只改变一
种因素,看这种因素与探究的问题存在怎样的关系。
(2)多角度辩证地看问题
①研究反应物中各微粒的性质(即内因)。
②研究反应条件的影响(如温度、浓度、环境中的其他物质)。
2.物质性质综合实验探究题的审题思路
强化证据意识:
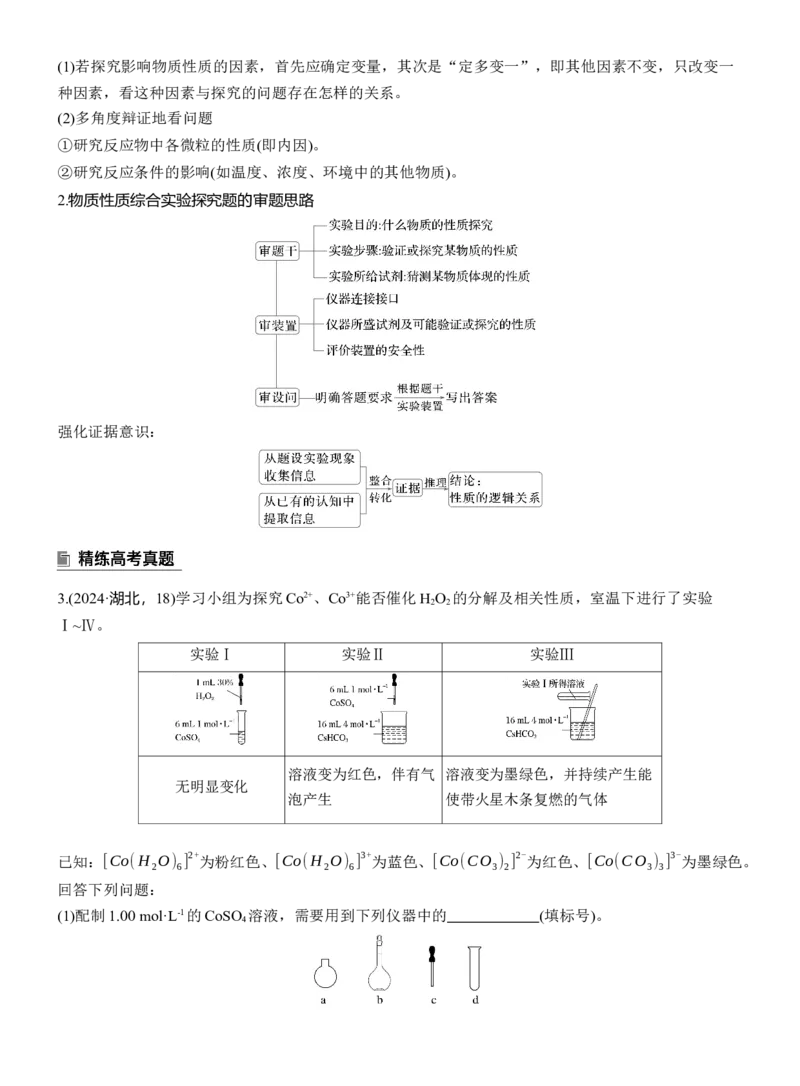
3.(2024·湖北,18)学习小组为探究Co2+、Co3+能否催化H O 的分解及相关性质,室温下进行了实验
2 2
Ⅰ~Ⅳ。
实验Ⅰ 实验Ⅱ 实验Ⅲ
溶液变为红色,伴有气 溶液变为墨绿色,并持续产生能
无明显变化
泡产生 使带火星木条复燃的气体
已知:[Co(H O) ] 2+ 为粉红色、[Co(H O) ] 3+ 为蓝色、[Co(CO ) ] 2- 为红色、[Co(CO ) ] 3- 为墨绿色。
2 6 2 6 3 2 3 3
回答下列问题:
(1)配制1.00 mol·L-1的CoSO 溶液,需要用到下列仪器中的 (填标号)。
4(2)实验Ⅰ表明[Co(H O) ] 2+ (填“能”或“不能”)催化H O 的分解。实验Ⅱ中HCO- 大
2 6 2 2 3
大过量的原因是 。
实验Ⅲ初步表明[Co(CO ) ] 3- 能催化H O 的分解,写出H O 在实验Ⅲ中所发生反应的离子方程式
3 3 2 2 2 2
、 。
(3)实验Ⅰ表明,反应2[Co(H O) ] 2+ +H O +2H+ 2[Co(H O) ]3++2H O难以正向进行,利用化学平衡
2 6 2 2 2 6 2
移动原理,分析Co3+、Co2+分别与CO2-配位后,正向反应能够进行的原因 。
3
(4)实验Ⅳ中,A到B溶液变为蓝色,并产生气体;B到C溶液变为粉红色,并产生气体。从A到C所
产生的气体的分子式分别为 、 。
实验Ⅳ:
答案 (1)bc (2)不能 吸收产生的H+,维持pH,促进反应正向进行
2Co2++10HCO-
3
+H O ===2[Co(CO ) ]3-+6H O+4CO ↑ 2H O 2H O+O ↑ (3)实验Ⅲ的现象表明,Co3+、Co2+分
2 2 3 3 2 2 2 2 2 2
别与CO2- 配位时,[Co(H O) ] 3+ 更易与CO2- 反应生成[Co(CO ) ] 3- (该反应为快反应),导致
3 2 6 3 3 3
[Co(H O) ] 2+ 几乎不能转化为[Co(CO ) ] 2- ,这样使得[Co(H O) ] 3+ 的浓度减小的幅度远远大于
2 6 3 2 2 6
[Co(H O) ] 2+ 减小的幅度,根据化学平衡移动原理,减小生成物浓度能使化学平衡向正反应方向移动,
2 6
因此,上述反应能够正向进行 (4)CO O
2 2
解析 实验Ⅰ中无明显变化,证明 [Co(H O) ] 2+ 不能催化H O 的分解;实验Ⅱ中溶液变为红色,证明
2 6 2 2
[Co(H O) ] 2+ 易转化为[Co(CO ) ] 2- ;实验Ⅲ中溶液变为墨绿色,说明[Co(H O) ] 3+ 更易与CO2- 反应
2 6 3 2 2 6 3
生成[Co(CO ) ] 3- ,并且初步证明[Co(H O) ] 2+ 在HCO- 的作用下易被H O 氧化为[Co(CO ) ] 3- ;实
3 3 2 6 3 2 2 3 3
验Ⅳ中溶液先变蓝后变红,并且前后均有气体生成,证明在酸性条件下,[Co(CO ) ] 3- 易转化为
3 3
[Co(H O) ] 3+ ,[Co(H O) ] 3+ 氧化性强,可以把H O氧化为O 。(2)CoSO 溶液中存在大量的
2 6 2 6 2 2 4
[Co(H O) ] 2+ ,向其中加入30%的H O 后无明显变化,因此实验Ⅰ表明[Co(H O) ] 2+ 不能催化H O 的
2 6 2 2 2 6 2 2
分解。(4)实验Ⅳ中,A到B溶液变为蓝色,并产生气体,说明发生了[Co(CO ) ] 3- +6H++3H O===
3 3 2
[Co(H O) ] 3+ +3CO ↑;B到C溶液变为粉红色,并产生气体,说明发生了4[Co(H O) ] 3+ +2H O===4[Co
2 6 2 2 6 2
(H O) ]2++O ↑+4H+,因此从A到C所产生的气体的分子式分别为CO 和O 。
2 6 2 2 2
题型突破练(A) [分值:50 分]
1.(14分)(2023·河北邢台高三模拟)Na S O 是重要的化学试剂,遇高温分解,与酸发生反应。实验室可通过
2 2 3
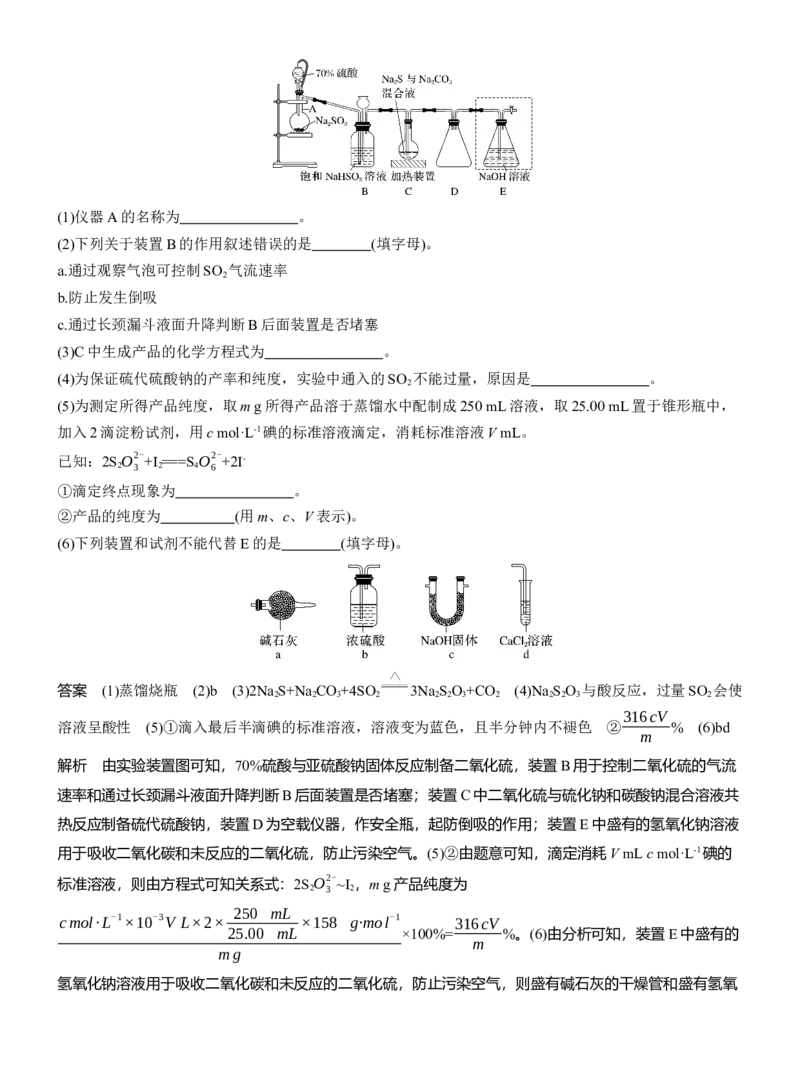
如图所示装置制备Na S O 。
2 2 3(1)仪器A的名称为 。
(2)下列关于装置B的作用叙述错误的是 (填字母)。
a.通过观察气泡可控制SO 气流速率
2
b.防止发生倒吸
c.通过长颈漏斗液面升降判断B后面装置是否堵塞
(3)C中生成产品的化学方程式为 。
(4)为保证硫代硫酸钠的产率和纯度,实验中通入的SO 不能过量,原因是 。
2
(5)为测定所得产品纯度,取m g所得产品溶于蒸馏水中配制成250 mL溶液,取25.00 mL置于锥形瓶中,
加入2滴淀粉试剂,用c mol·L-1碘的标准溶液滴定,消耗标准溶液V mL。
已知:2S O2- +I ===S O2- +2I-
2 3 2 4 6
①滴定终点现象为 。
②产品的纯度为 (用m、c、V表示)。
(6)下列装置和试剂不能代替E的是 (填字母)。
答案 (1)蒸馏烧瓶 (2)b (3)2Na S+Na CO +4SO 3Na S O +CO (4)Na S O 与酸反应,过量SO 会使
2 2 3 2 2 2 3 2 2 2 3 2
316cV
溶液呈酸性 (5)①滴入最后半滴碘的标准溶液,溶液变为蓝色,且半分钟内不褪色 ② % (6)bd
m
解析 由实验装置图可知,70%硫酸与亚硫酸钠固体反应制备二氧化硫,装置B用于控制二氧化硫的气流
速率和通过长颈漏斗液面升降判断B后面装置是否堵塞;装置C中二氧化硫与硫化钠和碳酸钠混合溶液共
热反应制备硫代硫酸钠,装置D为空载仪器,作安全瓶,起防倒吸的作用;装置E中盛有的氢氧化钠溶液
用于吸收二氧化碳和未反应的二氧化硫,防止污染空气。(5)②由题意可知,滴定消耗V mL c mol·L-1碘的
标准溶液,则由方程式可知关系式:2S
O2-
~I ,m g产品纯度为
2 3 2
250 mL
cmol·L-1×10-3V L×2× ×158 g·mol-1 316cV
25.00 mL ×100%= %。(6)由分析可知,装置E中盛有的
m
mg
氢氧化钠溶液用于吸收二氧化碳和未反应的二氧化硫,防止污染空气,则盛有碱石灰的干燥管和盛有氢氧化钠固体的U形管均能代替E,而浓硫酸、氯化钙溶液不能与二氧化碳和二氧化硫反应,则盛有浓硫酸的
洗气瓶和盛有氯化钙溶液的试管均不能代替E。
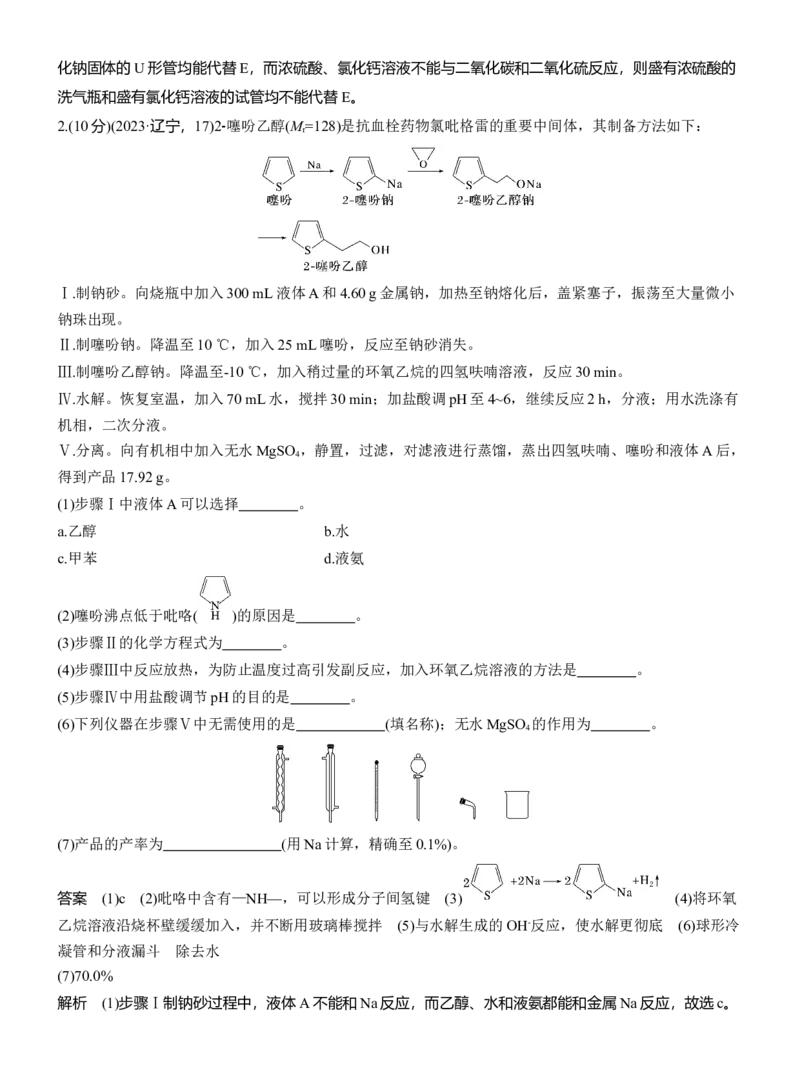
2.(10分)(2023·辽宁,17)2⁃ 噻吩乙醇(M
r
=128)是抗血栓药物氯吡格雷的重要中间体,其制备方法如下:
Ⅰ.制钠砂。向烧瓶中加入300 mL液体A和4.60 g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微小
钠珠出现。
Ⅱ.制噻吩钠。降温至10 ℃,加入25 mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10 ℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30 min。
Ⅳ.水解。恢复室温,加入70 mL水,搅拌30 min;加盐酸调pH至4~6,继续反应2 h,分液;用水洗涤有
机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO ,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A后,
4
得到产品17.92 g。
(1)步骤Ⅰ中液体A可以选择 。
a.乙醇 b.水
c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是 。
(3)步骤Ⅱ的化学方程式为 。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是 。
(5)步骤Ⅳ中用盐酸调节pH的目的是 。
(6)下列仪器在步骤Ⅴ中无需使用的是 (填名称);无水MgSO 的作用为 。
4
(7)产品的产率为 (用Na计算,精确至0.1%)。
答案 (1)c (2)吡咯中含有—NH—,可以形成分子间氢键 (3) (4)将环氧
乙烷溶液沿烧杯壁缓缓加入,并不断用玻璃棒搅拌 (5)与水解生成的OH-反应,使水解更彻底 (6)球形冷
凝管和分液漏斗 除去水
(7)70.0%
解析 (1)步骤Ⅰ制钠砂过程中,液体A不能和Na反应,而乙醇、水和液氨都能和金属Na反应,故选c。(5)2⁃噻吩乙醇钠水解生成2⁃噻吩乙醇的过程中有NaOH生成,用盐酸调节pH的目的是将NaOH中和,使
平衡正向移动,增大反应物的转化率。(6)步骤Ⅴ中的操作有过滤、蒸馏,蒸馏的过程中需要直形冷凝管,
不能用球形冷凝管,无需使用的是球形冷凝管和分液漏斗。(7)步骤Ⅰ中向烧瓶中加入300 mL液体A和
4.60 g
4.60 g金属钠,Na的物质的量为 =0.2 mol,步骤Ⅱ中Na完全反应,根据方程式可知,理论上
23 g·mol-1
17.92 g
可以生成0.2 mol 2⁃噻吩乙醇,产品的产率为
128 g·mol-1×0.2 mol
×100%=70.0%。
3.(10分)(2023·广东清远高三联考)全球对锂资源的需求不断增长,从海水、盐湖中提取锂越来越受到重视。
金属锂(Li)的化学性质与镁相似,在加热的条件下锂能与氮气反应生成氮化锂(Li N,遇水剧烈反应)。某课
3
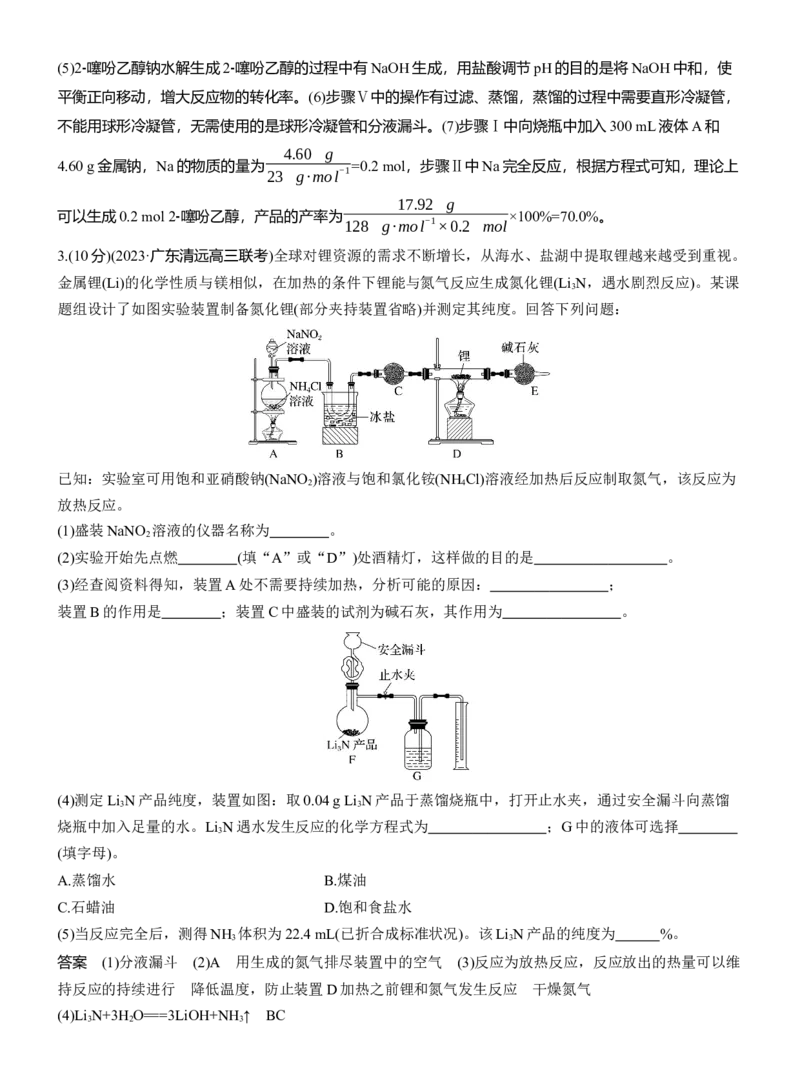
题组设计了如图实验装置制备氮化锂(部分夹持装置省略)并测定其纯度。回答下列问题:
已知:实验室可用饱和亚硝酸钠(NaNO )溶液与饱和氯化铵(NH Cl)溶液经加热后反应制取氮气,该反应为
2 4
放热反应。
(1)盛装NaNO 溶液的仪器名称为 。
2
(2)实验开始先点燃 (填“A”或“D”)处酒精灯,这样做的目的是 。
(3)经查阅资料得知,装置A处不需要持续加热,分析可能的原因: ;
装置B的作用是 ;装置C中盛装的试剂为碱石灰,其作用为 。
(4)测定Li N产品纯度,装置如图:取0.04 g Li N产品于蒸馏烧瓶中,打开止水夹,通过安全漏斗向蒸馏
3 3
烧瓶中加入足量的水。Li N遇水发生反应的化学方程式为 ;G中的液体可选择
3
(填字母)。
A.蒸馏水 B.煤油
C.石蜡油 D.饱和食盐水
(5)当反应完全后,测得NH 体积为22.4 mL(已折合成标准状况)。该Li N产品的纯度为 %。
3 3
答案 (1)分液漏斗 (2)A 用生成的氮气排尽装置中的空气 (3)反应为放热反应,反应放出的热量可以维
持反应的持续进行 降低温度,防止装置D加热之前锂和氮气发生反应 干燥氮气
(4)Li N+3H O===3LiOH+NH ↑ BC
3 2 3(5)87.5
解析 (2)锂化学性质活泼,会与空气中的氧气等反应,实验开始先点燃A处酒精灯,用生成的氮气排尽装
置中的空气。(3)Li N遇水剧烈反应,装置C中盛装的试剂为碱石灰,其作用为干燥氮气。(4)Li N遇水剧
3 3
烈反应,根据质量守恒可知,反应生成氢氧化锂和氨气:Li N+3H O===3LiOH+NH ↑;生成的氨气极易溶
3 2 3
于水,不溶于有机溶剂,故G中的液体选煤油、石蜡油。(5)测得NH 体积为22.4 mL(已折合成标准状况),
3
0.001mol×35 g·mol-1
即0.001 mol,该Li N产品的纯度为 ×100%=87.5%。
3 0.04 g
4.(16分)某小组同学根据Fe3+、Fe2+和Zn2+的氧化性推断溶液中Zn与Fe3+可能先后发生两个反应:2Fe3+
+Zn===2Fe2++Zn2+,Fe2++Zn===Fe+Zn2+,进行如下实验。
实验 试剂 现象
2 mL 0.1 mol·L-1 FeCl 溶液、 黄色溶液很快变浅,接着有无色气泡产
3
Ⅰ
过量锌粉 生,固体中未检出铁
片刻后有大量气体产生,出现红褐色浑
2 mL pH≈0.70的1 mol·L-1
Ⅱ 浊,约半小时后,产生红褐色沉淀,溶液
FeCl 溶液、过量锌粉
3
颜色变浅,产生少量铁
(1)实验Ⅰ结束后,Fe3+的最终还原产物为 。
(2)结合化学用语解释实验Ⅱ中产生红褐色浑浊的原因: 。
(3)实验Ⅲ和Ⅳ:用Fe (SO ) 溶液和Fe(NO ) 溶液替代实验Ⅱ中的FeCl 溶液:
2 4 3 3 3 3
实验 试剂 现象
2 mL pH≈0.70的1 mol·L-1 Fe(NO ) 溶 约半小时后,溶液变为深棕色且浑浊,
3 3
Ⅲ
液、过量锌粉 无铁产生
2 mL pH≈0.70的a mol·L-1 Fe (SO ) 约半小时后,溶液呈浅绿色且浑浊,有
2 4 3
Ⅳ
溶液、过量锌粉 少量铁产生
资料:Fe2++NO [Fe(NO)]2+,[Fe(NO)]2+在溶液中呈棕色。
①a= 。
②甲同学根据实验Ⅲ的现象,判断溶液中一定存在[Fe(NO)]2+,乙同学认为甲的结论不正确。深棕色可能是
生成的 导致的现象。乙同学设计了一个实验证明了深棕色溶液中存在[Fe(NO)]2+。其实验操作和
现象是 。
③对比实验Ⅱ和Ⅲ、Ⅳ,Fe(NO ) 溶液与过量锌粉反应没有生成铁的原因可能是 。
3 3(4)实验Ⅴ:将实验Ⅱ中FeCl 溶液换成FeCl 无水乙醇,加入足量锌粉,片刻后,反应放热,有大量铁产生。
3 3
由实验Ⅰ~Ⅴ可知:反应足够长时间后,锌能否与Fe3+反应得到单质铁,与Zn和Fe3+的物质的量、Fe3+的浓
度、 、 等有关。
答案 (1)Fe2+ (2)FeCl 溶液中存在水解平衡:Fe3++3H O Fe(OH) +3H+,加入锌粉,H+被消耗,Fe3+的
3 2 3
水解平衡正向移动,产生氢氧化铁沉淀 (3)①0.5 ②NO 过滤,取少量深棕色溶液,加热,溶液棕色
2
变浅,液面上方产生红棕色气体
③Fe2+与NO结合生成[Fe(NO)]2+,溶液中Fe2+的浓度减小,使得Fe2+与Zn反应的化学反应速率减小 (4)溶
剂 阴离子种类
解析 (1)向2 mL 0.1 mol·L-1 FeCl 溶液中加入过量锌粉,溶液颜色变浅,固体中没有铁,说明Fe3+的最终
3
还原产物为Fe2+。(3)①实验Ⅲ和Ⅳ是为了探究阴离子的影响,则Fe3+的物质的量应是定量,则
n(Fe3+)=c V =c V ,即1 mol·L-1×2×10-3L=a mol·L-1×2×2×10-3L,解得a=0.5。②NO 是红棕色气体,故推测
1 1 2 2 2
可能是生成的NO 导致的现象;由可逆反应Fe2++NO [Fe(NO)]2+可知,若实验 Ⅲ 中存在[Fe(NO)]2+,加
2
热溶液,会产生NO,NO会被空气中的O 氧化成NO ,则会观察到有红棕色气体产生。③Fe3+和H+、N
2 2
O- 反应生成Fe2+和NO,NO再与Fe2+结合生成[Fe(NO)]2+,而Fe3+和H+、SO2- 不反应,过量Zn与Fe3+反应
3 4
得到Fe2+,Zn再置换出Fe单质。(4)由实验Ⅴ可知,溶剂由水换成无水乙醇,有铁单质生成,则锌能否与
Fe3+反应得到单质铁与溶剂有关,实验Ⅲ和Ⅳ将Cl-换成NO- 和SO2-
,实验Ⅲ中无铁单质生成,则锌能否与
3 4
Fe3+反应得到单质铁与阴离子种类有关。
题型突破练(B) [分值:50 分]
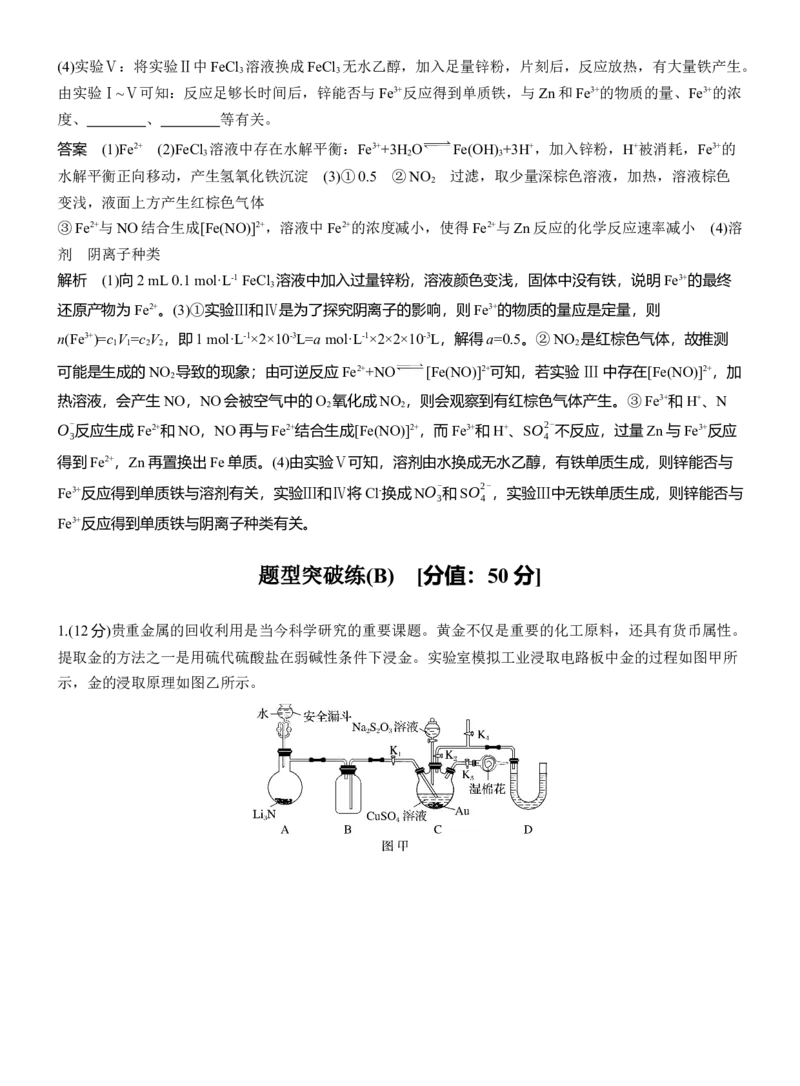
1.(12分)贵重金属的回收利用是当今科学研究的重要课题。黄金不仅是重要的化工原料,还具有货币属性。
提取金的方法之一是用硫代硫酸盐在弱碱性条件下浸金。实验室模拟工业浸取电路板中金的过程如图甲所
示,金的浸取原理如图乙所示。(1)打开K 、K ,关闭K 、K ,向A中烧瓶加水,制取NH 。
1 3 2 4 3
①请写出A装置中发生反应的化学方程式: 。
②安全漏斗的作用除加水外,还有 。
(2)当三颈烧瓶中出现 现象后,关闭K 、K ,打开K 、K ,滴入Na S O 溶液,请补全反应
1 3 2 4 2 2 3
的离子方程式: Au+ S O2- +O + === [Au(S O ) ]3-+ 。
2 3 2 2 3 2
(3)为了验证图乙原理中O 的作用,进行如下实验:关闭K ,反应一段时间后,温度无明显变化,U形管
2 4
内液柱左高右低,三颈烧瓶中溶液蓝色变浅。然后 (填操作和现象),此现象证实了上
述原理中O 的作用。由上述原理可知,[Cu(NH ) ]2+在浸金过程中起 作用。
2 3 4
答案 (1)①Li N+3H O===3LiOH+NH ↑
3 2 3
②液封,防止气体逸出 (2)蓝色沉淀消失 4 8 2H O 4 4OH- (3)打开K ,三颈烧瓶中溶液蓝色复原
2 4
催化
解析 装置A中氮化锂与水反应制取氨,B为安全瓶,防止氨溶于C中溶液时出现倒吸,由图乙可知
Na S O 与Au反应生成[Au(S O ) ]3-,铜离子变成[Cu(NH ) ]2+,该离子与Au反应生成[Cu(NH ) ]+,
2 2 3 2 3 2 3 4 3 2
[Cu(NH ) ]+与氧气反应生成[Cu(NH ) ]2+,通过该转化实现Au的浸取。(2)氨通入三颈烧瓶中与硫酸铜反应
3 2 3 4
先生成氢氧化铜蓝色沉淀,继续通入氨,直至沉淀溶解,关闭K 、K ,打开K 、K ,滴入Na S O 溶液,
1 3 2 4 2 2 3
由题中信息可知1 mol Au失去1 mol电子,1 mol氧气得到4 mol电子,根据得失电子守恒得反应的离子方
程式:4Au+8S
O2-
+O +2H O===4[Au(S O ) ]3-+4OH-。(3)关闭K ,反应一段时间后,温度无明显变化,U
2 3 2 2 2 3 2 4
形管内液柱左高右低,说明气体减少导致压强减小;三颈烧瓶中溶液蓝色变浅,可知[Cu(NH ) ]2+发生反应
3 4
生成[Cu(NH ) ]+。然后打开K ,三颈烧瓶中溶液蓝色复原,说明[Cu(NH ) ]+重新被氧气氧化为
3 2 4 3 2
[Cu(NH ) ]2+,[Cu(NH ) ]2+在浸金过程中作催化剂,实现了Au与氧气的反应。
3 4 3 4
2.(11分)碳酸镧[La (CO ) ,相对分子质量为458]能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸
2 3 3
钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组成员进行实验探究La (CO ) 的制备方法。
2 3 3
已知:①La (CO ) 难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[La(OH)CO ,相对分子质量
2 3 3 3
为216]。
②氯化镧(LaCl )与易溶的碳酸盐或碳酸氢盐反应可制备La (CO ) 。
3 2 3 3
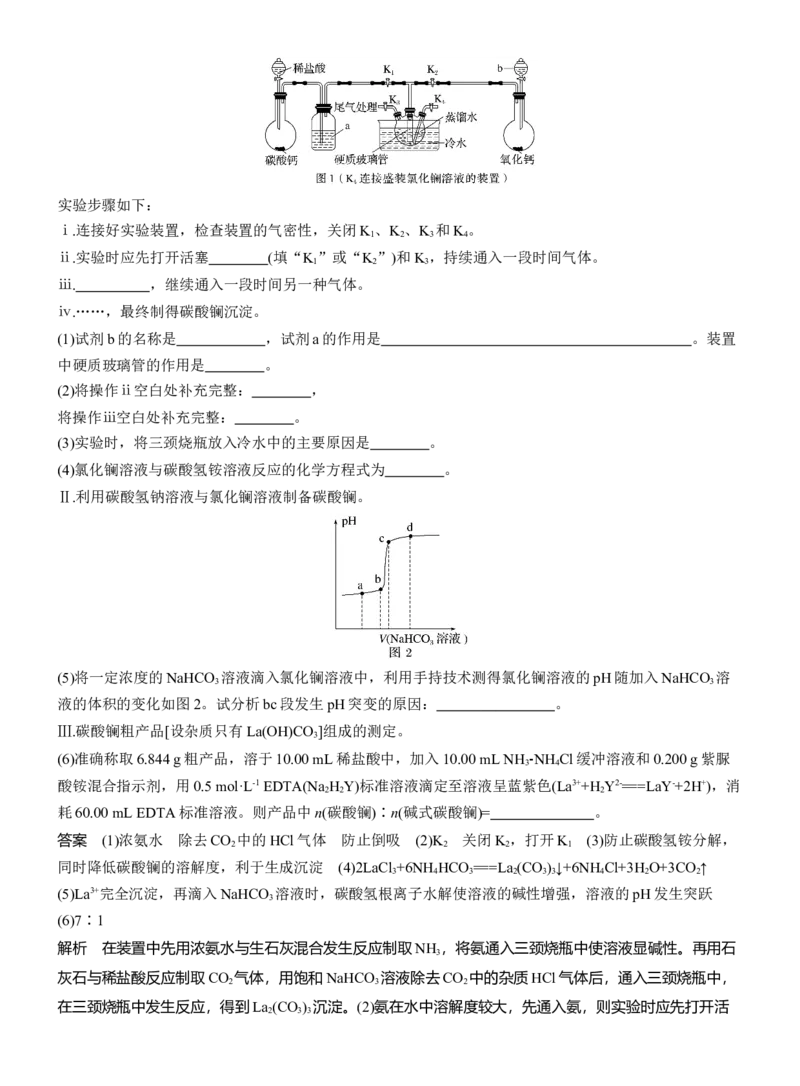
Ⅰ.利用氯化镧溶液与碳酸氢铵溶液制备碳酸镧(装置如图1,其中夹持装置已略去)。实验步骤如下:
ⅰ.连接好实验装置,检查装置的气密性,关闭K 、K 、K 和K 。
1 2 3 4
ⅱ.实验时应先打开活塞 (填“K ”或“K ”)和K ,持续通入一段时间气体。
1 2 3
ⅲ. ,继续通入一段时间另一种气体。
ⅳ.……,最终制得碳酸镧沉淀。
(1)试剂b的名称是 ,试剂a的作用是 。装置
中硬质玻璃管的作用是 。
(2)将操作ⅱ空白处补充完整: ,
将操作ⅲ空白处补充完整: 。
(3)实验时,将三颈烧瓶放入冷水中的主要原因是 。
(4)氯化镧溶液与碳酸氢铵溶液反应的化学方程式为 。
Ⅱ.利用碳酸氢钠溶液与氯化镧溶液制备碳酸镧。
(5)将一定浓度的NaHCO 溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入NaHCO 溶
3 3
液的体积的变化如图2。试分析bc段发生pH突变的原因: 。
Ⅲ.碳酸镧粗产品[设杂质只有La(OH)CO ]组成的测定。
3
(6)准确称取6.844 g粗产品,溶于10.00 mL稀盐酸中,加入10.00 mL NH 3⁃NH
4
Cl缓冲溶液和0.200 g紫脲
酸铵混合指示剂,用0.5 mol·L-1 EDTA(Na H Y)标准溶液滴定至溶液呈蓝紫色(La3++H Y2-===LaY-+2H+),消
2 2 2
耗60.00 mL EDTA标准溶液。则产品中n(碳酸镧)∶n(碱式碳酸镧)= 。
答案 (1)浓氨水 除去CO 中的HCl气体 防止倒吸 (2)K 关闭K ,打开K (3)防止碳酸氢铵分解,
2 2 2 1
同时降低碳酸镧的溶解度,利于生成沉淀 (4)2LaCl +6NH HCO ===La (CO ) ↓+6NH Cl+3H O+3CO ↑
3 4 3 2 3 3 4 2 2
(5)La3+完全沉淀,再滴入NaHCO 溶液时,碳酸氢根离子水解使溶液的碱性增强,溶液的pH发生突跃
3
(6)7∶1
解析 在装置中先用浓氨水与生石灰混合发生反应制取NH ,将氨通入三颈烧瓶中使溶液显碱性。再用石
3
灰石与稀盐酸反应制取CO 气体,用饱和NaHCO 溶液除去CO 中的杂质HCl气体后,通入三颈烧瓶中,
2 3 2
在三颈烧瓶中发生反应,得到La (CO ) 沉淀。(2)氨在水中溶解度较大,先通入氨,则实验时应先打开活
2 3 3塞K 和K ,持续通入一段时间NH ;然后关闭K ,打开K ,继续通入一段时间CO 。(6)根据La3++H Y2-
2 3 3 2 1 2 2
===LaY-+2H+得关系式:La3+~H Y2-,n(H Y2-)=0.5 mol·L-1×0.060 L=0.03 mol,则n(La3+)=0.03 mol,设
2 2
La (CO ) 为x mol,La(OH)CO 为y mol,则2x+y=0.03,458x+216y=6.844,解得x=0.014,y=0.002,n(碳酸
2 3 3 3
镧)∶n(碱式碳酸镧)=0.014∶0.002=7∶1。
3.(11分)(2023·河南新乡统考模拟)苯甲酸可用于医药、染料载体、增塑剂、果汁饮料的保香剂和食品防腐
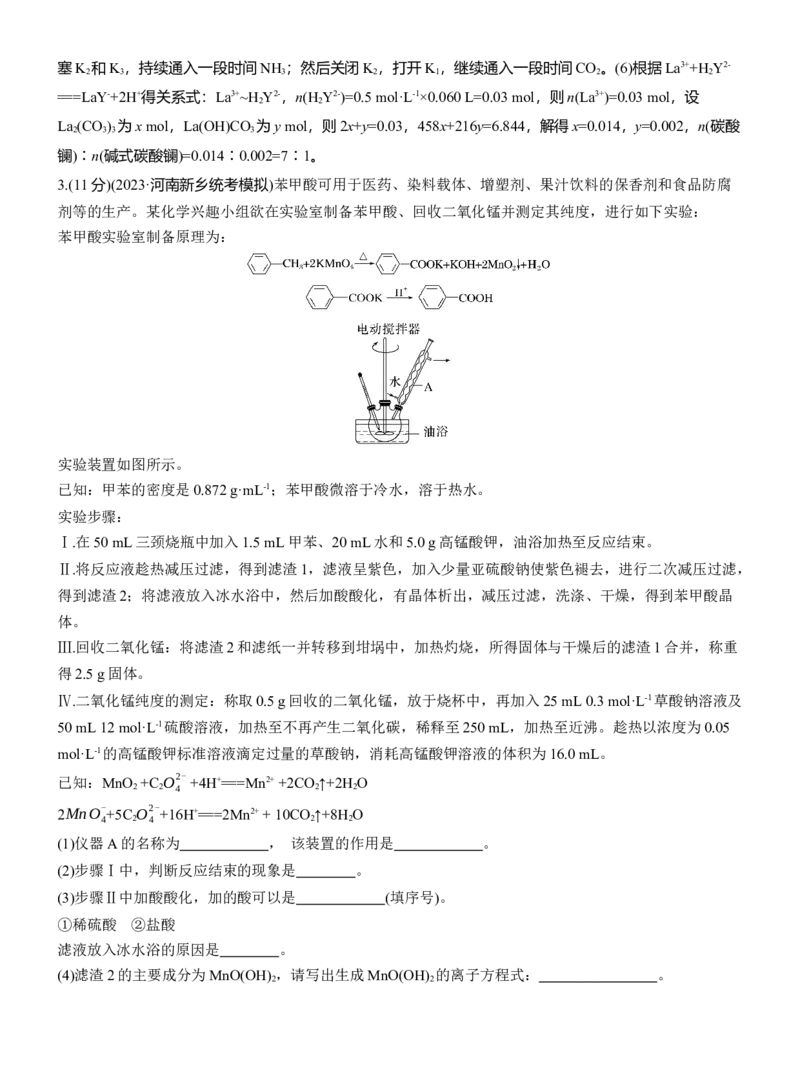
剂等的生产。某化学兴趣小组欲在实验室制备苯甲酸、回收二氧化锰并测定其纯度,进行如下实验:
苯甲酸实验室制备原理为:
实验装置如图所示。
已知:甲苯的密度是0.872 g·mL-1;苯甲酸微溶于冷水,溶于热水。
实验步骤:
Ⅰ.在50 mL三颈烧瓶中加入1.5 mL甲苯、20 mL水和5.0 g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1,滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,
得到滤渣2;将滤液放入冰水浴中,然后加酸酸化,有晶体析出,减压过滤,洗涤、干燥,得到苯甲酸晶
体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中,加热灼烧,所得固体与干燥后的滤渣1合并,称重
得2.5 g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5 g回收的二氧化锰,放于烧杯中,再加入25 mL 0.3 mol·L-1草酸钠溶液及
50 mL 12 mol·L-1硫酸溶液,加热至不再产生二氧化碳,稀释至250 mL,加热至近沸。趁热以浓度为0.05
mol·L-1的高锰酸钾标准溶液滴定过量的草酸钠,消耗高锰酸钾溶液的体积为16.0 mL。
已知:MnO +C O2- +4H+===Mn2+ +2CO ↑+2H O
2 2 4 2 2
2MnO- +5C O2- +16H+===2Mn2+ + 10CO ↑+8H O
4 2 4 2 2
(1)仪器A的名称为 , 该装置的作用是 。
(2)步骤Ⅰ中,判断反应结束的现象是 。
(3)步骤Ⅱ中加酸酸化,加的酸可以是 (填序号)。
①稀硫酸 ②盐酸
滤液放入冰水浴的原因是 。
(4)滤渣2的主要成分为MnO(OH) ,请写出生成MnO(OH) 的离子方程式: 。
2 2(5)用高锰酸钾标准溶液滴定时,滴定终点的现象是 ,二氧化锰的纯度
为 %。
答案 (1)球形冷凝管 冷凝回流,提高反应物的利用率 (2)三颈烧瓶中无油状物
(3)①② 降低苯甲酸的溶解度,使苯甲酸充分析出,提高产率
(4)2MnO- +3SO2- +3H O===2MnO(OH) ↓+3SO2- +2OH-
4 3 2 2 4
(5)当滴加最后半滴高锰酸钾标准溶液时,溶液变为浅红色,且半分钟内不褪色 95.7
解析 甲苯被酸性高锰酸钾氧化为苯甲酸盐,苯甲酸盐与酸反应得到苯甲酸。图示装置中球形冷凝管的目
的是使甲苯冷凝回流,提高反应物的利用率,苯甲酸在三颈烧瓶中生成,由于苯甲酸在冷水中的溶解度较
低,冰水浴有利于其析出。
(3)根据制备原理,苯甲酸盐与酸反应可得到苯甲酸晶体,盐酸和硫酸均可,故选①②;苯甲酸微溶于冷水,
溶于热水,冰水浴的目的是降低苯甲酸的溶解度,使苯甲酸充分析出,提高产率。
(5)草酸根离子能被酸性高锰酸钾氧化,用高锰酸钾标准溶液滴定时,滴定终点的现象是当滴加最后半滴高
锰酸钾标准溶液时,溶液变为浅红色,且半分钟内不褪色;草酸根离子一部分与二氧化锰反应,过量的草
5
酸根离子与高锰酸根离子反应,故二氧化锰消耗的草酸根离子的物质的量为(0.025×0.3- ×0.05×0.016)
2
5
(0.025×0.3- ×0.05×0.016) mol×87 g·mol-1
mol,二氧化锰的纯度为 2 ×100%=95.7%。
0.5 g
4.(16分)环己酮( )是一种重要的化工原料,一种由H O 氧化环己醇制备环己酮的实验方法如
2 2
下:
相关数据如下:
密度/ 沸点/℃ 与水形成共沸
物质 部分性质
(g·cm-3) (101 kPa) 物的沸点/℃
环己 能溶于水,具有还原性,易
0.96 161.0 97.8
醇 被氧化
155.0
环己 微溶于水,遇氧化剂易发生
0.95 98.0 95.0
酮 开环反应
/3.4 kPa(1)FeCl 的作用是 ;加入食盐的目的是 。
3
(2)环己酮的产率受H O 用量的影响,当环己酮产率达最大值后,增加H O 的用量其产率反而下降,原因
2 2 2 2
是 。
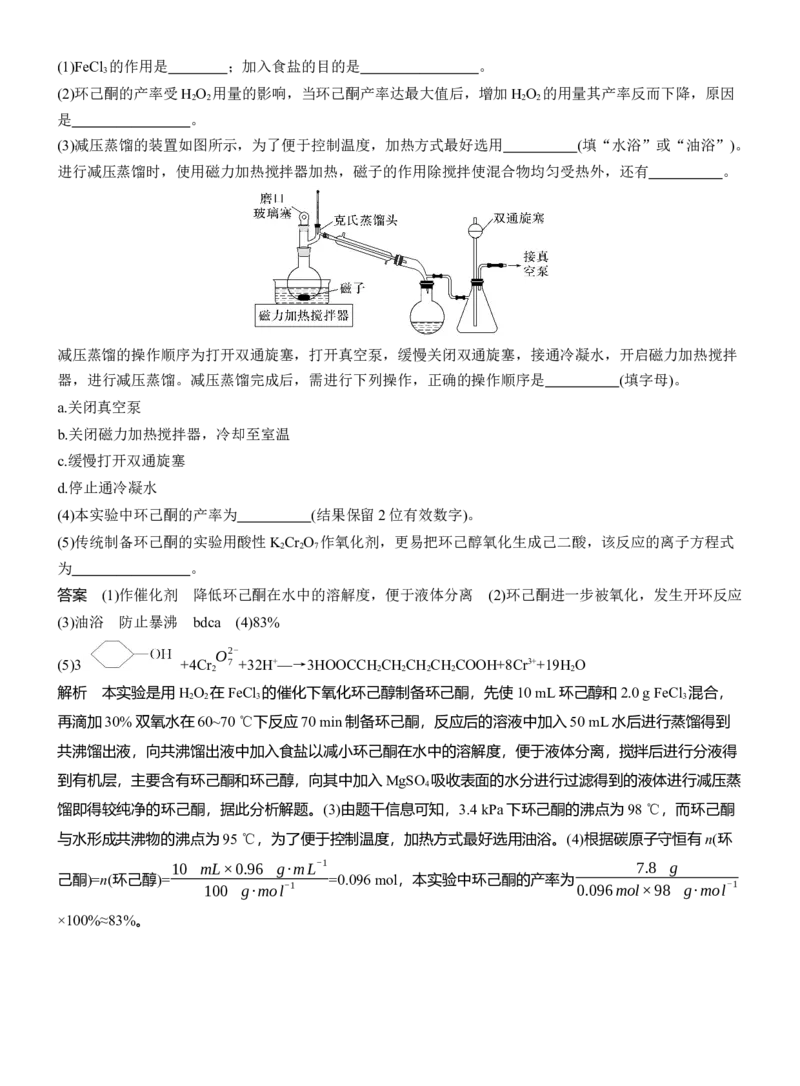
(3)减压蒸馏的装置如图所示,为了便于控制温度,加热方式最好选用 (填“水浴”或“油浴”)。
进行减压蒸馏时,使用磁力加热搅拌器加热,磁子的作用除搅拌使混合物均匀受热外,还有 。
减压蒸馏的操作顺序为打开双通旋塞,打开真空泵,缓慢关闭双通旋塞,接通冷凝水,开启磁力加热搅拌
器,进行减压蒸馏。减压蒸馏完成后,需进行下列操作,正确的操作顺序是 (填字母)。
a.关闭真空泵
b.关闭磁力加热搅拌器,冷却至室温
c.缓慢打开双通旋塞
d.停止通冷凝水
(4)本实验中环己酮的产率为 (结果保留2位有效数字)。
(5)传统制备环己酮的实验用酸性K Cr O 作氧化剂,更易把环己醇氧化生成己二酸,该反应的离子方程式
2 2 7
为 。
答案 (1)作催化剂 降低环己酮在水中的溶解度,便于液体分离 (2)环己酮进一步被氧化,发生开环反应
(3)油浴 防止暴沸 bdca (4)83%
O2-
(5)3 +4Cr 7 +32H+—→3HOOCCH CH CH CH COOH+8Cr3++19H O
2 2 2 2 2 2
解析 本实验是用H O 在FeCl 的催化下氧化环己醇制备环己酮,先使10 mL环己醇和2.0 g FeCl 混合,
2 2 3 3
再滴加30% 双氧水在60~70 ℃下反应70 min制备环己酮,反应后的溶液中加入50 mL水后进行蒸馏得到
共沸馏出液,向共沸馏出液中加入食盐以减小环己酮在水中的溶解度,便于液体分离,搅拌后进行分液得
到有机层,主要含有环己酮和环己醇,向其中加入MgSO 吸收表面的水分进行过滤得到的液体进行减压蒸
4
馏即得较纯净的环己酮,据此分析解题。(3)由题干信息可知,3.4 kPa下环己酮的沸点为98 ℃,而环己酮
与水形成共沸物的沸点为95 ℃,为了便于控制温度,加热方式最好选用油浴。(4)根据碳原子守恒有n(环
10 mL×0.96 g·mL-1 7.8 g
己酮)=n(环己醇)= =0.096 mol,本实验中环己酮的产率为
100 g·mol-1 0.096mol×98 g·mol-1
×100%≈83%。