文档内容
沈阳市第 120 中学 2023-2024 学年度上学期
高三年级第一次质量监测
化学试题
满分:100分 时间:75分钟 命题人:马明阳 赵敏芳 校对人:马明阳
可能用到的相对原子质量:C-12 O-16 Mg-24 Cl-35.5 Fe-56 Cu-64 I-127
一、选择题(每小题只有一个选项最符合题意,每小题3分,共45分)
1.化学与生活、生产密切相关。下列叙述正确的是
A.汽油、生物柴油、石蜡油的主要成分都是烃类
B.节日烟花呈现的是钠、钾、钡等金属单质的焰色,与电子跃迁有关
C.K FeO 在水处理过程中涉及:蛋白质变性、胶体聚沉、盐类水解、氧化还原
2 4
反应
D.氯化钙、生石灰、硫酸亚铁等都是食品包装袋中常用的干燥剂
2.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1molCl 与足量Fe 反应,转移的电子数为2N
2 A
B.32.5gFeCl 水解形成的Fe(OH) 胶粒数为0.2N
3 3 A
C.0.05mol·L-1NaHSO 溶液中,阳离子的数目为0.1N
4 A
D.5.6gFe 粉与足量水蒸气反应生成的H 在标况下的体积为2.24L
2
3.中国传统文化对人类文明贡献巨大。下列对文献记载内容理解正确的是
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.《天工开物》记载“凡火药,硫为纯阳,硝为纯阴”,“硫”“硝”分别指的是硫黄、
硝酸钾
C.《本草纲目》记载“盖此矾色绿,味酸,烧之则赤…”,矾指的是CuSO ·5H O
4 2
D.青铜为铜锌合金,博物馆中贵重青铜器常放在银质托盘上
4.下列各组离子能大量共存的是
A.使酚酞指示剂变红的溶液:NO -、Cl-、CO 2-、Na+
3 3
B.室温下,pH=1 的溶液:K+、NH +、Cl-、S2-
4
C.饱和SO 水溶液:Ba2+、Na+、Cl-、NO -
2 3
D.含有Fe2+的溶液中:K+、Na+、[Fe(CN) ]3-、Cl-
6
共8页 第 1 页
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}5.锰酸钾 (K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO22H O2MnOMnO 4OH。利用Cl 氧化K MnO 制备KMnO 的装
4 2 4 2 2 2 4 4
置如图所示(夹持装置略)。下列说法正确的是
A.装置甲中的固体可以是KClO
3
B.装置乙中放饱和NaHCO 溶液,以提高 KMnO 的产率
3 4
C.装置丙可以用NaOH作碱性介质
D.装置丙中每消耗0.5molCl ,则生成1molKMnO
2 4
6. 下列离子方程式书写正确的是
A.向Ca(ClO) 溶液中通入少量SO :
2 2
Ca2++3ClO-+SO +H O=CaSO ↓+2HClO+Cl-
2 2 4
B.向碳酸氢铵溶液中加入足量Ca(OH) 溶液:
2
Ca2++HCO+OH-=CaCO ↓+H O
3 3 2
C.酸化的高锰酸钾溶液与H O 溶液反应:
2 2
2MnO+3H O +6H+=2Mn2++3O ↑+6H O
4 2 2 2 2
D.稀硫酸与硫代硫酸钠溶液反应:
S O 2-+SO 2-+4H+=2SO ↑+S↓+2H O
2 3 4 2 2
7.氯气跟氢氧化钾溶液在一定条件下发生反应:Cl +KOH→KX+KY+H O(未配
2 2
平),KX在一定条件下能反应:KX→KY+KZ(未配平,KY与KZ 的物质的量之
比为1:3),以上KX、KY、KZ 均是含氯元素的一元酸的钾盐,推知在KX 中
氯元素的化合价是
A.+1 B.+3 C.+5 D.+7
共8页 第 2 页
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}8.补骨脂素对白血病细胞有较强的杀伤作用,其结构如图所示。
下列有关补骨脂素的说法正确的是
A.分子式为C HO B.该物质不易溶于水
11 8 3
C.所有原子不可能共平面 D.1mol 该物质最多可与6molH 反应
2
9.下列制备物质的工业生产流程合理的是
电解 石灰乳
A.由NaCl 制漂白粉:NaCl(aq) → Cl → 漂白粉
2
石灰乳 灼烧 电解
B.海水制镁:海水 → Mg(OH) → MgO → Mg
2
电解
C.由铝土矿冶炼铝:铝土矿 → Al
冰晶石
CO NH 加热
2 3
D.由食盐水制备纯碱:NaCl 溶液→→ NaHCO → Na CO
3 2 3
10.某无色混合气体中可能含有CO、H 、SO 、Cl 、HCl 中的一种或几种。将
2 2 2
此混合气体依次通入少量澄清石灰水、少量品红溶液,现象分别为无沉淀生成和
品红溶液褪色。继续将气体通入足量的氢氧化钠溶液,剩余的气体干燥后通过足
量红热的CuO粉末,粉末变成红色。最后再通入CaCl 溶液中,无沉淀生成。
2
则下列叙述正确的是
A.澄清石灰水中无沉淀,说明一定不含有SO
2
B.品红溶液褪色,可能是Cl 导致的
2
C.氧化铜粉末变红,说明CO和H 中至少有一种
2
D.CaCl 溶液中无沉淀,说明通过CuO后得到的气体中一定不含有CO
2 2
11.抗生素克拉维酸的结构简式如图所示,
下列关于克拉维酸的说法错误的是
A.存在顺反异构体
B.含有5种官能团
C.可形成分子内氢键和分子间氢键
D.1mol该物质最多可与1molNaOH 反应
共8页 第 3 页
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}12.下列实验设计及操作能达到相应实验目的的是
选项 实验目的 实验设计及操作
验证溴与苯发生取代 向苯与液溴的混合液中加入铁粉,将产生的气体通入
A
反应 AgNO 溶液中
3
证明乙二醇氧化成乙
B 向足量的酸性KMnO 溶液中加入乙二醇
4
二酸
C 证明Na O 没有变质 取久置的Na O 粉末,向其中滴加过量的盐酸
2 2 2 2
验证淀粉是否水解完 向淀粉溶液中加适量20%H SO 溶液,加热,冷却后
2 4
D
全 滴加少量碘水
13.含同种短周期主族元素的五种常见物质A、B、C、D、E 的转化关系如图所
示,其中A为单质。下列说法错误的是
A.若B、C均为氧化物,则A可能为碳单质
B.若D为Na CO ,则A一定为钠单质
2 3
C.若C、D均为氧化物,则A一定为非金属单质
D.若E为含氧强酸,则B 与C 可能反应生成A
14.某化学实验小组设计如下实验探究Zn 与溶液中Fe3+发生反应的原理。
实验 试剂 现象
2mL0.1 mol·L-1FeCl 溶 黄色溶液很快变浅,接着有无色气泡产生,固体
3
I
液、过量锌粉 中未检出铁单质
很快有大量气体产生,出现红褐色浑浊,30min
2mL1 mol·L-1FeCl 溶
3
Ⅱ 左右产生红褐色沉淀,溶液颜色变浅,产生少量
液(pH≈0.70)、过量锌粉
铁单质
下列说法错误的是
A.实验I说明Fe3+被还原为Fe2+
B.可用酸性KMnO 溶液检验实验I 得到的溶液中含有Fe2+
4
C.实验Ⅱ发生了置换反应和复分解反应
D.实验说明Fe3+、H+与Zn 的反应与离子浓度有关
共8页 第 4 页
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}15.Ag 是高新技术产业的基础材料之一,在一种光盘金属层中回收少量银(金属
层中其他金属含量过低,对实验的影响可忽略)的工艺流程如下:
已知:NaClO溶液在受热或酸性条件下易分解。则下列有关叙述正确的是
A.“氧化”过程最适宜的反应条件是加热和强酸性
B.“操作1”所用到的玻璃仪器是玻璃棒、烧杯、分液漏斗
C.“还原”过程中参加反应的n([Ag(NH ) ]+):n(N H ·H O)=1:4
3 2 2 4 2
D.AgCl 溶解在10%氨水中的化学方程式为:AgCl+2NH =[Ag(NH ) ]Cl
3 3 2
二、填空题(本题共4小题,共55分)
16.(14分)碘化亚铜(CuI)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业
上由冰铜制取无水碘化亚铜的流程。回答下列问题:
(1)步骤①中Cu S被转化为Cu,同时有大气污染物A生成,相关反应的化学方程
2
式为 。
(2)熔渣B 主要成分为黑色磁性物质,其化学式为 。
(3)步骤②中当温度高于40℃时,反应速率减慢,原因是 。
(4)步骤③中加入过量NaI涉及的主要反应的离子方程式为 。
(5)步骤④用乙醇洗涤的优点是 。
(6)准确称取m gCuI样品,加入足量的Fe (SO ) 溶液,发生反应为
2 4 3
2CuⅠ+4Fe3+=2Cu2++4Fe2++I ,待样品完全反应后,用amol/L酸性KMnO 溶液滴
2 4
定Fe(Ⅱ),消耗标准液的体积平均值为ⅴmL。样品中CuI的质量分数的计算表达
式为 。如果滴定前,滴定管未用标准液润洗,CuI的质量
分数 (填“偏低”、“偏高”或“无影响”)。
共8页 第 5 页
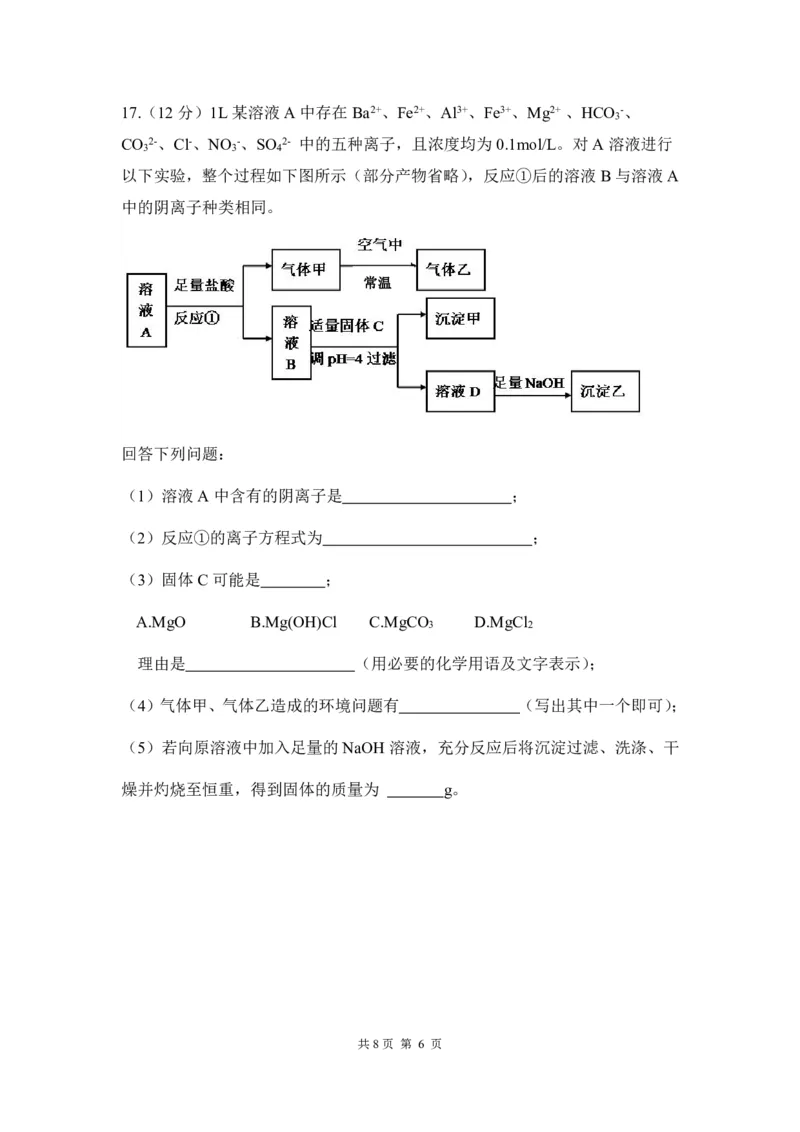
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}17.(12分)1L某溶液A中存在Ba2+、Fe2+、Al3+、Fe3+、Mg2+、HCO -、
3
CO 2-、Cl-、NO -、SO 2- 中的五种离子,且浓度均为0.1mol/L。对A 溶液进行
3 3 4
以下实验,整个过程如下图所示(部分产物省略),反应①后的溶液B与溶液A
中的阴离子种类相同。
常温
回答下列问题:
(1)溶液A中含有的阴离子是 ;
(2)反应①的离子方程式为 ;
(3)固体C 可能是 ;
A.MgO B.Mg(OH)Cl C.MgCO D.MgCl
3 2
理由是 (用必要的化学用语及文字表示);
(4)气体甲、气体乙造成的环境问题有 (写出其中一个即可);
(5)若向原溶液中加入足量的NaOH 溶液,充分反应后将沉淀过滤、洗涤、干
燥并灼烧至恒重,得到固体的质量为 g。
共8页 第 6 页
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}18.(15分)草酸亚铁(FeC O )常用作照相显影剂、新型电池材料等。实验室中
2 4
以铁粉为原料,制备水合草酸亚铁(FeC O ·xH O)的流程如图所示:
2 4 2
已知:
Ⅰ.草酸亚铁晶体为淡黄色粉末,难溶于水。
Ⅱ.pH4时,Fe2+易被氧气氧化。
回答下列问题:
(1)用铁屑制备硫酸亚铁铵[(NH ) Fe(SO ) ]时,为防止被氧化,可采用下列装置
4 2 4 2
进行实验:
①整个实验要先制备FeSO 溶液,然后使A中制得的FeSO 溶液进入B中发生
4 4
反应制备硫酸亚铁铵溶液。制备硫酸亚铁铵溶液时需 (填“打开”或“关闭”,
下同)分液漏斗的活塞、 K 、 K ;
1 2
②B 中应加入 (填化学式)。
(2)“制备”时加入H C O 而不是Na C O 等草酸盐的原因是 ,涉及的
2 2 4 2 2 4
主要离子方程式是 。
(3)析出水合草酸亚铁晶体后,需经过静置、 、低温烘干等操作,
得到干燥的水合草酸亚铁晶体。欲检验溶液A中Fe2+是否被氧化,可选用的化
学试剂是 (写名称)。
(4)已知:FeC O ·2H O(M=180g/mol)受热分解
2 4 2
时,固体质量随温度变化的曲线如图所示。加
热到400℃时,固体的成分是 (填化学
式)。
共8页 第 7 页
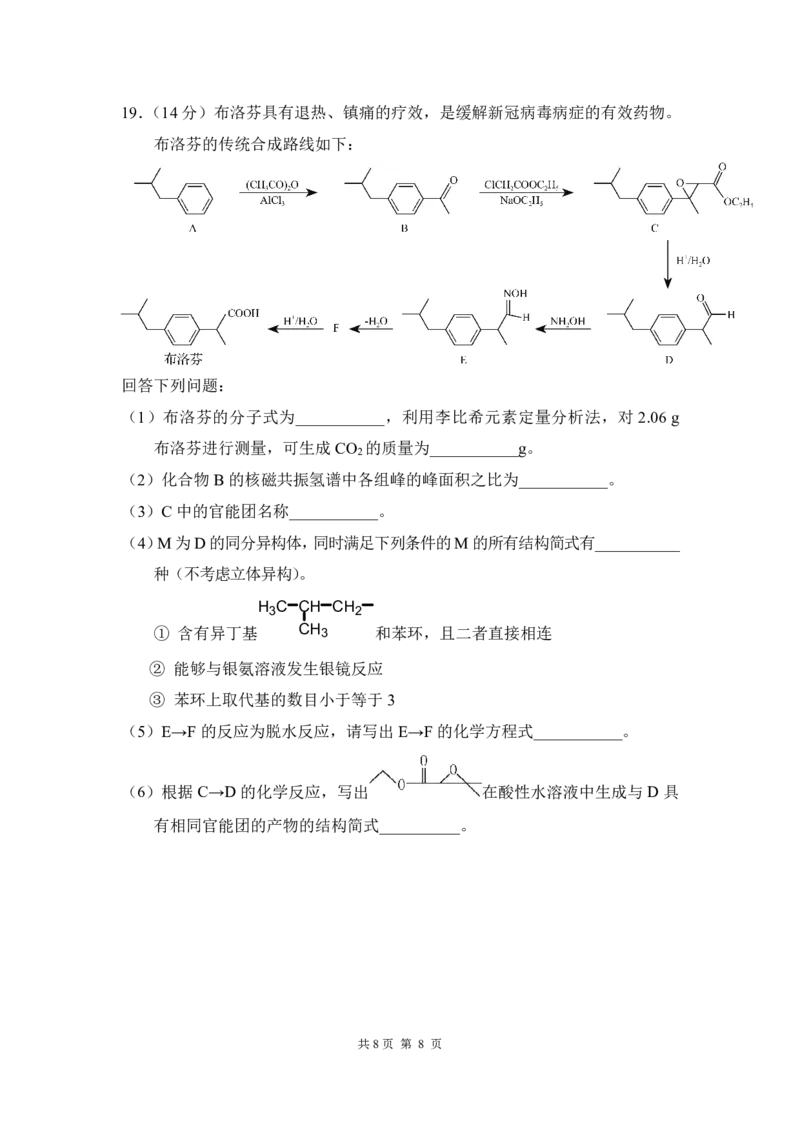
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}19.(14分)布洛芬具有退热、镇痛的疗效,是缓解新冠病毒病症的有效药物。
布洛芬的传统合成路线如下:
回答下列问题:
(1)布洛芬的分子式为___________,利用李比希元素定量分析法,对 2.06 g
布洛芬进行测量,可生成CO 的质量为___________g。
2
(2)化合物B 的核磁共振氢谱中各组峰的峰面积之比为___________。
(3)C 中的官能团名称___________。
(4)M为D的同分异构体,同时满足下列条件的M的所有结构简式有___________
种(不考虑立体异构)。
H C CH CH
3 2
① 含有异丁基 CH 3 和苯环,且二者直接相连
② 能够与银氨溶液发生银镜反应
③ 苯环上取代基的数目小于等于3
(5)E→F 的反应为脱水反应,请写出 E→F 的化学方程式___________。
(6)根据C→D 的化学反应,写出 在酸性水溶液中生成与D 具
有相同官能团的产物的结构简式__________。
共8页 第 8 页
{#{QQABIY6UggCoQBBAABgCUQVyCAOQkBEAAIgGwAAIIAAAyRFABAA=}#}