文档内容
2024 年高三教学测试
化学试题卷
(2024.04)
可能用到的相对原子质量:
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1.下列物质中含有共价键的盐是( )
A. B. C. D.
2.工业上将 通入到 的饱和 溶液中制取 ,下列说法不正确的是( )
A.食品膨松剂的成份之一是 B. 电离出 使 溶液显酸性
C. 不稳定,受热容易分解 D.盐酸与 反应放出大量气泡并吸收热量
3.下列表示不正确的是( )
A. 的电子式: B. 的价层电子对互斥模型:
C. 的 键的模型: D. 的名称:1,3,4-三甲苯
4.高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理,制备的一种方法其原理:
,下列说法不正确的是( )
A. 是还原剂 B. 既不是还原产物也不是氧化产物
C.生成 ,转移 电子 D.氧化产物与还原产物的物质的量之比为
5.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 溶液:
B. 的溶液:
C.水电离产生的 的溶液:D.使甲基橙变红的溶液:
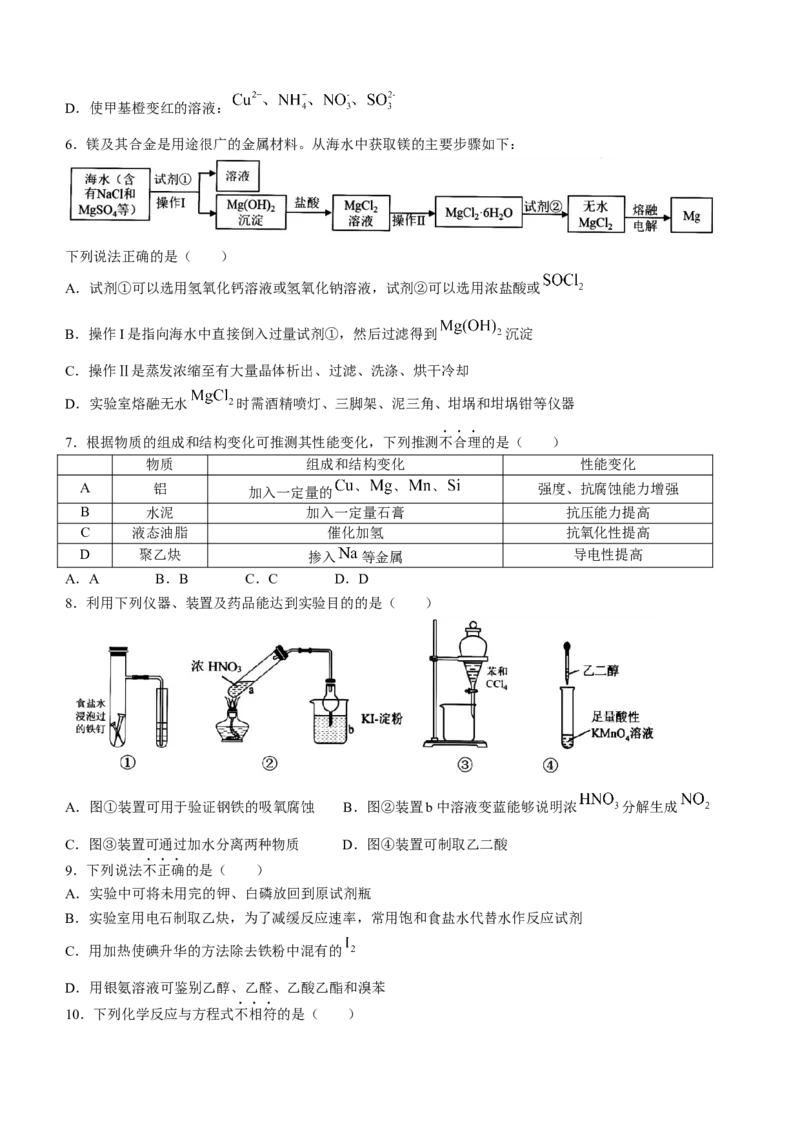
6.镁及其合金是用途很广的金属材料。从海水中获取镁的主要步骤如下:
下列说法正确的是( )
A.试剂①可以选用氢氧化钙溶液或氢氧化钠溶液,试剂②可以选用浓盐酸或
B.操作I是指向海水中直接倒入过量试剂①,然后过滤得到 沉淀
C.操作Ⅱ是蒸发浓缩至有大量晶体析出、过滤、洗涤、烘干冷却
D.实验室熔融无水 时需酒精喷灯、三脚架、泥三角、坩埚和坩埚钳等仪器
7.根据物质的组成和结构变化可推测其性能变化,下列推测不合理的是( )
物质 组成和结构变化 性能变化
A 铝 加入一定量的 强度、抗腐蚀能力增强
B 水泥 加入一定量石膏 抗压能力提高
C 液态油脂 催化加氢 抗氧化性提高
D 聚乙炔 掺入 等金属 导电性提高
A.A B.B C.C D.D
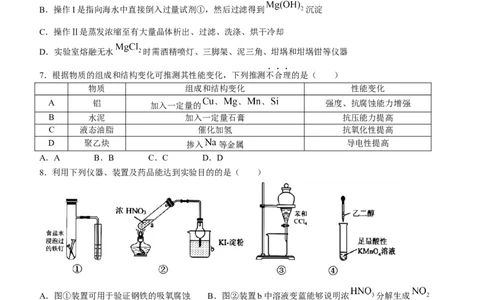
8.利用下列仪器、装置及药品能达到实验目的的是( )
A.图①装置可用于验证钢铁的吸氧腐蚀 B.图②装置b中溶液变蓝能够说明浓 分解生成
C.图③装置可通过加水分离两种物质 D.图④装置可制取乙二酸
9.下列说法不正确的是( )
A.实验中可将未用完的钾、白磷放回到原试剂瓶
B.实验室用电石制取乙炔,为了减缓反应速率,常用饱和食盐水代替水作反应试剂
C.用加热使碘升华的方法除去铁粉中混有的
D.用银氨溶液可鉴别乙醇、乙醛、乙酸乙酯和溴苯
10.下列化学反应与方程式不相符的是( )A.向银氨溶液中加入过量盐酸:
B. 溶液中加入 产生沉淀:
C.将二氧化硫通入氢硫酸中产生黄色沉淀:
D.乙醇与 酸性溶液反应:
11.聚乙烯醇缩甲醛(维纶)是一种优质的合成材料,可用于生产服装、绳索等,一种合成路线如下所示。
下列说法不正确的是( )
A.X的结构简式为 B.试剂Y可以是氢氧化钠溶液
C.甲醛易溶于水,其水溶液具有杀菌、防腐的作用 D.生成 需要 和
12.化合物 可用作电极材料,其中X、Y、Z为原子序数依次增大的短周期元素,X、Y同周期,Y
原子的电子总数与Z原子的L层电子数相等。基态W原子的价层电子排布式为 。该电极材料
所含阴离子的结构如图所示。下列说法不正确的是( )
A.简单离子半径: B.简单氢化物的熔沸点:
C.X单质在Y单质中燃烧,其产物中含有非极性共价键 D.W原子有15种空间运动状态不同的电子
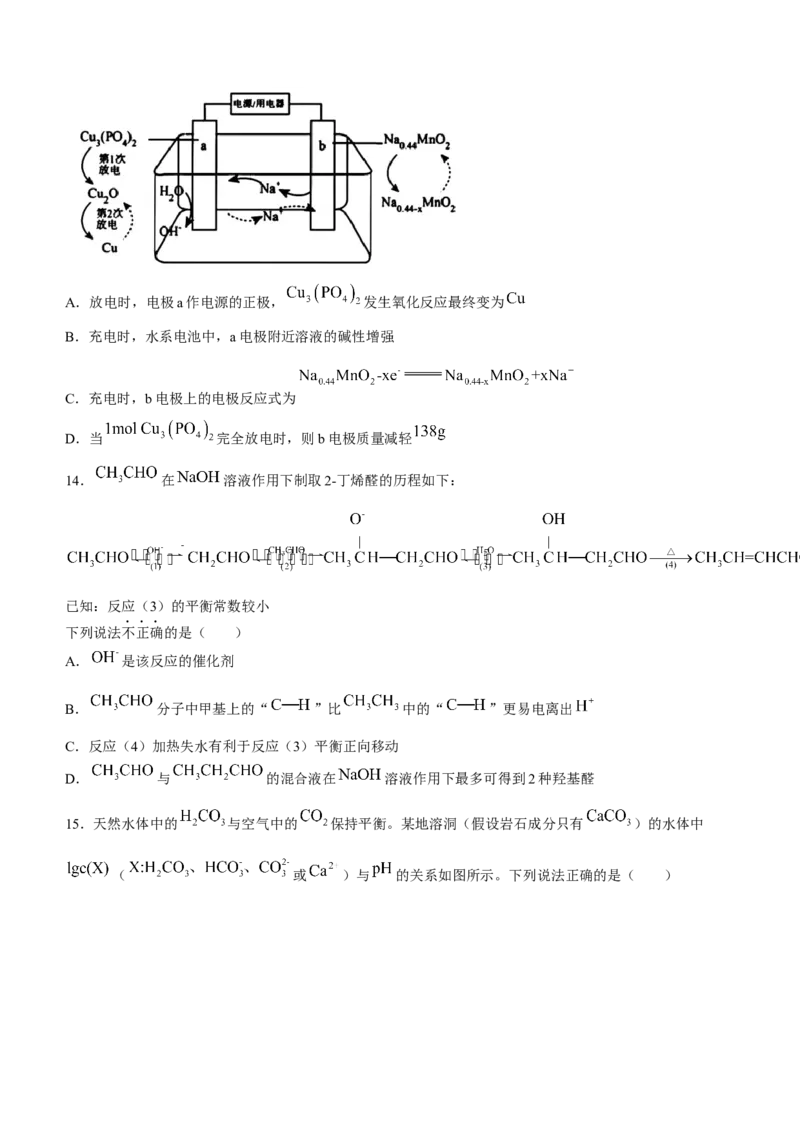
13.水系双离子电池原理如图所示,下列有关叙述正确的是( )A.放电时,电极a作电源的正极, 发生氧化反应最终变为
B.充电时,水系电池中,a电极附近溶液的碱性增强
C.充电时,b电极上的电极反应式为
D.当 完全放电时,则b电极质量减轻
14. 在 溶液作用下制取2-丁烯醛的历程如下:
已知:反应(3)的平衡常数较小
下列说法不正确的是( )
A. 是该反应的催化剂
B. 分子中甲基上的“ ”比 中的“ ”更易电离出
C.反应(4)加热失水有利于反应(3)平衡正向移动
D. 与 的混合液在 溶液作用下最多可得到2种羟基醛
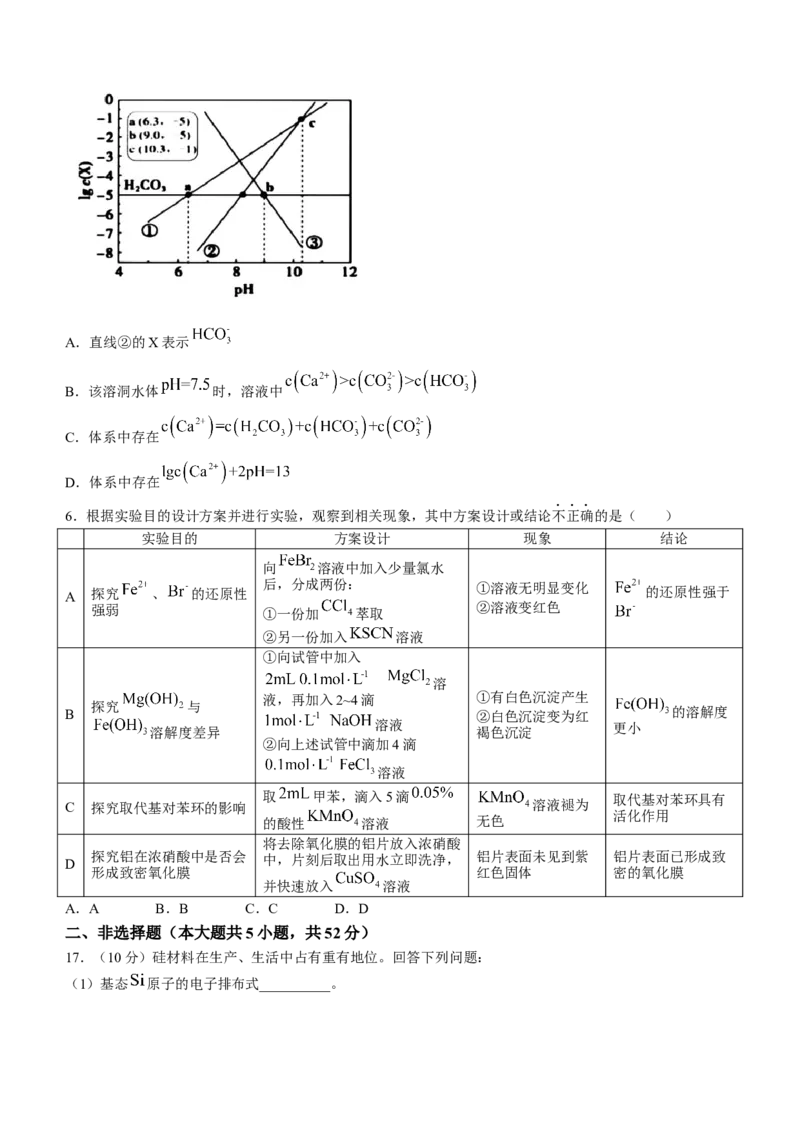
15.天然水体中的 与空气中的 保持平衡。某地溶洞(假设岩石成分只有 )的水体中
( 或 )与 的关系如图所示。下列说法正确的是( )A.直线②的X表示
B.该溶洞水体 时,溶液中
C.体系中存在
D.体系中存在
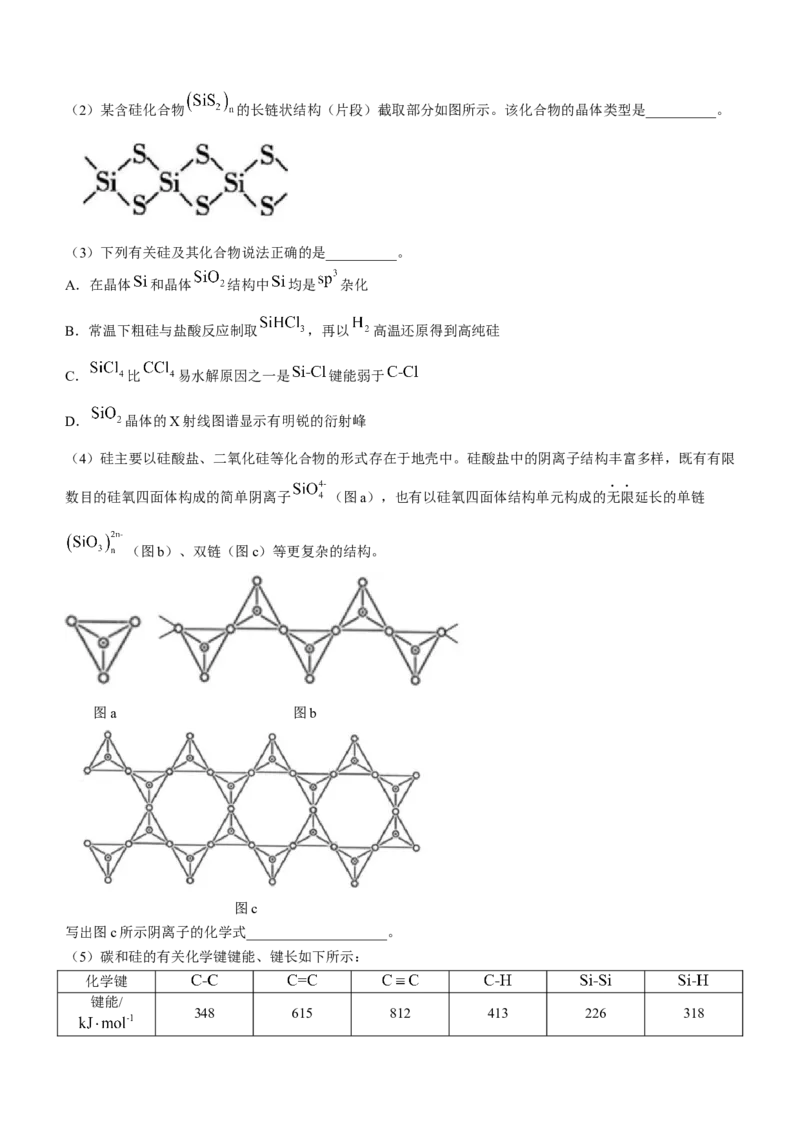
6.根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确的是( )
实验目的 方案设计 现象 结论
向 溶液中加入少量氯水
A 探究 、 的还原性 后,分成两份: ①溶液无明显变化 的还原性强于
强弱 ①一份加 萃取 ②溶液变红色
②另一份加入 溶液
①向试管中加入
溶
液,再加入2~4滴 ①有白色沉淀产生
探究 与
B ②白色沉淀变为红 的溶解度
溶液 更小
溶解度差异 褐色沉淀
②向上述试管中滴加4滴
溶液
取 甲苯,滴入5滴 取代基对苯环具有
C 探究取代基对苯环的影响 溶液褪为
活化作用
的酸性 溶液 无色
将去除氧化膜的铝片放入浓硝酸
探究铝在浓硝酸中是否会 中,片刻后取出用水立即洗净, 铝片表面未见到紫 铝片表面已形成致
D
形成致密氧化膜 红色固体 密的氧化膜
并快速放入 溶液
A.A B.B C.C D.D
二、非选择题(本大题共5小题,共52分)
17.(10分)硅材料在生产、生活中占有重有地位。回答下列问题:
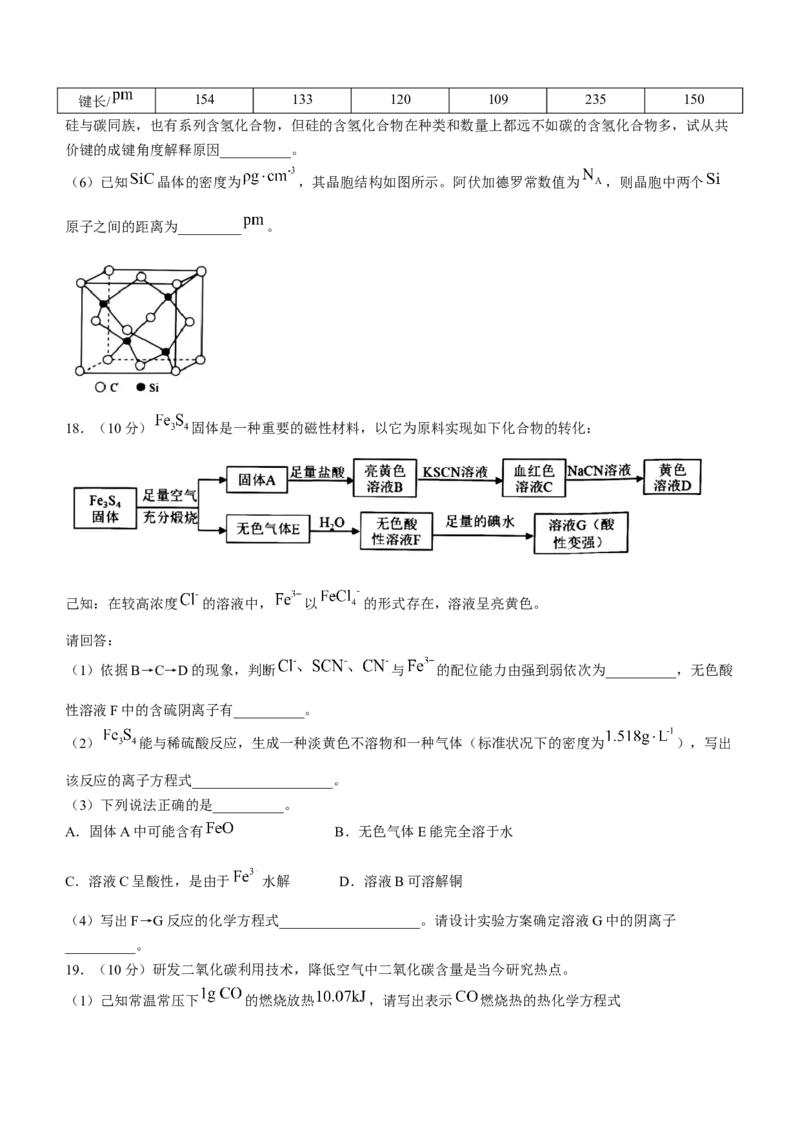
(1)基态 原子的电子排布式__________。(2)某含硅化合物 的长链状结构(片段)截取部分如图所示。该化合物的晶体类型是__________。
(3)下列有关硅及其化合物说法正确的是__________。
A.在晶体 和晶体 结构中 均是 杂化
B.常温下粗硅与盐酸反应制取 ,再以 高温还原得到高纯硅
C. 比 易水解原因之一是 键能弱于
D. 晶体的X射线图谱显示有明锐的衍射峰
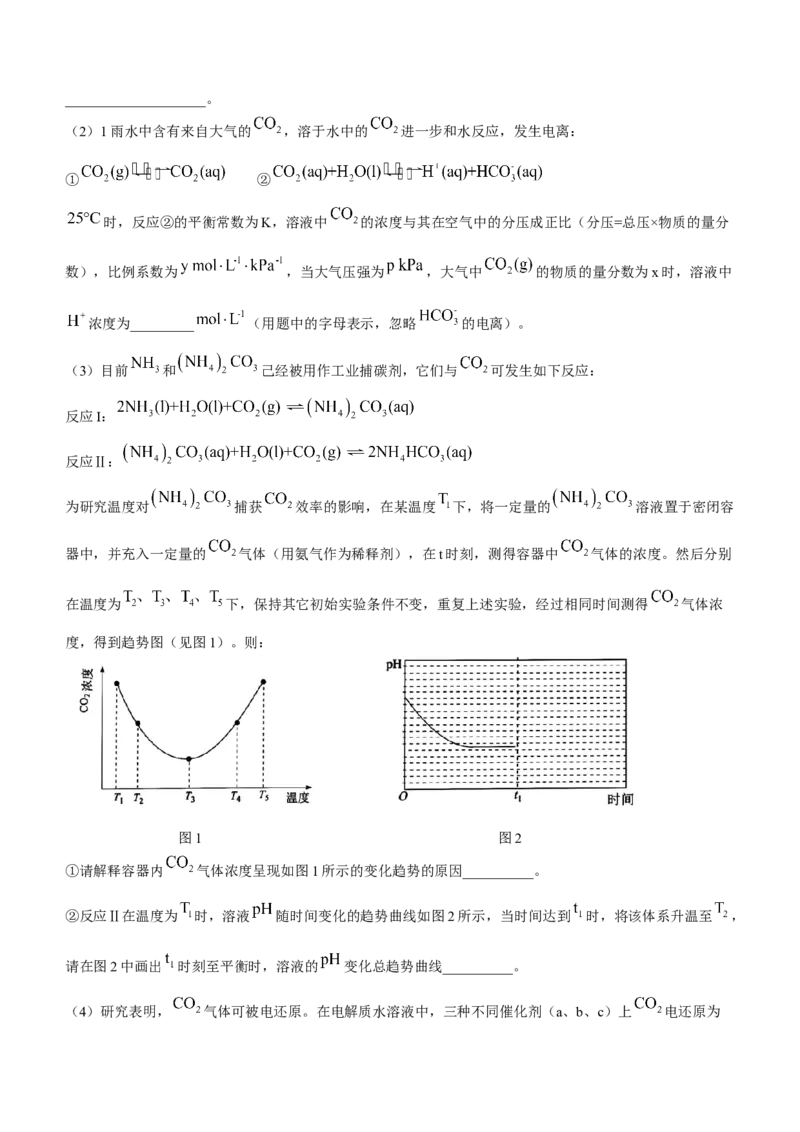
(4)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中。硅酸盐中的阴离子结构丰富多样,既有有限
数目的硅氧四面体构成的简单阴离子 (图a),也有以硅氧四面体结构单元构成的无限延长的单链
(图b)、双链(图c)等更复杂的结构。
图a 图b
图c
写出图c所示阴离子的化学式____________________。
(5)碳和硅的有关化学键键能、键长如下所示:
化学键
键能/
348 615 812 413 226 318键长/ 154 133 120 109 235 150
硅与碳同族,也有系列含氢化合物,但硅的含氢化合物在种类和数量上都远不如碳的含氢化合物多,试从共
价键的成键角度解释原因__________。
(6)已知 晶体的密度为 ,其晶胞结构如图所示。阿伏加德罗常数值为 ,则晶胞中两个
原子之间的距离为_________ 。
18.(10分) 固体是一种重要的磁性材料,以它为原料实现如下化合物的转化:
己知:在较高浓度 的溶液中, 以 的形式存在,溶液呈亮黄色。
请回答:
(1)依据B→C→D的现象,判断 与 的配位能力由强到弱依次为__________,无色酸
性溶液F中的含硫阴离子有__________。
(2) 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为 ),写出
该反应的离子方程式____________________。
(3)下列说法正确的是__________。
A.固体A中可能含有 B.无色气体E能完全溶于水
C.溶液C呈酸性,是由于 水解 D.溶液B可溶解铜
(4)写出F→G反应的化学方程式____________________。请设计实验方案确定溶液G中的阴离子
__________。
19.(10分)研发二氧化碳利用技术,降低空气中二氧化碳含量是当今研究热点。
(1)己知常温常压下 的燃烧放热 ,请写出表示 燃烧热的热化学方程式____________________。
(2)1雨水中含有来自大气的 ,溶于水中的 进一步和水反应,发生电离:
① ②
时,反应②的平衡常数为K,溶液中 的浓度与其在空气中的分压成正比(分压=总压×物质的量分
数),比例系数为 ,当大气压强为 ,大气中 的物质的量分数为x时,溶液中
浓度为_________ (用题中的字母表示,忽略 的电离)。
(3)目前 和 己经被用作工业捕碳剂,它们与 可发生如下反应:
反应I:
反应Ⅱ:
为研究温度对 捕获 效率的影响,在某温度 下,将一定量的 溶液置于密闭容
器中,并充入一定量的 气体(用氨气作为稀释剂),在t时刻,测得容器中 气体的浓度。然后分别
在温度为 下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得 气体浓
度,得到趋势图(见图1)。则:
图1 图2
①请解释容器内 气体浓度呈现如图1所示的变化趋势的原因__________。
②反应Ⅱ在温度为 时,溶液 随时间变化的趋势曲线如图2所示,当时间达到 时,将该体系升温至 ,
请在图2中画出 时刻至平衡时,溶液的 变化总趋势曲线__________。
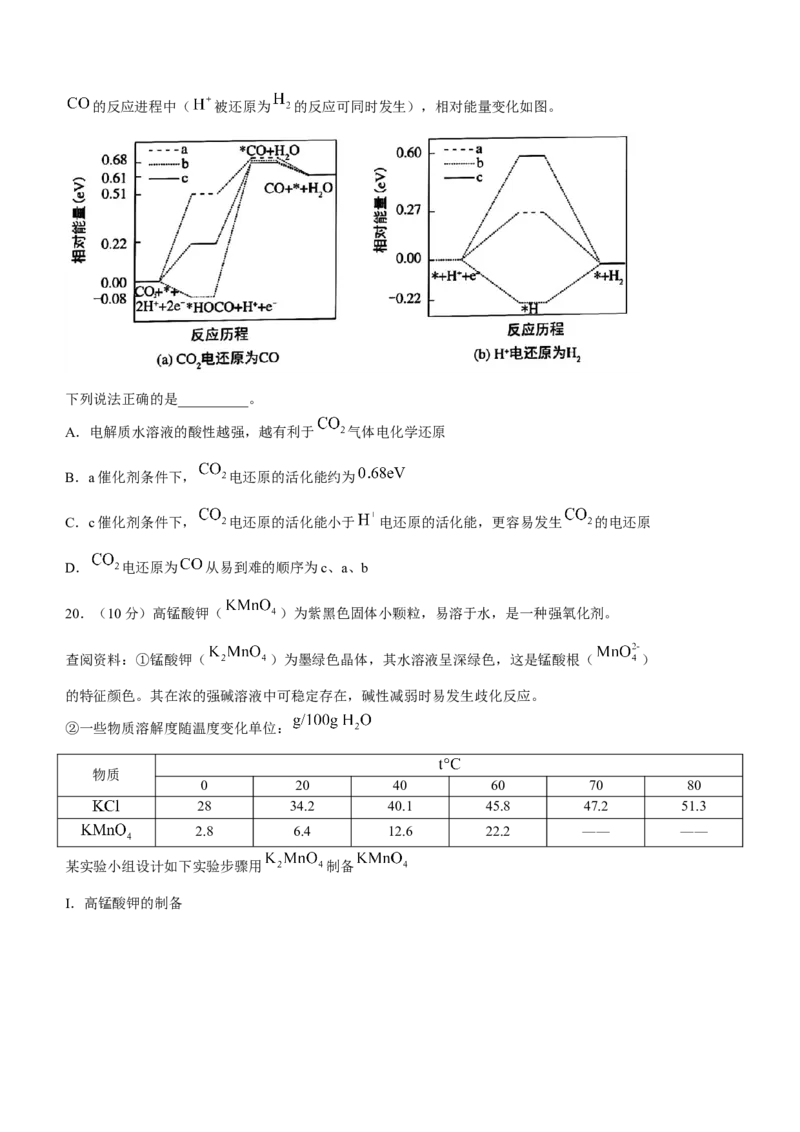
(4)研究表明, 气体可被电还原。在电解质水溶液中,三种不同催化剂(a、b、c)上 电还原为的反应进程中( 被还原为 的反应可同时发生),相对能量变化如图。
下列说法正确的是__________。
A.电解质水溶液的酸性越强,越有利于 气体电化学还原
B.a催化剂条件下, 电还原的活化能约为
C.c催化剂条件下, 电还原的活化能小于 电还原的活化能,更容易发生 的电还原
D. 电还原为 从易到难的顺序为c、a、b
20.(10分)高锰酸钾( )为紫黑色固体小颗粒,易溶于水,是一种强氧化剂。
查阅资料:①锰酸钾( )为墨绿色晶体,其水溶液呈深绿色,这是锰酸根( )
的特征颜色。其在浓的强碱溶液中可稳定存在,碱性减弱时易发生歧化反应。
②一些物质溶解度随温度变化单位:
物质
0 20 40 60 70 80
28 34.2 40.1 45.8 47.2 51.3
2.8 6.4 12.6 22.2 —— ——
某实验小组设计如下实验步骤用 制备
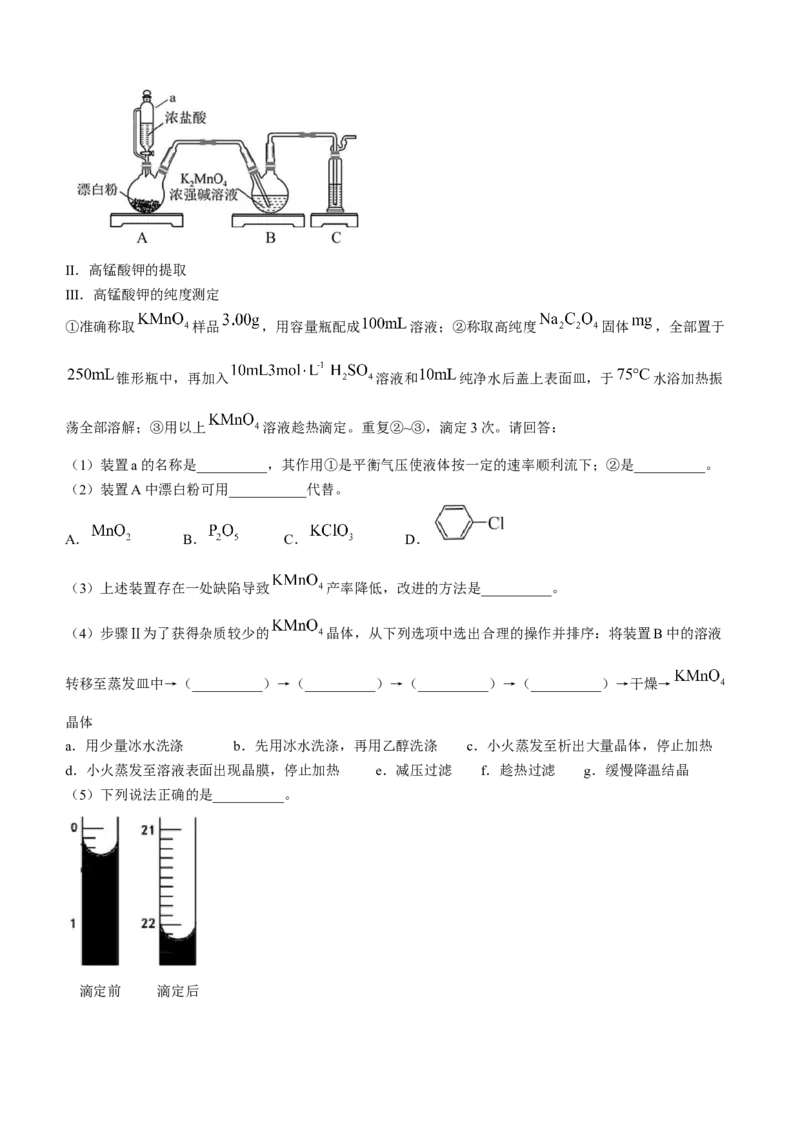
I.高锰酸钾的制备II.高锰酸钾的提取
III.高锰酸钾的纯度测定
①准确称取 样品 ,用容量瓶配成 溶液;②称取高纯度 固体 ,全部置于
锥形瓶中,再加入 溶液和 纯净水后盖上表面皿,于 水浴加热振
荡全部溶解;③用以上 溶液趁热滴定。重复②~③,滴定3次。请回答:
(1)装置a的名称是__________,其作用①是平衡气压使液体按一定的速率顺利流下;②是__________。
(2)装置A中漂白粉可用___________代替。
A. B. C. D.
(3)上述装置存在一处缺陷导致 产率降低,改进的方法是__________。
(4)步骤Ⅱ为了获得杂质较少的 晶体,从下列选项中选出合理的操作并排序:将装置B中的溶液
转移至蒸发皿中→(__________)→(__________)→(__________)→(__________)→干燥→
晶体
a.用少量冰水洗涤 b.先用冰水洗涤,再用乙醇洗涤 c.小火蒸发至析出大量晶体,停止加热
d.小火蒸发至溶液表面出现晶膜,停止加热 e.减压过滤 f.趁热过滤 g.缓慢降温结晶
(5)下列说法正确的是__________。
滴定前 滴定后A.步骤I装置C中应盛放浓
B.轻轻摇动装置B,若容器内壁未见暗绿色,说明反应完全
C.步骤IⅢ中的 可用 或 代替
D.一次平行操作滴定前与滴定后(终点)读数如右图,则本次消耗的 溶液体积为
(6)某次滴定,称取 固体质量 ,消耗 溶液体积 ,计算该次滴定实验测得
的高锰酸钾含量是__________ (精确到小数点后两位)。
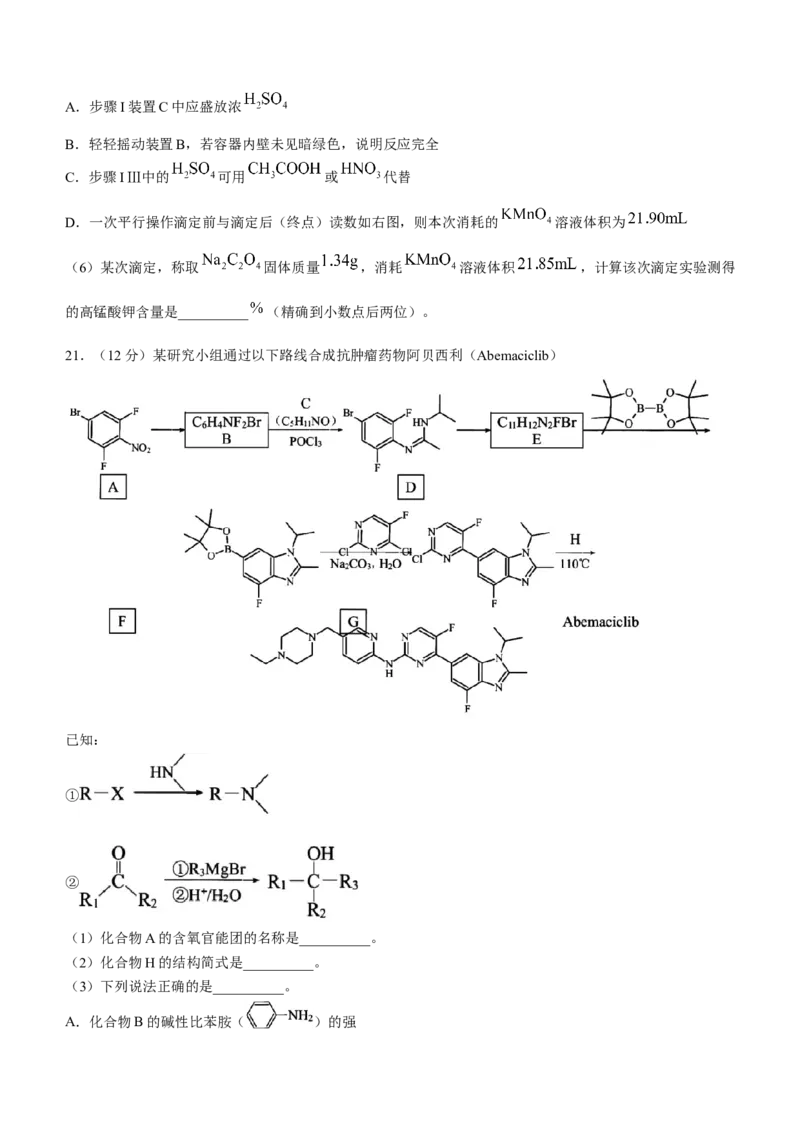
21.(12分)某研究小组通过以下路线合成抗肿瘤药物阿贝西利(Abemaciclib)
已知:
①
②
(1)化合物A的含氧官能团的名称是__________。
(2)化合物H的结构简式是__________。
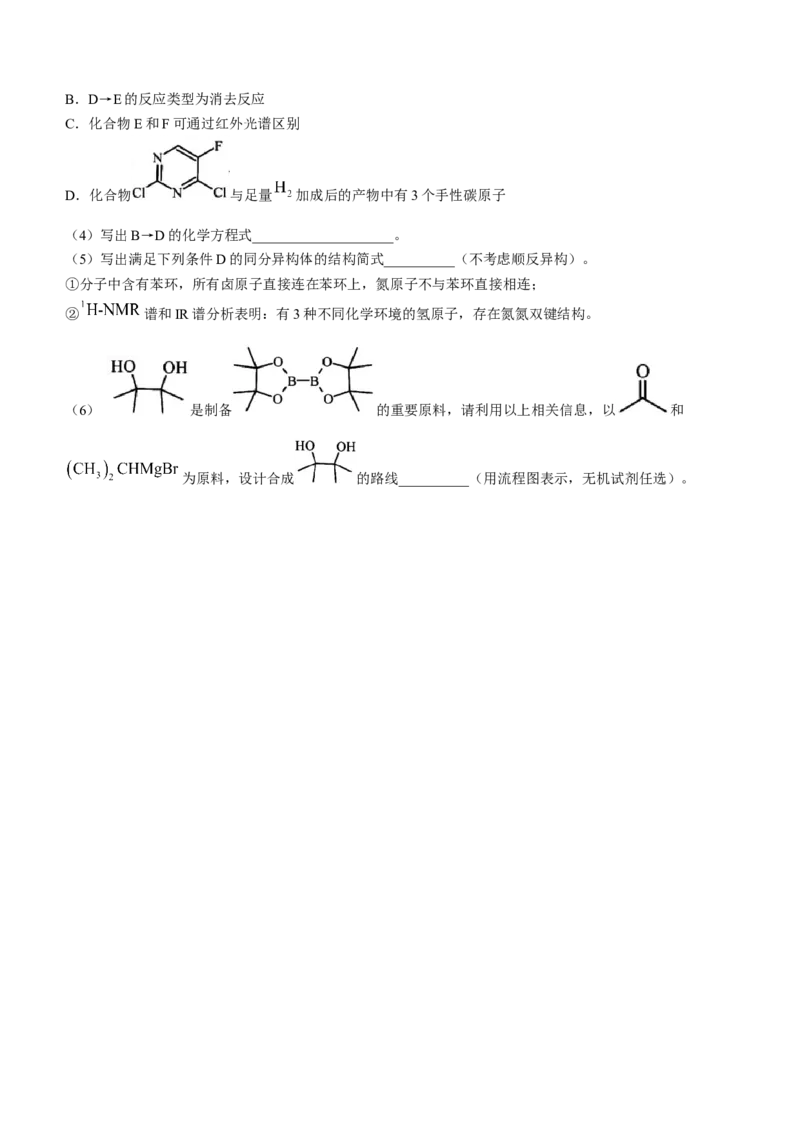
(3)下列说法正确的是__________。
A.化合物B的碱性比苯胺( )的强B.D→E的反应类型为消去反应
C.化合物E和F可通过红外光谱区别
D.化合物 与足量 加成后的产物中有3个手性碳原子
(4)写出B→D的化学方程式____________________。
(5)写出满足下列条件D的同分异构体的结构简式__________(不考虑顺反异构)。
①分子中含有苯环,所有卤原子直接连在苯环上,氮原子不与苯环直接相连;
② 谱和IR谱分析表明:有3种不同化学环境的氢原子,存在氮氮双键结构。
(6) 是制备 的重要原料,请利用以上相关信息,以 和
为原料,设计合成 的路线__________(用流程图表示,无机试剂任选)。2024 年高三教学测试
化学参考答案
一、选择题(48分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
B B D C A D B A C A D C D D D C
二、非选择题(52分)
17.(10分)
(1) (1分)。 (2)分子晶体(1分)。 (3)ACD(2分)。
(4) (2分)。
(5)①硅烷中的 键和 键的键能小于烷烃分子中 键和 键的键能,稳定性差,易断裂,导
致长链硅烷难以形成;② 的原子半径大,原子之间形成的 单键较长, 轨道肩并肩重叠的程度很小或
几乎不能重叠,难以形成 键(2分,每点1分)。
(6) (2分)。
18.(10分)
(1) (1分)。 (2分)。
(2) (2分)。
(3)D(2分)。
(4) (1分).
取溶液G,加入过量 溶液,若产生白色沉淀,则有 ;取上层清液,滴加 溶液,若黄色沉
淀产生,则有 (2分,其他合理答案也给分)。
19.(10分)
(1) (或281.9均可)(2分)。
【 得1分。化学方程式部分状态不写或错误扣1分,部分错误(无“-”、计算错误或仅列式“ ”、无单位)扣1分】
(2) (2分)。【唯一答案】
(3) 区间,化学反应未达到平衡,温度越高,化学反应的速率越快,所以 被捕获的浓度随温度
升高而增多,未被捕获的就越少。 区间,化学反应已达到平衡,由于正反应是放热反应,温度升高平
衡向逆反应方向移动,所以不利于 的捕获(2分)。
【答出 前,温度越高,化学反应速率越快得1分; 后温度升高平衡向逆反应方向移动得1分】
如图(2分)。【拐点前变化趋势正确(上凸或直线上升,不超过起点 得1分;拐点后水平直线得1分】
(4)CD(2分)。【选对1个得1分,错选0分】
20.(10分)
(1)恒压滴液漏斗(1分)【恒压漏斗、恒压分液漏斗均得分,仅分液漏斗或滴液漏斗不得分】。防止浓盐
酸挥发(1分)。【绿色安全之类笼统含糊说法不得分】
(2)C(1分)。【多选、错选不得分】
(3)在AB之间增加一个盛有饱和 溶液的洗气瓶(1分)。【或其他合理答案】
(4)dgea(2分)。【有错即0分】
(5)BD(2分)。【选对1个得1分,错选0分】
(6)96.41(2分)。【96.42也得分,96.4得1分,96不得分】
21.(12分)
(1)硝基(1分)。
(2) (1分)。
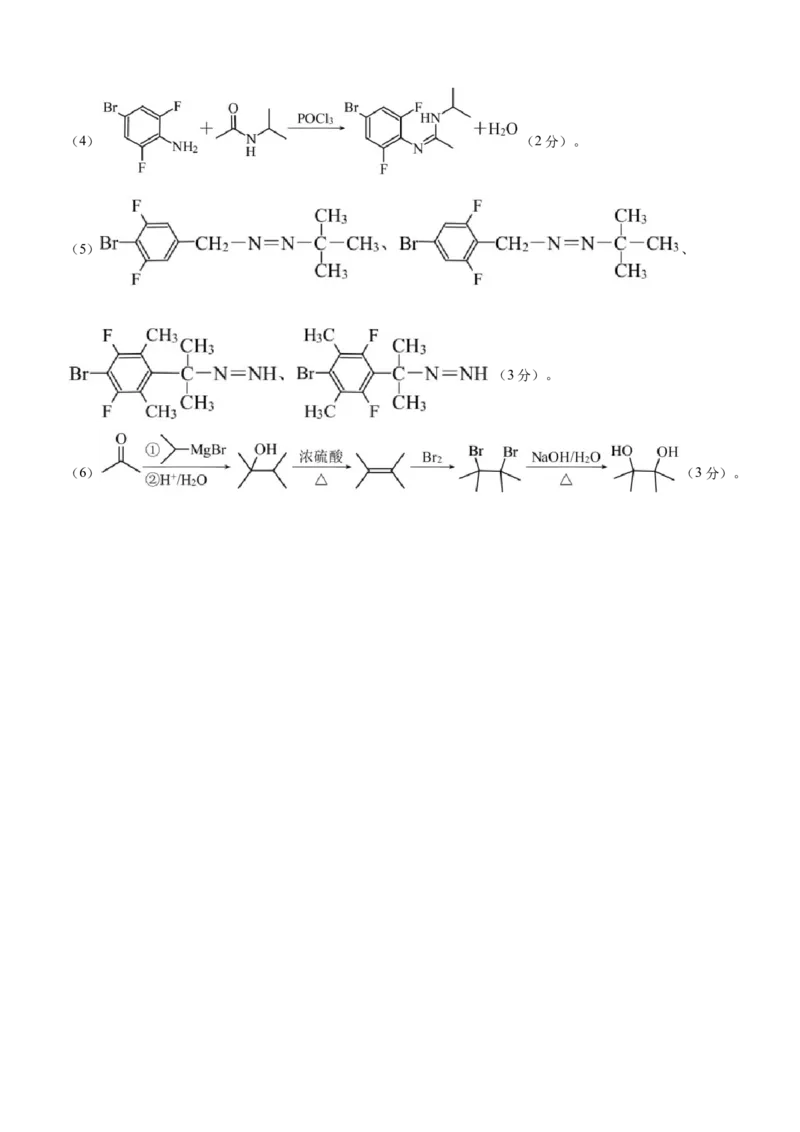
(3)CD(2分)。(4) (2分)。
(5) 、
(3分)。
(6) (3分)。