文档内容
1.1.1 反应热 焓变 练习(解析版)
1.下列说法正确的是( )
A.吸热反应不加热就不会发生
B.据能量守恒定律,反应物的总能量一定等于生成物的总能量
C.化学反应除了生成新的物质外,还伴随着能量的变化
D.放热的化学反应不需要加热就能发生
【答案】C
【解析】A、氯化铵与氢氧化钡反应吸热,常温下就可以反应,故A错误;
B、能量守恒定律是说能量既不会凭空产生,也不会凭空消失,它只能从一种形式转化为另一种形
式,或者从一个物体转移到另一个物体,在转移或转化过程中其总量保持不变,但化学反应中反应
物和生成物的能量是不同的,故B错误;
C、化学反应的实质就是旧键断裂新键形成的过程,断键吸收能量成键释放能量,故C正确;
D、燃烧都是放热反应,需要加热到着火点,故D错误;故选:C。
2.已知25℃、101kPa条件下:
4Al(s)+3O (g)═2Al O (s)放出2834.9kJ热量,
2 2 3
4Al(s)+2O (g)═2Al O (s)放出3119.91kJ热量.
3 2 3
由此得出的结论正确的是( )
A.等质量的O 比O 能量低,由O 变O 为吸热反应
2 3 2 3
B.等质量的O 比O 能量低,由O 变O 为放热反应
2 3 2 3
C.O 比O 稳定,由O 变O 为吸热反应
3 2 2 3
D.O 比O 稳定,由O 变O 为放热反应
2 3 2 3
【答案】A
【解析】4Al (s)+3O (g)═2Al O (s)△H=﹣2834.9kJ•mol﹣1
2 2 3
4Al (s)+2O (g)═2Al O (s)△H=﹣3119.91kJ•mol﹣1 ①
3 2 3
﹣ 得3O (g)═2O △H=+285.01kJ•mol﹣1 该反应吸热,等质②量的O 比O 能量低,所以O
2 3 2 3 2
①比O ②稳定,由O 变O 为吸热反应,故选:A。
3 2 3
3.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量.已知12g
石墨或金刚石完全燃烧时放出的热量依次为Q 和Q ,下列说法错误的是( )
1 2
A.Q <Q B.石墨不如金刚石稳定
1 2
C.石墨具有的能量比金刚石低 D.完全燃烧,生成的二氧化碳一样多
【答案】B
【解析】A、石墨在一定条件下可以转化为金刚石并需要吸收能量,说明石墨的能量低于金刚石的能量,12g石墨完全燃烧时放出的热量小于12g金刚石完全燃烧时放出的热量,即Q <Q ,故A不
1 2
选;
B、石墨转化为金刚石要吸收能量,说明石墨的能量低,石墨比金刚石稳定,故B选;
C、石石墨转化为金刚石要吸收能量,说明石墨的能量低,故C不选;
D、金刚石和石墨互为同分异构体,等质量的金刚石和石墨完全燃烧时生成的二氧化碳质量是一样
的,故D不选。故选:B。
4.下列反应的能量变化符合图的是( )
A.CH 燃烧 B.食物腐败变质
4
C.NaOH溶液滴定HCl溶液 D.Ba(OH) •8H O与NH Cl反应制冷
2 2 4
【答案】D
【解析】A.CH 的燃烧的反应为放热反应,故A错误;
4
B.食物腐败变质为缓慢氧化过程,缓慢氧化为放热反应,故B错误;
C.NaOH溶液滴定HCl溶液为中和反应,中和反应为放热反应,故C错误;
D.Ba(OH) •8H O与NH Cl反应制冷的过程属于吸热反应,故D正确;故选:D。
2 2 4
5.下列说法正确的是( )
需要加热才能发生的反应一定是吸热反应
①放热反应在常温下一定很容易发生
②一个化学反应是放热反应还是吸热反应,决定于反应物和生成物所具有的总能量的相对大
③小
化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因.
④A. B. C. D.
【答案】①D④ ①② ②③ ③④
【解析】 因需要加热才能发生的反应不一定是吸热反应,如铝热反应需要加热才能发生,但它
是放热反应①,故错误;
因铝热反应是放热反应,需要加热才能发生,故错误;
②放热反应是指:反应物所具有的总能量高于生成的总能量,在反应中会有一部分能量转变为热
③能的形式释放,反之,就是吸热反应,故正确;因化学反应中发生能量变化的主要原因是化学键的断裂和形成,故正确;故选:D。
④6.下列关于化学反应与能量的说法不正确的是( )
A.乙醇的燃烧是放热反应 B.Mg与盐酸的反应是吸热反应
C.反应物化学键的断裂要吸收能量 D.化学反应伴随有能量的变化
【答案】B
【解析】A、燃烧是放热、发光的化学变化,所以乙醇的燃烧是放热反应,故A正确;
B、Mg与盐酸的反应是放热反应,故B错误;
C、形成化学键需要放出能量,断裂化学键需要吸收能量,故C正确;
D、化学变化中的能量变化主要是由化学键变化引起的,物质发生化学反应伴随有化学键的断裂与
形成,必然伴随着能量的变化,故D正确;故选:B。
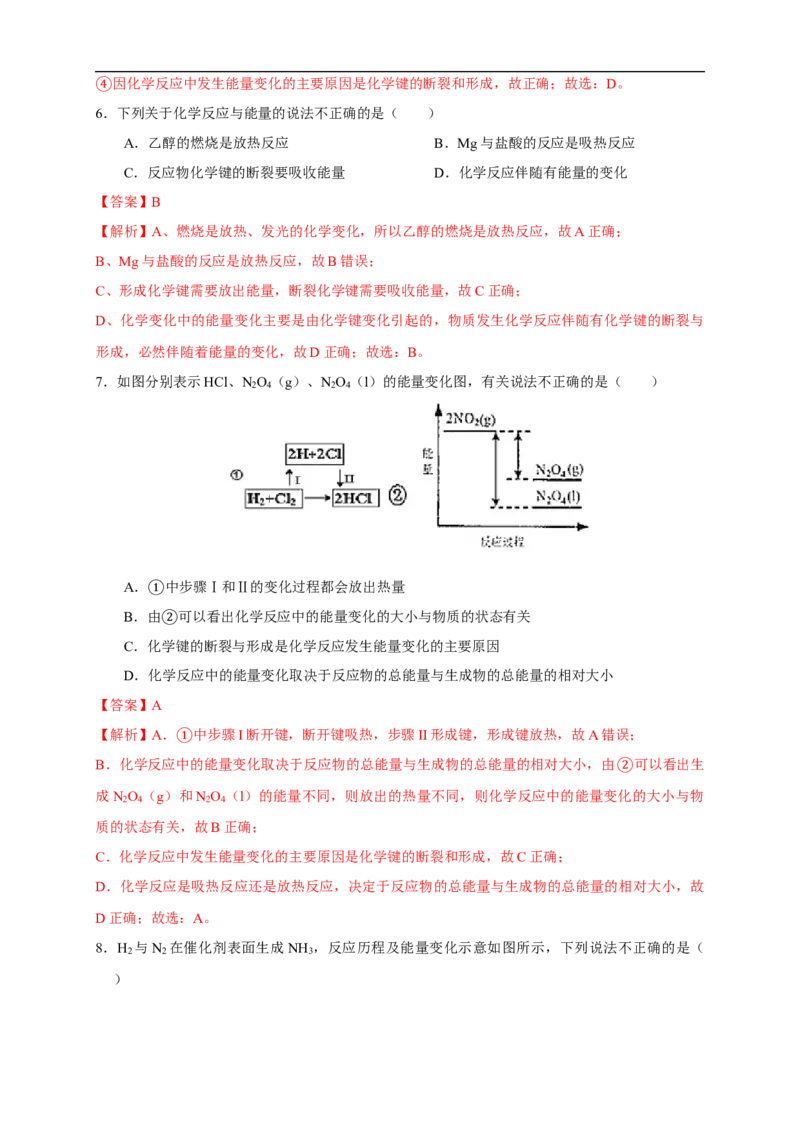
7.如图分别表示HCl、N O (g)、N O (l)的能量变化图,有关说法不正确的是( )
2 4 2 4
A. 中步骤Ⅰ和Ⅱ的变化过程都会放出热量
B.由① 可以看出化学反应中的能量变化的大小与物质的状态有关
C.化②学键的断裂与形成是化学反应发生能量变化的主要原因
D.化学反应中的能量变化取决于反应物的总能量与生成物的总能量的相对大小
【答案】A
【解析】A. 中步骤I断开键,断开键吸热,步骤II形成键,形成键放热,故A错误;
B.化学反应中①的能量变化取决于反应物的总能量与生成物的总能量的相对大小,由 可以看出生
成N O (g)和N O (l)的能量不同,则放出的热量不同,则化学反应中的能量变②化的大小与物
2 4 2 4
质的状态有关,故B正确;
C.化学反应中发生能量变化的主要原因是化学键的断裂和形成,故C正确;
D.化学反应是吸热反应还是放热反应,决定于反应物的总能量与生成物的总能量的相对大小,故
D正确;故选:A。
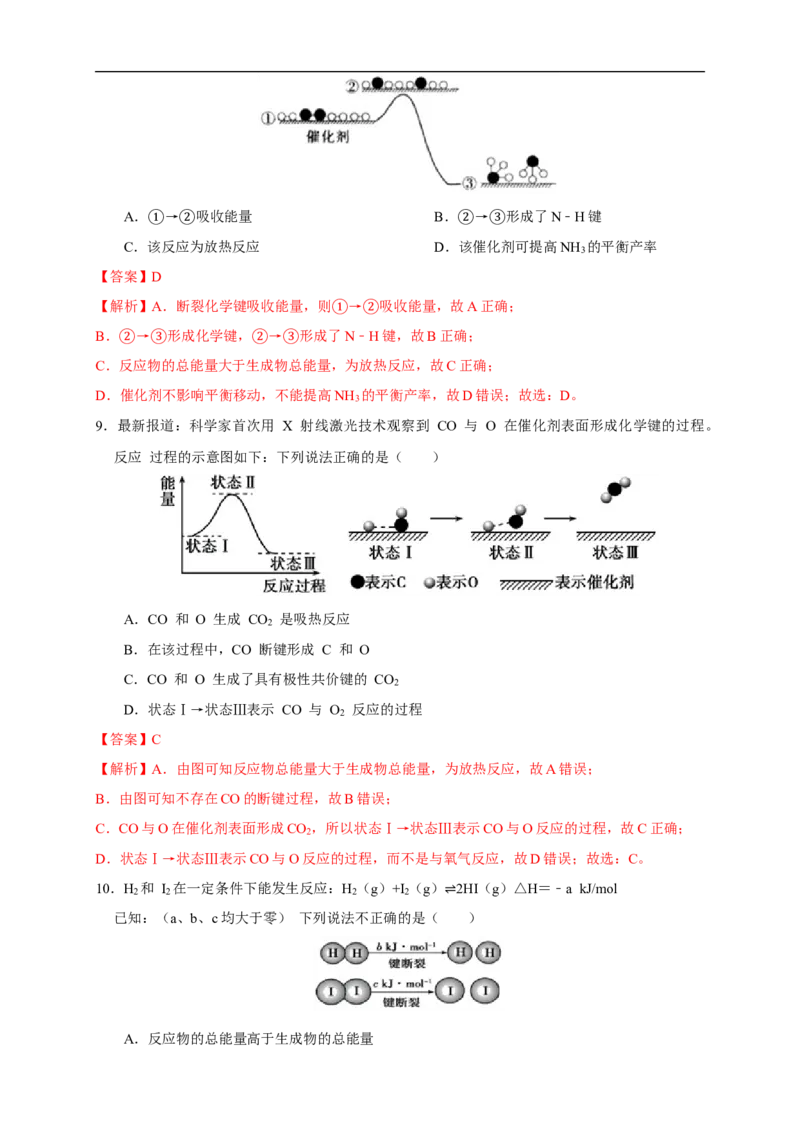
8.H 与N 在催化剂表面生成NH ,反应历程及能量变化示意如图所示,下列说法不正确的是(
2 2 3
)A. → 吸收能量 B. → 形成了N﹣H键
C.该①反应②为放热反应 D.②该催化③剂可提高NH
3
的平衡产率
【答案】D
【解析】A.断裂化学键吸收能量,则 → 吸收能量,故A正确;
B. → 形成化学键, → 形成了①N﹣②H键,故B正确;
C.②反应物③的总能量大于生②成物③总能量,为放热反应,故C正确;
D.催化剂不影响平衡移动,不能提高NH 的平衡产率,故D错误;故选:D。
3
9.最新报道:科学家首次用 X 射线激光技术观察到 CO 与 O 在催化剂表面形成化学键的过程。
反应 过程的示意图如下:下列说法正确的是( )
A.CO 和 O 生成 CO 是吸热反应
2
B.在该过程中,CO 断键形成 C 和 O
C.CO 和 O 生成了具有极性共价键的 CO
2
D.状态Ⅰ→状态Ⅲ表示 CO 与 O 反应的过程
2
【答案】C
【解析】A.由图可知反应物总能量大于生成物总能量,为放热反应,故A错误;
B.由图可知不存在CO的断键过程,故B错误;
C.CO与O在催化剂表面形成CO ,所以状态Ⅰ→状态Ⅲ表示CO与O反应的过程,故C正确;
2
D.状态Ⅰ→状态Ⅲ表示CO与O反应的过程,而不是与氧气反应,故D错误;故选:C。
10.H 和 I 在一定条件下能发生反应:H (g)+I (g) 2HI(g)△H=﹣a kJ/mol
2 2 2 2
已知:(a、b、c均大于零) 下列说法不正确的是( ⇌ )
A.反应物的总能量高于生成物的总能量B.断开 1 mol H﹣H 键和1 mol I﹣I键所需能量大于断开 2 mol H﹣I键所需能量
C.断开 2 mol H﹣I键所需能量约为(c+b+a) kJ
D.向密闭容器中加入2 mol H 和2 mol I ,充分反应后放出的热量小于 2a kJ
2 2
【答案】B
【解析】A.H 和I 在一定条件下能发生反应为:H (g)+I (g) 2HI(g)△H=﹣a kJ•mol﹣1
2 2 2 2
,该反应为放热反应,则反应物的总能量高于生成物的总能量,故A⇌正确;
B.断裂化学键吸收能量,形成化学键放出能量,反应是放热反应所以形成化学键放出的能量大于
断裂化学键吸收的能量,则断开1mol H﹣H键和1mol I﹣I键所需能量小于断开2mol H﹣I键所需
能量,故B错误;
C.△H=反应物断裂化学键需要的能量﹣生成物形成化学键放出的能量=bKJ/mol+cKJ/mol﹣2H﹣
I=﹣akJ/mol,得到断开2mol H﹣I键所需能量约为(a+b+c)kJ,故C正确;
D.反应是可逆反应不能进行彻底,依据焓变意义分析,向密闭容器中加入 2mol H 和2mol I ,充
2 2
分反应后放出的热量小于2a kJ,故D正确;故选:B。
11.H 与 O 发生反应的过程用模型图示如下(“﹣”表示化学键):下列说法不正确的是
2 2
( )
A.过程Ⅰ是吸热过程
B.过程Ⅲ一定是放热过程
C.该反应过程所有旧化学键都断裂,且形成了新化学键
D.该反应的能量转化形式只能以热能的形式进行
【答案】D
【解析】A、过程Ⅰ分子化学键断裂形成原子,属于吸热过程,故A正确;
B、过程Ⅲ为新化学键形成的过程,是放热过程,故B正确;
C、过程Ⅰ中所有的旧化学键断裂,过程Ⅲ为新化学键形成的过程,故C正确;
D、该反应可通过燃料电池,实现化学能到电能的转化,故D错误;故选:D。
12.(1)有关化学反应的能量变化如图所示。此反应是____________反应(填“吸热”或“放
热”)。判断依据是______________________。(2)CH (g)+1.5O (g)═CO(g)+2H O(l)△H =akJ/mol,则a____________﹣564.3
4 2 2 1
(填“>”、“<”、“=”)。
(3)已知2H (g)+O (g)═2H O(l),△H=﹣572kJ/mol;H﹣H键的键能为436kJ/mol;
2 2 2
O=O键的键能为498kJ/mol,则H O分子中O﹣H键的键能为___________kJ/mol。
2
【答案】(1)放热;反应物的总能量大于生成物的总能量;(2)<;(3)485.5。
【解析】(1)由图可知,反应物的总能量大于生成物的总能量,则该反应为放热反应;判断依据
是反应物的总能量大于生成物的总能量;
故答案为:放热;反应物的总能量大于生成物的总能量;
(2)从气态到液态放热,故CH (g)+1.5O (g)═CO(g)+2H O(l)△H =akJ/mol,放出的
4 2 2 1
热量大于564.3kJ,则a<﹣564.3,故答案为:<;
(3)设H O分子中O﹣H键的键能为xKJ,则2molH O中含有4molO﹣H,其总键能为4xKJ;
2 2
△H=反应物的总键能﹣生成物的总键能,即﹣572kJ/mol=436kJ/mol×2+498kJ/mol﹣4x,
所以x=485.5,即H O分子中O﹣H键的键能为485.5kJ/mol,故答案为:485.5。
2
13.化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是_____________(填字母)。
A.Na O与水反应 B.甲烷的燃烧反应
2
C.CaCO 受热分解 D.锌与盐酸反应
3
(2)获取能量变化的途径
通过化学键的键能计算。已知:
① 化学键种类 H﹣H O=O O﹣H
键能(kJ/mol) 436 498 463.4
计算可得:2H (g)+O (g)═2H O(g)△H=____________kJ•mol﹣1
2 2 2
通过物质所含能量计算。已知反应中A+B═C+D中A、B、C、D所含能量依次可表示为E
②、E 、E 、E ,该反应△H=____________。
A B C D
利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol•L﹣
③1的盐酸,则还需加入_____________(填序号)。
A.50mL0.50mol•L﹣1NaOH溶液
B.50mL0.55mol•L﹣1NaOH溶液C.1.0g NaOH固体
【答案】(1)C;(2) ﹣483.6; E +E ﹣(E +E ); B。
C D A B
【解析】(1)A、B、D①均为放热反应②,只有C为吸热反应,故③答案为:C;
(2) 2H (g)+O (g)═2H O(g)△H=(2×436+498﹣463.4×2×2)kJ/mol=﹣483.6kJ/
2 2 2
mol,故①答案为:﹣483.6;
反应中A+B═C+D中A、B、C、D所含能量依次可表示为E 、E 、E 、E ,该反应△H=
A B C D
②E +E ﹣(E +E ),故答案为:E +E ﹣(E +E );
C D A B C D A B
测定中和热,因盐酸易挥发,需加稍过量的NaOH,保证盐酸完全反应,且固体溶解放热,只有
③B合理,故答案为:B。
14.如图是H (g)+Cl (g)=2HCl(g)反应过程中的能量变化图.
2 2
(1)由图可知,1mol H (g)和1mol Cl (g)的总能量________(填“>”、“<”或者
2 2
“=”) 2mol HCl(g)的能量.
(2)该反应是_________(填“吸”或者“放”)热反应,从化学键的角度进行解释
_________________________________________________________________________.
【答案】(1)>;
(2)放;断裂1molH﹣H键和1molCl﹣Cl键吸收的总能量小于形成2molH﹣Cl键放出的总能量.
【解析】(1)由能量变化图可知反应物总能量大于生成物总能量,为放热反应,则1mol H (g)
2
和1mol Cl (g)的总能量大于 2mol HCl(g)的能量,故答案为:>;
2
(2)该反应为放热反应,则断裂1molH﹣H键和1molCl﹣Cl键吸收的总能量小于形成2molH﹣Cl
键放出的总能量,
故答案为:放;断裂1molH﹣H键和1molCl﹣Cl键吸收的总能量小于形成2molH﹣Cl键放出的总
能量.