文档内容
第四章 物质结构 元素周期律
第三节 化学键
第2课时 共价键
1.下列物质中,既含有极性共价键,又含有非极性共价键的是( )
A.CH B.CO C.NH Cl D.HO
4 2 4 2 2
2.下列物质中,既有离子键又有共价键的是( )
A.CaCl B.NaO C.HO D.NaCl
2 2 2 2
3.下列各组物质都是共价化合物的是( )
A.HS和NaO B.HO和NH Cl
2 2 2 2 4
C.NH 和N D.HNO 和HCl
3 2 3
4.(2020·湖北江夏·金口中学月考)在下列化学反应中既有离子键、极性键、非极性键断裂,又有离子键、
极性键、非极性键形成的是( )
A.Cl+HO=HClO+HCl
2 2
B.MgN+6HO=3Mg(OH) ↓+2NH ↑
3 2 2 2 3
C.2NaO+2HO=4NaOH+O↑
2 2 2 2
D.NH Cl+NaOH NaCl+NH ↑+HO
4 3 2
5.下列各组物质的晶体中,化学键类型相同、晶体类型、物质发生状态变化所克服的粒子间的相互作用
也相同的是( )
A.SO 和HCl B.KCl和Mg C.NaCl和HO D.CCl 和SiO
3 2 4 2
6.(2020·江苏高考真题)反应 可用于氯气管道的检漏。下列表示相关微粒
的化学用语正确的是
A.中子数为9的氮原子:
B.N 分子的电子式:
2
C.Cl 分子的结构式:Cl—Cl
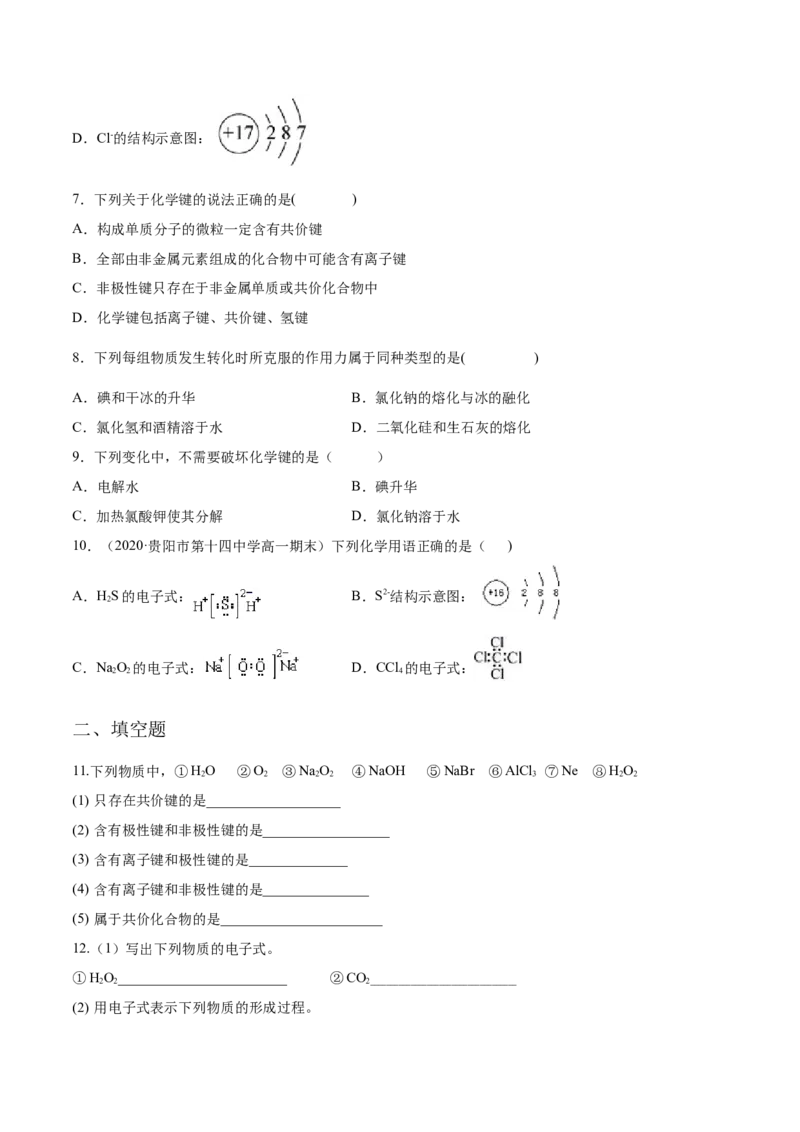
2D.Cl-的结构示意图:
7.下列关于化学键的说法正确的是( )
A.构成单质分子的微粒一定含有共价键
B.全部由非金属元素组成的化合物中可能含有离子键
C.非极性键只存在于非金属单质或共价化合物中
D.化学键包括离子键、共价键、氢键
8.下列每组物质发生转化时所克服的作用力属于同种类型的是( )
A.碘和干冰的升华 B.氯化钠的熔化与冰的融化
C.氯化氢和酒精溶于水 D.二氧化硅和生石灰的熔化
9.下列变化中,不需要破坏化学键的是( )
A.电解水 B.碘升华
C.加热氯酸钾使其分解 D.氯化钠溶于水
10.(2020·贵阳市第十四中学高一期末)下列化学用语正确的是( )
A.HS的电子式: B.S2-结构示意图:
2
C.NaO 的电子式: D.CCl 的电子式:
2 2 4
二、填空题
11.下列物质中,①HO ②O ③NaO ④NaOH ⑤NaBr ⑥AlCl ⑦Ne ⑧HO
2 2 2 2 3 2 2
(1) 只存在共价键的是___________________
(2) 含有极性键和非极性键的是__________________
(3) 含有离子键和极性键的是______________
(4) 含有离子键和非极性键的是_______________
(5) 属于共价化合物的是_______________________
12.(1)写出下列物质的电子式。
①HO________________________ ②CO
2 2 2____________________________________
(2) 用电子式表示下列物质的形成过程。HO________________________
2
13.(2020·福建莆田一中高一期末)下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答
下列问题。
族
IA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
2 ① ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)②的原子结构示意图是____。
(2)化学性质最不活泼的元素是_____(填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是__________。(填离子符
号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学
方程式为_________。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有____。
(6)由元素⑧和⑨形成的某种化合物可表示为XY(其中各原子均满足8电子稳定结构),写出XY 的电子式:
2 2 2 2
______。