文档内容
人教版(2019)必修第一册第一章第三节 氧化还原反应
课时训练五
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.黑火药是中国古代四大发明之一,其爆炸反应为2KNO+S+3C=KS+N↑+3CO ↑。
3 2 2 2
下列说法正确的是
A.黑火药中含有两种单质 B.爆炸时吸收热量
C.反应中S作还原剂 D.反应为置换反应
2.根据下列实验操作和现象所得到的结论正确的是
选
实验操作和现象 结论
项
向淀粉溶液中加适量20%H SO 溶液,加热,冷却后加NaOH溶
A 2 4 淀粉未水解
液至中性,再滴加少量碘水,溶液变蓝
室温下,向 HCl溶液中加入少量镁粉,产生大量气 镁与盐酸反
B
泡,测得溶液温度上升 应放热
室温下,向浓度均为 的BaCl 和CaCl 混合溶液中加 白色沉淀是
C 2 2
入Na 2 CO 3 溶液,出现白色沉淀 BaCO 3
HO 具有氧
D 向 HO 溶液中滴加 KMnO 溶液,溶液褪色 2 2
2 2 4 化性
A.A B.B C.C D.D
3.为了实现下列各变化,需加入还原剂的是
A.KClO→O B.NH →NH C.Fe→FeCl D.CO→CO
3 2 3 3 2
4.下列物质的应用中,利用了氧化还原反应的是
A.用石灰乳脱除烟气中的SO
2
B.用明矾[KAl(SO)•12H O]处理污水
4 2 2
C.用盐酸去除铁锈(主要成分Fe O•xH O)
2 3 2
D.用84消毒液(有效成分NaClO)杀灭细菌
5.氧化还原反应的本质是
A.有氧元素参与反应 B.有电子转移
C.物质状态发生变化 D.质量保持不变
6.氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时的化学反应原理为:NaH + H O = NaOH + H ↑。下列有关该反应的说法中,正确的是
2 2
A.HO中的氢元素被还原 B.该反应属于复分解反应
2
C.NaH是氧化剂 D.该反应属于置换反应
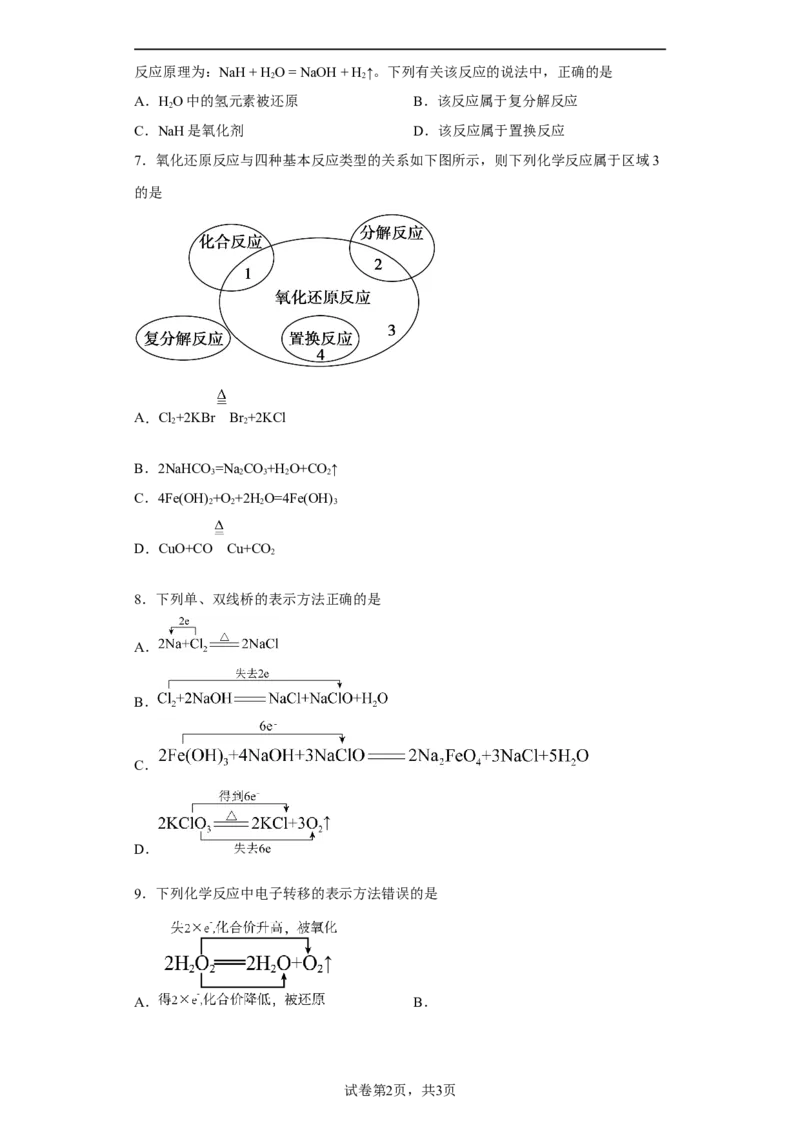
7.氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于区域3
的是
A.Cl+2KBr Br +2KCl
2 2
B.2NaHCO =Na CO+H O+CO↑
3 2 3 2 2
C.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
D.CuO+CO Cu+CO
2
8.下列单、双线桥的表示方法正确的是
A.
B.
C.
D.
9.下列化学反应中电子转移的表示方法错误的是
A. B.
试卷第2页,共3页C. D.
10.根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是
I+SO+2H O=HSO +2HI;2FeCl +Cl=2FeCl ;2FeCl +2HI=2FeCl +2HCl+I
2 2 2 2 4 2 2 3 3 2 2
A.I->Fe2+>Cl->SO B.Cl->Fe2+>SO I-
2 2>
C.Fe2+>I->Cl->SO D.SO >I->Fe2+>Cl-
2 2
11.硫酸盐(含SO 、HSO )气溶胶是PM 的成分之一。近期科研人员提出了雾霾微
2.5
颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是
A.该过程有HO参与 B.NO 是生成硫酸盐的氧化剂
2 2
C.硫酸盐气溶胶呈酸性 D.该过程没有生成硫氧键
12.在常温下,发生下列几种反应:
①
②
③
根据上述反应,下列结论判断错误的是
A.溶液中可发生反应:B. 在①、③反应中为还原剂
C.氧化性强弱的顺序为:
D. 是 的还原产物
13.反应 中,作还原剂的是
A. B. C. D.
14.已知三个氧化还原反应:①2FeCl +2KI=2FeCl +2KCl+I,②2FeCl +
3 2 2 2
Cl=2FeCl ,③2KMnO +16HCl(浓)= 2KCl+2MnCl +8HO+5Cl↑。若某溶液中有
2 3 4 2 2 2
Fe2+、I-、Cl-共存,要将I-氧化除去而不氧化Fe2+和Cl-,则可加入的试剂是
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
15.日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是
A.铜铸塑像上出现铜绿[Cu (OH) CO]
2 2 3
B.铁制菜刀生锈
C.大理石雕像被酸雨腐蚀毁坏
D.铝锅表面生成致密的氧化膜
二、填空题
16.从铜氨废液含[Cu(NH )·CO]+、[Cu(NH )]2+、[Cu(NH )]2+、NH 、CHCOO−、
3 3 3 2 3 4 3 3
等中回收铜的工艺流程如图:
回答下列问题:
(1)步骤(Ⅰ)中被氧化的元素是_____________,由步骤(Ⅱ)可确定NH 与H+的结合能力比
3
与Cu2+的_____________ (填“强”或“弱”)。
(2)步骤(Ⅲ)“沉铜”时,发生的主要反应的离子方程式为_______________________,
试卷第4页,共3页利用NaS溶液而不选用NaOH溶液“沉铜”的优点是_______________________。
2
(3)步骤(Ⅳ)反应中,氧化剂与还原剂的物质的量之比为_____________。
(4)该流程中可以循环利用的物质是__________________________(填化学式)。
(5)碱式氯化铜在400℃时能完全分解为CuO、HO和HCl。为测定碱式氯化铜的组成
2
进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体
32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为
__________________________。
17.按要求回答下列各题:
I.已知实验室制取氯气的反应原理为:MnO +4HCl(浓) MnCl +Cl↑+2H O,据此回
2 2 2 2
答下列问题:
(1)氧化剂是___________(填写化学式);还原剂是___________(填写化学式);氧化剂和
还原剂个数比是 ___________。
(2)该实验室制取氯气反应的离子方程式为___________。
II.用双线桥法表示电子转移的方向和数目:KClO+6HCl(浓) KCl+3Cl ↑+3H O
3 2 2
___________
III.医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离
子方程式,并填上合适的微粒:_________ ____H++____MnO +____H C O
2 2 4
=____CO ↑+____Mn2++____
2
18.二氧化氯(ClO )是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的
2
气体,易溶于水,沸点为11℃。
(1)用NH Cl、盐酸、NaClO(亚氯酸钠)为原料制备ClO 的流程如图所示:
4 2 2
①写出电解时发生反应的化学方程式:___。
②ClO 的消毒效率(以转移电子数目的多少为依据)是等物质的量的Cl 的___倍。
2 2
(2)产品中ClO 含量的测量:向锥形瓶中加入由适量碘化钾、3mL硫酸组成的混合溶液,
2将上述反应过程中生成的一部分ClO 气体通入锥形瓶中充分反应。再加入几滴淀粉溶
2
液,用cmol/L硫代硫酸钠标准溶液滴定(I+2 =2I-+S ,通入的气体中不存在
2
能与I、 反应的成分),共用去VmL硫代硫酸钠溶液。
2
①请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式:___。
②滴定终点的现象是___。
③测得通入ClO 的质量m(ClO )=___(用含c、V的代数式表示)。
2 2
19.二氧化氯(ClO )是一种高效、广谱的灭菌消毒剂。已知ClO 为橙黄色气体,极易
2 2
溶于水,在混合气体中浓度过高时易发生爆炸。请回答下列问题:
(1)“二氧化氯泡腾片”的有效成分为NaClO、NaHSO、NaHCO ,能快速溶于水,生
2 4 3
成的ClO 溶于水得到ClO 溶液,同时生成另一种气体而放出大量气泡。每生成
2 2
1molClO 消耗NaClO 的量为___________mol;产生另一种气体的离子方程式为
2 2
___________。
(2)在处理废水时,ClO 可与水中的有毒离子(如CN—)反应生成两种无毒气体,反应的
2
离子方程式为___________。
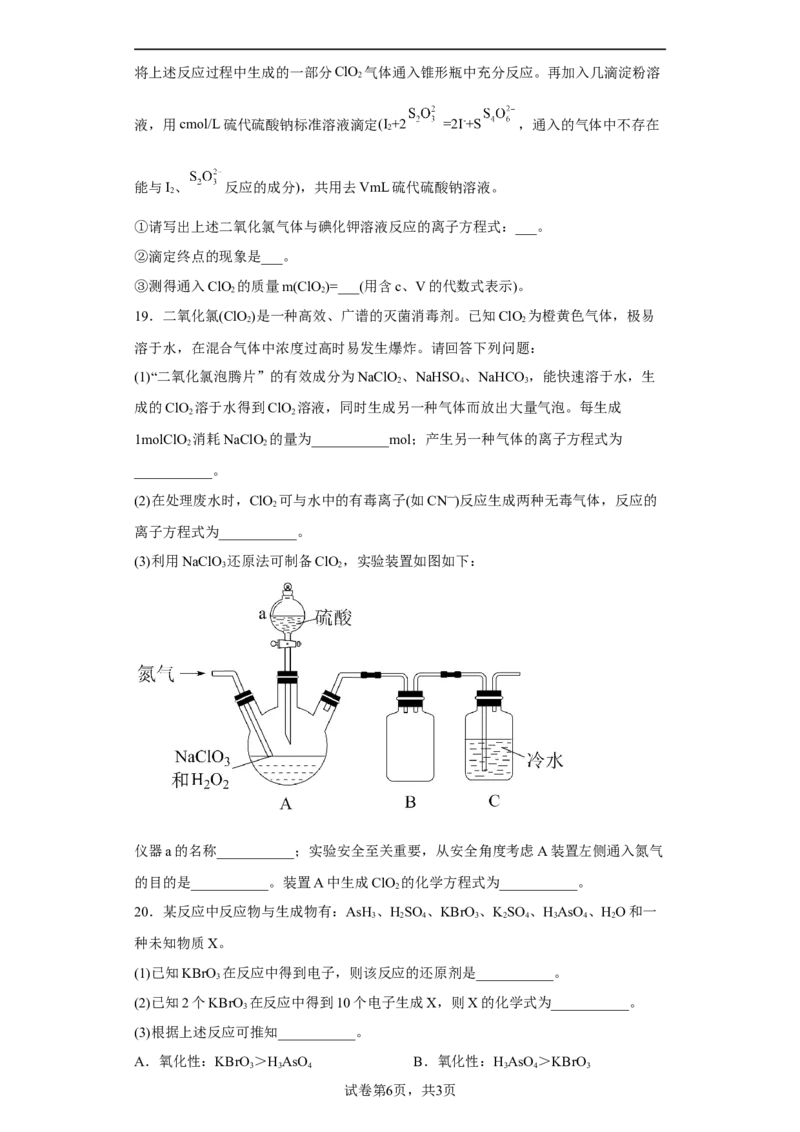
(3)利用NaClO 还原法可制备ClO ,实验装置如图如下:
3 2
仪器a的名称___________;实验安全至关重要,从安全角度考虑A装置左侧通入氮气
的目的是___________。装置A中生成ClO 的化学方程式为___________。
2
20.某反应中反应物与生成物有:AsH 、HSO 、KBrO 、KSO 、HAsO 、HO和一
3 2 4 3 2 4 3 4 2
种未知物质X。
(1)已知KBrO 在反应中得到电子,则该反应的还原剂是___________。
3
(2)已知2个KBrO 在反应中得到10个电子生成X,则X的化学式为___________。
3
(3)根据上述反应可推知___________。
A.氧化性:KBrO >HAsO B.氧化性:HAsO >KBrO
3 3 4 3 4 3
试卷第6页,共3页C.还原性:AsH >X D.还原性:X>AsH
3 3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥法标出
电子转移的方向和数目: 。___________
三、实验题
21.ClO 是一种易溶于水的黄绿色气体,具有强氧化性,可用于水处理。其体积分数
2
超过10%时易引起爆炸。
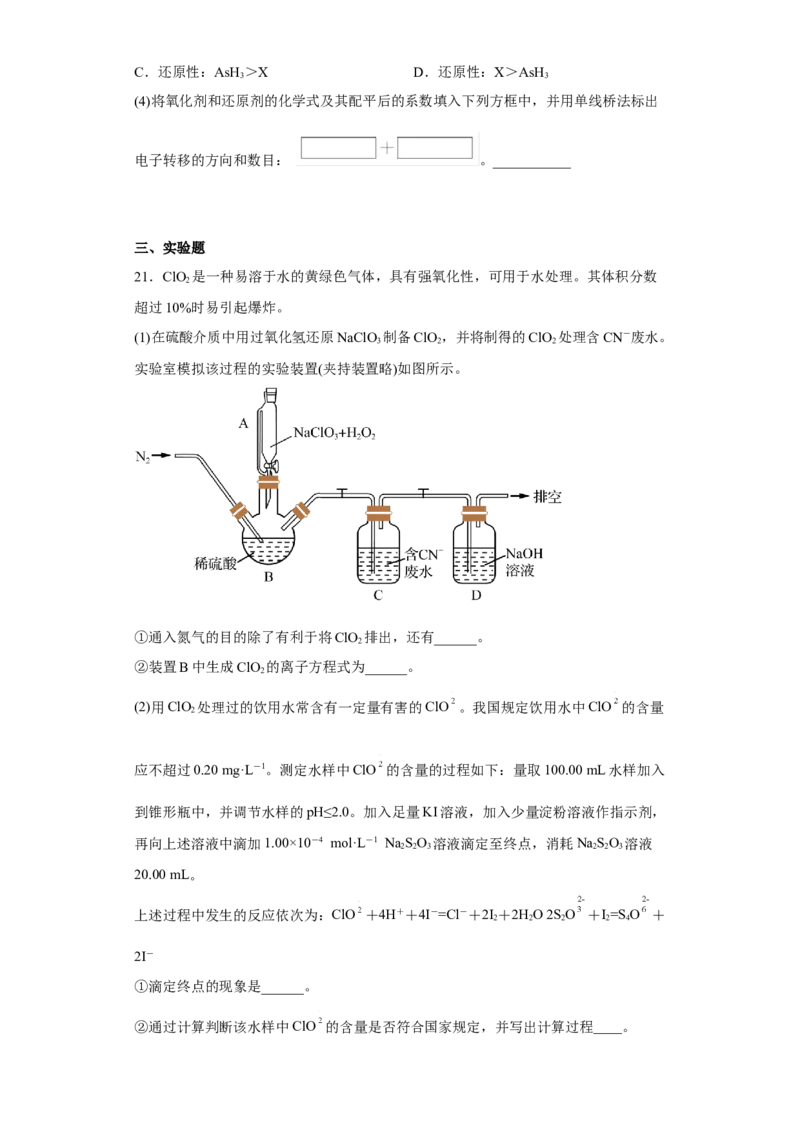
(1)在硫酸介质中用过氧化氢还原NaClO 制备ClO ,并将制得的ClO 处理含CN-废水。
3 2 2
实验室模拟该过程的实验装置(夹持装置略)如图所示。
①通入氮气的目的除了有利于将ClO 排出,还有______。
2
②装置B中生成ClO 的离子方程式为______。
2
(2)用ClO 处理过的饮用水常含有一定量有害的ClO 。我国规定饮用水中ClO 的含量
2
应不超过0.20 mg·L-1。测定水样中ClO 的含量的过程如下:量取100.00 mL水样加入
到锥形瓶中,并调节水样的pH≤2.0。加入足量KI溶液,加入少量淀粉溶液作指示剂,
再向上述溶液中滴加1.00×10-4 mol·L-1 Na SO 溶液滴定至终点,消耗NaSO 溶液
2 2 3 2 2 3
20.00 mL。
上述过程中发生的反应依次为:ClO +4H++4I-=Cl-+2I+2HO 2SO +I=S O +
2 2 2 2 4
2I-
①滴定终点的现象是______。
②通过计算判断该水样中ClO 的含量是否符合国家规定,并写出计算过程____。22.连二亚硫酸钠( )是一种淡黄色粉末,具有较强的还原性,不溶于乙醇,易
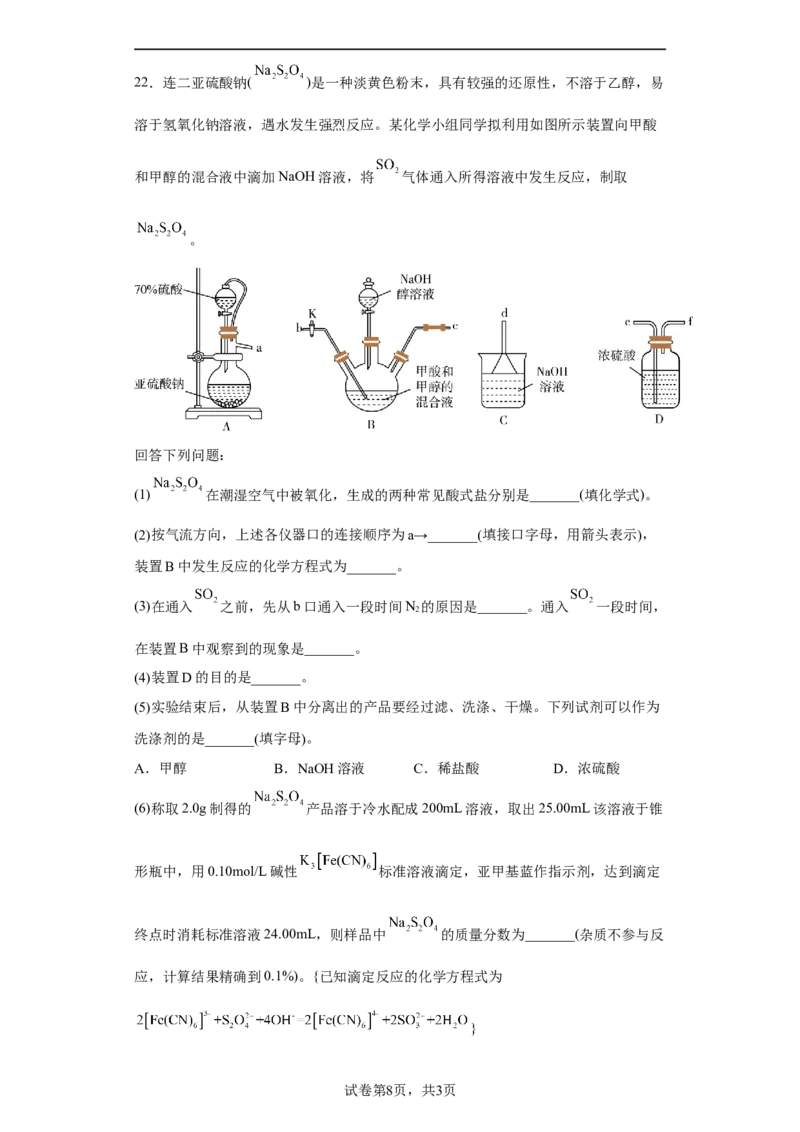
溶于氢氧化钠溶液,遇水发生强烈反应。某化学小组同学拟利用如图所示装置向甲酸
和甲醇的混合液中滴加NaOH溶液,将 气体通入所得溶液中发生反应,制取
。
回答下列问题:
(1) 在潮湿空气中被氧化,生成的两种常见酸式盐分别是_______(填化学式)。
(2)按气流方向,上述各仪器口的连接顺序为a→_______(填接口字母,用箭头表示),
装置B中发生反应的化学方程式为_______。
(3)在通入 之前,先从b口通入一段时间N 的原因是_______。通入 一段时间,
2
在装置B中观察到的现象是_______。
(4)装置D的目的是_______。
(5)实验结束后,从装置B中分离出的产品要经过滤、洗涤、干燥。下列试剂可以作为
洗涤剂的是_______(填字母)。
A.甲醇 B.NaOH溶液 C.稀盐酸 D.浓硫酸
(6)称取2.0g制得的 产品溶于冷水配成200mL溶液,取出25.00mL该溶液于锥
形瓶中,用0.10mol/L碱性 标准溶液滴定,亚甲基蓝作指示剂,达到滴定
终点时消耗标准溶液24.00mL,则样品中 的质量分数为_______(杂质不参与反
应,计算结果精确到0.1%)。{已知滴定反应的化学方程式为
}
试卷第8页,共3页参考答案:
1.A
【详解】A.黑火药中含有S、C两种单质,A正确;
B.爆炸反应为放热反应,B错误;
C.该反应中S元素化合价降低,作氧化剂,C错误;
D.该反应不符合“单质+化合物=另一种单质+另一种化合物”的形式,不是置换反应,D
错误;
综上所述答案为A。
2.B
【详解】A .加入碘水后,溶液呈蓝色,只能说明溶液中含有淀粉,并不能说明淀粉是否发
生了水解反应,故A错误;
B.加入盐酸后,产生大量气泡,说明镁与盐酸发生化学反应,此时溶液温度上升,可证明
镁与盐酸反应放热,故B正确;
C.BaCl 、CaCl 均能与NaCO 反应,反应产生了白色沉淀,沉淀可能为BaCO 或CaCO 或
2 2 2 3 3 3
二者混合物,故C错误;
D.向HO 溶液中加入高锰酸钾后,发生化学反应
2 2
2KMnO +3H O=2MnO+2KOH+2H O+3O↑等(中性条件),该反应中HO 被氧化,体现出
4 2 2 2 2 2 2 2
还原性,故D错误;
综上所述,故答案为:B。
【点睛】淀粉在稀硫酸作催化剂下的水解程度确定试验较为典型,一般分三种考法:①淀
粉未发生水解:向充分反应后的溶液中加入碘单质,溶液变蓝,然后加入过量氢氧化钠溶
液使溶液呈碱性,然后加入新制氢氧化铜溶液并加热,未生成砖红色沉淀;②淀粉部分发
生水解:向充分反应后的溶液中加入碘单质,溶液变蓝,然后加入过量氢氧化钠溶液使溶
液呈碱性,然后加入新制氢氧化铜溶液并加热,生成砖红色沉淀;③向充分反应后的溶液
中加入碘单质,溶液不变蓝,然后加入过量氢氧化钠溶液使溶液呈碱性,然后加入新制氢
氧化铜溶液并加热,生成砖红色沉淀。此实验中需要注意:①碘单质需在加入氢氧化钠溶
液之前加入,否则氢氧化钠与碘单质反应,不能完成淀粉的检验;②酸性水解后的溶液需
要加入氢氧化钠溶液碱化,否则无法完成葡萄糖的检验;③利用新制氢氧化铜溶液或银氨
溶液检验葡萄糖试验中,均需要加热,银镜反应一般为水浴加热。
3.D
【详解】A .KClO 自身分解可生成O,无需加入还原剂,故A错误;
3 2B.NH 转化为NH 无化合价变化,不需还原剂,故B错误;
3
C.Fe转化为FeCl ,化合价升高,Fe为还原剂,需加入氧化剂,故C错误;
3
D.CO 转化为CO过程中碳元素化合价降低,为氧化剂,需加入还原剂,故D正确;
2
故答案选D。
4.D
【详解】A.SO 是酸性氧化物,可与碱反应,用石灰乳脱除烟气中的SO 时,SO 与氢氧
2 2 2
化钙反应生成亚硫酸钙或亚硫酸氢钙,反应过程中无元素的化合价变化,没有利用氧化还
原反应,故A不符合题意;
B.用明矾[KAl(SO)•12H O]溶于水中,电离出的铝离子发生水解生成氢氧化铝胶体,利
4 2 2
用胶体的吸附性可吸附污水中的固体颗粒物,该过程利用胶体的吸附性,发生的反应没有
发生化合价变化,没有利用氧化还原反应,故B不符合题意;
C.用盐酸去除铁锈(主要成分Fe O•xH O),发生的主要反应为:6HCl+
2 3 2
Fe O=2FeCl +3H O,反应中没有元素化合价的变化,没有利用氧化还原反应,故C不符合
2 3 3 2
题意;
D.用84消毒液有效成分NaClO,具有强氧化性,能使蛋白质发生变性从而杀死细菌病毒,
杀菌消毒的过程利用了氧化还原反应,故D符合题意;
答案选D。
5.B
【详解】氧化还原反应的本质是电子转移,包括电子得失和共用电子对偏移。
答案选B。
6.A
【分析】由方程式可知,反应中氢化钠中氢元素化合价升高被氧化,氢化钠是反应的还原
剂,水分子中氢元素的化合价降低被还原,水是氧化剂。
【详解】A.由分析可知,反应中水分子中氢元素的化合价降低被还原,故A正确;
B.由分析可知,该反应为氧化还原反应,不是复分解反应,故B错误;
C.由分析可知,反应中氢化钠中氢元素化合价升高被氧化,氢化钠是反应的还原剂,故C
错误;
D.由方程式可知,反应中没有单质参与反应,该反应不属于置换反应,故D错误;
故选A。
7.D
答案第2页,共2页【详解】区域3表示属于氧化还原反应,但不属于置换反应的化学反应。根据置换反应和
氧化还原反应的定义可知,D项中的化学反应属于区域3。
故答案为:D。
8.C
【详解】A.钠元素的化合价升高,氯元素的化合价降低,转移的电子数为2e-,但电子转
移方向应该从钠到氯,故A错误;
B.该反应中Cl元素的化合价既升高又降低,转移的电子数为e-,正确的表示为
,故B错误;
C.氢氧化铁中的铁元素化合价升高,次氯酸钠中氯元素化合价降低,电子从铁转移到氯
且转移电子数为6e-,故C正确;
D.氯元素化合价降低,氧元素化合价升高,双线桥表示正确,但转移电子数应为12e-,故
D错误;
故答案为C。
9.D
【详解】A.过氧化氢中O元素既得电子又失电子,转移电子数为2,用双线桥表示电子转
移为: ,故A正确;
B.该反应中,氯元素由0价部分降低到-1价,部分升高到+5价,氯气既做氧化剂又做还
原剂,氯酸钾为氧化产物,氯化钾为还原产物;生成1个KClO,失去5e-,生成5个
3KCl,得到5e-,用双线桥表示电子转移为: ,故B正
确;
C.该反应中,钠元素由0价升高到+1价,发生氧化反应,作还原剂,氯元素由0价降低
到-1价,发生还原反应,作氧化剂;2个Na完全反应,失去2e-,1个Cl 完全反应得到
2
2e-,还原剂钠把电子转移给氧化剂氯气,用单线桥表示电子转移为:
,故C正确;
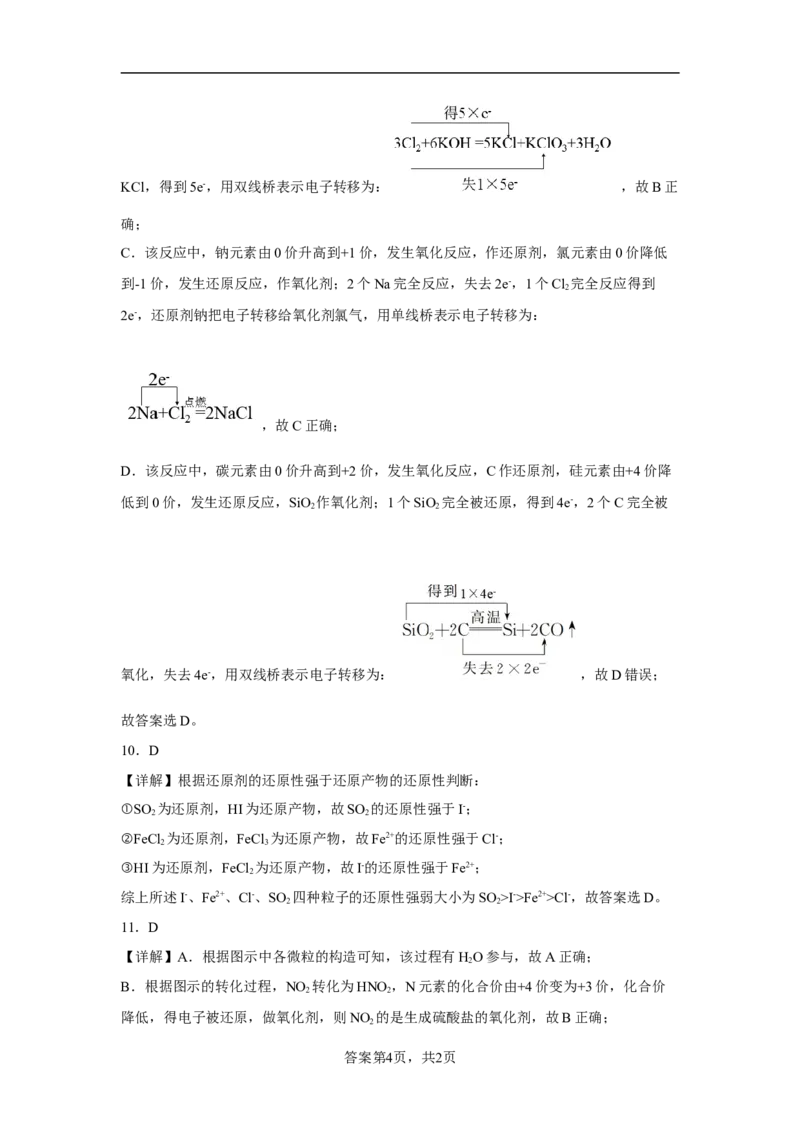
D.该反应中,碳元素由0价升高到+2价,发生氧化反应,C作还原剂,硅元素由+4价降
低到0价,发生还原反应,SiO 作氧化剂;1个SiO 完全被还原,得到4e-,2个C完全被
2 2
氧化,失去4e-,用双线桥表示电子转移为: ,故D错误;
故答案选D。
10.D
【详解】根据还原剂的还原性强于还原产物的还原性判断:
①SO 为还原剂,HI为还原产物,故SO 的还原性强于I-;
2 2
②FeCl 为还原剂,FeCl 为还原产物,故Fe2+的还原性强于Cl-;
2 3
③HI为还原剂,FeCl 为还原产物,故I-的还原性强于Fe2+;
2
综上所述I-、Fe2+、Cl-、SO 四种粒子的还原性强弱大小为SO >I->Fe2+>Cl-,故答案选D。
2 2
11.D
【详解】A.根据图示中各微粒的构造可知,该过程有HO参与,故A正确;
2
B.根据图示的转化过程,NO 转化为HNO,N元素的化合价由+4价变为+3价,化合价
2 2
降低,得电子被还原,做氧化剂,则NO 的是生成硫酸盐的氧化剂,故B正确;
2
答案第4页,共2页C.硫酸盐(含SO 、HSO )气溶胶中含有HSO ,转化过程有水参与,则HSO 在水中可
电离生成H+和SO ,则硫酸盐气溶胶呈酸性,故C正确;
D.根据图示转化过程中,由SO 转化为HSO ,根据图示对照,有硫氧键生成,故D错
误;
答案选D。
12.B
【详解】 ,氧化性: ;
,氧化性: ;
,氧化性: ,所以氧化性关系为: ,则
还原性为 ;
A.氧化性: ,则溶液中可发生: ,选项A正确;
B. ,还原性: 是还原剂;
,反应中 是氧化剂;选项B错误;
C.由分析可知,氧化性关系为: ,选项C正确;
D.氧化剂得电子化合价降低,发生还原反应,得到还原产物,则 是 的还原产物,
选项D正确。
答案选B。
13.B
【详解】还原剂中元素的化合价升高,从方程式中可以看出,C元素由0价升高为+4价,
还原剂为C,故选B。
14.C
【详解】根据同一氧化还原反应中,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物;则由题给方程式得出,氧化性由强至弱的顺序为: >Cl>Fe3+>I,还原性
2 2
由强至弱的顺序为I->Fe2+>Cl->Mn2+;
A.氯气能将Fe2+、I-均氧化,故A不符合题意;
B.KMnO 能将Fe2+、I-和Cl-均氧化,故B不符合题意;
4
C.FeCl 能氧化除去I-而不氧化Fe2+和Cl-,故C符合题意;
3
D.HCl与三种离子均不反应,故D不符合题意;
故答案为C。
15.C
【详解】A.金属铜和氧气、二氧化碳、水发生化合反应生成铜绿,该反应中Cu元素的化
合价由0价升至+2价,O 中氧元素的化合价由0价降至-2价,与氧化还原反应有关,故A
2
不符合题意;
B.铁制菜刀生锈,即Fe→Fe O,该反应中Fe元素的化合价由0价升至+3价,O元素的
2 3
化合价由0价降至-2价,与氧化还原反应有关,故B不符合题意;
C.酸雨腐蚀大理石雕像是因为碳酸钙能和酸反应,该反应中没有元素化合价的变化,与
氧化还原反应无关,故C符合题意;
D.铝易被氧气氧化生成氧化铝,该反应中Al元素的化合价由0价升至+3价,O元素的化
合价由0价降至-2价,与氧化还原反应有关,故D不符合题意;
故答案为C。
16. Cu、C 强 Cu2++S2-=CuS↓ CuS的溶解度比Cu(OH) 小,能
2
使Cu2+充分沉淀,提高Cu的回收率 2:3 HNO Cu (OH) Cl
3 2 3
【分析】从铜氨废液含[Cu(NH )·CO]+、[Cu(NH )]2+、[Cu(NH )]2+、NH 、CHCOO−、
3 3 3 2 3 4 3 3
等中回收铜,废液中通入热空气,并加热,可生成CO,NH,得到含有[Cu(NH )]2+、
2 3 3 4
CHCOO−、 的溶液,加入20%的硫酸,调节pH =2,得到硫酸铜,硫酸铵溶液,加入
3
20%的硫化钠溶液生成CuS沉淀,在沉淀中加入硝酸可生成NO、S和硝酸铜,加入硫酸生
成硫酸铜,经过滤、洗涤、干燥得到五水硫酸铜晶体。
向含有[Cu(NH )]2+、CHCOO−、 的溶液中加入盐酸,经过滤、洗涤、干燥,可得到碱
3 4 3
式氯化铜。
答案第6页,共2页【详解】(1)步骤(Ⅰ)“吹脱”时通入空气,氧气把Cu+氧化为Cu2+,将CO氧化生成CO 吹出,
2
吹出游离的NH 等,步骤(Ⅱ)中加入硫酸生成硫酸铵,可确定NH 与H+的结合能力比与
3 3
Cu2+结合能力强,故答案为Cu、C 强;
(2)步骤(Ⅲ)“沉铜”时,NaS溶液与CuSO 溶液反应生成CuS沉淀和NaSO ,主要反应的
2 4 2 4
离子方程式为Cu2++S2-=CuS↓,因为硫化铜的溶解度小于氢氧化铜的溶解度,能使
Cu2+充分沉淀,提高Cu的回收率,所以“沉铜”选用NaS溶液而不选用NaOH溶液,故
2
答案为Cu2++S2-=CuS↓ CuS的溶解度比Cu(OH) 小,能使Cu2+充分沉淀,提高Cu的回
2
收率。
(3)步骤(Ⅳ)反应中CuS和硝酸反应生成NO、S,反应中S元素化合价由-2价升高到0价,
N元素的化合价由+5价降低为+2价,则氧化剂与还原剂的物质的量之比为2:3,故答案为
2:3。
(4)在第(Ⅴ)硝酸铜溶液中加入硫酸制硫酸铜,同时生成HNO,则HNO 可循环利用,故答
3 3
案为HNO。
3
(5)碱式氯化铜在400℃时能完全分解为CuO、HO和HCl。为测定碱式氯化铜的组成进行
2
如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将
生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。CuO的物质的量为32.0g÷80g/
mol=0.4mol, HO的物质的量为3.6g÷18g/mol=0.2mol, HCl的物质的量为
2
(42.9g-32.0g-3.6g)÷36.5g/mol=0.2mol,则CuO:HO:HCl=0.4:0.2:0.2=2:1:1,则碱式氯化铜的化
2
学式为Cu (OH) Cl。故答案为Cu (OH) Cl。
2 3 2 3
17. MnO HCl 1:2 MnO +4H++2Cl-(浓) Mn2++Cl↑+2H O
2 2 2 2
6H++2MnO +5H C O =10CO ↑+2Mn2++8H O
2 2 4 2 2
【详解】I. (1)在氧化还原反应中,氧化剂是反应物中得到电子化合价降低被还原的物质,
故为:MnO ,还原剂是反应物中失去电子化合价升高被氧化的物质,故为:HCl;由于反
2
应中4分子的HCl中只有2分子的Cl化合价升高被氧化,故氧化剂和还原剂个数比是1:
2,故答案为:MnO ; HCl;1:2;
2
(2)根据离子方程式的书写原则可知,该实验室制取氯气反应的离子方程式为MnO +4H+
2+2Cl-(浓) Mn2++Cl↑+2H O,故答案为:MnO +4H++2Cl-(浓) Mn2++Cl↑+2H O;
2 2 2 2 2
II.反应KClO+6HCl(浓) KCl+3Cl ↑+3H O中KClO 中的Cl由+5价降低为Cl 中的0价,
3 2 2 3 2
HCl中的Cl由-1价升高为Cl 中的0价,故用双线桥法表示电子转移的方向和数目为:
2
,故答案为: ;
III.根据元素守恒可推知另一种生成物为HO,根据氧化还原反应的配平原则可知,反应
2
中Mn由MnO 中的+7价变为+2价的Mn2+,化合价降低了5,而C则由HC O 的+3价升
2 2 4
高为+4价的CO,化合价生高了2,根据化合价升高和降低的总数相等的最小公倍数法进
2
行配平可得,该离子方程式为:6H++2MnO +5H C O =10CO ↑+2Mn2++8H O,故答案为:
2 2 4 2 2
6H++2MnO +5H C O =10CO ↑+2Mn2++8H O。
2 2 4 2 2
18. NH Cl+2HCl 3H↑+NCl 2.5 8H++2ClO +10I-=5I +2Cl-
4 2 3 2 2
+4H O 蓝色消失并在30s内不复原 13.5cV×10-3g
2
【详解】(1)①由流程知,电解时反应物有HCl、NH Cl,生成物有H、NCl ,故可先写出
4 2 3
NH Cl+HCl→H ↑+NCl ,然后再利用得失电子守恒、质量守恒原理配平NH Cl+2HCl
4 2 3 4
3H↑+NCl ;
2 3
②在消毒过程中,氯元素最终均被还原为Cl-,变化过程中,1molClO、1molCl 分别得到
2 2
5mol、2mol电子,故ClO 消毒效率是氯气的2.5倍;
2
(2)①ClO 与KI反应时,氯元素被还原为Cl-,I-被氧化为I,故可写出2ClO +10I-
2 2 2
→5I+2Cl-,再结合电荷守恒及溶液呈酸性知有H+参加反应、有水生成,由此可确定最终的
2
答案第8页,共2页离子方程式:8H++2ClO +10I- 5I+2Cl-+4H O;
2 2 2
②滴定终点时溶液由蓝色变为无色,所以滴定终点的现象是蓝色消失并在30s内不复原;
③由相关的方程式可得ClO ~2.5I ~5S O2-,故m(ClO )=0.2cmol/L×10-
2 2 2 3 2
3VL×67.5g·mol-1=13.5cV×10-3g。
19. 1.25 +H+=H O+CO↑ 2ClO +2CN—=2CO +N +2C1— 分液漏
2 2 2 2 2
斗 稀释ClO ,防止因ClO 的浓度过高而发生爆炸
2 2
NaClO+H O+H SO =Na SO +2ClO ↑+O ↑+2H O
3 2 2 2 4 2 4 2 2 2
【详解】(1)由二氧化氯泡腾片的有效成分为NaClO、NaHSO、NaHCO ,能快速溶于水,
2 4 3
生成的ClO 溶于水得到ClO 溶液,同时生成另一种气体而放出大量气泡可知,溶于水时发
2 2
生的反应为NaClO 与NaHSO 发生氧化还原反应生成NaCl、NaSO 、ClO 和HO ,
2 4 2 4 2 2
NaHSO 与NaHCO 反应生成NaSO 、CO 和HO,反应的化学方程式分别为
4 3 2 4 2 2
5NaClO+4NaHSO =NaCl+4Na SO +4ClO ↑+2H O,NaHSO+NaHCO=
2 4 2 4 2 2 4 3
NaSO +CO ↑+H O,由方程式可知,每生成1mol ClO 消耗NaClO 的量为1mol ×
2 4 2 2 2 2
=1.25mol,生成二氧化碳的离子方程式为 +H+=H O+CO↑,故答案为:1.25;
2 2
+H+=H O+CO↑;
2 2
(2)由题意可知,处理废水时发生的反应为ClO 与水中的CN—离子反应生成NaCl、N 和
2 2
CO,反应的离子方程式为2ClO +2CN—=2CO +N +2C1—,故答案为:2ClO +2CN—
2 2 2 2 2
=2CO +N +2C1—;
2 2
(3)由实验装置图可知,仪器a为分液漏斗;装置A发生的反应为NaClO、HO 和HSO 发
3 2 2 2 4
生反应生成ClO 、NaSO 、O 和HO,反应的化学方程式为
2 2 4 2 2
2NaClO+H O+H SO =Na SO +2ClO ↑+O ↑+2H O;由题干信息可知,ClO 在混合气体中浓
3 2 2 2 4 2 4 2 2 2 2
度过高时易发生爆炸,为防止因浓度过高而发生爆炸,实验时应从A装置左侧通入氮气的
稀释ClO ,故答案为:稀释ClO ,防止因ClO 的浓度过高而发生爆炸;
2 2 2
NaClO+H O+H SO =Na SO +2ClO ↑+O ↑+2H O。
3 2 2 2 4 2 4 2 2 2
20.(1)AsH
3
(2)Br
2
(3)AC(4)
【分析】(1)
.KBrO 在反应中得到电子,作氧化剂,则必有作还原剂的另一物质,其应为含有As元素
3
的物质,AsH 中As的化合价为-3价、HAsO 中As的化合价为+5价,则AsH 为还原剂。
3 3 4 3
(2)
2个KBrO 在反应中得到10个电子生成X,则Br由+5价降低5价而成为0价的Br,从而
3
得出X的化学式为Br 。
2
(3)
上述反应可写成AsH +KBrO+H SO →HAsO +K SO +Br +H O,KBrO 为氧化剂,HAsO
3 3 2 4 3 4 2 4 2 2 3 3 4
为氧化产物,AsH 为还原剂,Br 为还原产物:
3 2
A.氧化性:氧化剂>氧化产物,则KBrO >HAsO ,正确;
3 3 4
B.由A可知,氧化性:HAsO <KBrO ,不正确;
3 4 3
C.还原性:还原剂>还原产物,则AsH >X(Br ),正确;
3 2
D.由C可知,还原性:X(Br )<AsH ,不正确;
2 3
故选AC;
(4)
反应中1个KBrO 得到5个电子,1个AsH 失去8个电子,根据得失电子守恒、原子守恒,
3 3
反应的化学方程式为5AsH +8KBrO+4H SO =5H AsO +4K SO +4Br +4H O中,用单线桥法
3 3 2 4 3 4 2 4 2 2
标出电子转移的方向和数目: 。
21. 稀释ClO ,防止其发生爆炸 2ClO +HO+2H+=2ClO +O↑+
2 2 2 2 2
2HO 溶液蓝色褪去 n(Na SO)=1.00×10-4mol·L-1×20.00×10-3 L=2.00×10-6
2 2 2 3
mol; ~ 2I ~ 4 ,则n( )= n(Na SO)= ×2.00×10-6mol=5.00×10-7 mol ;m(
2 2 2 3
)=5.00×10-7 mol×67.5 g·mol-1=3.375 ×10-5 g=3.375×10-2 mg;w( )=
答案第10页,共2页, 该水样中 的含量>0.20 mg·L-1,因此不符合国家规定。
【分析】B装置中NaClO 和HO 在酸性条件下反应生成ClO 、O、HO;通入N 可以将
3 2 2 2 2 2 2
ClO 排出并且能够稀释ClO ,防止其发生爆炸;C装置中ClO 具有强氧化性,可以和CN-
2 2 2
发生氧化还原反应,从而除去废水中的CN-;D装置中装有NaOH溶液,可以吸收ClO ,
2
防止污染空气。
【详解】(1)①通入氮气有利于将ClO 排出,还有稀释ClO ,防止其发生爆炸;
2 2
②装置B中生成ClO 的离子方程式为2ClO +HO+2H+=2ClO +O↑+2HO;
2 2 2 2 2 2
(2)①淀粉溶液遇碘变蓝,故滴定终点的现象是溶液蓝色褪去;
②n(Na SO)=1.00×10-4mol·L-1×20.00×10-3 L=2.00×10-6 mol; ~ 2I ~ 4
2 2 3 2
n( )= n(Na SO)= ×2.00×10-6mol=5.00×10-7 mol ;m( )=5.00×10-7 mol×67.5
2 2 3
g·mol-1=3.375 ×10-5 g=3.375×10-2 mg;w( )= , 该水样中
的含量>0.20 mg·L-1,因此不符合国家规定。
22.(1) 和
(2) (或 )
, (或
)
(3) 排尽装置中的空气,防止连二亚硫酸钠被氧化 有黄色晶体析出,并产生大
量气泡
(4)阻止装置C中水蒸气进入装置B中,避免生成的 与水反应
(5)A
(6)83.5%【分析】A中亚硫酸钠和70%硫酸反应制备二氧化硫气体,为防止 遇水发生强烈
反应,前后都通过浓硫酸干燥二氧化硫气体,然后通入B中生成 ,最后通入C中
尾气吸收。
(1)
中S为+3价,故在空气中被氧化生成两种常见酸式盐为 和 。
(2)
根据分析可知,按气流方向,上述各仪器口的连接顺序为a→
(或 )。装置B中二氧化硫、甲酸和氢氧化钠反应
的化学方程式为 ,
(或
)。
(3)
因 具有较强的还原性,为防止 被氧化,先从b口通入一段时间N,排尽
2
装置中的空气。通入 一段时间,发生上述反应,产生不溶于乙醇的淡黄色固体
和产生大量气泡。
(4)
因 遇水发生强烈反应,装置D中浓硫酸的作用为阻止装置C中水蒸气进入装置B
中,避免生成的 与水反应。
(5)
答案第12页,共2页因 具有较强的还原性,不溶于乙醇,易溶于氢氧化钠溶液,遇水发生强烈反应,
故选甲醇为洗涤剂。
(6)
25.00mL溶液消耗 的物质的量为0.10mol/L×0.024mL=0.0024mol,则200mL溶
液消耗 的物质的量为0.0192mol,根据
可得 的物质的量为
0.0096mol,则样品中 的质量分数为 。答案第14页,共2页