文档内容
第三章 水溶液中的离子反应与平衡
第一节 电离平衡
一、强电解质和弱电解质
1、电解质:在水溶液中或 熔融状态下 能导电的化合物。
2、非电解质:在水溶液中和 熔融状态下 均以分子形式存在,因而不能导电的化合物。
3、强电解质和弱电解质
(1)实验探究盐酸和醋酸的电离程度
酸 0.1 mol·L-1盐酸 0.1 mol·L-1醋酸
pH 较 小 较 大
导电能力 较 强 较 弱
与镁条反应的现象 产生无色气泡 较快 产生无色气泡 较慢
实验表明盐酸中c(H+) 更大 ,说明盐酸的电离程度 大于 醋酸的电离程
实验结论
度
(2)强电解质与弱电解质的比较
强电解质 弱电解质
概念 在水溶液中能 全部 电离的电解质 在水溶液中只能 部分 电离的电解质
电解质在溶液
只有 阴、阳离子 既有 阴、阳离子 ,又有电解质 分子
中的存在形式
化合物类型 离子化合物、部分共价化合物 共价化合物
①多数盐(包括难溶性盐); ① 弱酸 ,如CHCOOH、HClO等;
3
实例 ② 强酸 ,如HCl、HSO 等; ② 弱碱 ,如NH ·H O等;
2 4 3 2
③ 强碱 ,如KOH、Ba(OH) 等 ③水
2
二、弱电解质的电离平衡
1、电离平衡状态
(1)概念:在一定条件(如温度、浓度)下,弱电解质分子 电离成离子的速率 与 离子结合成弱电解质
分子的速率 相等,溶液中各分子和离子的 浓度 都不再发生变化,电离过程就达到了电离平衡状态。
(2)建立过程
学科网(北京)股份有限公司2、电离方程式的书写
(1)强电解质:完全电离,在写电离方程式时,用“===”。
(2)弱电解质:部分电离,在写电离方程式时,用“
⇄
”。
3、电离平衡的影响因素
(1)温度:弱电解质的电离一般是 吸热 过程,升高温度使电离平衡向 电离 的方向移动,电离程
度 增大 。
(2)浓度:在一定温度下,同一弱电解质溶液,浓度越小,离子相互碰撞结合为分子的几率 越小 ,
电离程度 越大 。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方
向移动,电离程度 减小 。
(4)化学反应:加入能与弱电解质电离出的离子发生反应的离子时,电离平衡向 电离 方向移动。
三、电离平衡常数
1、概念:在一定条件下,当弱电解质的电离达到平衡时,溶液中弱电解质电离所生成的 各种离子浓度
的乘积 ,与溶液中 未电离分子的浓度 之比是一个常数,简称电离常数,用K表示。
2、电离平衡常数的表示方法
AB=A++B- K=
3、弱电解质的电离能力。一定温度下,K值越大,弱电解质的电离程度越 大 ,酸(或碱)性越 强 。
4.电离常数的影响因素
(1)内因:同一温度下,不同的弱电解质的电离常数 不同 ,说明电离常数首先由物质的 本性 所决定。
(2)外因:对于同一弱电解质,电离平衡常数只与 温度 有关,由于电离为 吸热 过程,所以电离平衡
常数随 温度升高 而增大。
5、电离常数的计算——三段式法
例:25 ℃ a mol·L-1的CHCOOH
3
CHCOOH CHCOO-+H+
3 3
起始浓度/mol·L-1 : a 0 0
⇄
变化浓度/mol·L-1 : x x x
平衡浓度/mol·L-1 : a-x x x
则K==≈
a
6、实验探究:CHCOOH与HCO 酸性强弱比较
3 2 3
实验操作
实验现象 有 气泡 产生
实验结论 CHCOOH酸性大于碳酸
3
K 大小比较 K(CHCOOH) 大于 K (H CO)
a a 3 a1 2 3
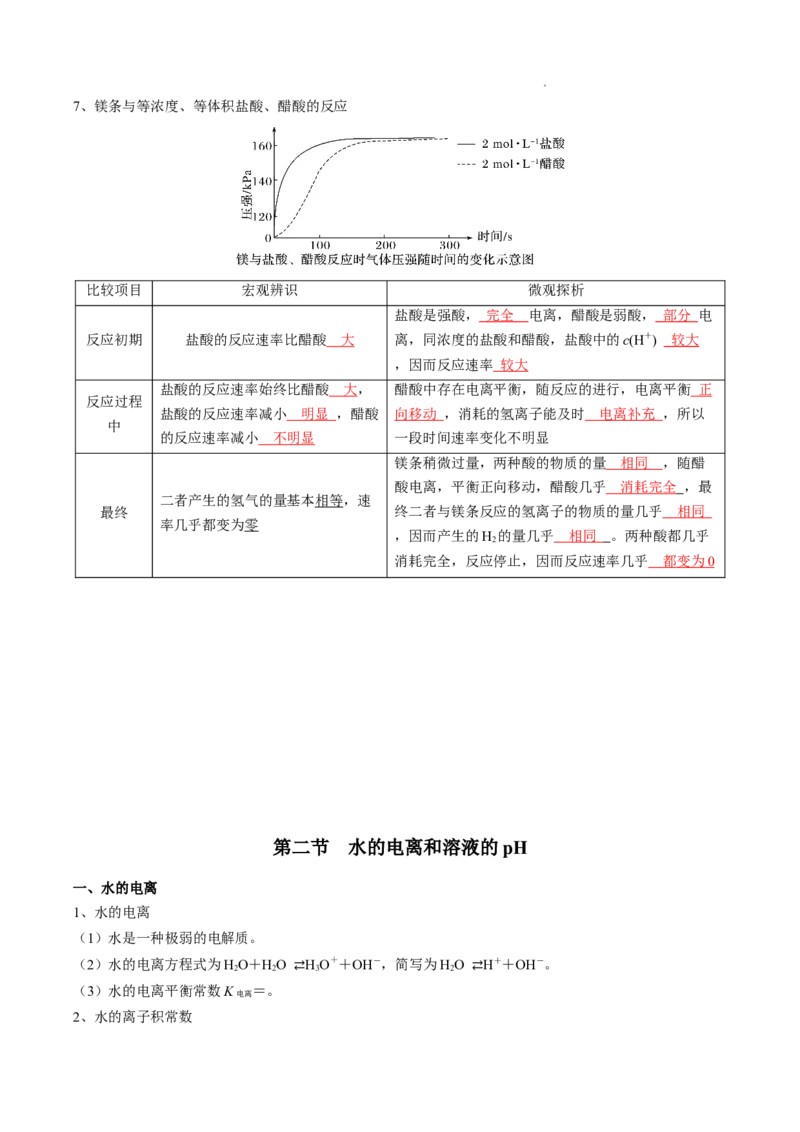
学科网(北京)股份有限公司7、镁条与等浓度、等体积盐酸、醋酸的反应
比较项目 宏观辨识 微观探析
盐酸是强酸, 完全 电离,醋酸是弱酸, 部分 电
反应初期 盐酸的反应速率比醋酸 大 离,同浓度的盐酸和醋酸,盐酸中的c(H+) 较大
,因而反应速率 较大
盐酸的反应速率始终比醋酸 大, 醋酸中存在电离平衡,随反应的进行,电离平衡 正
反应过程
盐酸的反应速率减小 明显 ,醋酸 向移动 ,消耗的氢离子能及时 电离补充 ,所以
中
的反应速率减小 不明显 一段时间速率变化不明显
镁条稍微过量,两种酸的物质的量 相同 ,随醋
酸电离,平衡正向移动,醋酸几乎 消耗完全 ,最
二者产生的氢气的量基本相等,速
最终 终二者与镁条反应的氢离子的物质的量几乎 相同
率几乎都变为零
,因而产生的H 的量几乎 相同 。两种酸都几乎
2
消耗完全,反应停止,因而反应速率几乎 都变为 0
第二节 水的电离和溶液的pH
一、水的电离
1、水的电离
(1)水是一种极弱的电解质。
(2)水的电离方程式为HO+HO HO++OH-,简写为HO H++OH-。
2 2 3 2
(3)水的电离平衡常数K =。
电离 ⇄ ⇄
2、水的离子积常数
学科网(北京)股份有限公司(1)含义:因为水的浓度可看作常数,所以水中的 c(H + )·c(OH - ) 可看作常数,称为水的 离子积常数 ,
简称水的离子积,用K 表示。
W
(2)表达式与数值:表达式K = c(H + )·c(OH - ) ,室温时,K =1.0×10-14。
W W
(3)影响因素:K 只受温度影响,由于水的电离是 吸热 过程,温度升高,K 增大。
W W
3、外界条件对水的电离平衡的影响
分析下列条件的改变对水的电离平衡HO H++OH- ΔH>0的影响,并填写下表:
2
改变条件 平衡移动方向 c(H+) c(OH-) 水的电离程度 K
⇄ w
升高温度 右移 增大 增大 增大 增大
加入HCl(g) 左移 增大 减小 减小 不变
加入NaOH(s) 左移 减小 增大 减小 不变
加入金属Na 右移 减小 增大 增大 不变
加入NaHSO(s) 左移 增大 减小 减小 不变
4
二、溶液的酸碱性与pH
1.25 ℃时,分析下列溶液的氢离子和氢氧根离子浓度
纯水 0.1 mol·L-1 NaOH溶液 0.1 mol·L-1盐酸
c(H+)/mol·L-1 1×10 - 7 1×10 - 13 0.1
c(OH-)/mol·L-1 1×10 - 7 0.1 1×10 - 13
c(H+) 、c(OH-)
c (H + ) = c (OH - ) c(H+)< c(OH-) c(H+)> c(OH-)
的相对大小
溶液的酸碱性 中性 碱性 酸性
2、溶液的酸碱性与溶液中c(H+)、c(OH-)的关系
c(H+)与c(OH-)的关系 c(H+)的范围(室温下)
酸性溶液 c(H+)>c(OH-) c(H+)> 1×10 - 7 mol·L-1
中性溶液 c(H+)=c(OH-) c(H+)= 1×1 0 - 7 mol·L-1
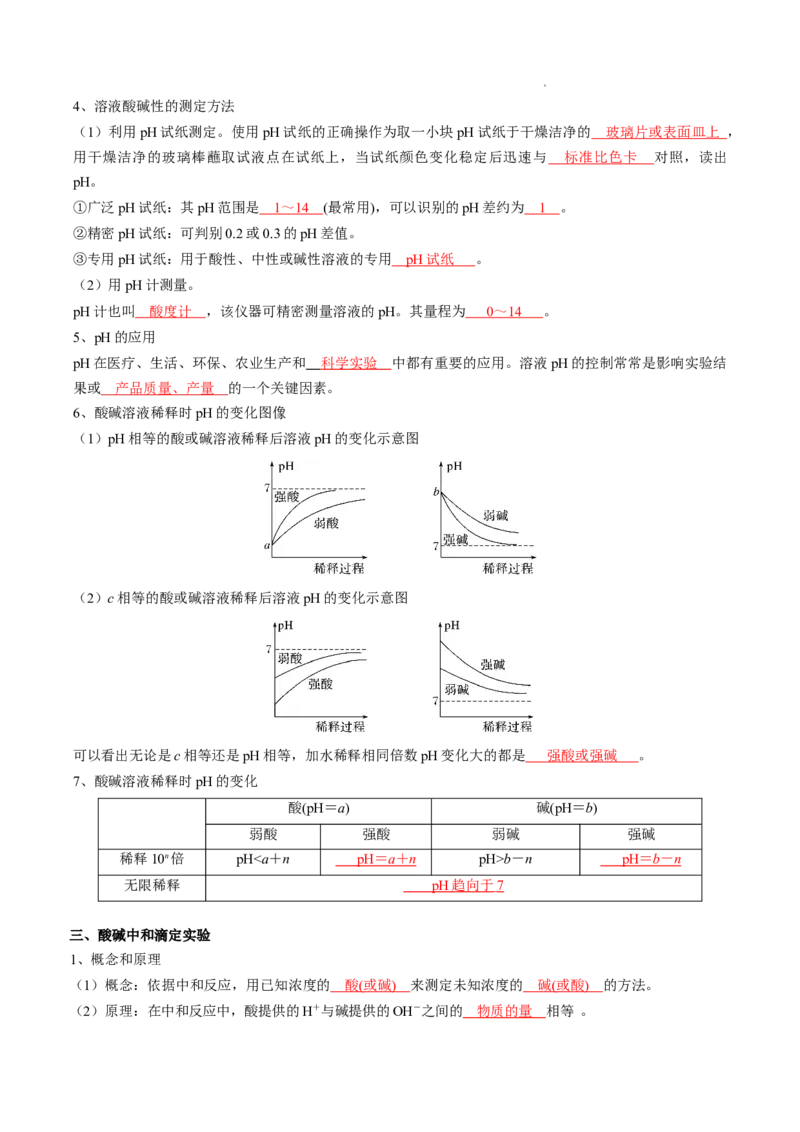
碱性溶液 c(H+)b-n pH = b - n
无限稀释 pH 趋向于 7
三、酸碱中和滴定实验
1、概念和原理
(1)概念:依据中和反应,用已知浓度的 酸 ( 或碱 ) 来测定未知浓度的 碱 ( 或酸 ) 的方法。
(2)原理:在中和反应中,酸提供的H+与碱提供的OH-之间的 物质的量 相等 。
学科网(北京)股份有限公司即: c (H + ) · V = c (OH - ) · V ,则c(H+)=或c(OH-)=。
酸 碱
2、主要仪器使用
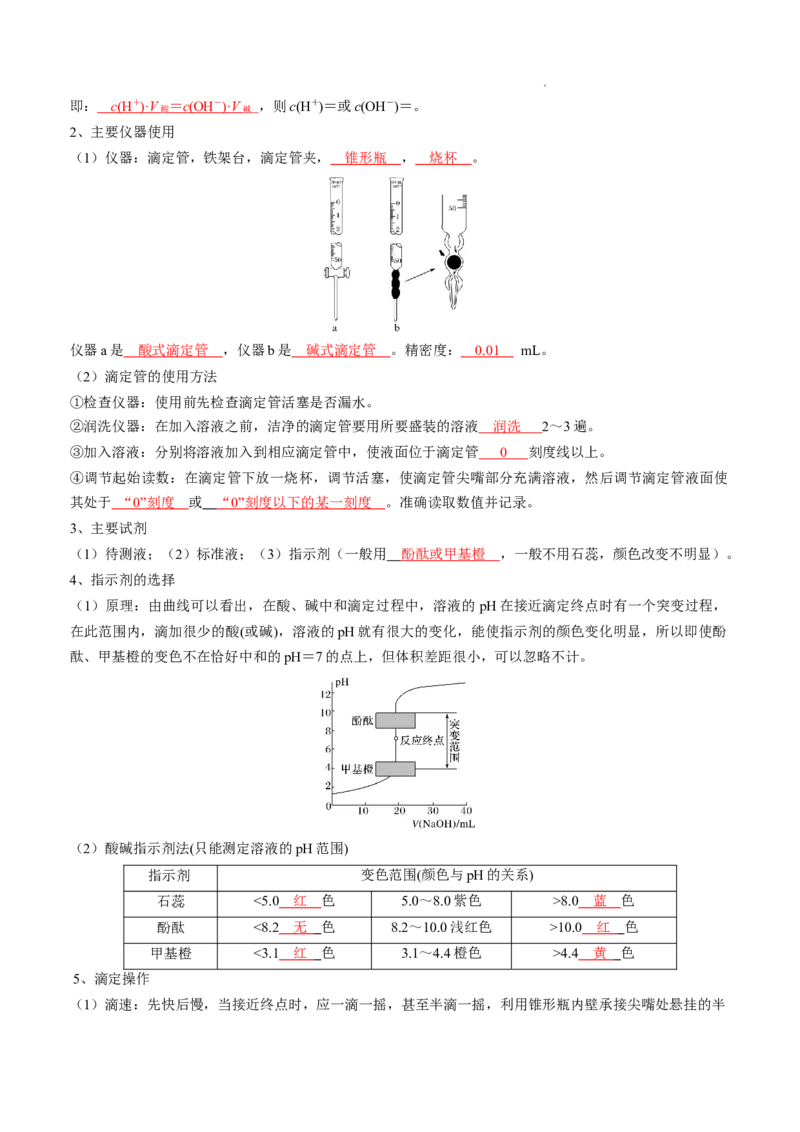
(1)仪器:滴定管,铁架台,滴定管夹, 锥形瓶 , 烧杯 。
仪器a是 酸式滴定管 ,仪器b是 碱式滴定管 。精密度: 0.01 mL。
(2)滴定管的使用方法
①检查仪器:使用前先检查滴定管活塞是否漏水。
②润洗仪器:在加入溶液之前,洁净的滴定管要用所要盛装的溶液 润洗 2~3遍。
③加入溶液:分别将溶液加入到相应滴定管中,使液面位于滴定管 0 刻度线以上。
④调节起始读数:在滴定管下放一烧杯,调节活塞,使滴定管尖嘴部分充满溶液,然后调节滴定管液面使
其处于 “ 0 ” 刻度 或 “ 0 ” 刻度以下的某一刻度 。准确读取数值并记录。
3、主要试剂
(1)待测液;(2)标准液;(3)指示剂(一般用 酚酞或甲基橙 ,一般不用石蕊,颜色改变不明显)。
4、指示剂的选择
(1)原理:由曲线可以看出,在酸、碱中和滴定过程中,溶液的pH在接近滴定终点时有一个突变过程,
在此范围内,滴加很少的酸(或碱),溶液的pH就有很大的变化,能使指示剂的颜色变化明显,所以即使酚
酞、甲基橙的变色不在恰好中和的pH=7的点上,但体积差距很小,可以忽略不计。
(2)酸碱指示剂法(只能测定溶液的pH范围)
指示剂 变色范围(颜色与pH的关系)
石蕊 <5.0 红 色 5.0~8.0紫色 >8.0 蓝 色
酚酞 <8.2 无 色 8.2~10.0浅红色 >10.0 红 色
甲基橙 <3.1 红 色 3.1~4.4橙色 >4.4 黄 色
5、滴定操作
(1)滴速:先快后慢,当接近终点时,应一滴一摇,甚至半滴一摇,利用锥形瓶内壁承接尖嘴处悬挂的半
学科网(北京)股份有限公司滴溶液。
(2)终点的判断:滴入最后一滴标准液,指示剂变色,且在 半分钟 内不变回原色,视为 滴定 终点。
6、数据处理
为减少实验误差,重复实验 2 ~ 3 次,求出所用标准溶液体积的 平均值 ,然后再计算待测液的 物质
的量 浓度。
7、常见的误差分析
步骤 操作 V c
标准 待测
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用标准溶液润洗 变小 偏低
洗涤
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
取液 放出碱液的滴定管开始有气泡,放出液体后气泡消失 变小 偏低
酸式滴定管滴定前有气泡,滴定终点时气泡消失 变大 偏高
振荡锥形瓶时部分液体溅出 变小 偏低
滴定 部分酸液滴出锥形瓶外 变大 偏高
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴
变大 偏高
NaOH溶液无变化
滴定前读数正确,滴定后俯视读数(或前仰后俯) 变小 偏低
读数
滴定前读数正确,滴定后仰视读数(或前俯后仰) 变大 偏高
第三节 盐类的水解
一、盐类的水解
1、探究盐溶液的酸碱性
盐溶液 NaCl NaSO NaCO NaHCO CHCOONa NH Cl (NH )SO
2 4 2 3 3 3 4 4 2 4
pH pH=7 pH=7 pH>7 pH>7 pH>7 pH<7 pH<7
盐的类型 强酸强碱盐 强碱弱酸 盐 强酸弱碱 盐
溶液酸碱性 中 性 碱 性 酸 性
2、盐溶液呈现不同酸碱性的原因
CH COO - 和 H + 结合生成弱电解质 CHCOOH ,使水的电离平衡向电离方向移
3 3
微粒变化
动
平衡时酸碱性 使溶液中c(H+)<c(OH-),溶液呈碱性
水解方程式 CHCOO-+HO CH COOH + OH -
3 2 3
微粒变化 NH 和 OH - 结合生成弱电解质 NH ·H O ,使水的电离平衡向 电离 的方向移动
⇄ 3 2
平衡时酸碱性 使溶液中c(H+)>c(OH-),溶液呈 酸 性
水解方程式 NH+HO NH ·H O + H +
2 3 2
⇄
学科网(北京)股份有限公司水解方程式 HO H++OH-,NaCl===Cl-+Na+
2
理论解释:溶液中不生成 弱电解质 ,水的电离平衡未受影响,溶液中c(H+)=c(OH-),溶液呈 中
⇄
性。
3、盐类的水解
(1)概念:在溶液中,由盐电离出来的弱离子跟水电离出来的H+或OH-结合生成弱电解质的反应。
(2)实质:生成弱酸或弱碱,使水的电离平衡被破坏而建立起新的平衡。
(3)特征:①一般是可逆反应,在 一定 条件下达到化学平衡;②盐类水解反应是 中和 反应的逆反应。
③盐类水解是 吸热 反应。
二、影响盐类水解的主要因素
1、反应物本身性质的影响
盐类水解程度的大小主要由 盐的性质 所决定的,生成盐的弱酸(或弱碱)越难 电离 (电离常数越小),
盐的水解程度 越大 ,即越弱越水解。
2、实验探究反应条件对盐类水解程度的影响
已知FeCl 发生水解反应的离子方程式:Fe3++3HO Fe(OH) +3H+,根据实验操作填写下表:
3 2 3
影响因素 实验步骤 实验现象 解释
⇄
加入FeCl 固
3
溶液颜色变 深 ,溶 加入FeCl 固体,c(Fe3+)增大,水解平衡向
3
盐的浓度 体,再测溶液的
液的pH 变小 正反应 方向移动
pH
加盐酸后,测溶 溶液颜色变 浅 ,溶 加入盐酸,c(H+)增大,水解平衡向 逆反应
液的pH 液的pH 变小 方向移动,但c(H+)仍比原平衡中c(H+)大
溶液的酸碱度
加入少量NaOH 加入氢氧化钠后,OH-消耗H+,c(H+)减
产生 红褐 色沉淀
溶液 小,水解平衡向 正反应 方向移动
温度 升高温度 溶液颜色变深 升高温度,水解平衡正向移动
3、盐的水解常数
(1)表达式
以CHCOONa为例:CHCOO-+HO CHCOOH+OH-
3 3 2 3
K =,只与 温度 有关。
h ⇄
(2)与对应弱酸电离常数的关系
K= 所以,K ·K=K 或K =。
a h a w h
弱酸或弱碱的电离常数 越小 (越弱),其生成的盐水解的程度就 越大 。
三、盐类水解的应用
1、在化学实验中的应用
应用 举例
判断溶液的酸碱性 FeCl 溶液显酸性,原因是Fe3++3HO===Fe(OH) +3H+
3 2 3
判断酸性强弱 相同浓度的NaX、NaY、NaZ溶液的pH分别为8、9、10,则酸性:
学科网(北京)股份有限公司HX>HY>HZ
配制或贮存易水解 配制CuSO 溶液时,加入少量 H SO ,抑制Cu2+水解;贮存NaCO 溶液
4 2 4 2 3
的盐溶液 不能用 磨口 玻璃塞
胶体的制取 制取Fe(OH) 胶体的离子反应:Fe3++3HO=====Fe(OH) (胶体)+3H+
3 2 3
制备无水盐 将挥发性酸的弱碱盐如AlCl 、FeCl 溶液蒸干时,在通HCl的气流中加热蒸干
3 3
Al3+与CO、HCO、S2-、HS-、AlO;Fe3+与HCO、CO、AlO;NH与AlO、
判断离子是否共存
SiO因相互促进水解强烈而 不能大量 共存。
判断中和反应至中 如NH ·H O与HCl反应至中性, NH ·H O 过量,CHCOOH与NaOH反应
3 2 3 2 3
性的试剂用量 至中性时 CH COOH 过量。
3
如用TiCl 制备TiO,其反应的化学方程式为:
4 2
制备无机化合物 TiCl +(x+2)H O===TiO·xHO↓+4HCl
4 2 2 2
加入大量的水,同时加热,促使水解趋于完全。
2、在生产生活中的应用
泡沫灭火器中药品成分为NaHCO 与Al (SO ),发生的反应为:
3 2 4 3
泡沫灭火器原理
Al3++3HCO===Al(OH) ↓+3CO↑
3 2
作净水剂 明矾可作净水剂,原理为Al3++3HO===Al(OH) (胶体)+3H+
2 3
化肥的使用 铵态氮肥与草木灰不得混合施用
NH Cl溶液与ZnCl 溶液可作焊接时的除锈剂,原理为:
4 2
除锈剂
NH+HO===NH ·H O+H+、Zn2++2HO===Zn(OH) +2H+
2 3 2 2 2
热纯碱去污能力强 加热,促进NaCO 的水解,使c(OH-)增大,去污能力增强
2 3
四、溶液中的守恒关系
1、电荷守恒:电解质溶液中 阳离子 所带的电荷总数与 阴离子 所带的电荷总数 相等 。即电荷
守恒,溶液呈 电中性 。
2、元素质量守恒:
在电解质溶液中,由于某些离子发生水解或电离, 离子 的存在形式发生了变化,就该 离子 所含的
某种元素来说,其质量在反应前后是 守恒 的,即 元素质量 守恒。
如:NaCO 溶液中:
2 3
①=,即n(Na+)=2c(CO),CO在水中部分会水解成HCO、HCO,共三种含碳元素的存在形式。
2 3
②c(Na+)=2[c(CO)+c(HCO)+c(H CO)]。
2 3
3、质子守恒
方法一:可以由电荷守恒与元素质量守恒推导出来。
如NaCO 中将电荷守恒和元素质量守恒中的金属阳离子消去得c(OH-)=c(H+)+c(HCO)+2c(H CO)。
2 3 2 3
方法二:质子守恒是依据水的电离平衡:HO=H++OH-,水电离产生的H+和OH-的物质的量总是相等
2
的,无论在溶液中由水电离出的H+和OH-以什么形式存在。
如:NaCO 溶液中即:c(OH-)=2c(H CO)+c(HCO)+c(H O+)或c(OH-)=2c(H CO)+c(HCO)+c(H+)。
2 3 2 3 3 2 3
学科网(北京)股份有限公司第四节 沉淀溶解平衡
一、难溶电解质的沉淀溶解平衡
1、25 ℃时,溶解性与溶解度的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 >10 g 1~10 g 0.01 ~ 1 g <0.01 g
2、难溶电解质的沉淀溶解平衡
(1)沉淀溶解平衡的建立
(2)沉淀溶解平衡方程式
以AgCl沉淀溶解平衡为例:AgCl(s)===Ag+(aq)+Cl-(aq)。
(3)沉淀、溶解之间这种动态平衡也决定了Ag+与Cl-的反应 不能完全 进行到底。一般情况下,当溶
液中剩余离子的浓度小于 1×1 0 - 5 mol·L - 1 时,化学上通常认为生成沉淀的反应进行 完全 了。
3、难溶电解质沉淀溶解平衡的影响因素
已知沉淀溶解平衡:Mg(OH) (s)===Mg2+(aq)+2OH-(aq)
2
条件改变 移动方向 c(Mg2+) c(OH-)
加少量水 正向移动 不变 不变
升温 正向移动 增大 增大
加MgCl (s) 逆向移动 增大 减小
2
加盐酸 正向移动 增大 减小
加NaOH(s) 逆向移动 减小 增大
Q:离子积对于A B (s)===mAn+(aq)+nBm-(aq)任意时刻Q=cm(An+)·cn(Bm-)。
m n
(1)Q>K ,溶液过饱和,有 沉淀 析出,直至溶液 饱和 ,达到新的平衡。
sp
(2)Q=K ,溶液饱和,沉淀与溶解处于 平衡状态 。
sp
(3)Q