文档内容
第八章 单元过关检测
时间:90分钟 满分:100分
一、选择题(本题共14小题,每小题3分,共42分)
1.环境问题越来越引起人类的重视,下列有关环境问题的描述不正确的是(
)
A.水体的富营养化主要是向水体中排放大量含N、P的物质造成的
B.低碳生活是指少用煤炭的生活
C.氟氯代烷的大量排放造成了臭氧层空洞
D.造成光化学烟雾的是包括NO、NO 等多种气体
2
答案 B
解析 A项,含N、P的物质易导致水体富营养化;B项,少用煤炭的生活
只是低碳生活的一个方面;C项,氟氯代烷是导致臭氧层空洞的因素之一;D项,
NO 能导致光化学烟雾。
x
2.某工厂排出的废水经检验pH<7,并含有较多的Cu2+,它们对人体、牲畜
和农作物都有害,从回收利用和环境保护的角度考虑,切合实际的合理方案是加
入( )
A.NaCl和HCl B.Na SO 和MgCl
2 4 2
C.CaO和铁粉 D.石灰石和Ag
答案 C
解析 NaCl和HCl不但不能回收可溶性铜盐而且会使废水酸性增强,故 A
不符合题意;加入Na SO 和MgCl 既不能与废水中的酸反应,也不能和可溶性
2 4 2
铜盐反应而达到回收铜的目的,故 B不符合题意;加入铁粉可以与铜离子反应
生成铜从而回收铜,加入的生石灰可以降低废水的酸性,故 C符合题意;加入
石灰石能与酸反应从而降低废水的酸性,银不能与含铜离子的盐反应,故不能回
收铜,故D不符合题意。
3.下列物质不属于高分子化合物的是( )
①甘油 ②油脂 ③纤维素 ④淀粉 ⑤有机玻璃
⑥蛋白质 ⑦蔗糖 ⑧天然橡胶 ⑨苯 ⑩涤纶
A.①④⑥⑦ B.①②⑦⑨
C.③⑤⑥⑩ D.②③⑦⑧
答案 B
4.绿色化学要求利用化学反应原理从源头上减少或消除污染。以铜为原料
制备硫酸铜,下列四种原理设计,其中最能体现“绿色化学”要求的是( )
A.Cu+2H SO (浓)=====CuSO +SO ↑+2H O
2 4 4 2 2
B.Cu+Cl =====CuCl ,CuCl +H SO (浓)=====CuSO +2HCl↑
2 2 2 2 4 4C.Cu+H SO +H O =====CuSO +2H O
2 4 2 2 4 2
D . 3Cu + 8HNO ===3Cu(NO ) + 2NO↑ + 4H O , Cu(NO ) +
3 3 2 2 3 2
H SO (浓)=====CuSO +2HNO ↑
2 4 4 3
答案 C
解析 根据题意可知,A项放出有毒气体SO ,B项利用了有毒气体Cl ,D
2 2
项放出有毒气体NO,均不符合“绿色化学”的要求。
5.热还原法冶炼金属的反应一定是( )
A.置换反应 B.分解反应
C.复分解反应 D.氧化还原反应
答案 D
解析 热还原法冶炼金属常用的还原剂是C、H 、CO、Al等,若是单质作
2
还原剂,发生的是置换反应,同时也属于氧化还原反应;若是 CO作还原剂,则
发生氧化还原反应。
6.将煤块粉碎,经脱硫处理,在适当过量的空气中燃烧,这样处理的目的
是( )
①使煤充分燃烧,提高煤的利用率 ②减少SO 的产生,避免造成“酸雨”
2
③减少有毒的CO产生,避免污染空气 ④减少CO 的产生,避免“温室效应”
2
A.①②③ B.②③④
C.①③④ D.①②④
答案 A
解析 将煤块粉碎,目的是使煤充分燃烧,提高煤的利用率;对煤进行脱硫
处理,目的是减少煤燃烧过程中产生过多的 SO ;将煤在适当过量的空气中燃烧,
2
是使煤充分燃烧,减少CO的产生,减轻空气污染,但不会减少 CO 的产生,无
2
法避免“温室效应”。
7.下列化学实验符合“绿色化学”要求的有( )
①在萃取操作的演示实验中,将 CCl 萃取溴水改为 CCl 萃取碘水 ②在制
4 4
备CuSO 时,用铜与浓硫酸反应,将铜片改为可调节高度的铜丝 ③将实验室
4
的废酸液或废碱液进行处理后再排放 ④加成反应、酯化反应和加聚反应最符合
“原子经济性”
A.②③ B.①③
C.①④ D.②④
答案 B
解析 ①Br 易挥发,I 不易挥发,将CCl 萃取溴水改为萃取碘水可减少空
2 2 4
气污染;②铜丝仍与浓硫酸反应生成SO ,造成污染;③实验室中的废酸液或废
2
碱液会污染环境,应处理后再排放;④酯化反应中有副产物 H O生成,不符合
2
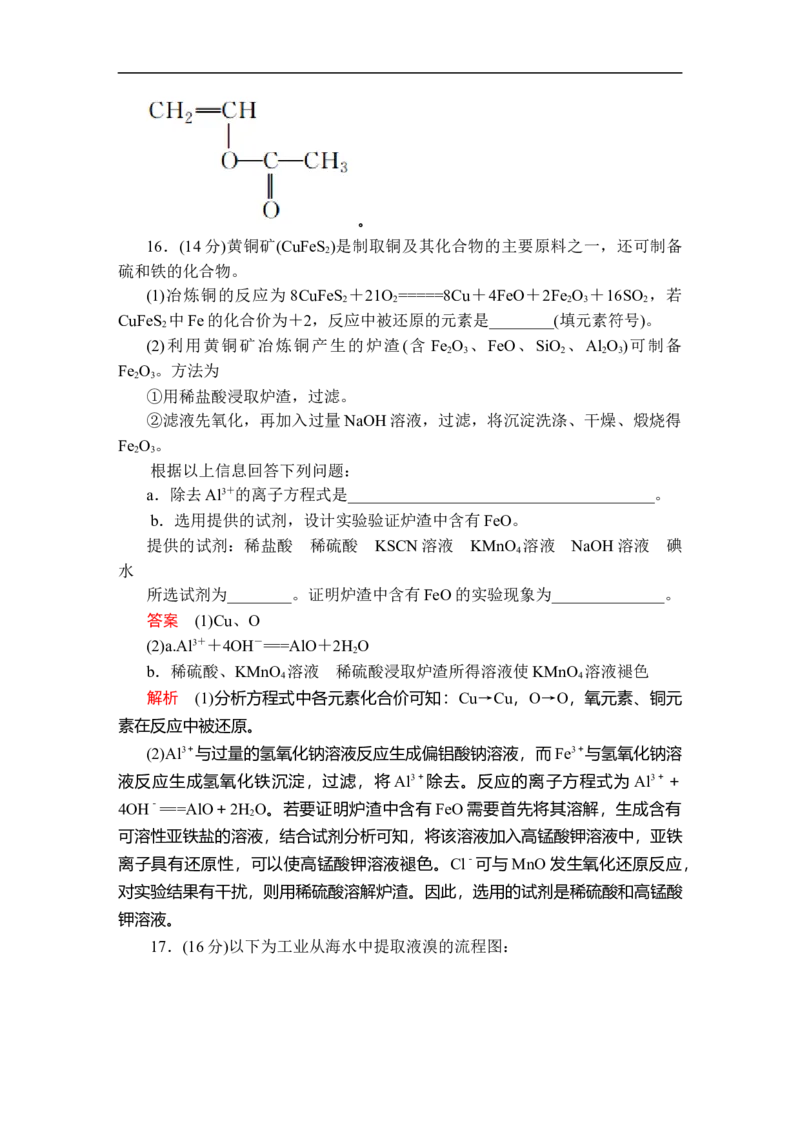
“原子经济性”。8.聚丙烯酸酯的结构简式可表示为 ,由丙烯酸酯加
聚得到。下列关于聚丙烯酸酯的说法不正确的是( )
A.属于高分子化合物
B.链节为—CH —CH—
2
C.单体为CH ===CH—COOR
2
D.n为聚合度
答案 B
解析 依据高分子化合物聚丙烯酸酯的结构简式,可确定其链节为
,n 为聚合度,故
B不正确。
9.关于百年经典药物阿司匹林的叙述正确的是( )
A.阿司匹林是治胃酸药
B.阿司匹林属于抗生素
C.阿司匹林是一种白色晶体,易水解
D.阿司匹林之所以成为经典药物是因为服用该药物没有不良反应
答案 C
解析 阿司匹林属于解热镇痛药,不属于抗生素,故 A、B错误;阿司匹林
结构中含酯基,可水解,C正确;阿司匹林之所以成为百年经典药物是因为很早
之前人类就发现了该物质的疗效,D错误。
10.海水中蕴藏着丰富的资源。海水综合利用的示意图如图所示。下列说法
正确的是( )
A.通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等
B.金属镁在空气中燃烧只生成MgO
C.粗盐精制的过程只发生物理变化
D.在高温下用氢气还原MgCl 可制取金属镁
2
答案 A解析 A 项,氯碱工业主要产品是氢氧化钠、氢气和氯气,还可以制取
NaClO、盐酸等产品,正确;B 项,Mg在点燃条件下能与空气中的 O 、N 、
2 2
CO 反应,所以Mg在空气中燃烧的产物有 MgO、Mg N 、C,错误;C项,粗
2 3 2
盐精制的过程既有物理变化,也有化学变化,如除去杂质 SO、Mg2+、Ca2+需要
通过化学反应来完成,属于化学变化,错误;D项,镁是活泼金属,无法用H
2
还原MgCl 来获得金属Mg,工业上用电解熔融MgCl 的方法冶炼镁,错误。
2 2
11.下列化学反应方程式中不属于化学科学解决环境问题的是( )
答案 D
解析 用化学科学解决环境问题主要有:绿色化学理念(原子经济性:反应
物原子全部转化为期望的生成物,无副产物生成),减少和消除化学污染,避免
产生污染气体和对污染气体治理。D中,用苯和液溴制备溴苯,有HBr生成,
不属于化学科学解决环境问题。
12.溴是海水中的重要元素,海水中溴元素的含量一般为0.067 g/L,晒盐浓
缩后的苦卤中含有浓度较高的溴离子,向苦卤中通入氯气,可以得到单质溴。下
列有关说法正确的是( )
A.向苦卤中通入氯气发生反应的离子方程式为
Br-+Cl ===Cl-+Br
2 2
B.向苦卤中通入氯气时,溴元素化合价升高,被还原
C.将单质溴从溴水中分离出来,可以利用裂化汽油进行萃取
D.将单质溴从溴水中分离出来,可以利用苯、四氯化碳等多种有机溶剂进
行萃取
答案 D解析 A项,离子方程式未配平,错误;B项,向苦卤中通入氯气时,溴元
素化合价升高,被氧化,错误;C项,裂化汽油中含有大量不饱和烃,会与溴发
生加成反应,因此不能用作溴的萃取剂,错误;D项,Br 在苯、CCl 中溶解度
2 4
很大,且不与之发生反应,苯、CCl 与水不互溶,因此可用苯、CCl 等萃取溴
4 4
水中的溴,正确。
13.乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制
取氢气具有良好的应用前景。已知通过乙醇制取氢气有如下两条路线:
a.水蒸气催化重整:CH CH OH(g)+H O(g)―→4H (g)+2CO(g) 1 mol乙
3 2 2 2
醇反应吸收255.58 kJ能量
b.部分催化氧化:CH CH OH (g)+O (g)―→3H (g)+2CO(g) 1 mol乙醇反
3 2 2 2
应吸收13.76 kJ能量
则下列说法错误的是 ( )
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.降低温度,可提高b路线中乙醇的反应速率
答案 D
解析 相同质量的乙醇,a路线生成的氢气多;b路线需要的能量远远小于a
路线;降低温度,反应速率减小。
14.人造光卤石(KCl·MgCl ·6H O)是盐化工生产的中间产物。以光卤石为原
2 2
料制得金属镁,可有下列步骤:
①过滤,②溶解,③加入适量Ca(OH) ,④蒸发,⑤用盐酸溶解,⑥电解熔
2
融MgCl ,⑦在HCl气流中加热MgCl ·6H O晶体。
2 2 2
正确的顺序是( )
A.⑤③①②④⑥⑦ B.②③①⑤④⑦⑥
C.②④①③⑦⑤⑥ D.⑤③①④②⑦⑥
答案 B
解析 提纯光卤石得到 MgCl 的步骤为先将光卤石溶于水,因为 KCl、
2
MgCl 均易溶于水,然后沉淀Mg2+;Mg(OH) 的溶解度比Ca(OH) 更小,故加入
2 2 2
适量的Ca(OH) 过滤后得Mg(OH) ,洗涤后溶于适量的盐酸发生反应:Mg(OH)
2 2 2
+2HCl===MgCl +2H O,蒸发溶液得 MgCl ·6H O。在 HCl 气流中加热
2 2 2 2
MgCl ·6H O得到纯净的MgCl ,最后电解熔融MgCl 得到金属镁。
2 2 2 2
二、非选择题(本题共4小题,共58分)
15.(13分)2017年初,我国北方大部分地区出现了严重的空气污染,其主
要原因是化石燃料的大量使用。提高燃料利用率,减少化石燃料的燃烧造成的环
境污染,已成为人类面临的重大挑战。(1)氢气是人类理想的能源,为了有效发展民用氢能源,首先必须制得廉价
的氢气。下列可供开发且比较经济的制氢气的方法是________(填序号)。
①电解水 ②锌与稀硫酸反应 ③光解海水
制得氢气后还需要解决的问题是________(写出其中一个)。
(2)将CO 转化成有机物可有效实现碳循环。CO 转化成有机物的例子很多,
2 2
如:
a.6CO +6H O――→ +6O
2 2 C6H 12O6 2
b.CO +3H ――→CH OH+H O
2 2 3 2
c.CO +CH ――→CH COOH
2 4 3
d.2CO +6H ――→CH ===CH +4H O
2 2 2 2 2
以上反应中,最节能的是________,原子利用率最高的是________(填字母)。
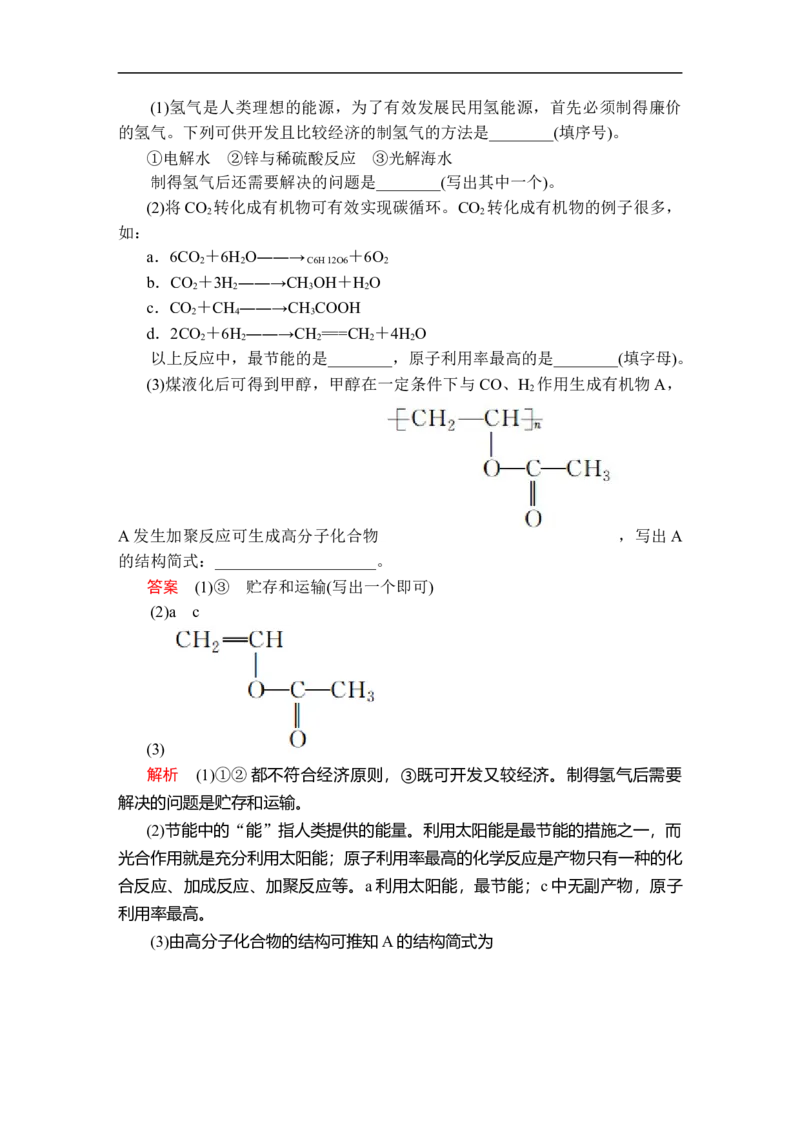
(3)煤液化后可得到甲醇,甲醇在一定条件下与 CO、H 作用生成有机物A,
2
A发生加聚反应可生成高分子化合物 ,写出A
的结构简式:____________________。
答案 (1)③ 贮存和运输(写出一个即可)
(2)a c
(3)
解析 (1)①②都不符合经济原则,③既可开发又较经济。制得氢气后需要
解决的问题是贮存和运输。
(2)节能中的“能”指人类提供的能量。利用太阳能是最节能的措施之一,而
光合作用就是充分利用太阳能;原子利用率最高的化学反应是产物只有一种的化
合反应、加成反应、加聚反应等。a利用太阳能,最节能;c中无副产物,原子
利用率最高。
(3)由高分子化合物的结构可推知A的结构简式为。
16.(14分)黄铜矿(CuFeS )是制取铜及其化合物的主要原料之一,还可制备
2
硫和铁的化合物。
(1)冶炼铜的反应为 8CuFeS +21O =====8Cu+4FeO+2Fe O +16SO ,若
2 2 2 3 2
CuFeS 中Fe的化合价为+2,反应中被还原的元素是________(填元素符号)。
2
(2)利用黄铜矿冶炼铜产生的炉渣(含 Fe O 、FeO、SiO 、Al O )可制备
2 3 2 2 3
Fe O 。方法为
2 3
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得
Fe O 。
2 3
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是______________________________________。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO 溶液 NaOH溶液 碘
4
水
所选试剂为________。证明炉渣中含有FeO的实验现象为______________。
答案 (1)Cu、O
(2)a.Al3++4OH-===AlO+2H O
2
b.稀硫酸、KMnO 溶液 稀硫酸浸取炉渣所得溶液使KMnO 溶液褪色
4 4
解析 (1)分析方程式中各元素化合价可知:Cu→Cu,O→O,氧元素、铜元
素在反应中被还原。
(2)Al3+与过量的氢氧化钠溶液反应生成偏铝酸钠溶液,而Fe3+与氢氧化钠溶
液反应生成氢氧化铁沉淀,过滤,将 Al3+除去。反应的离子方程式为 Al3++
4OH-===AlO+2H O。若要证明炉渣中含有 FeO需要首先将其溶解,生成含有
2
可溶性亚铁盐的溶液,结合试剂分析可知,将该溶液加入高锰酸钾溶液中,亚铁
离子具有还原性,可以使高锰酸钾溶液褪色。Cl-可与MnO发生氧化还原反应,
对实验结果有干扰,则用稀硫酸溶解炉渣。因此,选用的试剂是稀硫酸和高锰酸
钾溶液。
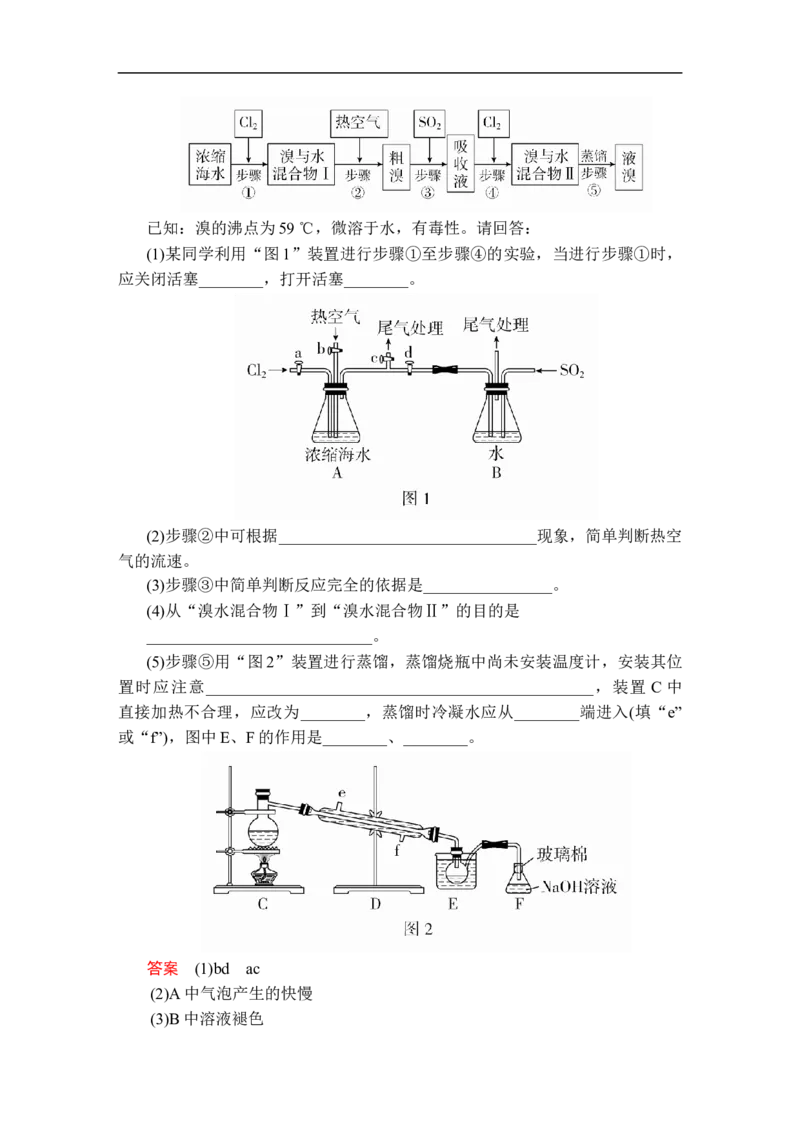
17.(16分)以下为工业从海水中提取液溴的流程图:已知:溴的沸点为59 ℃,微溶于水,有毒性。请回答:
(1)某同学利用“图1”装置进行步骤①至步骤④的实验,当进行步骤①时,
应关闭活塞________,打开活塞________。
(2)步骤②中可根据________________________________现象,简单判断热空
气的流速。
(3)步骤③中简单判断反应完全的依据是________________。
(4)从“溴水混合物Ⅰ”到“溴水混合物Ⅱ”的目的是
____________________________。
(5)步骤⑤用“图2”装置进行蒸馏,蒸馏烧瓶中尚未安装温度计,安装其位
置时应注意________________________________________________,装置 C 中
直接加热不合理,应改为________,蒸馏时冷凝水应从________端进入(填“e”
或“f”),图中E、F的作用是________、________。
答案 (1)bd ac
(2)A中气泡产生的快慢
(3)B中溶液褪色(4)浓缩Br 或富集溴
2
(5)温度计的水银球在蒸馏烧瓶的支管口附近 水浴加热 f 收集溴 吸收
尾气
解析 (1)根据提取溴的流程图,操作是制取Br →吹出Br →用SO 富集溴→
2 2 2
用氯气把Br-氧化,进行步骤①时,通入氯气,因此关闭 bd,打开ac,因为氯
气有毒,尾气必须处理。
(2)通入热空气的目的,是把溴吹入到B装置中,因此判断热空气流速,可
以通过观察气泡产生快慢来判断。
(3)SO +Br +2H O===H SO +2HBr,溴水显(橙)黄色,当反应完全后溶液
2 2 2 2 4
的颜色褪去。
(4)海水中含Br-的百分含量很低,通过一系列的反应,可以提高溴的含量,
因此“溴水混合物Ⅰ”到“溴水混合物Ⅱ”的目的是富集溴或浓缩Br 。
2
(5)蒸馏实验时,温度计的水银球在蒸馏烧瓶的支管口附近,目的是测物质的
沸点,溴的沸点为59 ℃,直接加热不利于温度的控制,可能造成溴单质中含有
大量水分,因此采用水浴加热,蒸馏时为了增强冷凝效果,应从下口入水,从上
口流出,即从f端进入,E的作用是收集液溴,但溴有毒,必须处理尾气,因此
F的作用是吸收尾气。
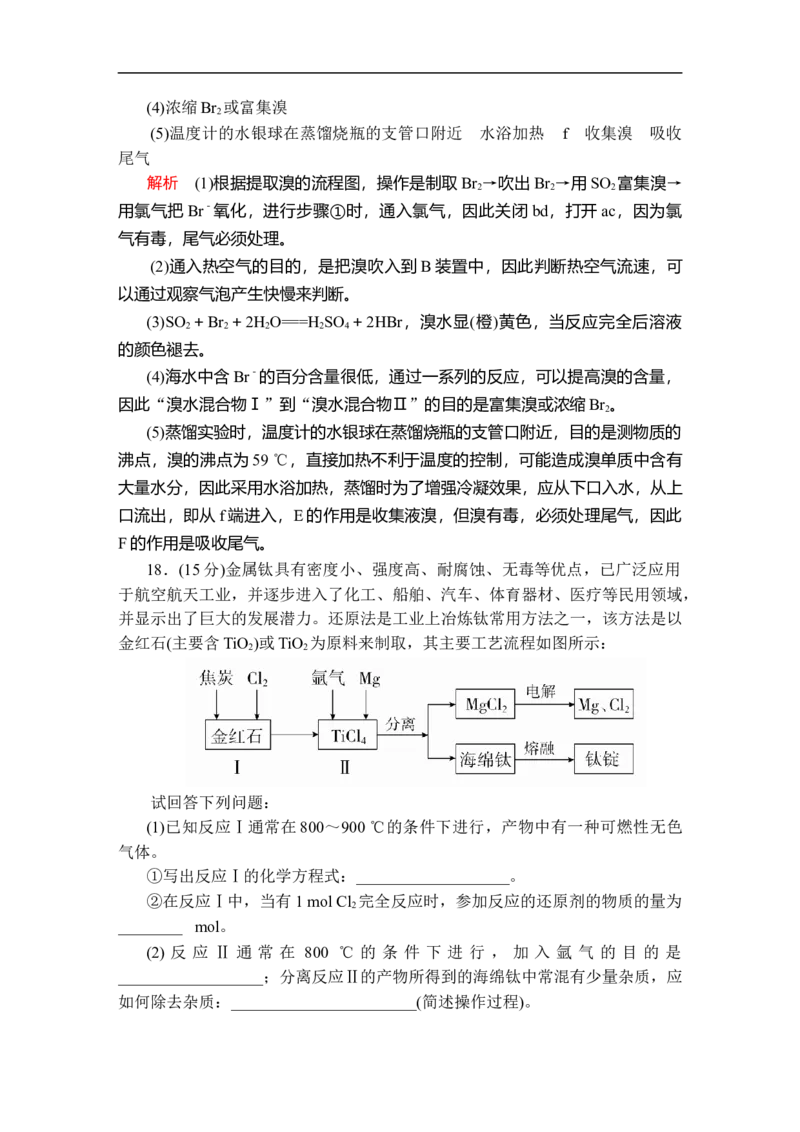
18.(15分)金属钛具有密度小、强度高、耐腐蚀、无毒等优点,已广泛应用
于航空航天工业,并逐步进入了化工、船舶、汽车、体育器材、医疗等民用领域,
并显示出了巨大的发展潜力。还原法是工业上冶炼钛常用方法之一,该方法是以
金红石(主要含TiO )或TiO 为原料来制取,其主要工艺流程如图所示:
2 2
试回答下列问题:
(1)已知反应Ⅰ通常在800~900 ℃的条件下进行,产物中有一种可燃性无色
气体。
①写出反应Ⅰ的化学方程式:___________________。
②在反应Ⅰ中,当有1 mol Cl 完全反应时,参加反应的还原剂的物质的量为
2
________ mol。
(2) 反 应 Ⅱ 通 常 在 800 ℃ 的 条 件 下 进 行 , 加 入 氩 气 的 目 的 是
__________________;分离反应Ⅱ的产物所得到的海绵钛中常混有少量杂质,应
如何除去杂质:_______________________(简述操作过程)。(3)在上述工艺流程中可以循环使用的物质是________。
答案 (1)①TiO +2C+2Cl =====TiCl +2CO ②1
2 2 4
(2)防止镁和钛在高温条件下被空气中的氧气氧化 将海绵钛置于盐酸中酸
洗,然后过滤即可得到纯净的钛
(3)Cl 、Mg和MgCl
2 2
解析 (1)反应Ⅰ的反应物为TiO 、C、Cl ,结合流程图知有TiCl 生成,利
2 2 4
用原子守恒及题给信息可知另一气体产物是 CO,所以反应的化学方程式为 TiO
2
+2C+2Cl =====TiCl +2CO,C在反应中被Cl 氧化,当有 1 mol Cl 完全反应
2 4 2 2
时,参加反应的还原剂(C)的物质的量为1 mol。
(2)反应Ⅱ中反应物Mg以及产物Ti在高温下都易被空气中的氧气氧化,所以
加入氩气的目的是防止镁和钛在高温条件下被空气中的氧气氧化;此法制得的金
属钛中含有少量金属镁和MgCl ,结合镁和钛(题中信息:钛耐腐蚀)的性质可知,
2
可采用盐酸或硫酸酸洗海绵钛即可除去Mg和MgCl 。
2
(3)由流程图知可循环使用的物质为Cl 、Mg以及MgCl 。
2 2