文档内容
高一下学期期末测试卷01
(人教版2019)
高一化学·全解全析
1 2 3 4 5 6 7 8 9 10
A B B C D C B B C A
11 12 13 14
D A D D
1.【答案】A
【解析】
A.明矾——KAl(SO )·12H O,故A正确
4 2 2
B.胆矾——CuSO ·5H O,故B错误
4 2
C.小苏打——NaHCO ,故C错误
3
D.铁红——Fe O,故D错误
2 3
2.【答案】B
【解析】
A. 中子数为20的氯原子: Cl,故A错误
B. B. HO的电子式: ,故B正确
2
C. Na+的结构示意图: ,故C错误
D. Na SO 中有离子键和共价键,故D错误
2 3
3.【答案】D
【解析】
A明矾可水解生成具有吸附性的氢氧化铝胶体,但不具有氧化性,不能用于杀菌消毒,故A错误;
B. 钠是活泼金属,具有还原性,可用与TiCl 熔融固体反应制取金属Ti,溶液中钠与水剧烈反应,不能用
4
Na与溶液反应制备金属,故B错误;
C高温下,氧化铝能与NaOH反应,氧化铝不能用于制造熔融烧碱的坩埚,故C错误;
D. Cu与氯化铁反应生成氯化亚铁、氯化铜,则可用于蚀刻印刷电路板,故D正确;本题选D。
4.【答案】C
【解析】
A. 夜里的月色形成的本质是形成了气溶胶,故A错误;B. 雾是一种胶体,光不是,故B错误;
C. 题干中所提及的雾,是空气中的小液滴,是一种胶体,本质特征是分散质粒子的直径在1∼100nm,故C
正确;
D. 烟雾作为一种胶体,分散质微粒对光的散射能发生丁达尔效应,但这不是月光穿过薄雾所形成的种种美
景的本质原因,故D错误;
5.【答案】D
【解析】
A.用图1所示装置制取少量乙酸乙酯,,导管应在液面以上,故A错误
B.用图2所示装置用品红溶液验证SO 的漂白性,故B错误
2
C.用图3所示装置配制100 mL 0.100 mol·L-1的硫酸溶液,应先将浓硫酸稀释,故C错误
D.用图4所示装置分离水和溴苯,两种液体不互溶,故D正确
6.【答案】C
【分析】
由图可知,A、D为生成物,B、C为反应物,最终各物质的浓度不变且均不为零,该反应为可逆反应,同
一化学反应中,各物质的物质的量变化量之比等于化学方程式中相应物质的化学计量数之比,
Δn(A)∶Δn(B)∶Δn(C)∶Δn(D)=(1.2-0)mol∶(1.0-0.4) mol∶(1.0-0.2)mol∶(0.4-0)mol=6∶3∶4∶2,反应的化学方程
式为3B+4C 6A+2D。
【详解】
A项、由图可知,A、D为生成物,B、C为反应物,反应的化学方程式为3B+4C 6A+2D,故A错误;
B项、各物质的物质的量变化量之比等于化学方程式中相应物质的化学计量数之比,由方程式可知v(A) ≠
v(D),故B错误;
C项、0~6 s内,Δn(B)为0.6 mol,Δc(B)为0.3 mol/L,则B表示的平均反应速率为0.05 mol·(L·s)-1,故C
正确;
D项、各物质表示的反应速率之比均等于化学计量数之比,由方程式可知各物质表示的反应速率不相等,
故D错误。
7.【答案】B
【解析】
A. 酸性溶液中有H+,CO2﹣和H+会反应,不能大量共存,故A错误;
3
B. 澄清透明的溶液中Na+、K+、MnO ﹣和AlO﹣相互不反应,可以大量共存,故B正确;
4 2
C. Fe3+、SCN-结合生成络离子,不能大量共存,故C错误;
D. 能与金属铝反应放出H 的溶液可能是碱性或者酸性,酸性溶液中HCO ﹣不能共存,碱性溶液中Mg2+和
2 3HCO -不能共存,故D错误;
3
8.【答案】B
【解析】
A.氯气溶于水生成氯离子,氯离子抑制了氯气的溶解,所以氯气在饱和食盐水中的溶解度小于在水中的
溶解度,故A正确;
B.反应过程中试管壁上有油珠产生,为二氯甲烷、三氯甲烷、四氯化碳的混合物,不溶于水,为油状液
滴,一氯甲烷是气体,故B错误;
C.CH 和Cl 发生取代反应,生成HCl,HCl遇水形成的白色的酸雾,故C正确;
4 2
D.由实验过程中产生的现象可推知,甲烷与氯气在光照条件下能发生取代反应生成氯化氢和各种卤代烃,
故D正确,
9.【答案】C
【解析】
A.5.6g铁的物质的量为0.1mol,而铁和稀硫酸反应后变为+2价,故0.1mol铁反应后转移0.2N 个电子,故
A
A错误;
B.常温常压下气体摩尔体积大于22.4L/mol,故22.4L二氧化碳的物质的量小于1mol,分子数小于N 个,
A
故B错误;
C.钠离子中含10个电子,故1mol钠离子中含10N 个电子,故C正确;
A
D.溶液体积不明确,故溶液中钠离子的个数无法计算,故D错误
10.【答案】A
【解析】试题分析:银离子能与氯离子、碳酸根离子、银离子结合,镁离子能与碳酸根离子和氢氧根离子
结合,钡离子只能与碳酸根离子结合,故先加入硝酸钡溶液,检验出碳酸根离子,过滤除去生成的沉淀;
然后加入硝酸镁溶液,检验出氢氧根离子,过滤除去生成的沉淀;最后加入硝酸银溶液,检验出氯离子,
故正确的顺序是④②①②③,故选A。
11.【答案】D
【解析】
A、铜不能直接转化为氢氧化铜,A错误;
B、常温下钠与氧气反应生成氧化钠,点燃时生成过氧化钠,B错误;
C、铁不能直接转化为氢氧化铁,故C错误
D、铝与盐酸、氢氧化钠、硫酸分别反应生成氯化铝、偏铝酸钠和硫酸铝,氯化铝与氢氧化钠反应生成偏
铝酸钠,偏铝酸钠与硫酸反应生成硫酸铝,硫酸铝与氯化钡反应生成硫酸钡和氯化铝,D正确,
12.【答案】A
【解析】A.步骤①操作中,硫化锌与稀硫酸反应生成硫酸锌和硫化氢气体,硫化氢气体能与碱反应,可用碱液吸
收,故A正确;
B.由分析可知,滤液1中含有铁离子,若选用硫氰化钾溶液和新制的氯水检验亚铁离子,铁离子会干扰
亚铁离子检验,故B错误;
C.由分析可知,滤渣1含有与稀硫酸不反应的二氧化硅和硫化铜,滤渣2为硫和二氧化硅,故C错误;
D.硫酸是高沸点酸,则滤液2经蒸发浓缩、冷却结晶、过滤得到粗胆矾时,不需要要滴加稀硫酸防止硫
酸铜水解,故D错误;
13.【答案】D
【解析】根据以上分析可知A为O,B为Na,C为S,D为Cl。
A.同周期元素从左到右,元素的原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大,则r >r
Na S
>r >r ,即r(B)>r(C)>r(D)>r(A),故A正确。
Cl O
B.O与Na可生成NaO或NaO 两种化合物,故B正确;
2 2 2
C.非金属性Cl>S,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C正确;
D.非金属性O>S,元素的非金属性越强,对应的氢化物越稳定,故D错误;
14.【答案】D
【解析】
A.因为原电池的构成条件之一为自发的放热的氧化还原反应,所以该反应为放热反应,则2molCu与1
molAg O的总能量高于1 molCu O与2molAg具有的总能量,故A项错误;
2 2
B.原电池工作时,阴离子向负极移动,阳离子向正极移动,故 B项错误;
C.原理示意图中,经分析,Cu是负极,Ag O/Ag是正极,电流方向从正极流向负极,即从Ag O流向
2 2
Cu,故C项错误;
D.从化学方程式可以看出2Cu+Ag O=Cu O+2Ag ,Cu是还原剂,失电子,做负极,Ag O 得电子,则
2 2 2
Ag O/Ag做正极,故D项正确;
2
15.【答案】
(1)OHCCHO (2分)
(2)碳碳双键(3分)
(3)CHCHBr+NaOH CH=CH +NaBr+H O (3分)
3 2 2 2 2
(4)氧化反应(3分)
(5) (3分)
【分析】根据反应流程分析可知,F被氧化生成乙二酸,则F是乙二醛,其结构简式为OHCCHO,E被氧化生成
F,则E是乙二醇,其结构简式为HOCH CHOH,B是一溴代物,B发生消去反应生成C,C和溴水发生
2 2
加成反应生成D,D发生取代反应生成E,则这几种分子中的碳原子个数相同,所以B是1-溴乙烷,其结
构简式为CHCHBr,C是CH=CH ,D是CHBrCHBr,据此可分析解答问题。
3 2 2 2 2 2
【详解】
(1)通过上述分析可知,C是乙烯,其结构简式为CH=CH ,,F是乙二醛,其结构简式为OHCCHO,故答
2 2
案为:CH=CH ;OHCCHO;
2 2
(2)C是乙烯,所以官能团为碳碳双键
(3)B发生消去反应生成C,反应方程式为:CHCHBr+NaOH CH=CH +NaBr+H O
3 2 2 2 2
(4)E是乙二醇,F是乙二醛,E在Cu作催化剂加热的条件下被氧化生成F,反应方程式为:
HOCH CHOH+O OHCCHO+2H O,故为氧化反应
2 2 2 2
(5)乙二醇和乙二酸在浓硫酸加热的条件下可发生酯化反应生成环酯,该环酯的结构简式为
,故答案为: 。
16.【答案】
(1)2Fe(OH) ===Fe O+3H O(3分)
3 2 3 2
(2)4Fe+NO-+10H+=4NH++4Fe3++3H O(3分)
3 4 2
(3)①abd(3分)
②4Fe(NO)2++O +4H+=4NO+4Fe3++2H O(3分)
2 2
【解析】
(1)红褐色固体是氢氧化铁,铁红是氧化铁,根据元素守恒,写出化学方程式
2Fe(OH) ===Fe O+3H O
3 2 3 2
(2)没有气体放出,分离中有含有铵盐的溶液,所以硝酸根离子生成了铵根离子,铁被氧化为三价铁,
写出离子方程式4Fe+NO-+10H+=4NH++4Fe3++3H O
3 4 2
(3)①a中-1价硫生成硫酸根离子,b氧气变为-2价氧,d同a,c三价铁水解,没有化合价变化,故不是
氧化还原反应
②根据图形分析,反应物为4Fe(NO)2+和O,生成物为NO和Fe3+
217.【答案】
(1) 分液漏斗 (2分)
(2) MnO+4HCl(浓) MnCl +Cl↑+2H O (3分) a (2分) 淡黄色沉淀生成(2分) S2-
2 2 2 2
+Cl═S↓+2Cl- (3分)
2
(3) 1:5 (3分)
【分析】
(1)a为分液漏斗,A中浓盐酸与二氧化锰反应生成氯气;
(2)B中饱和食盐水可除去HCl,C中氯气与NaS溶液反应生成S,可比较非金属性,D中NaOH溶液吸收
2
尾气;
(3)反应后装置D中c(ClO-):c(ClO -)=5:1,可知失去电子为5×(1-0)+1×(5-0)=10,由电子守恒
3
可知,2molCl失去电子与10molCl得到电子相等。
【详解】
(1)仪器a的名称为分液漏斗,装置A中发生反应的化学方程式为MnO +4HCl(浓) MnCl +Cl↑+2H O,
2 2 2 2
故答案为:分液漏斗;MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2
(2)C中氯气与NaS溶液反应生成S,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子
2
方程式为S2-+Cl═S↓+2Cl-,故答案为:a;淡黄色沉淀生成;S2-+Cl═S↓+2Cl-;
2 2
(3)反应后装置D中c(ClO-):c(ClO -)=5:1,可知失去电子为5×(1-0)+1×(5-0)=10,由电子守恒
3
可知,2molCl失去电子与10molCl得到电子相等,则反应中被氧化的Cl原子与被还原的Cl原子个数比为
2mol:10mol=1:5,故答案为:1:5。
18.【答案】
(1) Fe3+ (2分)
(2)100mL容量瓶 (2分) 过滤 (2分) Zn+2Fe3+=Zn2++2Fe2+ (3分)
(3)10.1% (4分)
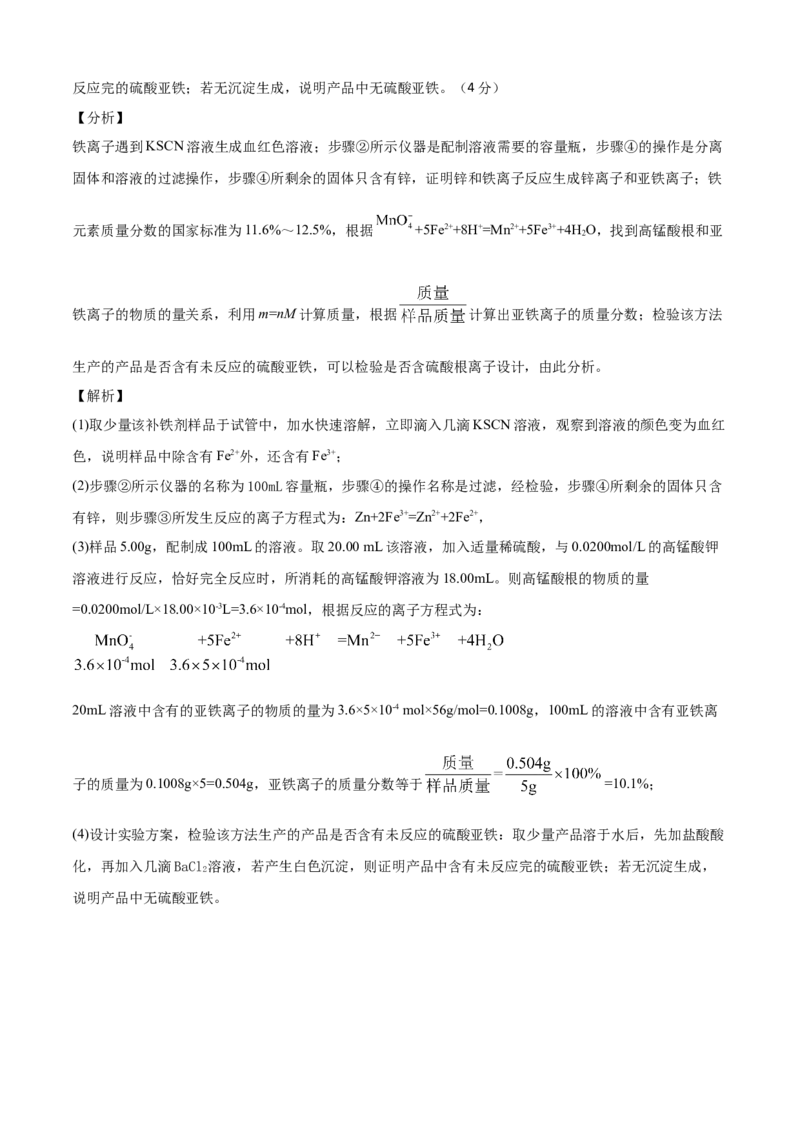
(4)取少量产品溶于水后,先加盐酸酸化,再加入几滴BaCl 溶液,若产生白色沉淀,则证明产品中含有未
2反应完的硫酸亚铁;若无沉淀生成,说明产品中无硫酸亚铁。(4分)
【分析】
铁离子遇到KSCN溶液生成血红色溶液;步骤②所示仪器是配制溶液需要的容量瓶,步骤④的操作是分离
固体和溶液的过滤操作,步骤④所剩余的固体只含有锌,证明锌和铁离子反应生成锌离子和亚铁离子;铁
元素质量分数的国家标准为11.6%~12.5%,根据 +5Fe2++8H+=Mn2++5Fe3++4H O,找到高锰酸根和亚
2
铁离子的物质的量关系,利用m=nM计算质量,根据 计算出亚铁离子的质量分数;检验该方法
生产的产品是否含有未反应的硫酸亚铁,可以检验是否含硫酸根离子设计,由此分析。
【解析】
(1)取少量该补铁剂样品于试管中,加水快速溶解,立即滴入几滴KSCN溶液,观察到溶液的颜色变为血红
色,说明样品中除含有Fe2+外,还含有Fe3+;
(2)步骤②所示仪器的名称为100mL容量瓶,步骤④的操作名称是过滤,经检验,步骤④所剩余的固体只含
有锌,则步骤③所发生反应的离子方程式为:Zn+2Fe3+=Zn2++2Fe2+,
(3)样品5.00g,配制成100mL的溶液。取20.00 mL该溶液,加入适量稀硫酸,与0.0200mol/L的高锰酸钾
溶液进行反应,恰好完全反应时,所消耗的高锰酸钾溶液为18.00mL。则高锰酸根的物质的量
=0.0200mol/L×18.00×10-3L=3.6×10-4mol,根据反应的离子方程式为:
20mL溶液中含有的亚铁离子的物质的量为3.6×5×10-4 mol×56g/mol=0.1008g,100mL的溶液中含有亚铁离
子的质量为0.1008g×5=0.504g,亚铁离子的质量分数等于 =10.1%;
(4)设计实验方案,检验该方法生产的产品是否含有未反应的硫酸亚铁:取少量产品溶于水后,先加盐酸酸
化,再加入几滴BaCl 溶液,若产生白色沉淀,则证明产品中含有未反应完的硫酸亚铁;若无沉淀生成,
2
说明产品中无硫酸亚铁。