文档内容
A. 水边夜色本身就很美
下学期期末测试卷 01
B 光线是一种胶体
高一化学
C. 颗粒直径约为1 nm~100 nm的小水滴分散在空气中
D. 烟雾是一种胶体,能产生丁达尔现象
(考试时间:75分钟 试卷满分:100分)
5.下列有关实验装置正确且能达到实验目的的是( )
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:新人教版(2019)必修1、2全册。
5.考试结束后,将本试卷和答题卡一并交回。
6.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Cl 35.5 K 39 Mn55 Fe 56
A.用图1所示装置制取少量乙酸乙酯
第Ⅰ卷 B.用图2所示装置验证SO 的漂白性
2
C.用图3所示装置配制100 mL 0.100 mol·L-1的硫酸溶液
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要 D.用图4所示装置分离水和溴苯
6.定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图
求。
1.下列常见物质的俗名与化学式对应正确的是 所示,则下列对该反应的推断合理的是( )
A.明矾——KAl(SO )·12H O B.铜绿——CuSO ·5H O
4 2 2 4 2
C.苏打——NaHCO D.铁红——Fe O
3 3 4
2. 反应Cl+Na SO +H O=Na SO +2HCl可用于污水脱氯。下列相关微粒说法正确的是( )
2 2 3 2 2 4
A. 中子数为20的氯原子: Cl B. HO的电子式:
2
A.该反应的化学方程式为3B+4D 6A+2C
C. Na+的结构示意图: D. Na 2 SO 3 中只有离子键 B.0~1 s内,v(A)=v(D)
C.0~6 s内,用B表示的平均反应速率为0.05 mol·(L·s)-1
D.0~6 s内,用各物质表示的反应速率相等
3.下列有关物质的性质与用途具有对应关系的是
7.下列各组离子在水溶液中能大量共存的是
A.明矾溶于水能形成胶体,可用于自来水的杀菌消毒
A.酸性溶液中:K+、NO、Cl—、CO2—
3
B.金属钠具有强还原性,可用于与TiCl 溶液反应制取金属Ti
4
B.澄清透明的溶液中:Na+、K+、MnO -、AlO—
4 2
C.Al O 具有很高的熔点,可用于制造熔融烧碱的坩埚
2 3
C.在含大量Fe3+的溶液中:NH +、Na+、Cl—、SCN—
4
D.FeCl 溶液能与Cu反应,可用于蚀刻印刷电路板
3
D.能与金属铝反应放出H 的溶液:HCO —、Na+、Mg2+、SO 2—
2 3 4
4. “烟笼寒水月笼沙”所描绘的景色,其本质原因是( )8.取一支大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,将试管倒置于盛有饱和食 其次外层电子数的3倍,B单质的焰色试验结果为黄色。下列说法错误的是
盐水的水槽中,放在光亮处,进行如图所示的实验。光照一段时间后,试管内液面上升,气体颜色逐渐变
A. 原子半径的大小顺序:r(B)>r(C)>r(D)>r(A) B. 元素A与B可形成两种化合物
浅,试管壁出现油状液滴,试管中出现了少量白雾。下列关于该实验的说法不正确的是( )
C. 最高价氧化物对应的水化物的酸性:C<D D. 气态氢化物的热稳定性:A<C
A.氯气在饱和食盐水中的溶解度小于在水中的溶解度
CH和Cl 14.普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一特点,科学家们发明了电动势法测
4 2
B.试管壁出现了油状液滴,是因为该反应生成了一氯甲烷
水泥的初凝时间。此法的原理如图所示,反应的化学方程式为 2Cu+Ag O===Cu O+2Ag,下列有关说法正
2 2
C.试管中的白雾是反应生成的氯化氢气体遇水形成的酸雾
确的是( )
饱和
D.由实验过程中产生的现象可推知,甲烷与氯气在光照条件下能
食盐水
发生取代反应
9.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 5.6g铁粉与足量稀硫酸反应转移电子数为0.3 N
A
B.常温常压下,22.4LCO 含有的分子数为N A.2 mol Cu与1 mol Ag O的总能量低于1 mol Cu O与2 mol Ag具有的总能量
2 A 2 2
C.1mol钠离子所含电子数为10N B.电池工作时,OH-向正极移动
A
D.常温下,1 mol·L-1的NaCO 溶液中含有Na+个数为2N C.原理示意图中,电流从Cu流向Ag O
2 3 A 2
D.Ag O/Ag电极为正极
2
10.某溶液中含有较大量的Cl-、 、 OH-三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依
次检验出来,下列实验操作顺序正确的是
第II卷(非选择题 58分)
15(14分).有以下一系列反应,最终产物为草酸(乙二酸)。
①滴加足量的Mg(NO) 溶液;②过滤;③滴加适量的AgNO 溶液;④滴加足量的Ba(NO ) 溶液
3 2 3 3 2
A.④②①②③ B.①②④②③ C.①②③②④ D.④②③②①
11.如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能
实现图示转化关系的是
选项 W X Y Z
已知B为某一溴代物。
A Cu CuO CuCl Cu(OH)
2 2
B Na NaO NaOH NaCl
2 2 (1)推测用字母代表的化合物的结构简式:F____________
C Fe FeCl Fe(OH) FeCl
3 3 2
D Al AlCl 3 NaAlO 2 Al 2 (SO 4 ) 3 (2)C物质中的官能团名称 ____________
12.某废催化剂含SiO、ZnS、CuS及少量的Fe O。某实验小组以该废催化剂为原料,回收锌和铜,设计
2 3 4
(3)写出化学方程式:B→C_________________________
实验流程如图:
(4)E→F的反应类型_______________
(5)E和草酸在一定条件下生成的环状化合物的结构简式为____________________
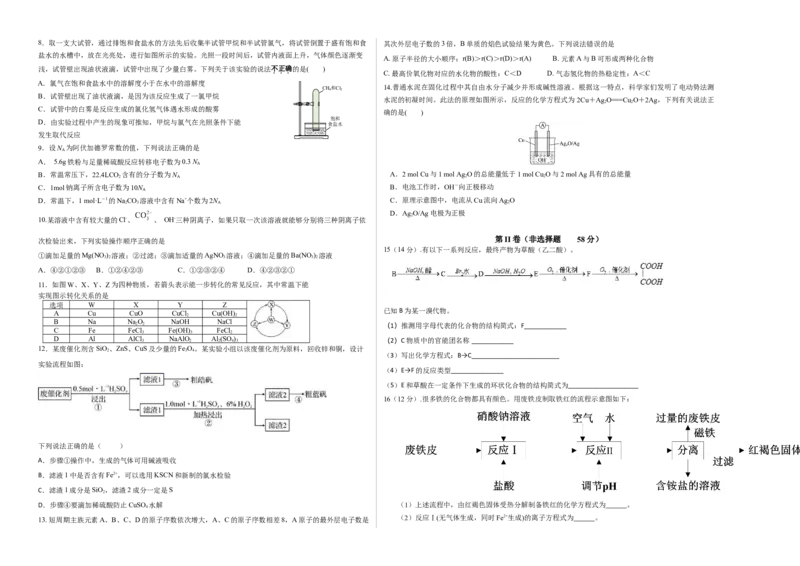
16(12分).很多铁的化合物都具有颜色。用废铁皮制取铁红的流程示意图如下:
下列说法正确的是( )
A.步骤①操作中,生成的气体可用碱液吸收
B.滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水检验
C.滤渣1成分是SiO,滤渣2成分一定是S
2
D.步骤④要滴加稀硫酸防止CuSO 水解 (1)上述流程中,由红褐色固体受热分解制备铁红的化学方程式为 。
4
13. 短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数相差8,A原子的最外层电子数是
(2)反应Ⅰ(无气体生成,同时Fe2+生成)的离子方程式为 。(3)黄铁矿(主要成分为二硫化亚铁:FeS )因黄色和明亮的金属光泽,常被误认为是黄金,故又称
2
溶液 溶液 溶液
为“愚人金”。
①黄铁矿在空气中氧化的四步反应模型如下左图所示。a,b,c,d四个反应中属于非氧化还原反
若反应后装置D中 : :1,则反应中被氧化的Cl原子与被还原的Cl原子个数比
应的是 (填字母)。
②一种酸性条件下催化氧化黄铁矿的物质转化关系如下右图所示,写出该过程
为______。
中Fe(NO)2+与O 反应的离子方程式: 。
2 18.(17分)葡萄糖酸亚铁(C H O Fe)是一种常用的补铁剂,其铁元素和三价铁质量分数的国家标准如下
12 22 14
表所示。
葡萄糖酸亚铁补铁剂国家标准(部分)
项 目(质量分数) 指 标
铁元素(%) 11.6~12.5
三价铁(%) ≤ 2.0
为探究某粉末状葡萄糖酸亚铁补铁剂的铁元素和三价铁质量分数是否符合国家标准,同学们在老
师的指导下进行以下实验:
(1)取少量该补铁剂样品于试管中加水快速溶解,立即滴入几滴KSCN溶液,观察到溶液的颜色变为
血红色,说明样品中除含有Fe2+外还含有 离子。
(2)称取该样品5.00 g,按下图所示实验步骤处理样品,得到铁元素质量分数待测液:
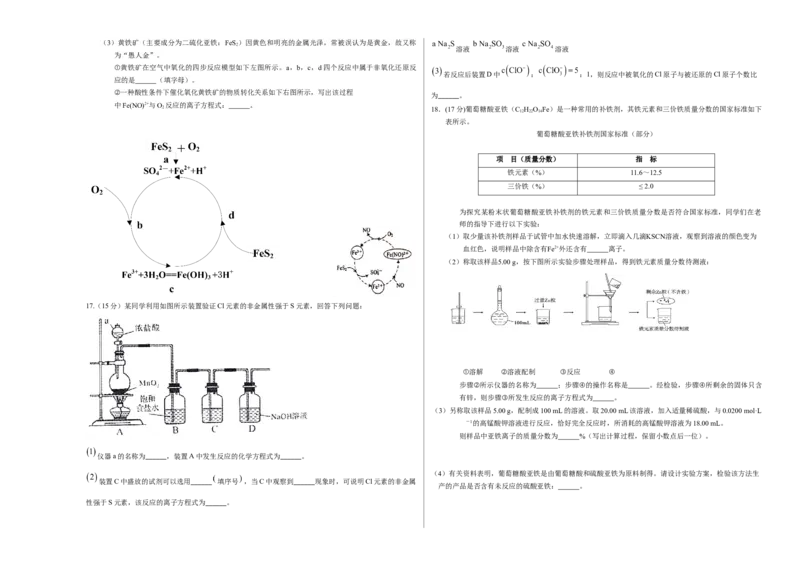
17.(15分)某同学利用如图所示装置验证Cl元素的非金属性强于S元素,回答下列问题:
①溶解 ②溶液配制 ③反应 ④
步骤②所示仪器的名称为 ;步骤④的操作名称是 。经检验,步骤④所剩余的固体只含
有锌,则步骤③所发生反应的离子方程式为 。
(3)另称取该样品5.00 g,配制成100 mL的溶液。取20.00 mL该溶液,加入适量稀硫酸,与0.0200 mol·L
-1的高锰酸钾溶液进行反应,恰好完全反应时,所消耗的高锰酸钾溶液为18.00 mL。
则样品中亚铁离子的质量分数为 %(写出计算过程,保留小数点后一位)。
仪器a的名称为______,装置A中发生反应的化学方程式为______。
(4)有关资料表明,葡萄糖酸亚铁是由葡萄糖酸和硫酸亚铁为原料制得。请设计实验方案,检验该方法生
装置C中盛放的试剂可以选用______ 填序号 ,当C中观察到______现象时,可说明Cl元素的非金属
产的产品是否含有未反应的硫酸亚铁: 。
性强于S元素,该反应的离子方程式为______。