文档内容
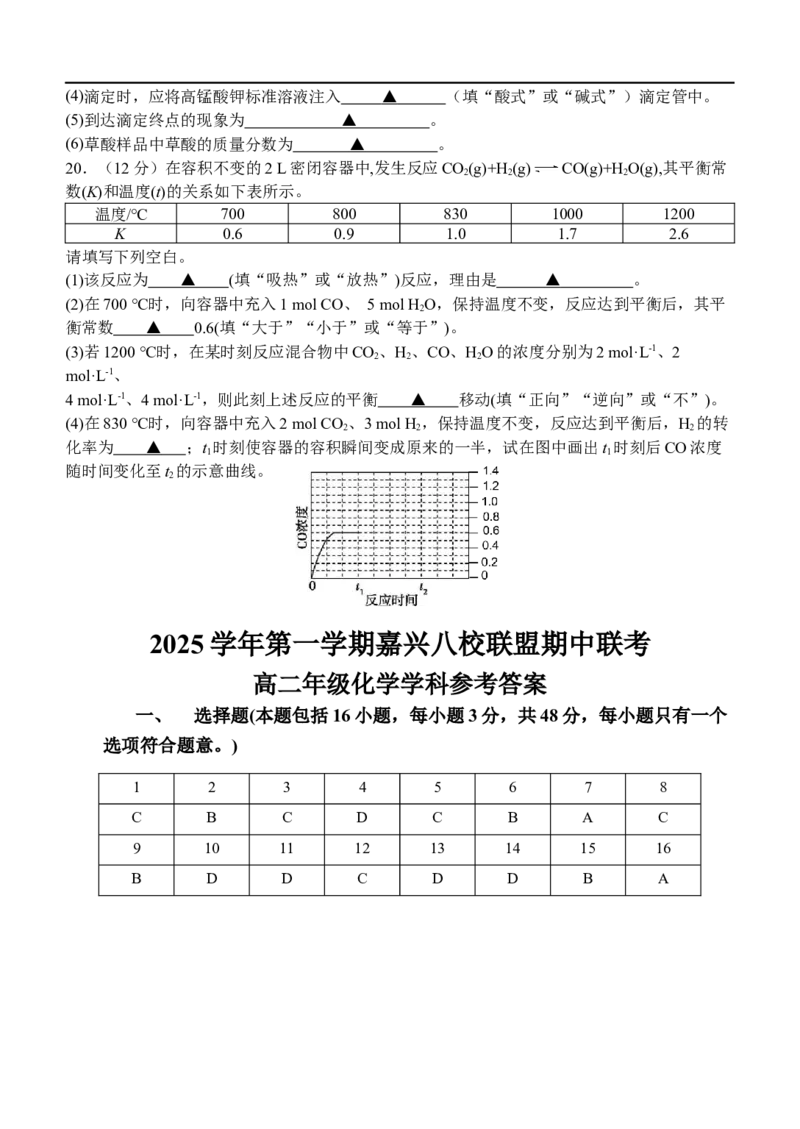
b>c D.取相同pH的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗盐酸的体积较 小 15.一定温度下,水溶液中H+和OH-的浓度变化曲线如图所示,下列说法正确的是( ) A.升高温度,可能引起由c向b的变化 B.该温度下,水的离子积常数为1.0×10-14 C.该温度下,加入少量FeCl 固体可能引起由a向b的变化 3 D.该温度下,加少量NaOH固体可能引起由c向d的变化 16.根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计和结论都正确的是( ) 选项 方案设计 现象 结论等体积pH=2的HX和HY两种酸 HX放出的氢气 A 分别与足量的铁反应,用排水法 证明酸性是HX比HY弱 多且反应速率快 收集气体 将0.2mol·L-1的KI溶液和 0.05mol·L-1的FeCl 溶液等体积混 验证Fe3+与I-的反应有一定 B 3 产生黄色沉淀 合,充分反应后,取少许混合液 限度 滴加AgNO 溶液 3 在容积不变的密闭容器中发生反 说明化学反应速率不受压强 C 应:N(g)+3H(g) 2NH (g) 反应速率不变 2 2 3 影响 向其中通入氩气 [Cu(H O) ]2+(蓝色)+4Cl- 2 4 加热盛有2mL0.5mol/LCuCl 溶液 溶液由蓝色变为 [CuCl ]2-(黄色) D 2 4 的试管 黄色 +4H O 2 说明上述反应的ΔH<0 非选择题部分 二、填空题(本题包括4小题,共52分) 17.(16分)试回答下列问题: (1)25℃时,有0.01mol·L-1的醋酸溶液, ①写出醋酸的电离平衡常数表达式:K= ▲ ,一般情况下,当温度升高时,K ▲ (填 a a “增大”、“减小”或“不变”)。 ②已知25℃时,HClO的K=4.0×10-8,CHCOOH的K=1.75×10-5,相同浓度的CHCOOH溶液 a 3 a 3 和HClO溶液,酸性较强的是 ▲ ,则CHCOOH与NaClO溶液 ▲ (填“能”或“不能”) 3 反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式 ▲ 。 ③常温下,0.1mol/L CH COOH溶液加水稀释过程中,下列表达式中数据变大的是__▲___。 3 A.c(H+) B. C.c(H+)·c(OH-) D. (2)已知室温时,0.1 mol∙L-1某一元碱BOH在水中有0.1%发生电离,回答下列问题: 此BOH溶液的pH= ▲ ;由水电离出来的c(H+)= ▲ mol∙L-1。 18.(12分)回答下列问题: (1)肼(NH)是一种可燃性液体,可用作火箭燃料。在常温常压下,已知16 g肼在氧气中完全燃 2 4 烧放出312 kJ热量,写出表示肼燃烧热的热化学方程式 ▲ 。 (2)如图所示的简易量热计可用于测定中和反应的反应热,内筒盛有一定量的盐酸和氢氧化钠溶 液。下列有关实验的描述正确的是 ▲ 。A. 仪器M可以为铁制搅拌器 B. 实验过程中需记录体系的最高温度 C. 实验过程中,将量筒中的NaOH溶液缓慢倒入盛有盐酸的量热计内筒中 D. 实验中如果用同体积同浓度的醋酸代替盐酸,测得的反应热ΔH偏大 (3)氢气是最清洁的能源。甲烷-水蒸气重整制氢主要涉及的反应为 Ⅰ.CH(g)+HO(g) 3H(g)+CO(g) ΔH= +206.3 kJ·mol-1 4 2 2 1 Ⅱ.CH(g)+2HO(g) 4H(g)+CO (g) ΔH= +165.3 kJ·mol-1 4 2 2 2 2 ①反应Ⅰ自发进行的条件 ▲ (填“低温”“高温”或“任意温度”)。 ②根据盖斯定律,CO(g)+HO(g) H(g)+CO (g)的ΔH= ▲ kJ·mol-1 2 2 2 ③已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,部分键能数据如下表 所示,请结合反应Ⅰ,求出H-H共价键的键能是 ▲ kJ·mol-1 共价键 C-H CO(C≡O) O-H 键能/kJ·mol-1 414 1076 464 (4)NO是大气污染物,理论上可采用加热使NO分解而除去:2NO(g) N(g)+O(g)。已知该反 2 2 应正反应活化能为728 kJ·mol-1,逆反应活化能为910 kJ·mol-1;正反应熵变为 - 24.8J·K-1·mol-1 。实际反应时发现加热至600℃时NO仍没有明显分解,请结合上述数据解释原因 ▲ 。 19.(12分)滴定分析是一种操作简便、准确度高的定量分析方法,它可广泛应用于中和滴 定、氧化还原反应等滴定中。 I.用NaOH标准溶液滴定未知浓度的盐酸,完成以下填空: (1)滴定时边滴边摇动锥形瓶,眼睛应注意观察 ▲ 。 (2)如图为盛放盐酸的滴定管中液面位置,其读数为 ▲ mL。 (3)以下操作会导致测得的待测液浓度偏大的是 ▲ 。 A.滴定管未用标准溶液润洗就直接注入标准溶液 B.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥 C.装标准溶液的滴定管在滴定前有气泡,滴定后气泡消失 D.滴定结束时俯视读数 II.某同学通过高锰酸钾溶液来测定草酸(H C O)样品中草酸的质量分数(样品中杂质不与高锰酸 2 2 4 钾反应),其反应的离子方程式:2MnO - + 5H C O + 6H+ = 2Mn2+ + 10CO ↑+ 8H O。某同学称 4 2 2 4 2 2 取2.000g草酸样品,配制成100mL溶液,移取40.00mL溶液于锥形瓶中,用0.1000mol/L的 KMnO 标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL。 4(4)滴定时,应将高锰酸钾标准溶液注入 ▲ (填“酸式”或“碱式”)滴定管中。 (5)到达滴定终点的现象为 ▲ 。 (6)草酸样品中草酸的质量分数为 ▲ 。 20.(12分)在容积不变的2 L密闭容器中,发生反应CO(g)+H(g) CO(g)+HO(g),其平衡常 2 2 2 数(K)和温度(t)的关系如下表所示。 温度/℃ 700 800 830 1000 1200 K 0.6 0.9 1.0 1.7 2.6 请填写下列空白。 (1)该反应为 ▲ (填“吸热”或“放热”)反应,理由是 ▲ 。 (2)在700 ℃时,向容器中充入1 mol CO、 5 mol H O,保持温度不变,反应达到平衡后,其平 2 衡常数 ▲ 0.6(填“大于”“小于”或“等于”)。 (3)若1200 ℃时,在某时刻反应混合物中CO、H、CO、HO的浓度分别为2 mol·L-1、2 2 2 2 mol·L-1、 4 mol·L-1、4 mol·L-1,则此刻上述反应的平衡 ▲ 移动(填“正向”“逆向”或“不”)。 (4)在830 ℃时,向容器中充入2 mol CO 、3 mol H ,保持温度不变,反应达到平衡后,H 的转 2 2 2 化率为 ▲ ;t 时刻使容器的容积瞬间变成原来的一半,试在图中画出t 时刻后CO浓度 1 1 随时间变化至t 的示意曲线。 2 2025 学年第一学期嘉兴八校联盟期中联考 高二年级化学学科参考答案 一、 选择题(本题包括16小题,每小题3分,共48分,每小题只有一个 选项符合题意。) 1 2 3 4 5 6 7 8 C B C D C B A C 9 10 11 12 13 14 15 16 B D D C D D B A二、填空题(本题有4小题,每空2分,共52分) 17.(16分) (1)① (2分) 增大(2分) ②CHCOOH (2分) 能(2分) ClO- + CHCOOH = CH COO- + HClO(2分) 3 3 3 ③B(2分) (2)10(2分) 1×10-10 (2分) 18.(12分) (1)NH(g)+O(g)=N(g)+2HO(l) ΔH= -624 kJ•mol-1 (2分) 2 4 2 2 2 (各物质的聚集状态均标注正确得1分,△H的数值正确得1分) (2)BD (2分) (选对一个得1分,多选、错选不得分) (3)①高温(2分) ②-41(2分) ③433.9(2分) (4)反应虽然可以自发进行,但是正反应活化能较大,在较低温度下反应速率缓慢,故现象 不明 显。(2分)( “正反应活化能较大”得1分,“反应速率缓慢”得1分) 19.(12分) (1)锥形瓶中溶液颜色变化(2分) (2)22.80 (2分) (读数必须精准到小数点后两位) (3) AC (2分)(选对一个得1分,多选、错选不得分) (4)酸式(2分) (5)滴入最后半滴高锰酸钾溶液,溶液由无色变成浅红色且30s内不褪色(2分) (颜色变化描述正确得1分,“30s内不褪色”得1分) (6) 56.25%(2分) 20.(12分) (1)吸热(2分) 升高温度,K增大,平衡正移,说明正反应方向吸热。(2分) (温度对K的影响1分,移动方向与吸热1分) (2)等于(2分) (3)逆向(2分) (4) 40%(2分)(2分)(起点1.2正确1分,趋势正确1分)