文档内容
高二年级化学试卷
时间:75 分钟 分数:100 分
试卷说明:试卷共二部分:第一部分:选择题型(1-15 题 45
分)
第二部分:非选择题(16-19 题 55
分) 第 I 卷(选择题 共 45 分)
可能用到的相对原子质量:H-1 Li-7 C-120-16 C1-35.5 Nb-93 Ga70 As75
一、单项选择,每题 3 分
1. 下列化学用语表示正确的是
A. 固 体HF 中的链状结构片段:
B. 的 VSEPR 模型:
C.Cl-C1 中 p-pσ 键的形成示意图:
D. 顺-2-丁烯的结构简式为
2. 下列表述中,与盐类水解有关的是
①明矾和FeCl₃ 可作净水剂
②为保存FeCl₂ 溶液,要在溶液中加少量铁粉
③A1Cl₃ 溶液蒸干,灼烧,最后得到的主要固体产物是Al₂O₃
④NH₄C1 与 ZnCl₂ 溶液可作焊接中的除锈剂
⑤实验室盛放NaOH 溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥用NaHCO₃ 与 Al₂ (SO4)₃ 两种溶液可作泡沫灭火剂
⑦草木灰与铵态氮肥不能混合施用
A.①③④⑥⑦ B.①②③⑤⑥⑦ C.①③⑤⑥⑦ D. 全有关
高二年级化学试卷 第1页共10页3. 某 烃 一的一氯代物(不考虑立体异构)有
A.3 种 B.4 种 C.5 种 D.6 种
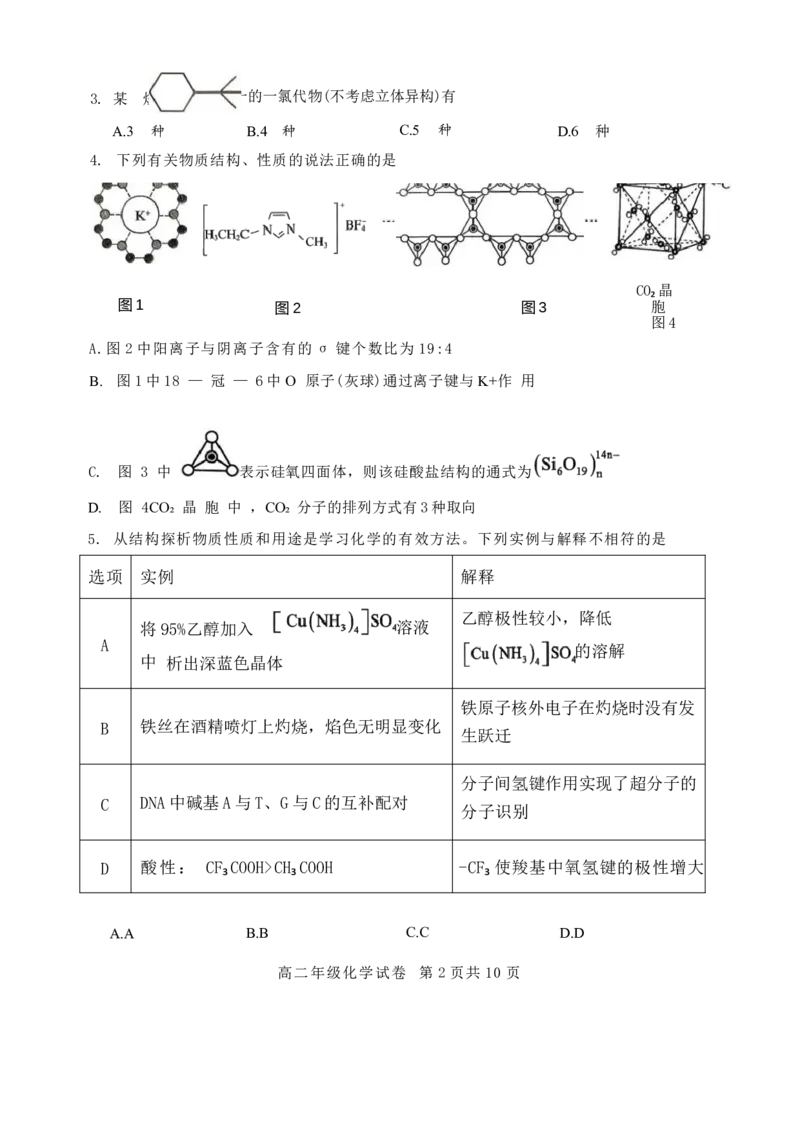
4. 下列有关物质结构、性质的说法正确的是
CO₂ 晶
图1 图2 图3 胞
图4
A.图 2 中阳离子与阴离子含有的 σ 键个数比为 19:4
B. 图1中18 — 冠 — 6中O 原子(灰球)通过离子键与K+作 用
C. 图 3 中 表示硅氧四面体,则该硅酸盐结构的通式为
D. 图 4CO₂ 晶 胞 中 ,CO₂ 分子的排列方式有3种取向
5. 从结构探析物质性质和用途是学习化学的有效方法。下列实例与解释不相符的是
选项 实例 解释
乙醇极性较小,降低
将95%乙醇加入 溶液
A
的溶解
中 析出深蓝色晶体
铁原子核外电子在灼烧时没有发
B 铁丝在酒精喷灯上灼烧,焰色无明显变化
生跃迁
分子间氢键作用实现了超分子的
C DNA中碱基A与T、G与C的互补配对
分子识别
D 酸性: CF₃COOH>CH₃COOH -CF₃ 使羧基中氧氢键的极性增大
A.A B.B C.C D.D
高二年级化学试卷 第 2 页共 10 页6. 碳原子的杂化轨道中s 成分的含量越多,则该碳原子形成的C—H 键的键长越短。
对
于有机化合物 下列说法错误的是
A.1mol 该物质最多可消耗3molH₂
B. 该有机物分子中,位于同一平面上的原子最多有9个
C. 该有机物中三种C—H 键的键能:②>①>③
D. 该有机物不含有手性碳
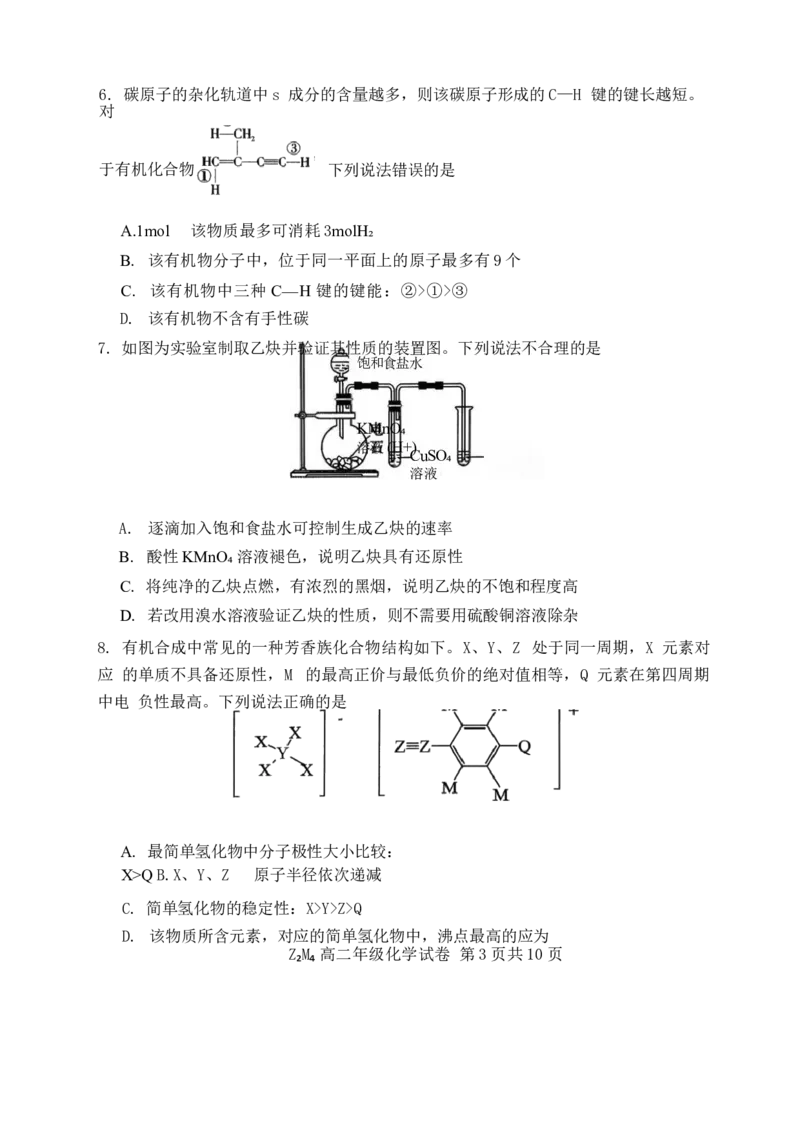
7. 如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
饱和食盐水
KMnO₄
溶液(H+)
CuSO₄
溶液
A. 逐滴加入饱和食盐水可控制生成乙炔的速率
B. 酸性KMnO₄ 溶液褪色,说明乙炔具有还原性
C. 将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔的不饱和程度高
D. 若改用溴水溶液验证乙炔的性质,则不需要用硫酸铜溶液除杂
8. 有机合成中常见的一种芳香族化合物结构如下。X、Y、Z 处于同一周期,X 元素对
应 的单质不具备还原性,M 的最高正价与最低负价的绝对值相等,Q 元素在第四周期
中电 负性最高。下列说法正确的是
A. 最简单氢化物中分子极性大小比较:
X>Q B.X、Y、Z 原子半径依次递减
C. 简单氢化物的稳定性:X>Y>Z>Q
D. 该物质所含元素,对应的简单氢化物中,沸点最高的应为
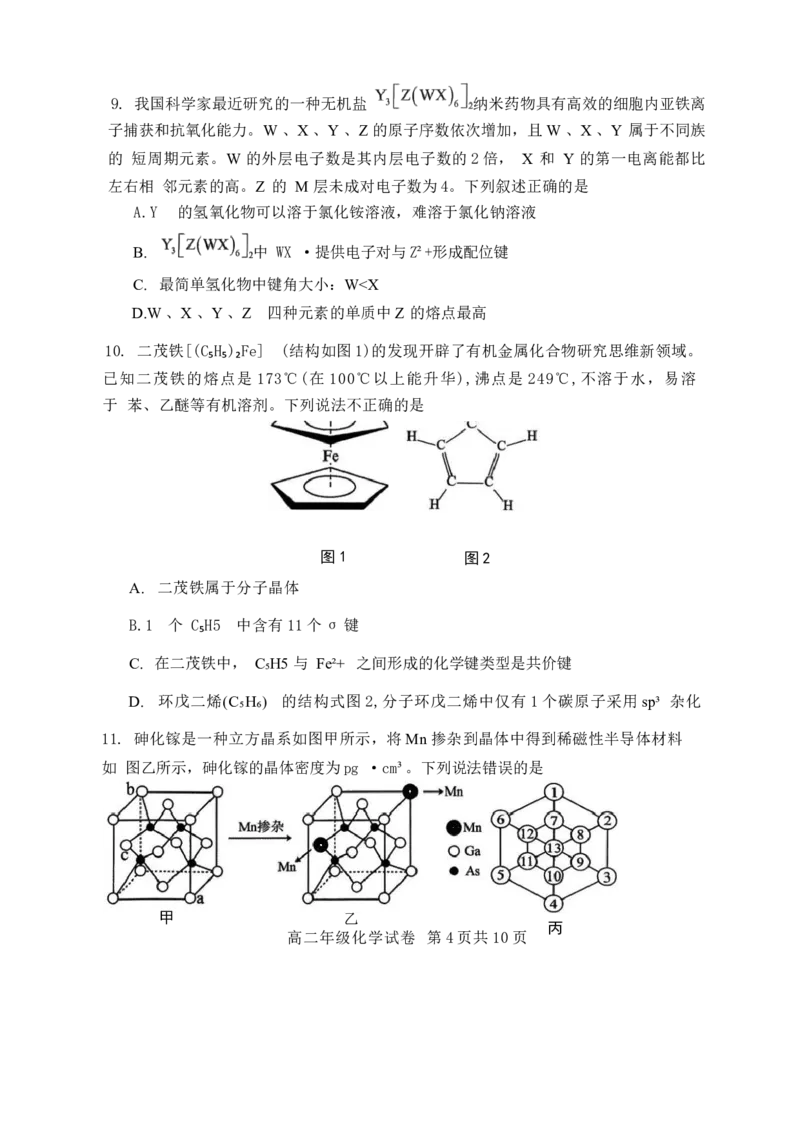
Z₂M₄ 高二年级化学试卷 第3页共10页9. 我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁离
子捕获和抗氧化能力。W 、X 、Y 、Z 的原子序数依次增加,且W 、X 、Y 属于不同族
的 短周期元素。W 的外层电子数是其内层电子数的2倍, X 和 Y 的第一电离能都比
左右相 邻元素的高。Z 的 M 层未成对电子数为4。下列叙述正确的是
A.Y 的氢氧化物可以溶于氯化铵溶液,难溶于氯化钠溶液
B. 中 WX ·提供电子对与Z²+形成配位键
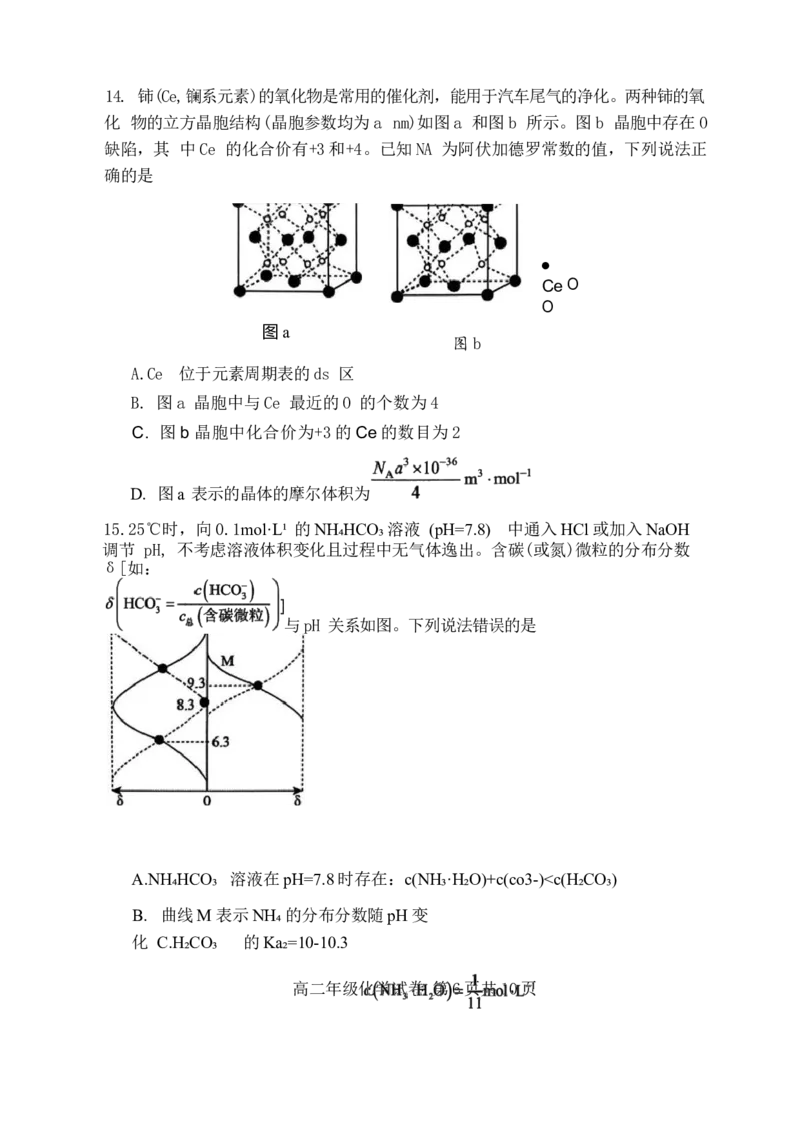
C. 最简单氢化物中键角大小:W”)
(3)Y的结构简式为
(4)X 存在顺反异构,写出它的反式异构体的结构简式: _;
(5)化合物W 与异戊二烯属于官能团类别异构(碳骨架不变),则W 用系统命名法其名
称
(6)某高分子化合物的结构为 ,该高分子化合物的单体为 o
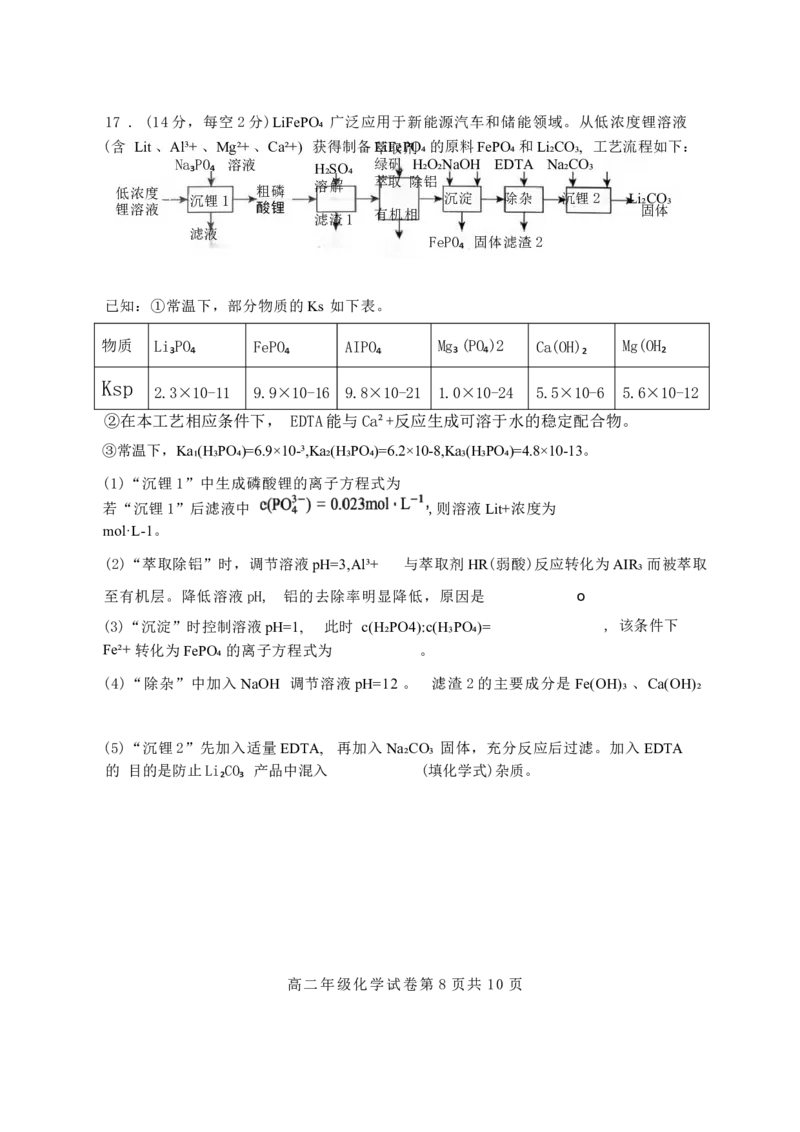
高二年级化学试卷 第 7 页共 10 页17 . (14分,每空2分)LiFePO₄ 广泛应用于新能源汽车和储能领域。从低浓度锂溶液
(含 Lit 、Al³+ 、Mg²+ 、Ca²+) 获得制备萃LiF取eP剂O₄ 的原料FePO₄ 和Li₂CO₃, 工艺流程如下:
Na₃PO₄ 溶液
H₂SO₄
绿矾 H₂O₂NaOH EDTA Na₂CO₃
萃取 除铝
溶解
低浓度_ 粗磷
沉锂1 沉淀 除杂 沉锂2 Li₂CO₃
锂溶液 酸锂 有机相 固体
滤渣1
滤液
FePO₄ 固体滤渣2
已知:①常温下,部分物质的Ks 如下表。
物质 Li₃PO₄ FePO₄ AIPO₄ Mg₃ (PO₄)2 Ca(OH)₂ Mg(OH₂
Ksp
2.3×10-11 9.9×10-16 9.8×10-21 1.0×10-24 5.5×10-6 5.6×10-12
②在本工艺相应条件下, EDTA能与Ca²+反应生成可溶于水的稳定配合物。
③常温下,Ka₁(H₃PO₄)=6.9×10-³,Ka₂(H₃PO₄)=6.2×10-8,Ka₃(H₃PO₄)=4.8×10-13。
(1)“沉锂1”中生成磷酸锂的离子方程式为
若“沉锂1”后滤液中 ,则溶液Lit+浓度为
mol·L-1。
(2)“萃取除铝”时,调节溶液pH=3,Al³+ 与萃取剂HR(弱酸)反应转化为AIR₃ 而被萃取
至有机层。降低溶液pH, 铝的去除率明显降低,原因是 o
(3)“沉淀”时控制溶液pH=1, 此时 c(H₂PO4):c(H₃PO₄)= , 该条件下
Fe²+ 转化为FePO₄ 的离子方程式为 。
(4)“除杂”中加入NaOH 调节溶液pH=12 。 滤渣2的主要成分是Fe(OH)₃ 、Ca(OH)₂
(5)“沉锂2”先加入适量EDTA, 再加入Na₂CO₃ 固体,充分反应后过滤。加入EDTA
的 目的是防止Li₂CO₃ 产品中混入 (填化学式)杂质。
高二年级化学试卷第 8 页共 10 页18. (17 分,第一个空为 1 分,其余每空均为 2 分。)
“结构决定性质”,我们生活的环境正因丰富多彩的物质结构而富有生机活力。
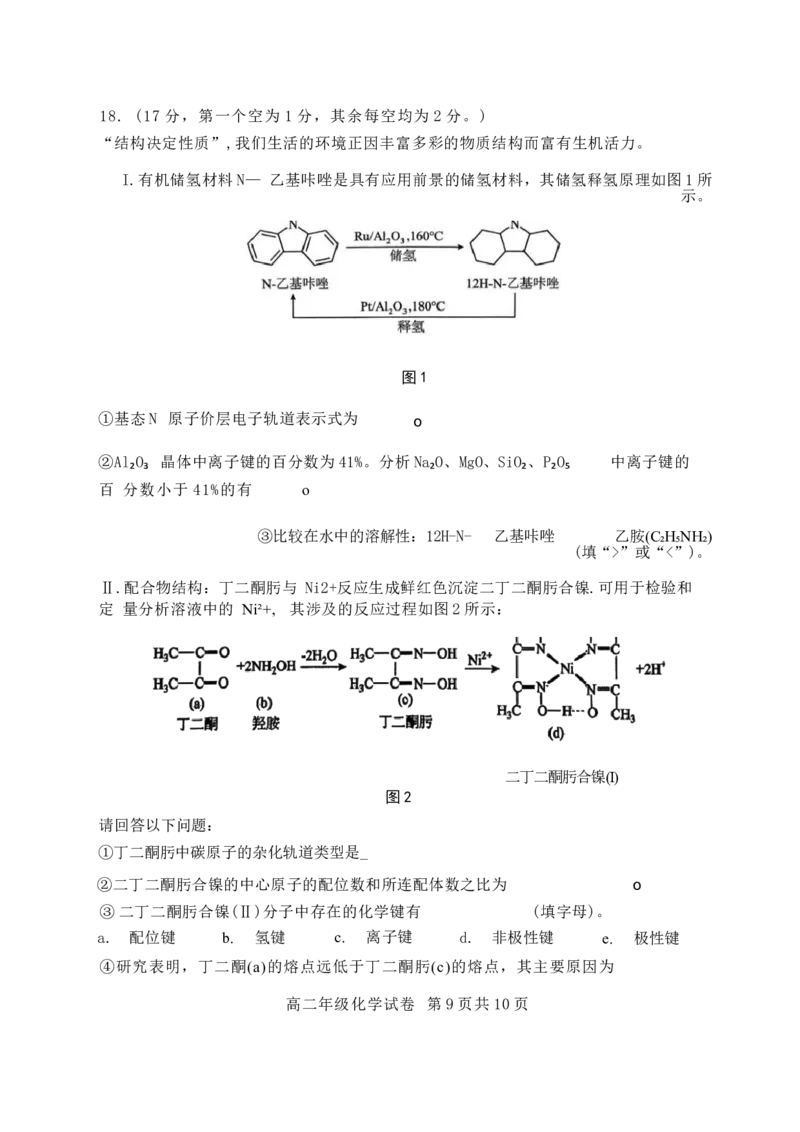
I.有机储氢材料N— 乙基咔唑是具有应用前景的储氢材料,其储氢释氢原理如图1所
示。
图1
①基态N 原子价层电子轨道表示式为
o
②Al₂O₃ 晶体中离子键的百分数为41%。分析Na₂O、MgO、SiO₂、P₂O₅ 中离子键的
百 分数小于 41%的有 o
③比较在水中的溶解性:12H-N- 乙基咔 唑 乙胺(C₂H₅NH₂)
(填“>”或“<”)。
Ⅱ.配合物结构:丁二酮肟与 Ni2+反应生成鲜红色沉淀二丁二酮肟合镍.可用于检验和
定 量分析溶液中的 Ni²+, 其涉及的反应过程如图2所示:
二丁二酮肟合镍(I)
图2
请回答以下问题:
①丁二酮肟中碳原子的杂化轨道类型是_
②二丁二酮肟合镍的中心原子的配位数和所连配体数之比为 o
③二丁二酮肟合镍(Ⅱ)分子中存在的化学键有 (填字母)。
a. 配位键 b. 氢键 c. 离子键 d. 非极性键 e. 极性键
④研究表明,丁二酮(a)的熔点远低于丁二酮肟(c)的熔点,其主要原因为
高二年级化学试卷 第9页共10页Ⅲ .有机物结构:不饱和键在有机反应中起着至关重要的作用。
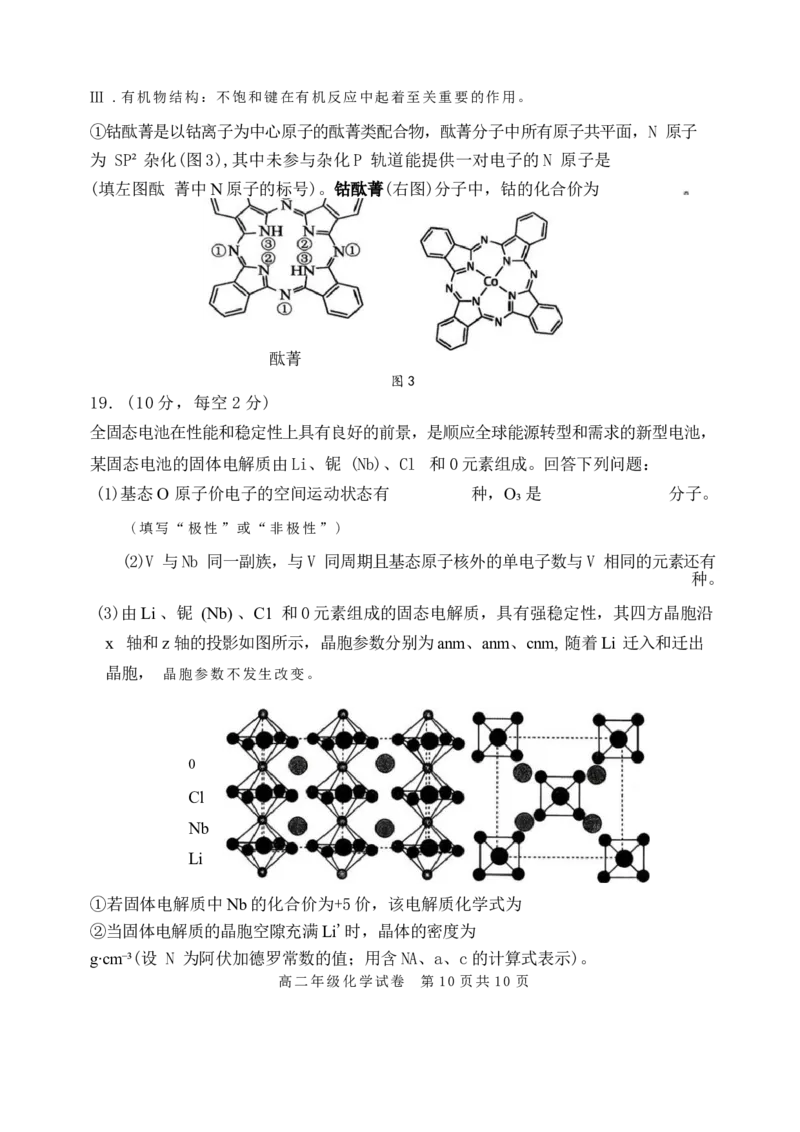
①钴酞菁是以钴离子为中心原子的酞菁类配合物,酞菁分子中所有原子共平面,N 原子
为 SP²杂化(图3),其中未参与杂化P 轨道能提供一对电子的N 原子是
(填左图酞 菁中N原子的标号)。钴酞菁(右图)分子中,钴的化合价为
酞菁
图3
19. (10 分,每空 2 分)
全固态电池在性能和稳定性上具有良好的前景,是顺应全球能源转型和需求的新型电池,
某固态电池的固体电解质由Li、铌 (Nb)、Cl 和0元素组成。回答下列问题:
(1)基态O 原子价电子的空间运动状态有 种,O₃ 是 分子。
(填写“极性”或“非极性”)
(2)V 与Nb 同一副族,与V 同周期且基态原子核外的单电子数与V 相同的元素还有
种。
(3)由Li 、铌 (Nb) 、C1 和0元素组成的固态电解质,具有强稳定性,其四方晶胞沿
x 轴和z 轴的投影如图所示,晶胞参数分别为anm、anm、cnm, 随着Li 迁入和迁出
晶胞, 晶胞参数不发生改变。
0
Cl
Nb
Li
①若固体电解质中Nb的化合价为+5价,该电解质化学式为
②当固体电解质的晶胞空隙充满Li'时,晶体的密度为
g·cm⁻³(设 N 为阿伏加德罗常数的值;用含NA、a、c的计算式表示)。
高二年级化学试卷 第 10 页共 10 页高二年级化学试卷答案
考试时间:75 分钟 考试分数:100 分
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C A B C D A A B
题号 11 12 13 14 15
答案 B B C C D
16. (14分,每空2
分) (1)3
(答案不唯一,写对即可);
(3)
(4)
(5)3-甲基-1-丁炔
(6)
17. (14 分,每空 2 分)
(1)3Li++PO4-=Li₃PO₄↓ 1.0×10-³
(2)酸性增强,H++R→HR 平衡正向移动,导致R- 浓度降低,难以与铝离子配位
(3)6.9×10-² 2Fe²++H₂O₂+2H₃PO₄=2FePO₄ ↓+2H₂O+4H+ (配平错不得分)
(4)Mg(OH)₂
(5)CaCO₃
18. (17分,第一个空为1分,其余每空均为2
分。) I.① ( 1 分 )
②SiO₂ 、P₂O, (少写一个得1分,写错一个不得
分) ③<
7Ⅱ.①sp² 、sp³ (少写一个得1分,填错一个不得
分) ②2:1
③ade (写对两个得 1 分,写错不得分,字母大小写均可)
④丁二酮肟中含有2个羟基,可以形成分子间氢键,使其熔点升高。(答出分子
间 氢键,无其他知识性错误即可)
Ⅲ ③; +2
19. (10分)
(1)4(2 分);极性(1 分)
(2)2(2 分)
(3)①LiNbOCl4(2 分 ) ;
77