文档内容
重庆复旦中学教共体 2025~2026 学年度上期定时作业
高 2027 届化学试题
尊重自己!爱护复旦!复旦过去的光荣,将来的灿烂,全赖我们共同爱护,共同发展!同
学:今天在考试的时候,不要忘记自己!不要忘记复旦!考场秩序井然,人人洁身自爱。
本试卷分为I卷和Ⅱ卷,考试时间60 分钟,满分 100 分。请将答案工整地书写在答题
卡上。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ti-48 Cr-52 Mn-55
Fe-56 Cu-64 Zn-65
第 I卷(选择题 共 42分)
一、选择题(本题包括 14 小题,每小题3分,共 42分。每小题只有一个选项符合题意)
1.(原创)化学知识可以指导生产、生活,下列有关说法错误的是( )
A.明矾在水中可形成氢氧化铝的悬浊液,可用明矾沉降水中悬浮物
B.室温下醋酸的电离平衡常数大于碳酸,可用醋酸除去烧水壶中的水垢
C.钢铁的电化学腐蚀和化学腐蚀都是铁发生了氧化反应
D.硫化钠溶液有臭味,是因为该盐发生了水解。
2.下列物质的水溶液呈碱性且促进水的电离的是( )
A.Na SO B.小苏打 C.苛性钠 D.CH COONH
2 4 3 4
3.CO 与NH 混合,一定条件下反应:2NH (g)+CO (g) CO(NH ) (s) +H O(g) △H<0。则下列说法
2 3 3 2 2 2 2
错误的是( )
A.该反应的ΔS<0,在低温时可以自发进行
B.升高温度,该反应的平衡常数会减小
C.使用催化剂,可以降低反应热,提高尿素的生成速率
D.及时分离出H O,有利于提高CO(NH ) 的平衡产率
2 2 2
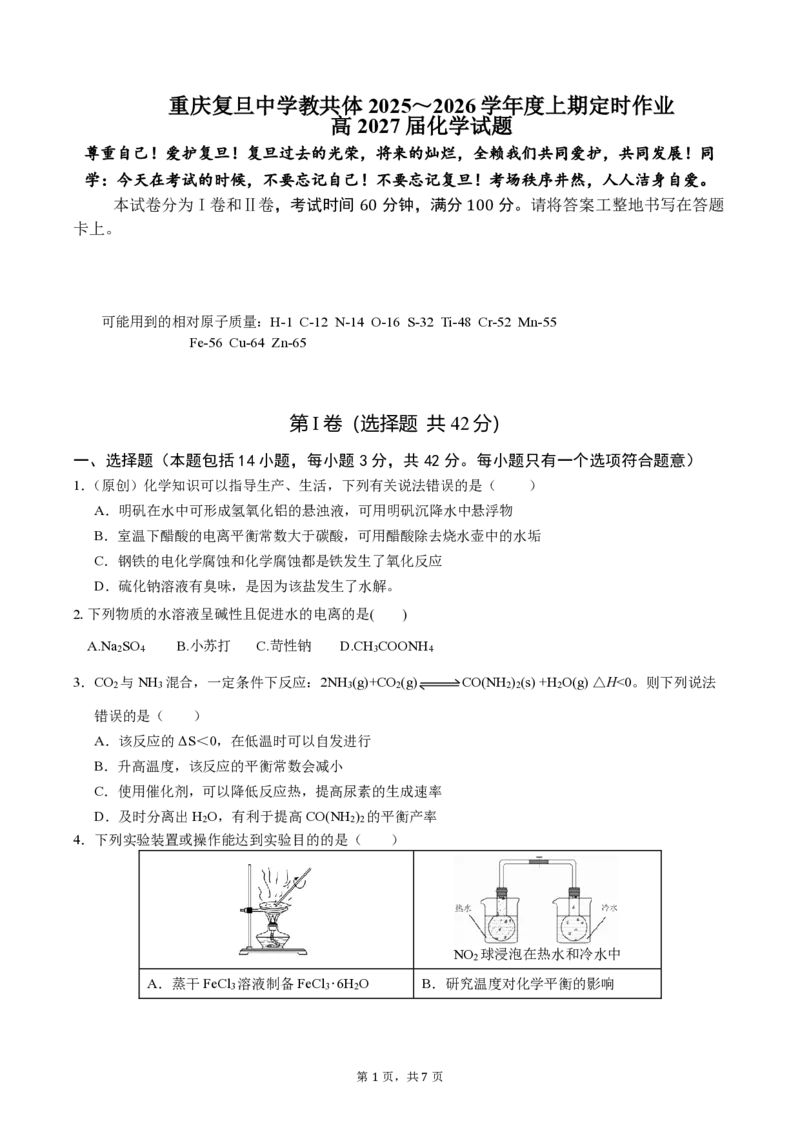
4.下列实验装置或操作能达到实验目的的是( )
NO 球浸泡在热水和冷水中
2
A.蒸干FeCl 溶液制备FeCl ‧6H O B.研究温度对化学平衡的影响
3 3 2
第1页,共7页
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}C.定性测定盐酸与碳酸氢钠反应的热效
D.钢闸门的电化学防腐
应
5.下列有关方程式正确的是( )
A.草酸溶液显酸性:H C O =2H++C O 2-
2 2 4 2 4
B.用TiCl 制备TiO :TiCl +xH O TiO ·xH O↓+4HCl
4 2 4 2 2 2
C.少量的H S气体通入硫酸铜溶液中:H S+Cu2+=CuS↓+2H+
2 2
D.铅酸蓄电池放电时的负极反应式:Pb-2e-=Pb2+
6.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.当c(Fe3+)=1mol·L-1的溶液:Mg2+、Ba2+、NO -、I-
3
B.甲基橙为红色的溶液中:Na+、K+、SO2−、MnO−
3 4
C.在水电离出的c(OH-)=1×10-10的溶液中:NH +、SO 2-、Cl-、HCO -
4 4 3
D.
第2页,共7页
c (
K
O W H − ) = 0 .1 m o l L − 1 的溶液中:Na+、Al3+、Br-、Cl−
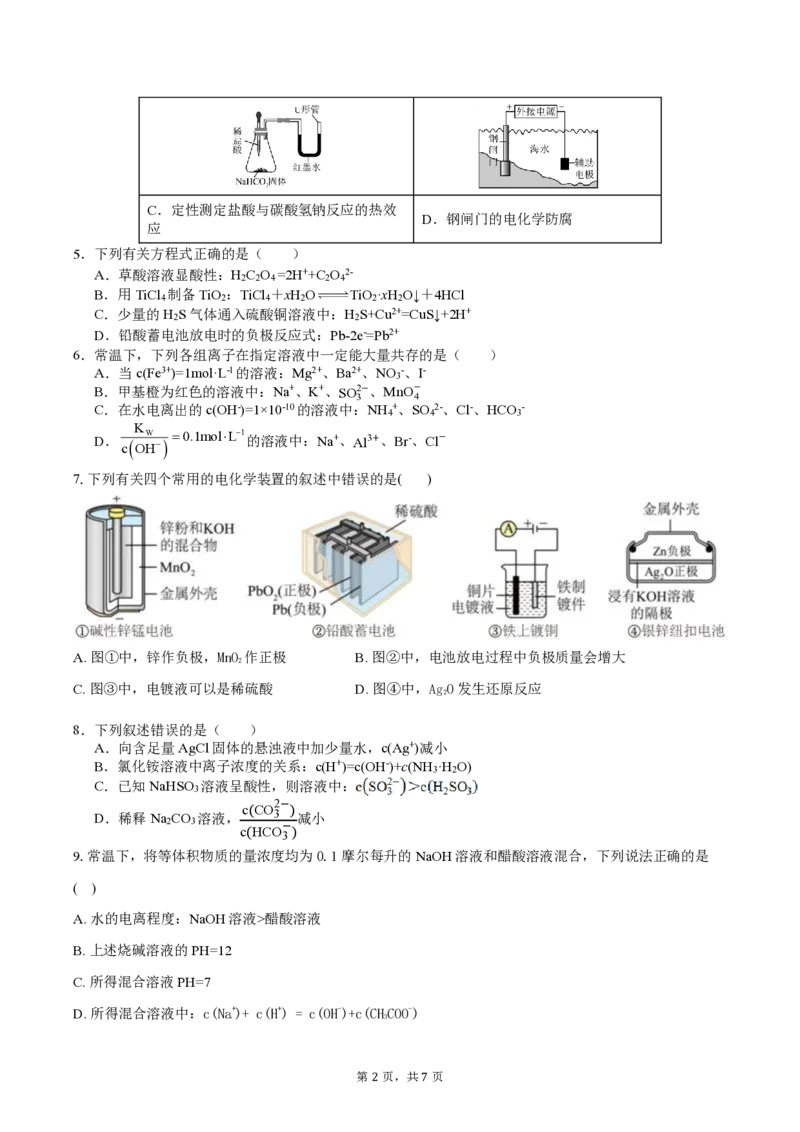
7.下列有关四个常用的电化学装置的叙述中错误的是( )
A. 图①中,锌作负极,MnO 作正极 B. 图②中,电池放电过程中负极质量会增大
2
C. 图③中,电镀液可以是稀硫酸 D. 图④中,AgO发生还原反应
2
8.下列叙述错误的是( )
A.向含足量AgCl固体的悬浊液中加少量水,c(Ag+)减小
B.氯化铵溶液中离子浓度的关系:c(H+)=c(OH-)+c(NH ·H O)
3 2
C.已知NaHSO 溶液呈酸性,则溶液中:
3
2−
c(CO )
D.稀释Na CO 溶液, 3 减小
2 3 −
c(HCO )
3
9.常温下,将等体积物质的量浓度均为0.1摩尔每升的NaOH溶液和醋酸溶液混合,下列说法正确的是
( )
A. 水的电离程度:NaOH溶液>醋酸溶液
B. 上述烧碱溶液的PH=12
C. 所得混合溶液PH=7
D. 所得混合溶液中:c(Na+)+ c(H+) = c(OH-)+c(CHCOO-)
3
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}10.有关下列三个电化学装置的叙述中,正确的是( )
A.装置I铜电极上发生氧化反应
B.装置II电池工作一段时间后,甲池的c(SO 2-)减小
4
C.装置III正极反应为:AgCl+e-===Ag+Cl-
D.装置III电路中转移0.02 mol e-时,交换膜右侧溶液中约增加0.04 mol离子
11.下列实验装置或操作不能达到实验目的的是( )
A.验证𝐾 (𝐴𝑔𝐵𝑟)>𝐾 (𝐴𝑔𝐼) B.牺牲锌保护铁
𝑠𝑝 𝑠𝑝
C.中和热的测定 D.用HCl标准溶液滴定NaOH溶液
A. A B. B C. C D. D
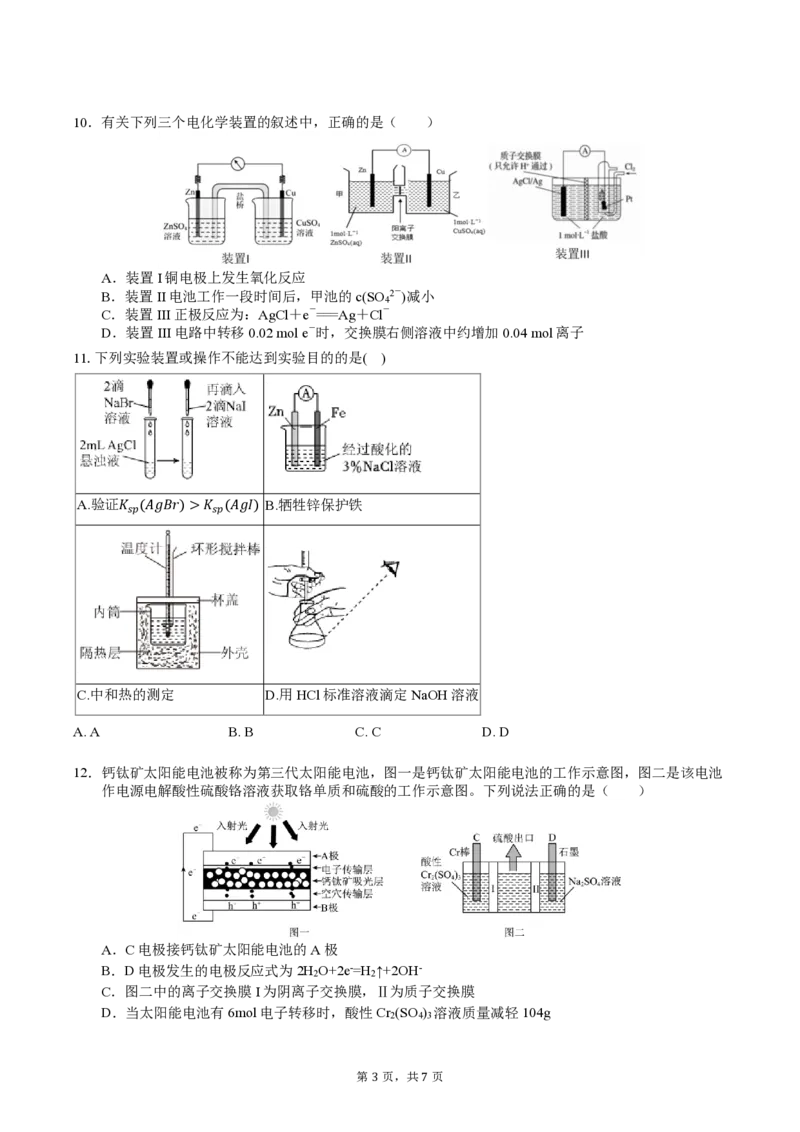
12.钙钛矿太阳能电池被称为第三代太阳能电池,图一是钙钛矿太阳能电池的工作示意图,图二是该电池
作电源电解酸性硫酸铬溶液获取铬单质和硫酸的工作示意图。下列说法正确的是( )
A.C电极接钙钛矿太阳能电池的A极
B.D电极发生的电极反应式为2H O+2e-=H ↑+2OH-
2 2
C.图二中的离子交换膜I为阴离子交换膜,Ⅱ为质子交换膜
D.当太阳能电池有6mol电子转移时,酸性Cr (SO ) 溶液质量减轻104g
2 4 3
第3页,共7页
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}13.常温时,1mol/L的HA和1mol/L的HB两种酸溶液,起始时的体积均为V ,分别将两溶液加水稀
0
释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是( )
A.两者均为弱酸,且酸性强弱为:HB>HA
−
c(B )
B.将 =1的溶液加水稀释至 =3时, 减小
−
c(A )
C.M点水的电离程度大于N
D.在
第4页,共7页
0 p H 5 时,HB溶液满足: p H = lg
V
V
0
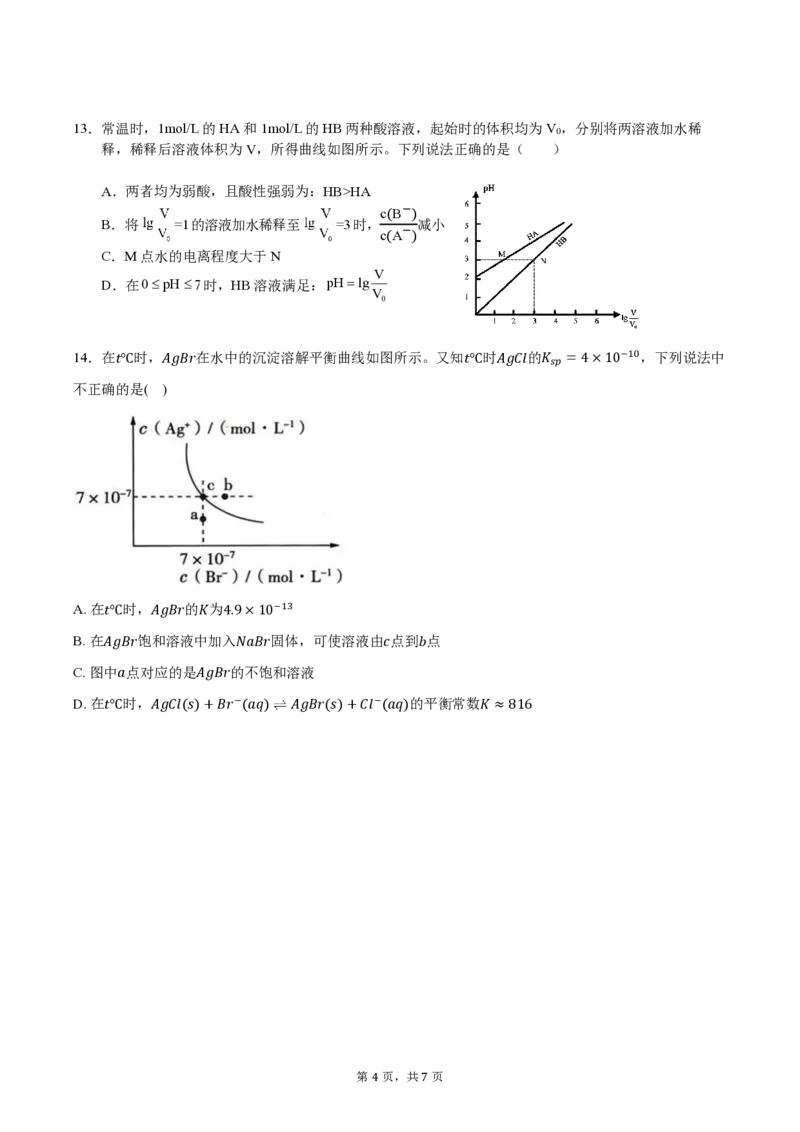
14.在𝑡℃时,𝐴𝑔𝐵𝑟在水中的沉淀溶解平衡曲线如图所示。又知𝑡℃时𝐴𝑔𝐶𝑙的𝐾 =4×10−10,下列说法中
𝑠𝑝
不正确的是( )
A. 在𝑡℃时,𝐴𝑔𝐵𝑟的𝐾为4.9×10−13
B. 在𝐴𝑔𝐵𝑟饱和溶液中加入𝑁𝑎𝐵𝑟固体,可使溶液由𝑐点到𝑏点
C. 图中𝑎点对应的是𝐴𝑔𝐵𝑟的不饱和溶液
D. 在𝑡℃时,𝐴𝑔𝐶𝑙(𝑠)+𝐵𝑟−(𝑎𝑞) 𝐴𝑔𝐵𝑟(𝑠)+𝐶𝑙−(𝑎𝑞)的平衡常数𝐾 ≈816
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}第 II卷(非选择题 共 58分)
15.( 14分 )部分弱电解质的电离常数如下表:
弱电解质 𝐻𝐹 𝐻𝐶𝑁 𝐻 𝐶𝑂
2 3
电离常数(25℃) 𝐾 =4.0×10−4 𝐾 =4.9×10−10 𝐾 =4.3×10−7 𝐾 =5.6×10−11
𝑎 𝑎 𝑎1 𝑎2
(1)根据上述数据,可判断常温下同浓度的𝑁𝑎𝐹、𝑁𝑎𝐶𝑁、𝑁𝑎 𝐶𝑂 三种溶液的𝑝𝐻值由大到小的顺序是:
2 3
____________________________ 。
(2)中和体积、𝑝𝐻均相等的𝐻𝐹、𝐻𝐶𝑁溶液,__ __消耗的𝑁𝑎𝑂𝐻更多。
(3)向𝑁𝑎𝐶𝑁溶液中通入少量𝐶𝑂 ,离子方程式为:_____________________________。
2
(4) 𝑁𝑎 𝐶𝑂 溶液呈碱性的主要原因(离子方程式表示):_________________________。
2 3
(5) 𝑁𝑎 𝐶𝑂 溶液中各离子浓度由大到小的顺序为:______________________________。该溶液中可满足关
2 3
系:𝑐(𝑁𝑎+)=2𝑐(𝐶𝑂2−)+_____________。
3
(6)常温下,浓度相等的𝐻𝐹与𝑁𝑎𝐹溶液等体积混合,溶液呈酸性。请通过计算来解释该混合溶液呈酸性的
原因:________________________________________________。
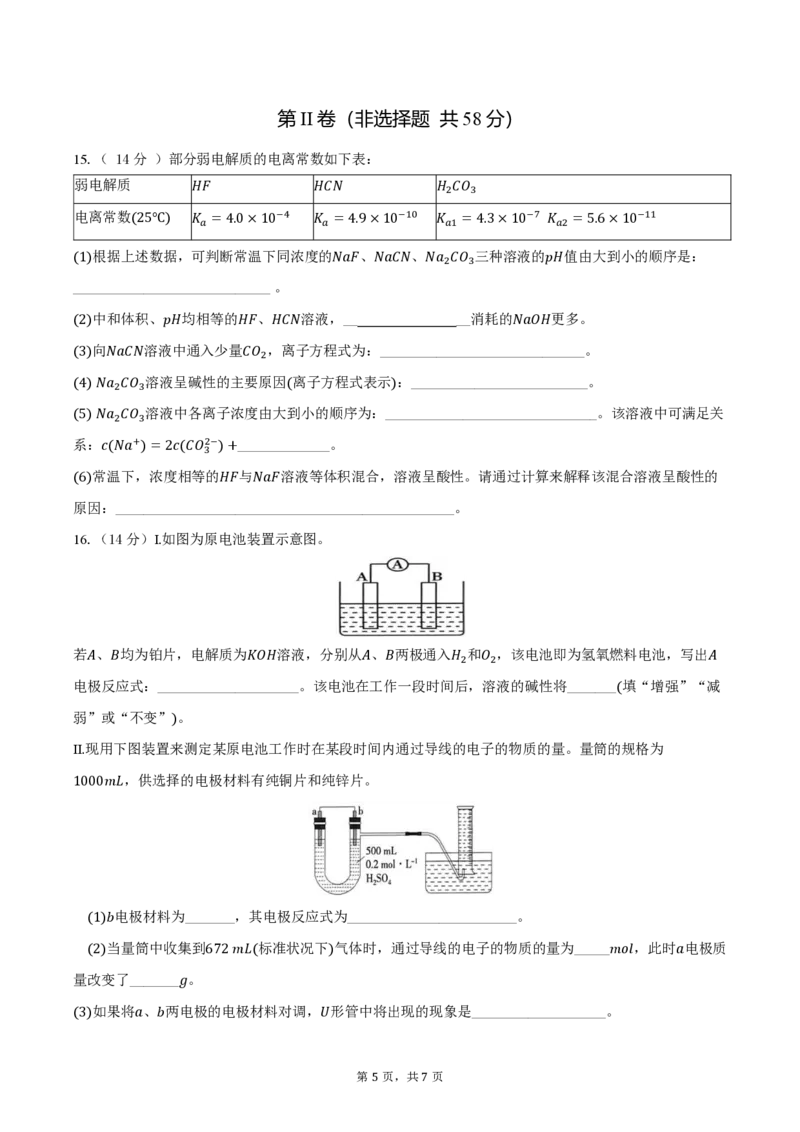
16.(14分)Ⅰ.如图为原电池装置示意图。
若𝐴、𝐵均为铂片,电解质为𝐾𝑂𝐻溶液,分别从𝐴、𝐵两极通入𝐻 和𝑂 ,该电池即为氢氧燃料电池,写出𝐴
2 2
电极反应式:____________________。该电池在工作一段时间后,溶液的碱性将_______(填“增强”“减
弱”或“不变”)。
Ⅱ.现用下图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为
1000𝑚𝐿,供选择的电极材料有纯铜片和纯锌片。
(1)𝑏电极材料为_______,其电极反应式为________________________。
(2)当量筒中收集到672 𝑚𝐿(标准状况下)气体时,通过导线的电子的物质的量为_____𝑚𝑜𝑙,此时𝑎电极质
量改变了_______𝑔。
(3)如果将𝑎、𝑏两电极的电极材料对调,𝑈形管中将出现的现象是___________________。
第5页,共7页
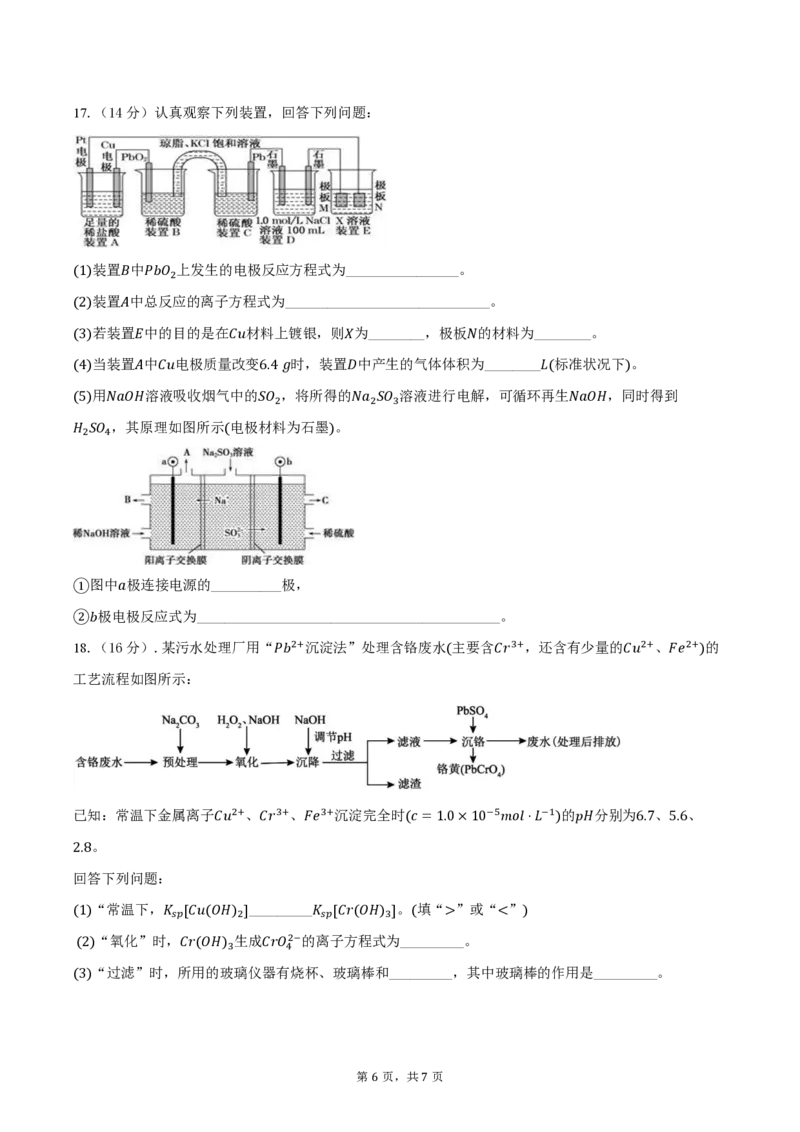
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}17.(14分)认真观察下列装置,回答下列问题:
(1)装置𝐵中𝑃𝑏𝑂 上发生的电极反应方程式为________________。
2
(2)装置𝐴中总反应的离子方程式为_____________________________。
(3)若装置𝐸中的目的是在𝐶𝑢材料上镀银,则𝑋为________,极板𝑁的材料为________。
(4)当装置𝐴中𝐶𝑢电极质量改变6.4 𝑔时,装置𝐷中产生的气体体积为________𝐿(标准状况下)。
(5)用𝑁𝑎𝑂𝐻溶液吸收烟气中的𝑆𝑂 ,将所得的𝑁𝑎 𝑆𝑂 溶液进行电解,可循环再生𝑁𝑎𝑂𝐻,同时得到
2 2 3
𝐻 𝑆𝑂 ,其原理如图所示(电极材料为石墨)。
2 4
①图中𝑎极连接电源的__________极,
②𝑏极电极反应式为___________________________________________。
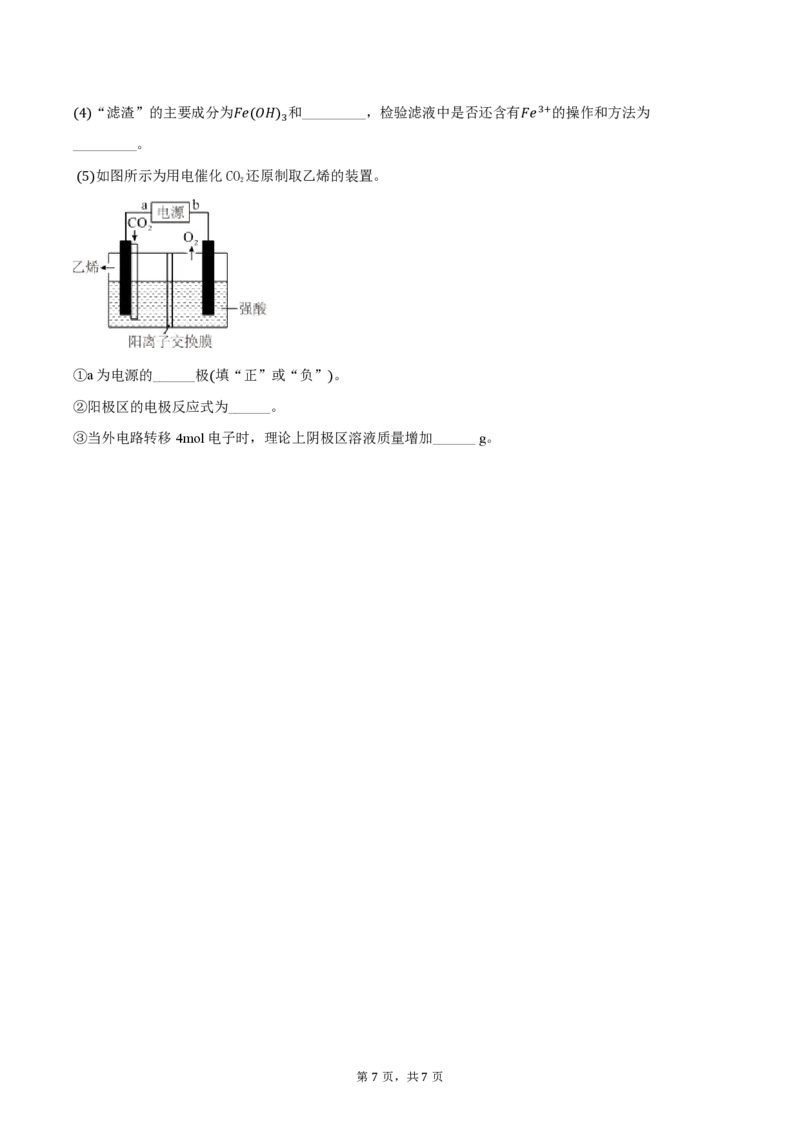
18.(16分).某污水处理厂用“𝑃𝑏2+沉淀法”处理含铬废水(主要含𝐶𝑟3+,还含有少量的𝐶𝑢2+、𝐹𝑒2+)的
工艺流程如图所示:
已知:常温下金属离子𝐶𝑢2+、𝐶𝑟3+、𝐹𝑒3+沉淀完全时(𝑐 =1.0×10−5𝑚𝑜𝑙·𝐿−1)的𝑝𝐻分别为6.7、5.6、
2.8。
回答下列问题:
(1)“常温下,𝐾 [𝐶𝑢(𝑂𝐻) ]_________𝐾 [𝐶𝑟(𝑂𝐻) ]。(填“>”或“<”)
𝑠𝑝 2 𝑠𝑝 3
(2)“氧化”时,𝐶𝑟(𝑂𝐻) 生成𝐶𝑟𝑂2−的离子方程式为_________。
3 4
(3)“过滤”时,所用的玻璃仪器有烧杯、玻璃棒和_________,其中玻璃棒的作用是_________。
第6页,共7页
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}(4)“滤渣”的主要成分为𝐹𝑒(𝑂𝐻) 和_________,检验滤液中是否还含有𝐹𝑒3+的操作和方法为
3
_________。
(5)如图所示为用电催化CO 还原制取乙烯的装置。
2
①a为电源的______极(填“正”或“负”)。
②阳极区的电极反应式为______。
③当外电路转移4mol电子时,理论上阴极区溶液质量增加______ g。
第7页,共7页
{#{QQABAQs14gCwkISACT4qVwHiCwuYkIGhLIgMwRASuARrgAFIFIA=}#}