文档内容
万州二中高 2023 级高二下期期中考试 化学试题
命题人:牟雄 审题人:钟德友
(本试卷共 8 页,共 18 题,满分 100 分。考试用时 75 分钟)
可能用到的相对原子质量:H 1 C12 N14 O16 Fe56
一、单项选择题:本题共 14小题,每小题 3分,共 42分。
1.化学与生活紧密相关,下列说法错误的是( )
A. 聚乙炔可用于制备导电高分子材料
B. 碳纳米材料属于新型无机非金属材料,是一种新型化合物
C. 环保型量子点InP-HF在X射线衍射测试时呈现明锐的衍射峰,说明其具有晶体结构
D. 壁虎的足与墙体之间的作用力,本质上是足上的细毛与墙体之间的范德华力
2.某元素基态原子4s轨道上有1个电子,则该基态原子的价电子排布不可能是 ( )
A.3p64s1 B.4s1 C.3d54s1 D.3d104s1
3.下列图示或化学用语错误的是( )
A.Mn2+的价电子的轨道表示式:
B.H O的VSEPR模型:
2
C. 羟基的电子式:
D. 顺-2-丁烯的球棍模型为
4.下列说法正确的是( )
A.1molN 分子中的π键与1molCO 分子中的π键的数目之比为2∶1
2 2
B. 通常条件下的稳定性:甲烷>乙烯
C. 强度:氢键>化学键>范德华力
D. 沸点: >
5.下列关于乙烷、乙烯、乙炔的说法正确的是( )
①它们既不互为同系物,也不互为同分异构体
②乙烷是饱和烃,乙烯、乙炔是不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色
高二期中 化学 第1页 (共8页)④它们都能燃烧,乙炔燃烧火焰最明亮,有浓烟
⑤它们都能使酸性KMnO 溶液褪色
4
A.①③④ B.①②③⑤ C.②③④⑤ D.①②③④
6.实验室制取少量溴苯并提纯的过程中不能达到实验目的的是( )
A B C D
制备溴苯 吸收尾气 水洗后分液 蒸馏获得溴苯
7.下列命名正确的是( )
A. 2-乙基丙烷 B. 2-甲基-2-丙烯
C. 2,2,3-三甲基戊烷 D. 溴乙烷
8.下列有关有机物 的说法正确的是( )
A. 该分子中含有3种官能团 B. 分子式为C H O
9 10
C. 一氯代物最多有2种 D. 与 互为同分异构体
9.下列数据是对应物质的熔点,有关判断错误的是( )
A. 含有金属阳离子的晶体一定是离子晶体 B.AlCl 可形成分子晶体
3
C. 同族元素的氧化物可形成不同类型的晶体 D. 金属晶体的熔点不一定比分子晶体高
10. 和 均可发生水解反应,其中 和 水解机理示意图如图:
NCl3 SiCl4 NCl3 SiCl4
高二期中 化学 第2页 (共8页)(1)
(2)
下列说法正确的是( )
A. 和 均为非极性分子, 和 中的N均为 杂化
2
B. NCl3水S解iC过l4程中Si原子的杂化N方Cl式3 保N持H3不变 sp
C. SiCl4和 的水解反应机理相同
D.
NCl3水S解iC过l4程中只存在极性键的断裂和生成
11.我Si国Cl4科学家用如图所示的阴离子的盐作水系锌离子电池的电解质溶液,显示了优良的循环性能。X、Y、
Z、W均为短周期元素且原子序数依次增大,其中X、Y、Z位于同一周期,Y、W核外最外层电子数相等。
下列叙述正确的是( )
A. 简单离子半径大小顺序为
B.W氧化物对应的水化物一定W是>强Z>酸Y
C.Y的简单氢化物的沸点高于W的简单氢化物,是因为Y的非金属性强于W
D.X和Z形成的简单化合物各原子最外层均满足8电子稳定结构
12.某实验小组设计如图装置完成乙炔的制备和性质探究实验。下列有关说法正确的是( )
A.a装置中的饱和食盐水可以换成蒸馏水,使产生乙炔更为纯净
B.d、e装置中溶液都会发生褪色现象,反应原理各不相同
C.f处产生明亮淡蓝色火焰,且有黑烟生成
高二期中 化学 第3页 (共8页)D.收集乙炔气体时可采用向上排空气法
13.有8种物质:①乙烷 ②环己烷 ③丙炔 ④2-丁烯 ⑤环己烯 ⑥二氧化硫 ⑦聚乙烯 ⑧聚乙炔,
既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的有机物的是( )
.③④⑤⑥⑧ B.③④⑤⑧ C. ①②④⑥ D.①②⑥⑦
14.分子式为C H 的烃,可能有的同分异构体(不考虑C==C==C结构)的种数为( )
4 6
A. 5 B. 6 .7 D.8
二、非选择题:本题共 4 小题,共58分。
15.(15分)有机物的种类多,在日常生活中有重要的用途。请回答下列问题:
① ;② ;③ ;④
CH3CH=CH2 CH3CH OH CH3
(1)①被酸性高锰酸钾氧化的产物为
(2)请用系统命名法命名有机物②
(3)③可以发生加聚反应,其方程式为
(4)④中基态氧原子的核外电子的空间运动状态有 种。
(5)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示
式: , 该过程形成的原子光谱为 (填“吸收”或“发射”)光谱。
(6)在硅酸盐中,Si 的空间结构是正四面体(图1)结构,通过共用顶角氧离子可形成岛状、链状、层状、骨
4−
架网状四大类结O4构型式。图 2 为一种无限长单链结构的多硅酸根,其中 Si 原子的杂化方式
为 ,Si与O的原子数之比为 。
图1 图2
16.(15分)我国科学家屠呦呦因青蒿素研究获得诺贝尔奖,青蒿素是从传统药材中发现的能治疗疟疾的
有机化合物。青蒿素为无色针状晶体,熔点为156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
现某实验小组拟提取青蒿素。
Ⅰ.实验室流程如图所示:
高二期中 化学 第4页 (共8页)(1) 操作Ⅰ的名称是 。
(2) 操作Ⅱ可分离溶剂A和青蒿素,用到的主要玻璃仪器有酒精灯、温度计、 、
、尾接管、锥形瓶。
(3)操作Ⅲ是重结晶,其操作步骤为:加热溶解→ → →过滤、洗涤、干燥。
(4)关于有机物A的分子结构可用如下现代分析方法进行测定。
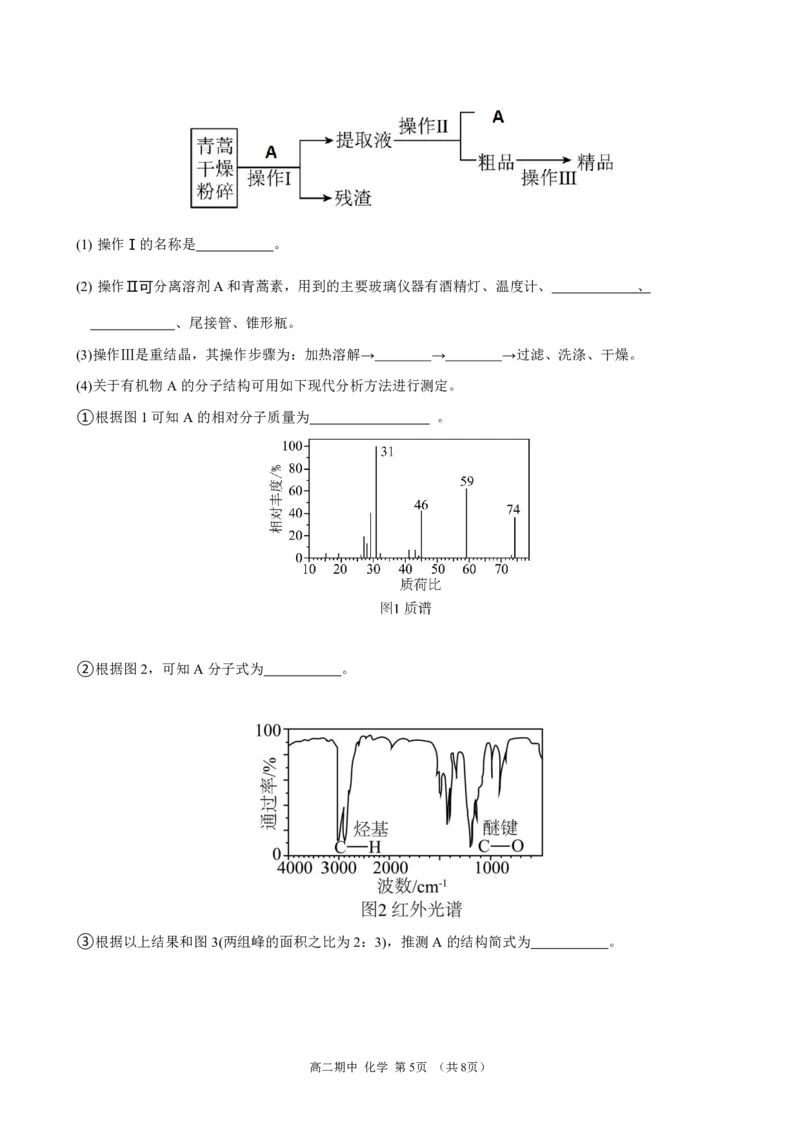
①根据图1可知A的相对分子质量为 。
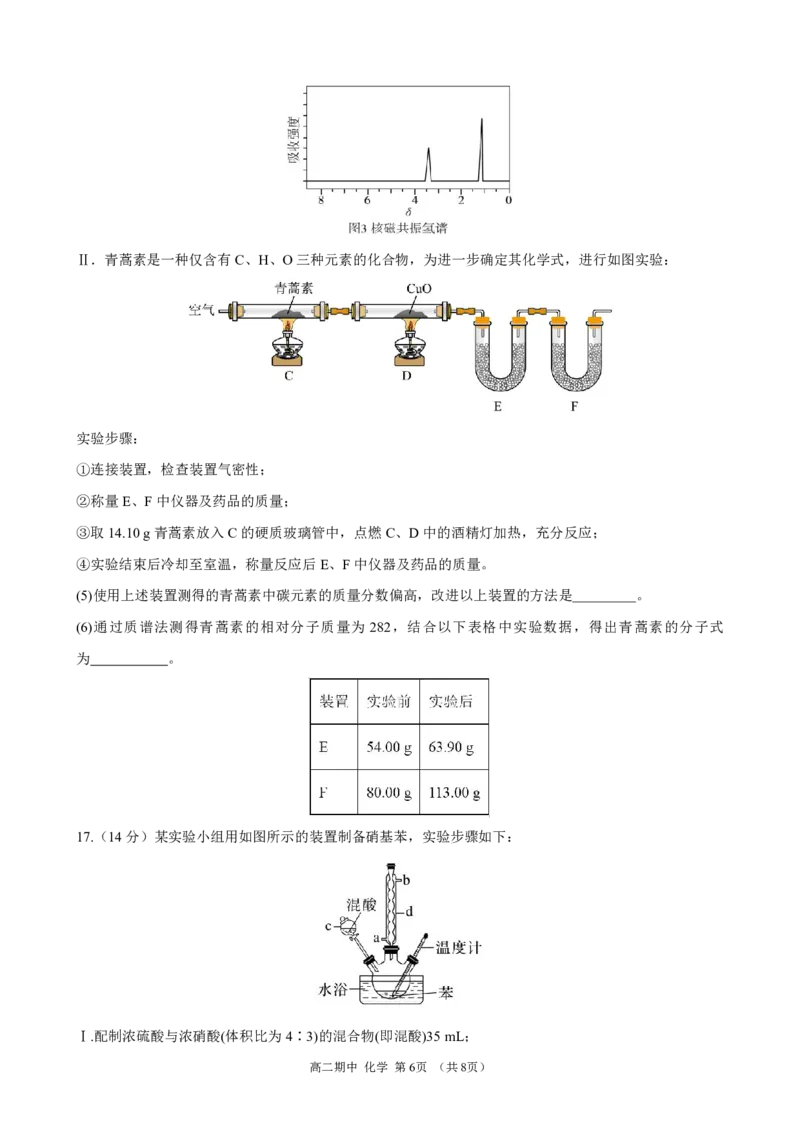
②根据图2,可知A分子式为 。
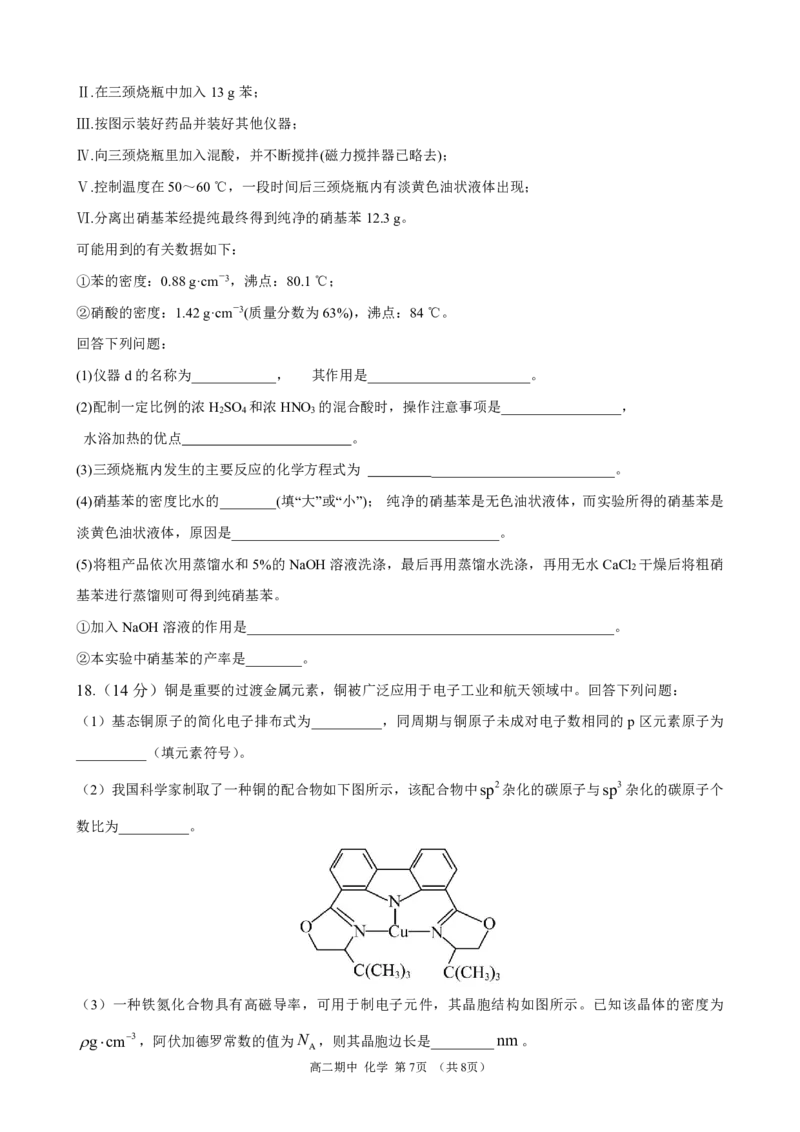
③根据以上结果和图3(两组峰的面积之比为2:3),推测A的结构简式为 。
高二期中 化学 第5页 (共8页)Ⅱ.青蒿素是一种仅含有C、H、O三种元素的化合物,为进一步确定其化学式,进行如图实验:
实验步骤:
①连接装置,检查装置气密性;
②称量E、F中仪器及药品的质量;
③取14.10g青蒿素放入C的硬质玻璃管中,点燃C、D中的酒精灯加热,充分反应;
④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量。
(5)使用上述装置测得的青蒿素中碳元素的质量分数偏高,改进以上装置的方法是 。
(6)通过质谱法测得青蒿素的相对分子质量为 282,结合以下表格中实验数据,得出青蒿素的分子式
为 。
17.(14分)某实验小组用如图所示的装置制备硝基苯,实验步骤如下:
Ⅰ.配制浓硫酸与浓硝酸(体积比为4∶3)的混合物(即混酸)35mL;
高二期中 化学 第6页 (共8页)Ⅱ.在三颈烧瓶中加入13g苯;
Ⅲ.按图示装好药品并装好其他仪器;
Ⅳ.向三颈烧瓶里加入混酸,并不断搅拌(磁力搅拌器已略去);
Ⅴ.控制温度在50~60℃,一段时间后三颈烧瓶内有淡黄色油状液体出现;
Ⅵ.分离出硝基苯经提纯最终得到纯净的硝基苯12.3g。
可能用到的有关数据如下:
①苯的密度:0.88g·cm-3,沸点:80.1℃;
②硝酸的密度:1.42g·cm-3(质量分数为63%),沸点:84℃。
回答下列问题:
(1)仪器d的名称为____________, 其作用是_______________________。
(2)配制一定比例的浓H SO 和浓HNO 的混合酸时,操作注意事项是_________________,
2 4 3
水浴加热的优点 。
(3)三颈烧瓶内发生的主要反应的化学方程式为 __________________________。
(4)硝基苯的密度比水的________(填“大”或“小”); 纯净的硝基苯是无色油状液体,而实验所得的硝基苯是
淡黄色油状液体,原因是______________________________________。
(5)将粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后再用蒸馏水洗涤,再用无水CaCl 干燥后将粗硝
2
基苯进行蒸馏则可得到纯硝基苯。
①加入NaOH溶液的作用是____________________________________________________。
②本实验中硝基苯的产率是________。
18.(14分)铜是重要的过渡金属元素,铜被广泛应用于电子工业和航天领域中。回答下列问题:
(1)基态铜原子的简化电子排布式为__________,同周期与铜原子未成对电子数相同的p区元素原子为
__________(填元素符号)。
(2)我国科学家制取了一种铜的配合物如下图所示,该配合物中sp2杂化的碳原子与sp3杂化的碳原子个
数比为__________。
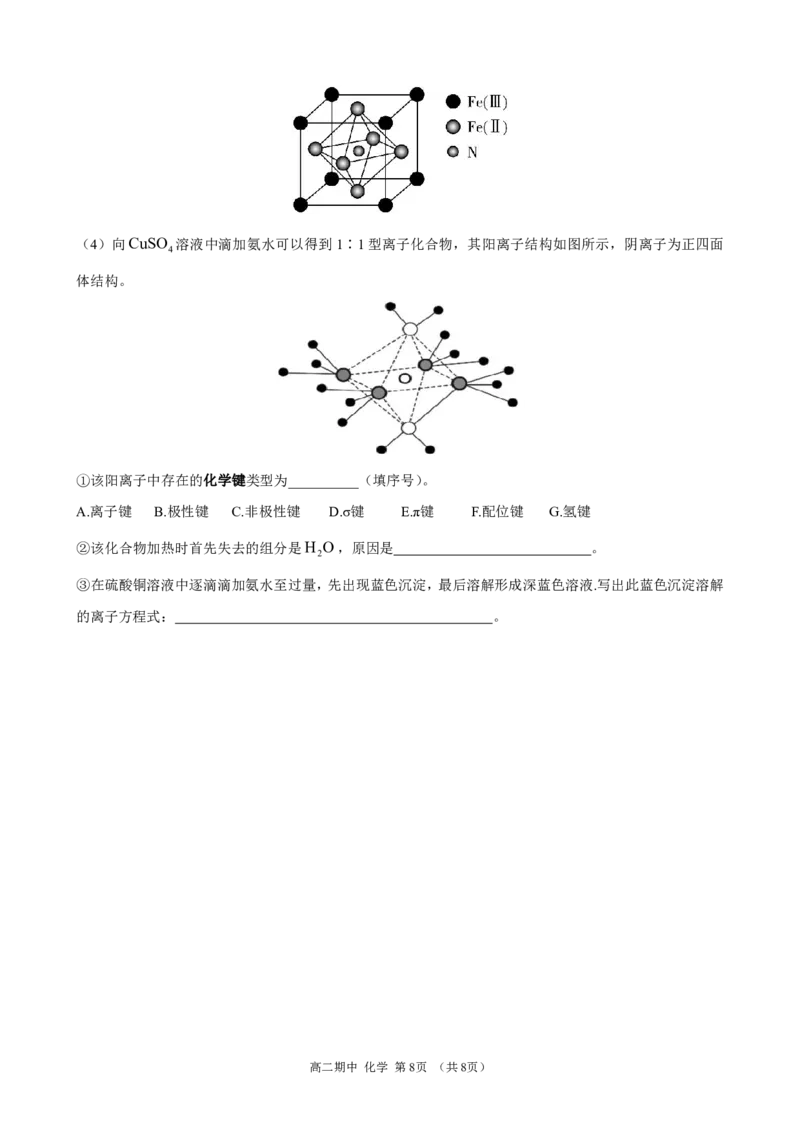
(3)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。已知该晶体的密度为
gcm3,阿伏加德罗常数的值为N ,则其晶胞边长是_________nm。
A
高二期中 化学 第7页 (共8页)(4)向CuSO 溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示,阴离子为正四面
4
体结构。
①该阳离子中存在的化学键类型为__________(填序号)。
A.离子键 B.极性键 C.非极性键 D.σ键 E.π键 F.配位键 G.氢键
②该化合物加热时首先失去的组分是H O,原因是 。
2
③在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液.写出此蓝色沉淀溶解
的离子方程式: 。
高二期中 化学 第8页 (共8页)