文档内容
绝密★启用前 试卷类型:A B.CaF 晶体中,每个晶胞平均有4个Ca2+,每个Ca2+周围最近的Ca2+有6个
2
滕州实验高级中学 2024~2025 学年度第二学期第一次调研考试 C.金刚石晶体中,每个C原子被12个六元环所共用
D.立方氮化硼晶体中,硼原子的配位数为8
高二年级化学学科试题
4.超硬陶瓷材料氮化硅可由反应3SiH 4NH Si N 12H 制得。下列说法不正确的是
4 3 3 4 2
命题人: 鞠文学 出题时间:2025.3
A.NH 的VSEPR模型:四面体 B.Si N 属于分子晶体
3 3 4
注意事项: C.H 是一种非极性分子 D.SiH 为正四面体结构
2 4
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
5.下列关于物质的结构或性质的描述及解释正确的是
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,用橡皮擦干净
A.稳定性:H O>H S,是由于水分子间存在氢键
2 2
后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
B.利用“杯酚”可分离C 和C 是因为超分子具有“自组装”的特征
60 70
3.考试结束后,本试卷和答题卡一并交回。
C.AlF (1040℃)熔点远高于AlCl (178℃升华)是由于两者的晶体类型不同
3 3
本次考试用到相对原子质量:C 12 O 16 H 1 N 14 B 11 C 64 S 32
U
一、单选题(每题3分,只有一个答案) D.CO 与SO 的空间结构不同,是由于中心原子杂化方式相同,孤电子对数不同
2 2
1新材料助力嫦娥六号探月挖“宝”,下列有关说法正确的是
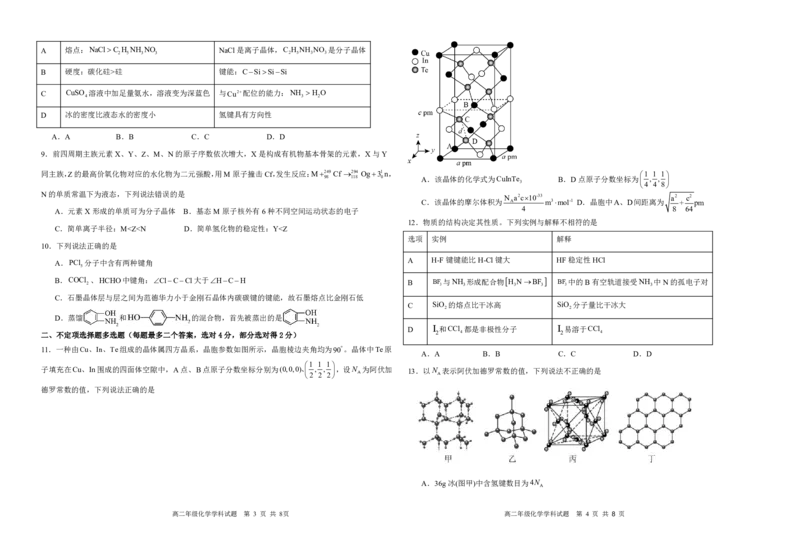
6.在硅酸盐中,SiO4四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类
4
A.“挖宝”所用钻杆由碳化硅增强铝基复合材料制造,碳化硅属于共价晶体
结构形式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式及化学式为
B.月面国旗由超细玄武岩纤维纺织而成,玄武岩纤维属于有机高分子
C.上升器激光陀螺仪应用了高纯石英玻璃,石英玻璃属于晶体
D.制造一同启程的小卫星“思源二号”,采用了特种镁合金与碳纤维,碳纤维属于纤维素
2.下列关于共价晶体、分子晶体的叙述中,正确的是
A.在SiO 晶体中,每个硅原子和2个氧原子形成2个共价键
2
B.12g石墨中含有σ键的物质的量为3mol
A.sp3 SiO 2n B.sp3 SiO4 C.sp2 Si O6 D.sp2 Si O6
3 n 4 2 7 3 9
C.HI的相对分子质量大于 HF,所以HI 的沸点高于HF
7.晶体是材料科学研究中非常重要的材料类型,下列说法错误的是
D.1mol金刚石中的C—C键数是2N
A
A.金属晶体中含有离子,但不存在离子键
3.有关晶体的结构如图所示,下列说法中正确的是
B.共价晶体中共价键越强,晶体的熔点越高
C.分子晶体中分子间作用力越大,该物质越稳定
D.离子晶体中一定存在离子键,可能存在共价键
8.下列原因分析不能正确解释性质差异的是
选项 性质差异 原因分析
A.NaCl晶体中,Na+位于Cl-构成的四面体空隙中
高二年级化学学科试题 第 1 页 共 8 页 高二年级化学学科试题 第 2 页 共 8 页
{#{QQABTYIs5ggwgBRACI6qUwECCUiQsIGTJSoOQUCaOARKgQFABAA=}#}A 熔点:NaClC H NH NO NaCl是离子晶体,C H NH NO 是分子晶体
2 5 3 3 2 5 3 3
B 硬度:碳化硅>硅 键能:CSiSiSi
C CuSO 溶液中加足量氨水,溶液变为深蓝色 与Cu2配位的能力:NH H O
4 3 2
D 冰的密度比液态水的密度小 氢键具有方向性
A.A B.B C.C D.D
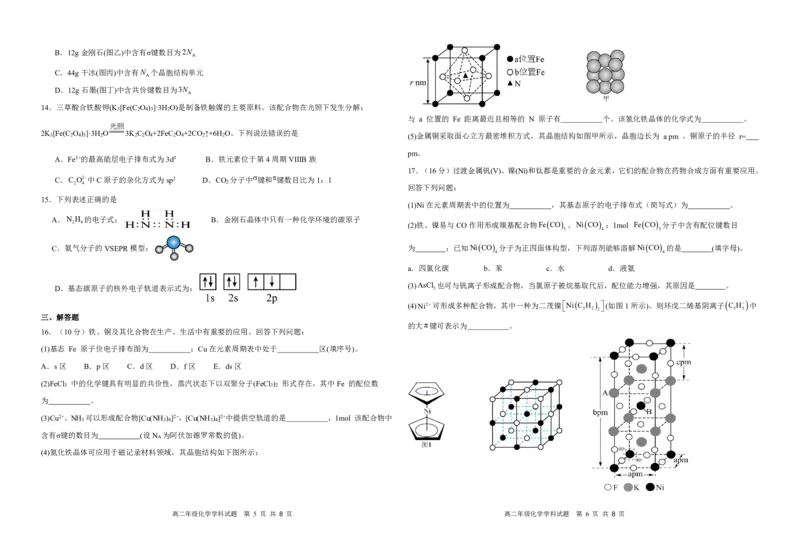
9.前四周期主族元素X、Y、Z、M、N的原子序数依次增大,X是构成有机物基本骨架的元素,X与Y
同主族,Z的最高价氧化物对应的水化物为二元强酸,用M原子撞击Cf,发生反应:M249 Cf 294 Og31n, 1 1 1
98 118 0 A.该晶体的化学式为CuInTe B.D点原子分数坐标为 , ,
3 4 4 8
N的单质常温下为液态,下列说法错误的是
N a2c10-33 a2 c2
C.该晶体的摩尔体积为 A m3mol-1 D.晶胞中A、D间距离为 + pm
A.元素X形成的单质可为分子晶体 B.基态M原子核外有6种不同空间运动状态的电子 4 8 64
12.物质的结构决定其性质。下列实例与解释不相符的是
C.简单离子半径:M