文档内容
2008 年南通市初中毕业、升学考试
化 学
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷1至3页,第Ⅱ卷4至8页。共100
分。考试时间100分钟。考试结束,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Fe-56
第Ⅰ卷(选择题 共40分)
注意事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、考试号、科目名称用2B铅笔涂写在答题卡上。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其它答案。不能答在试卷上。
一、 选择题(本题共15小题,每小题2分,共30分)每小题给出的四个选项中只有一个选项正
确,请将正确选项的序号填涂在答题卡上。
1.北京奥运火炬的外壳主要采用高品质的铝合金材料制造,燃烧系统内装环保型燃料——丙烷
(C H)。下列说法正确的是
3 8
A.铝合金制作的火炬质量轻、不易腐蚀 B.铝合金硬度小、不易导热
C.丙烷分子中C、H电子数之比为3∶8 D.丙烷在常温常压下是固体
2.把少量物质分别加入到另一物质中,充分搅拌,可以得到溶液的是
A.碘加入汽油中 B.面粉加入水中
C.高锰酸钾加入汽油中 D.植物油加入水中
3.分类是学习和研究化学物质的一种常用的科学方法,下列分类正确的是
A.碳酸氢钠能解离出H+,属于酸
B.一氧化碳中含有碳元素,属于有机物
C.氢氧化钠中含有氧元素,属于氧化物
D.绿矾可用化学式FeSO ·7H O表示,属于纯净物
4 2
4.要使一杯氯化铵不饱和溶液变为饱和溶液,可采取的方法是
A.加水 B.不断搅拌
C.升高温度 D.加氯化铵晶体
5.下列有关水的叙述中,不正确的是
A.水汽化时分子间隔发生了变化 B.用明矾溶液可以区分硬水和软水
C.工业废水处理后可以循环使用 D.水是能溶解多种物质的常用溶剂
6.古语道:“人要实,火要虚”。此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃
料需要架空,燃烧才能更旺。从燃烧的条件看,“火要虚”的实质是
A.增大可燃物的热值 B.提高空气中氧气的含量
C.提高可燃物的着火点 D.增大可燃物与空气的接触面积
7.下列关于分子、原子、离子构成物质的说法中,不正确的是
化学试卷 第 1 页 (共 10 页)A.汞原子聚集成金属汞
B.氢原子结合成氢气
C.氯原子和氢原子结合成氯化氢分子,氯化氢分子聚集成氯化氢
D.氯原子和钠原子得失电子形成氯离子和钠离子,两种离子结合成氯化钠
8.对有关实验现象的描述正确的是
A.碳在氧气中燃烧放出白烟 B.干冰在空气中升华周围出现白雾
C.铁丝在氧气中燃烧生成四氧化三铁 D.硫在氧气中燃烧发出淡蓝色的火焰
9.若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是
A.Mn + H
2
SO
4
= MnSO
4
+ H
2
↑ B.Mg + MnSO
4
= MgSO
4
+ Mn
C.Fe + MnSO = FeSO + Mn D.Mn + CuSO = MnSO + Cu
4 4 4 4
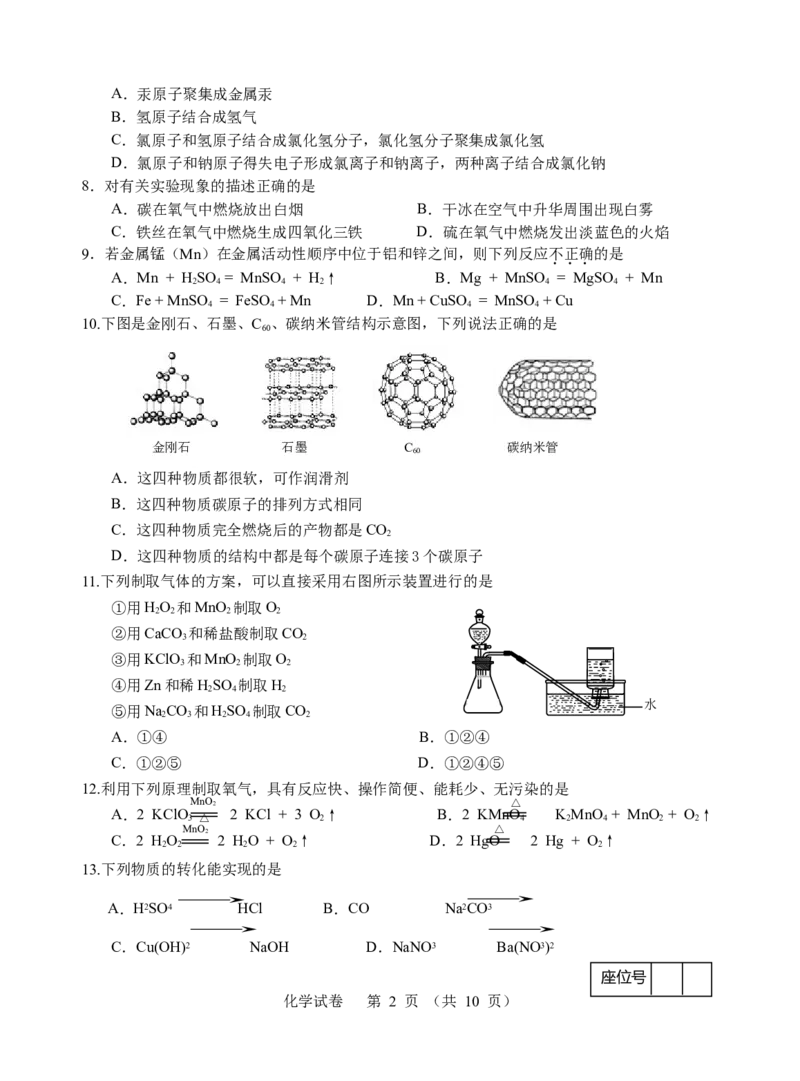
10.下图是金刚石、石墨、C 、碳纳米管结构示意图,下列说法正确的是
60
金刚石 石墨 C 碳纳米管
金刚石 石墨 C60 碳纳米管
60
A.这四种物质都很软,可作润滑剂
B.这四种物质碳原子的排列方式相同
C.这四种物质完全燃烧后的产物都是CO
2
D.这四种物质的结构中都是每个碳原子连接3个碳原子
11.下列制取气体的方案,可以直接采用右图所示装置进行的是
①用HO 和MnO 制取O
2 2 2 2
②用CaCO 和稀盐酸制取CO
3 2
③用KClO 和MnO 制取O
3 2 2
④用Zn和稀HSO 制取H
2 4 2
水
⑤用NaCO 和HSO 制取CO
2 3 2 4 2
A.①④ B.①②④
C.①②⑤ D.①②④⑤
12.利用下列原理制取氧气,具有反应快、操作简便、能耗少、无污染的是
MnO 2 △
A.2 KClO
3 △
2 KCl + 3 O
2
↑ B.2 KMnO
4
K
2
MnO
4
+ MnO
2
+ O
2
↑
MnO △
C.2 HO
2
2 HO + O↑ D.2 HgO 2 Hg + O↑
2 2 2 2 2
13.下列物质的转化能实现的是
A.H2SO4 HCl B.CO Na2CO3
C.Cu(OH)2 NaOH D.NaNO3 Ba(NO3)2
座位号
化学试卷 第 2 页 (共 10 页)
2
+BaCl +NaOH
3
+NaCl +BaCO14.下列说法不正确的是
A.碳酸氢钠可以用来治疗胃酸过多
B.氨水(NH ·HO)涂在蚊虫叮咬后的皮肤上,可减轻痛痒
3 2
C.通过大量使用农药,防治病虫害,以提高产量,符合可持续发展
D.汽油中加入适量乙醇作为汽车燃料,可节省石油资源、减少污染
15.氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便方法区别三种化肥,在农业生产中具有实
用性。区别下列相关化肥的方法可行的是
A.NH Cl与KCl:观察外观
4
B.NH HCO 与KCl:加水
4 3
C.KSO 与Ca (PO ):闻气味
2 4 3 4 2
D.(NH )SO 与KSO :加熟石灰研磨后闻气味
4 2 4 2 4
答案
二、选择题(本题共5小题,每小题2分,共10分)每小题有一个或两个选项符合题意。若正确
只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,
选两个且都正确的给2分,但只要选错一个,该小题就为0分。请将正确选项的序号填涂在答题
卡上。
高温
16.有关2 CuO + C 2 Cu + CO↑的反应,说法正确的是
2
A.CuO具有氧化性 B.C发生了还原反应
C.反应前后氧元素的化合价没有改变 D.反应前后固体质量不变
17.在生活、生产和科学研究中,常用pH试纸测定溶液的pH。以下测定操作正确是
A.将被测液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较
B.将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较
C.先用少量水湿润试纸,后滴上被测液,显色后,与标准比色卡比较
D.先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较
18.下列变化过程中吸收热量的是
A.Zn与盐酸反应 B.NaOH固体溶于水
C.CO
2
与C反应 D.NH
4
NO
3
固体溶于水
19.除去下列物质中所含少量杂质的方法正确的是
物 质 杂 质 除杂试剂 提 纯 方 法
A CO CO O 点燃
2 2
B KCl MnO 水 溶解、过滤、蒸发
2
C HO NaNO 活性炭 吸附、过滤
2 2
D NaCO NaSO BaCl 溶解、过滤、洗涤
2 3 2 4 2
20. A、B、C三种物质各15 g,它们化合时只能生成30 g新物质D。若增加10 g A,则反应停止后,
原反应物中只余C。根据上述条件推断下列说法中正确的是
A.第一次反应停止后,B剩余9 g B.第二次反应后,D的质量为50 g
C.反应中A和B的质量比是3∶2 D.反应中A和C的质量比是5∶2
第Ⅱ卷(非选择题 共60分)
化学试卷 第 3 页 (共 10 页)注意事项:
根据题目要求,用钢笔或圆珠笔将答案直接写在试卷上。
题号 三 四 五 六 Ⅱ卷总分 结分人 核分人
得分
得分 评卷人
三、(本题共4小题,每空1分,共20分)
21.(6分)化学可以帮助人类认识改造周围的世界,促进社会发展。
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质。下表为某品牌燕麦片标签中的一部
分。
每100 g含有 糖类 油脂 蛋白质 维生素C 钙 镁 钠 锌
营养成分 7.6 g 7.8 g 7.4 g 18 mg 201 mg 18.2 mg 30.8 mg 8.1 mg
① 燕麦片的营养成分中能与水反应生成氨基酸的营养物质是___________________;每克营养
物质氧化时放出能量最多的是__________;人体必需的微量元素是_______________。
② 维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红
色消失。因此,烹调富含维生素C的食物时,应该注意_____________;在碱性条件下,维生素C
易被空气氧化,烧煮时最好加一点________。
(2)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等。用灼烧法可初步鉴别
三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
纤维编号 ① ② ③
灼烧时的气味 特殊气味 烧纸气味 烧焦羽毛气味
则羊毛、棉花的编号分别为_________________________。
22.(4分)
(1)元素X的离子结构示意图为 ,元素 Y的原子结构示
意图为 。写出X的离子符号_____________;X与Y形成 溶 b
解
度
化合物的化学式为_____________。
/g
a
(2) a、b两种固体物质的溶解度曲线如右图所示。在______℃
时a、b的溶质质量分数相等。当a的饱和溶液含有少量b时,通
过_________________提纯a。 0 t 1 t 2 温
度/℃
化学试卷 第 4 页 (共 10 页)23.(4分)1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所
证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH )。反应的化学方程式为
3
_____________________________________________________。
(2)用 、 、 分别表示N、H、NH 。观察下图,写出符合在催化剂表面合成
2 2 3
氨反应过程的顺序________________________(将下面五张图按反应过程顺序用序号排列)。
① ② ③ ④ ⑤
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程。
在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O 的溶解,水膜呈中性。
2
若空气中CO 溶解,水膜呈酸性,写出该反应的化学方程式______________________。
2
在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应,产
生两种空气组成的气体,写出该反应的化学方程式________________________________。
24.(6分)右图中A、B、C、D、E、F、G、H分别 B
+Y
代表相关反应的一种物质。已知:X、H为黑色固 E
高温
通电
体单质,D是大理石的主要成分,Y为红棕色粉末。 B
H
常温下C、E、F、G均为无色气体,图中有部分生 F
成物未标出。请填写以下空白: +Y
A △ C +X G
(1)写出下列两种物质的化学式: 高温 高温
E_____________,X______________。 高温
+酸
(2)写出下列反应的化学方程式: D C
高温 +碱
① D C的反应:_____________________________________________。
碱
② C D的反应:_____________________________________________。
③ F与H的反应:__________________________________________________。
④ G与Y的反应:__________________________________________________。
得分 评卷人
四、(本题1小题,每空1分,共10分)
25.(10分)“嫦娥一号”卫星发射成功,标志月球探测成为中国航天的现实。
(1)“嫦娥一号”使用的燃料是液氢,助燃剂是液氧。氧气从淡蓝色液体变成无色气体发生了
_______变化,氢气燃烧的化学方程式为___________________。液态氢作燃料除燃烧时产生较
大的推动力外,另一个优点是_____________。对于目前全世界出现能源危机,以及燃烧对环境
的影响,我们应该合理开发利用的新能源有(至少填两种)__________________________。
(2)月球上的3He(3表示相对原子质量)蕴藏量巨大,探月的目标之一是探测核聚变燃料3He的
分布。地球上的氦元素主要以4He形式存在。从原子的构成来看,3He、4He两种原子的_______
数不同,化学性质_______________。
化学试卷 第 5 页 (共 10 页)(3)“嫦娥一号”另一个目标是探测下列14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、
Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆)。其中属于金属元素的有 种。
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为
“未来金属”。我国四川省有大型钒钛磁铁矿,由钒钛磁铁矿提取金属钛的主要工艺过程如下:
Fe
选矿 C
钒钛磁铁矿 钛铁矿
高温
TIO 2
C、Cl
2 TiCl 4
足量的Mg
Ti
①钛铁矿的主要成分是FeTiO (钛酸亚铁),其中钛的化 高温 合价为 高 温 价。
3
②TiCl 在高温下与足量Mg反应生成金属Ti,该反应属于_____________(填反应类型)。
4
③上述生产过程中得到的金属钛中混有少量金属杂质,可加入_________________除去。
得分 评卷人
五、(本题共3小题,每空1分,共21分)
26.(4分)规范的实验操作是实验成功的前提,请回答:
(1)量取8mL稀硫酸,应选用______________mL的量筒。
(2)胶头滴管用过后应____________,再去吸取其他药品。
(3)实验室用烧瓶制取蒸馏水时,烧瓶的底部应垫放______________。
(4)玻璃管插入带孔橡皮塞,先把玻璃管的一段______________,然后稍稍用力转动插入。
27.(8分)已知某纯碱试样中含有杂质氯化钠,为测定试样中纯碱的质量分数,可用下图装置进行
实验。
稀硫酸 B
A
碱石灰
(固体NaOH和CaO)
NaOH溶液 试样溶液 浓硫酸
主要步骤如下,请填空:
① 按图组装仪器,并检查__________________;② 将10 g试样放入锥形瓶中,加适量蒸馏水
溶解,得到试样溶液;③ 称量盛有碱石灰的U形管的质量为300 g;④ 从分液漏斗中滴入20%
的稀硫酸,直到________________为止,写出反应的化学方程式__________________________;
⑤ 从导管A处缓缓鼓入一定量的空气;⑥ 再次称量盛有碱石灰的U形管的质量;⑦ 重复⑤和
⑥的操作,直到U形管的质量基本不变,测得质量为303.3 g。
回答下列问题:
(1)装置中浓硫酸的作用是___________________________________。
(2)步骤⑤的目的是_________________________________________。
(3)试样中纯碱的质量分数为_________________________________。
(4)分液漏斗中的稀HSO 不能换成浓盐酸,理由是______________________________。
2 4
(5)若用生成沉淀的方法来测定试样中纯碱的质量分数,应选用的试剂是____________。
28.(9分)请你参与下列探究:
化学试卷 第 6 页 (共 10 页)【问题情景】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有
较多的气泡放出。这一现象激发起同学们的探究欲望,生成的是什么气体?
【提出猜想】从物质组成元素的角度,放出的气体可能是SO 、O、H。
2 2 2
【查阅资料】SO 易溶于水,它能与NaOH反应,生成NaSO 。
2 2 3
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O,则检验方法是_____________________________________。
2
(2)乙同学认为是SO ,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗
2
气瓶的质量。写出SO 与NaOH反应的化学方程式________________________________。
2
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
a
NaOH
浓
表面含CuO
溶液
HSO 的铜网
2 4
A B
如果放出的是O 和H,你认为方案中的安全隐患是 。
2 2
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指 ,
若不发出________________,方可采用上面的装置进行实验。
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通
入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;
停止通气,再次称量装置A,发现质量无增减。
结论:铁粉与硫酸铜溶液反应时,产生的气体是_________________。
【思维拓展】
SO
2
(1)由上述实验可以推出,硫酸铜溶液中可能含有____________物质。
(2)不通过称量,如何判断SO 与NaOH溶液发生了反应呢?有一同
2
学设计了右图所示的装置进行实验,发现试管内液面上升,就得出SO NaOH
2
溶 液
与NaOH溶液发生反应的结论。其他同学认为这一方案不严谨,理由是
__________________________________________。要得到科学严谨的结论,仍利用该装置,补
做的实验是___________________________________________________________________。
得分 评卷人
六、(本题共2小题,共9分)
29(. 4分)2008年5月12日四川汶川大地震后,为了预防疫情,防疫人员使用了各种消毒剂对环境
进行消毒。亚氯酸钠(NaClO)是一种重要的消毒剂。试计算:
2
(1)亚氯酸钠中Na、Cl、O三种元素的质量之比为_____________________________。
(2)现要配制质量分数为16%的亚氯酸钠消毒液1500 kg,需要亚氯酸钠_________kg。
30(. 5分)阳光牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水。使用一段时间后,其中
化学试卷 第 7 页 (共 10 页)的Fe粉会转变成Fe O 而变质。某化学兴趣小组欲探究使用过的阳光牌“脱氧剂”的变质程度
2 3
(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行如下探究过程。
步骤(1)取食品包装袋中的阳光牌“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干
燥滤渣。
步骤(2)取步骤(1)中的滤渣8.0 g,加入足量的稀HSO 与滤渣充分反应,过滤、洗涤、干
2 4
燥得固体1.2 g。
步骤(3)取步骤(2)中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,
充分加热、冷却、称量,得到8.0 g Fe O(注:滤液中的Fe元素已全部转化为Fe O)。
2 3 2 3
求:(1)8.0 g滤渣中Fe和Fe O 两种物质的总质量。
2 3
(2)该“脱氧剂”在未变质时,Fe粉和活性炭的质量之比。
(3)该“脱氧剂”的变质程度。
★保密材料
2008 年南通市初中毕业、升学考试
阅卷使用
化学试卷 第 8 页 (共 10 页)化学试题参考答案和评分标准
一、选择题(本题包括15小题,每小题2分,共30分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 A A D D B D B B C C A C A C D
二、选择题(本题共5小题,每小题2分,共10分)若正确答案只包括一个选项,多选时,该题为0
分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给2分,但只要
选错一个,该小题就为0分。
题号 16 17 18 19 20
答案 AC A CD B BD
三、(本题共4小题,每空1分,共20分)
21.(1)①蛋白质 油脂 锌 ②不要高温加热 食醋 (2)③②
22.(1)X2+ XY (2)t 蒸发结晶
2 1
23.(1)N
2
+ 3 H高
2
温
催
、
化
高
剂
压 2 NH
3
(2)⑤④①②③
催化剂
(3)H
2
O + CO
2
= H
2
CO
3
2 CO + 2 NO N
2
+ 2 CO
2
高温
24.(1)H C (2)① CaCO CaO + CO↑ ② Ca(OH) + CO = CaCO ↓+ HO
2 3 2 2 2 3 2
点燃 高温
③ 3 Fe + 2 O
2
Fe
3
O
4
④ Fe
2
O
3
+ 3 CO 2 Fe + 3 CO
2
四、(本题1小题,每空1分,共10分)
点燃
25.(1)物理 2 H
2
+ O
2
2 H
2
O 无污染 太阳能、风能
(2)中子 基本相同 (3)12 (4)+4 置换反应 稀盐酸
五、(本题共3小题,每空1分,共21分)
26.(1)10 (2)立即洗净 (3)石棉网 (4)用水润湿
27. ①装置的气密性 ④不再产生气体 NaCO + HSO = NaSO + CO↑+ HO
2 3 2 4 2 4 2 2
(1)除去水
(2)使反应产生的CO 全部导入U形管
2
(3)79.5%
(4)浓盐酸有挥发性,对测定有影响
(5)CaCl
2
28.【方案设计】
(1)用带火星的木条试验,看木条是否复燃
(2)SO + 2NaOH = NaSO + HO
2 2 3 2
(3)实验时在B处易发生爆炸事故 堵住试管囗,靠近火焰点火 尖锐的爆鸣声
【实验探究】H
2
化学试卷 第 9 页 (共 10 页)【思维拓展】
(1)酸性
(2)SO 易溶于水,也能使液面上升 将NaOH溶液换成水做对比实验
2
六、(本题共2小题,共9分)
29.(1)23∶35.5∶32 (2分)
(2)240 (2分)
30.解:
(1)1.2 g的固体是活性炭。 (1分)
8.0 g滤渣中Fe和Fe O 两种物质的总质量为8.0 g-1.2 g = 6.8 g (1
2 3
分)
(2)Fe元素的质量为:8.0 g× = 5.6 g
则Fe粉和活性炭的质量之比为5.6∶1.2 = 14∶3 (1
分)
(3)由于铁变质而增加的氧元素的质量为:6.8 g-5.6 g = 1.2 g
(1
变质铁的质量为1.2 g÷ = 2.8 g
分)
(1
脱氧剂的变质程度= ×100% = 50%
分)
答:略
注:卷Ⅱ中,其他合理答案均给分。
化学试卷 第 10 页 (共 10 页)