文档内容
第一章 第3节 氧化还原反应-课时作业2022-2023学年高中
化学人教版(2019)必修第一册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.在2HO 2HO + O↑反应中,MnO 的作用是
2 2 2 2 2
A.还原剂 B.氧化剂 C.催化剂 D.干燥剂
2.氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时的化学
反应原理为: 。下列有关该反应的说法中,正确的是
A.该反应属于置换反应 B. 是氧化剂
C. 中的氢元素被还原 D. 是氧化产物, 是还原产物
3.以下物质间的转化不能通过一步反应实现的是
A.Ca(OH) →NaOH B.CuO→Cu(OH) C.CaCO →CaO D.HO→H
2 2 3 2 2
4.在xR2++yH++O=mR3++nHO的离子方程式中,对m和R3+的判断正确的是(
2 2
)
A.m=2 R2+是还原剂 B.m=y R3+是氧化产物
C.m=2 R2+是氧化剂 D.m=y R3+是还原产物
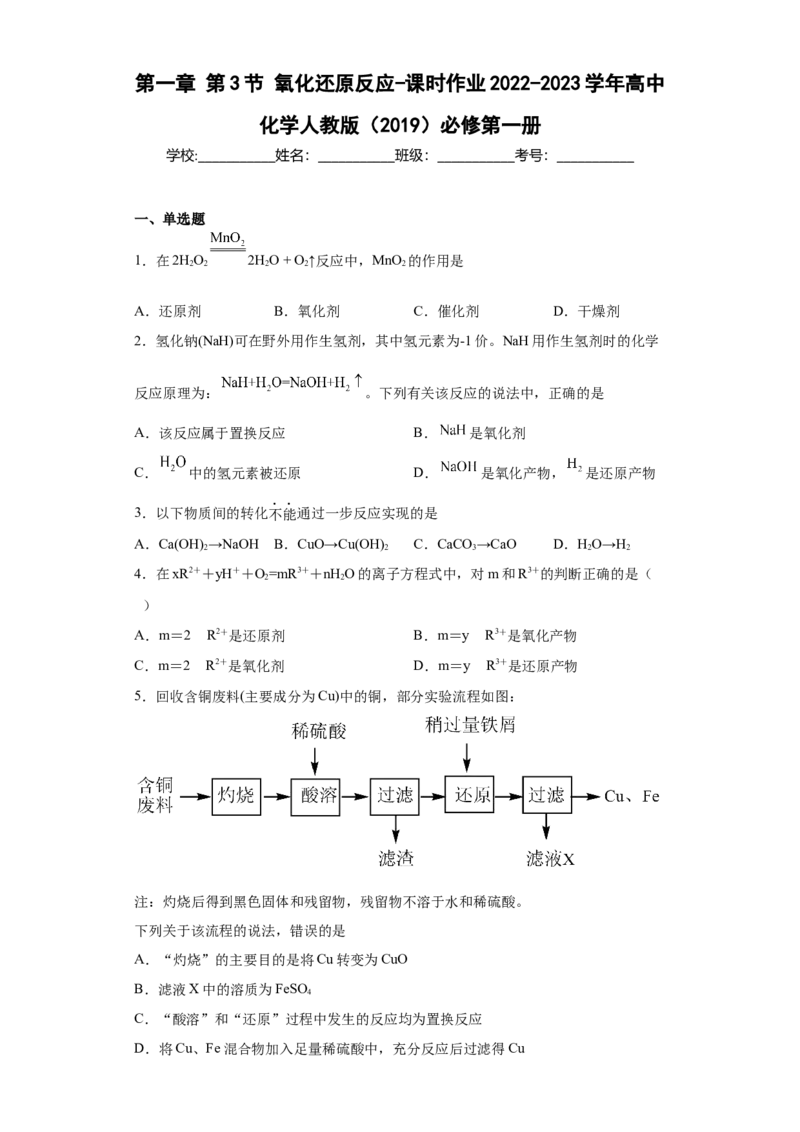
5.回收含铜废料(主要成分为Cu)中的铜,部分实验流程如图:
注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
下列关于该流程的说法,错误的是
A.“灼烧”的主要目的是将Cu转变为CuO
B.滤液X中的溶质为FeSO
4
C.“酸溶”和“还原”过程中发生的反应均为置换反应
D.将Cu、Fe混合物加入足量稀硫酸中,充分反应后过滤得Cu6.需要加入氧化剂才能实现下列反应的是( )
A.Cl Cl-
2
B.H+ H
2
C.MnO - Mn2+
4
D.Zn Zn2+
7.硒(Se)与硫属于同一主族元素,含硒的几种物质存在如图所示的转化关系。下列说
法错误的是
A.图中只有反应④和⑤不属于氧化还原反应
B.反应②中可能有 生成
C. 属于二元酸, 属于正盐
D.反应⑥中氧化产物与还原产物的物质的量之比为8:1
8.氢化钠( )可在野外用作生氢剂,其中氢元素为 价。 用作生氢剂时的化
学反应原理为: 。下列有关反应的说法中,正确的是
A. 是氧化剂 B. 中的氢元素被还原
C.该反应属于复分解反应 D.若生成 ,则反应中转移
电子
9.下列变化需要加入氧化剂才能实现的是
A.S2- HS- B. CO C.2Cl- Cl D.Cu2+ Cu
2 2
→ → → →
10.用下列方法均可制得氧气:
①2Na O+2H O=4NaOH+O ↑
2 2 2 2
②2HgO 2Hg+O↑
2
③2KMnO KMnO +MnO+O ↑
4 2 4 2 2
若要制得相同质量的氧气,反应中电子转移数目之比为
试卷第2页,共3页A.2∶2∶1 B.3∶1∶4 C.1∶1∶1 D.1∶2∶2
11.下列变化中,必须加入氧化剂才能实现的是
A.CO→CO B.HCO →CO C.KClO→O D.Br-→Br
2 3 2 2
12.Cu S与一定浓度的HNO 反应,生成Cu(NO )、CuSO 、NO 、NO和HO。当产
2 3 3 2 4 2 2
物n(NO )∶n(NO)=1∶1时。下列说法正确的是( )
2
A.1molCu S参加反应时有8mol电子转移
2
B.参加反应的n(Cu S)∶n(HNO)=1∶5
2 3
C.反应中Cu S既作氧化剂,又作还原剂
2
D.产物n[Cu(NO )]∶n[CuSO ]=1∶1
3 2 4
二、填空题
13.饮用水中NO 对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水
研究人员提出,可在碱性条件下用铝粉将NO 还原为N
2。
(1)配平方程式:_______。
_______Al+_______NO +_______OH-+_______H O=_______[Al(OH) ]-+_______N ↑
2 4 2
(2)上述反应中,还原剂与还原产物的物质的量之比是_______,反应中转移电子
0.3mol,生成_______mLN (标准状况下)。
2
14.把19.2g的Cu放入500mL2mol·L-1稀硝酸中,发生如下反应3Cu+8HNO (稀)=
3
3Cu(NO )+2NO↑+4HO,充分反应,Cu完全溶解。
3 2 2
(1)写出Cu与稀硝酸反应的离子方程式:_____________________,用单线桥标出电
子转移______________________________。
(2)还原剂是__________,被还原的元素是__________,还原产物是__________,氧
化剂与还原剂的物质的量比为________________。
(3)转移的电子的数目为__________(用含N 的式子表示),被还原的HNO 为
A 3
__________mol,反应后溶液中c(H+)为____________。(体积变化忽略不计)
三、实验题
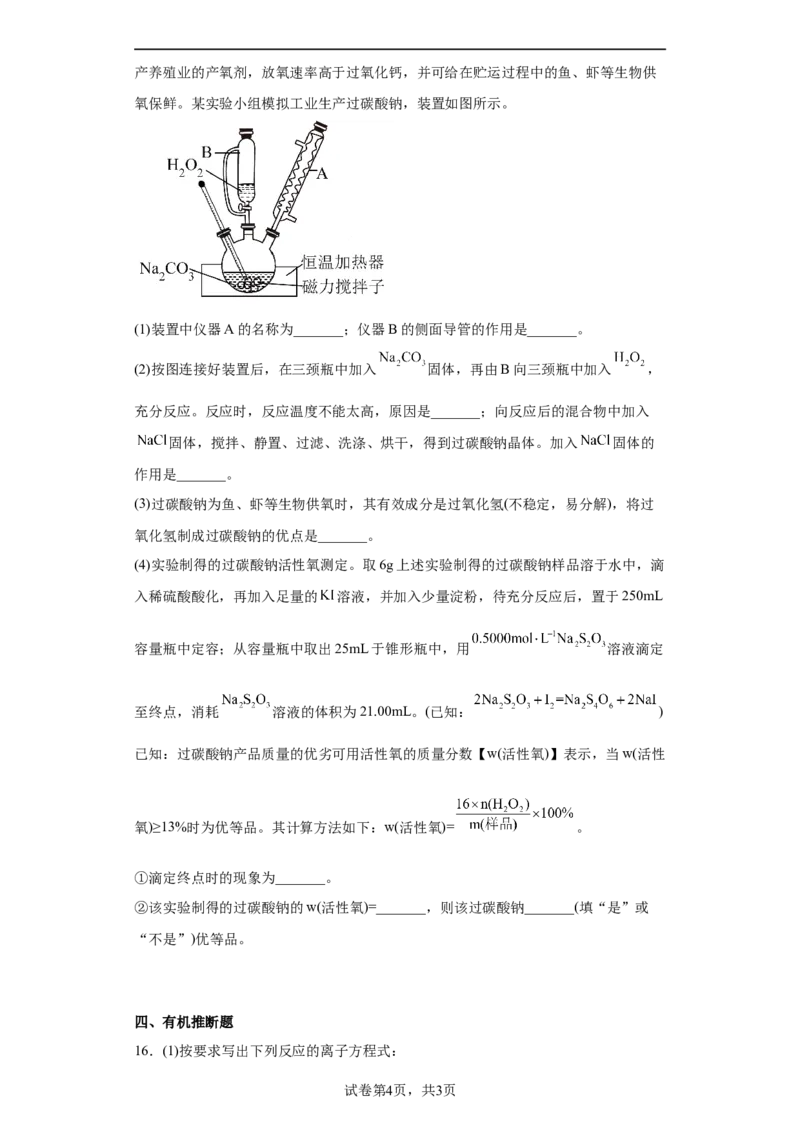
15.过碳酸钠( )俗称固体双氧水,易溶于水,可以替代过氧化钙作为水产养殖业的产氧剂,放氧速率高于过氧化钙,并可给在贮运过程中的鱼、虾等生物供
氧保鲜。某实验小组模拟工业生产过碳酸钠,装置如图所示。
(1)装置中仪器A的名称为_______;仪器B的侧面导管的作用是_______。
(2)按图连接好装置后,在三颈瓶中加入 固体,再由B向三颈瓶中加入 ,
充分反应。反应时,反应温度不能太高,原因是_______;向反应后的混合物中加入
固体,搅拌、静置、过滤、洗涤、烘干,得到过碳酸钠晶体。加入 固体的
作用是_______。
(3)过碳酸钠为鱼、虾等生物供氧时,其有效成分是过氧化氢(不稳定,易分解),将过
氧化氢制成过碳酸钠的优点是_______。
(4)实验制得的过碳酸钠活性氧测定。取6g上述实验制得的过碳酸钠样品溶于水中,滴
入稀硫酸酸化,再加入足量的 溶液,并加入少量淀粉,待充分反应后,置于250mL
容量瓶中定容;从容量瓶中取出25mL于锥形瓶中,用 溶液滴定
至终点,消耗 溶液的体积为21.00mL。(已知: )
已知:过碳酸钠产品质量的优劣可用活性氧的质量分数【w(活性氧)】表示,当w(活性
氧)≥13%时为优等品。其计算方法如下:w(活性氧)= 。
①滴定终点时的现象为_______。
②该实验制得的过碳酸钠的w(活性氧)=_______,则该过碳酸钠_______(填“是”或
“不是”)优等品。
四、有机推断题
16.(1)按要求写出下列反应的离子方程式:
试卷第4页,共3页①少量二氧化碳通入澄清石灰水_____________________________________________。
②硫酸氢钠与过量氢氧化钡溶液混合______________________________________。
③熔融状态下NaHSO 电离方程式__________________________。
4
(2)①用双线桥表示下列氧化还原反应电子转移:__________________________。
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
②配平下面方程式:_________。
KMnO + HO+ HSO — KSO + MnSO + O↑+ HO
4 2 2 2 4 2 4 4 2 2参考答案:
1.C
【详解】该反应中,MnO 作为催化剂,氧化剂为HO,还原剂为HO,氧化产物为O,
2 2 2 2 2 2
还原产物为HO;
2
答案选C。
2.C
【详解】A.反应物中没有单质,该反应不是置换反应,A错误;
B.氧化剂具有氧化性、元素化合价降低,而氢化钠中氢元素化合价升高,氢化钠是还原
剂,B错误;
C.水中氢元素化合价降低,水是氧化剂,氢元素被还原,C正确;
D.氢气既是氧化产物、又是还原产物,D错误;
答案选C。
3.B
【详解】A.氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,故可以一步转化,A不符合
题意;
B.氧化铜和盐酸反应生成氯化铜和水,氯化铜和氢氧化钠反应生成氢氧化铜和氯化钠,
故不能一步转化,B符合题意;
C.碳酸钙受热分解,生成氧化钙和二氧化碳,故可以一步转化,C不符合题意;
D.水通电生成氢气和氧气,故可以一步转化,D不符合题意;
故选B。
4.B
【详解】该反应中,R的化合价升高,故R2+做还原剂,R3+为氧化产物,O的化合价降,O
2
作氧化剂,HO作还原产物;O 的系数为1,则n=2,y=4,即转移4个电子,而
2 2
R2+→R3+的过程中转移1个电子,故x=m=4;故选B。
【点睛】在氧化还原反应的配平中,既要遵循质量守恒定律,又要考虑得失电子守恒。
5.C
【详解】A.铜在加热条件下能生成氧化铜,“灼烧”的主要目的是将Cu转变为CuO,A
项正确;
B.氧化铜能与稀硫酸反应生成硫酸铜和水,过量的铁和硫酸铜溶液反应生成硫酸亚铁溶
液和铜,则滤液X中的溶质为FeSO ,B项正确;
4
C.“酸溶”时氧化铜和稀硫酸反应生成硫酸铜和水,不是置换反应,C项错误;D.将Cu、Fe混合物加入足量稀硫酸中,Fe和稀硫酸反应生成硫酸亚铁和氢气,铜不与稀
硫酸反应,充分反应后过滤得Cu,D项正确;
答案选C。
6.D
【分析】氧化剂是得到电子,化合价降低,还原剂是失去电子,化合价升高,需要加入氧
化剂才能实现,说明所选应是化合价升高,据此分析;
【详解】A、Cl的化合价由0价→-1价,化合价降低, 需要加入还原剂,故A不符合题
意;
B、H的化合价由+1价→0价,化合价降低,需要加入还原剂,故B不符合题意;
C、Mn的价态由+7价→+2价,化合价降低,需要加入还原剂,故C不符合题意;
D、Zn的化合价由0价→+2价,化合价升高,需要加入氧化剂,故C符合题意;
答案选D。
7.D
【详解】A.反应④和⑤中元素化合价没有改变,不属于氧化还原反应,故A正确;
B.反应②中Se与HO反应生成HSeO,Se元素化合价升高,则HO为氧化剂,应有H
2 2 3 2 2
生成,故B正确;
C.由于HSeO 与过量的NaOH反应生成NaHSeO,故NaHSeO 为正盐、HSeO 为二元
6 6 2 4 6 2 4 6 6 6
酸,C正确;
D.反应⑥为归中反应 ,氧化产物和还原产物均为Se,两者
的物质的量之比为2:1,D错误。
8.B
【详解】A. 中氢元素化合价升高,是还原剂,A错误;
B. 中氢元素化合价降低,被还原,B正确;
C.该反应中氢元素化合价发生了变化,是氧化还原反应,C错误;
D.若生成 ,根据方程式,有0.1molNaH参与反应,反应中转移 电子,D
错误;
故选B。
9.C
【详解】A.S2-→HS-,没有发生元素化合价的变化,不需要加入氧化剂,A不符合题意;
答案第2页,共2页B. →CO,没有发生元素化合价的变化,不需要加入氧化剂,B不符合题意;
2
C.2Cl-→Cl,Cl元素由-1价升高到0价,失电子被氧化,作还原剂,需要加入氧化剂,C
2
符合题意;
D.Cu2+→Cu,Cu元素由+2价降低到0价,得电子被还原,作氧化剂,需要加入还原剂,
D不符合题意;
故选C。
10.D
【详解】根据化合价变化计算转移电子数,反应①中 由 价氧元素氧化得到,反应②、
③中 由 价氧元素氧化得到,当三个反应都制得相同质量 时,转移的电子数之比为
;
故选D。
11.D
【详解】A .CO→CO中碳元素化合价降低,CO 做氧化剂,需加入还原剂才能实现,A
2 2
错误;
B. → 中无元素化合价发生变化,没有发生氧化还原反应,不需要加入氧化剂,
可加入强碱可实现转化,B错误;
C .KClO→O 可在加热条件下发生分解反应实现,不需要加入氧化剂,C错误;
3 2
D .Br-→Br 中溴元素化合价升高,Br-做还原剂,需要加入氧化剂才能实现,D正确;
2
故选:D。
12.D
【分析】在Cu S中,Cu显+1价,S显-2价,在产物中Cu显+2价,S显+6价;在HNO 中,
2 3
一部分N的化合价不变,一部分由+5价降为+4价,一部分降为+2价。
【详解】A. 1molCu S参加反应时,有(2mol×1+1mol×8)=10mol电子转移,A不正确;
2
B. 1molCu S参加反应,失电子10mol,生成1mol(NO+NO),得电子4mol,则满足关系
2 2
2Cu S——5(NO +NO)——8HNO (酸性),参加反应的n(Cu S)∶n(HNO)=1∶9,B不正确;
2 2 3 2 3
C. 反应物Cu S中Cu、S的价态都升高,所以Cu S只作还原剂,C不正确;
2 2
D. 依据Cu S的组成关系,产物n[Cu(NO )]∶n[CuSO ]=1∶1,D正确;
2 3 2 4
故选D。【点睛】在进行氧化还原反应方程式的配平时,需利用质量守恒、电荷守恒原理;在分析
物质所表现的性质时,需分析元素的价态变化。
13.(1)10Al+6NO +4OH-+18H O=10[Al(OH) ]-+3N ↑
2 4 2
(2) 10:3 672
【解析】(1)
由未配平的离子方程式可知,碱性条件下,铝粉与硝酸根离子发生氧化还原反应生成四羟
基合铝离子和氮气,反应中铝做还原剂,硝酸根做氧化剂,反应转移的电子数目为30,配
平的离子方程式为:10Al+6NO +4OH-+18H O=10[Al(OH) ]-+3N ↑;
2 4 2
(2)
由方程式可知,还原剂铝与还原产物氮气的物质的量之比是10:3,生成3mol氮气,反应
转移30mol电子,则反应中转移电子0.3mol,标准状况下生成氮气的体积为
。
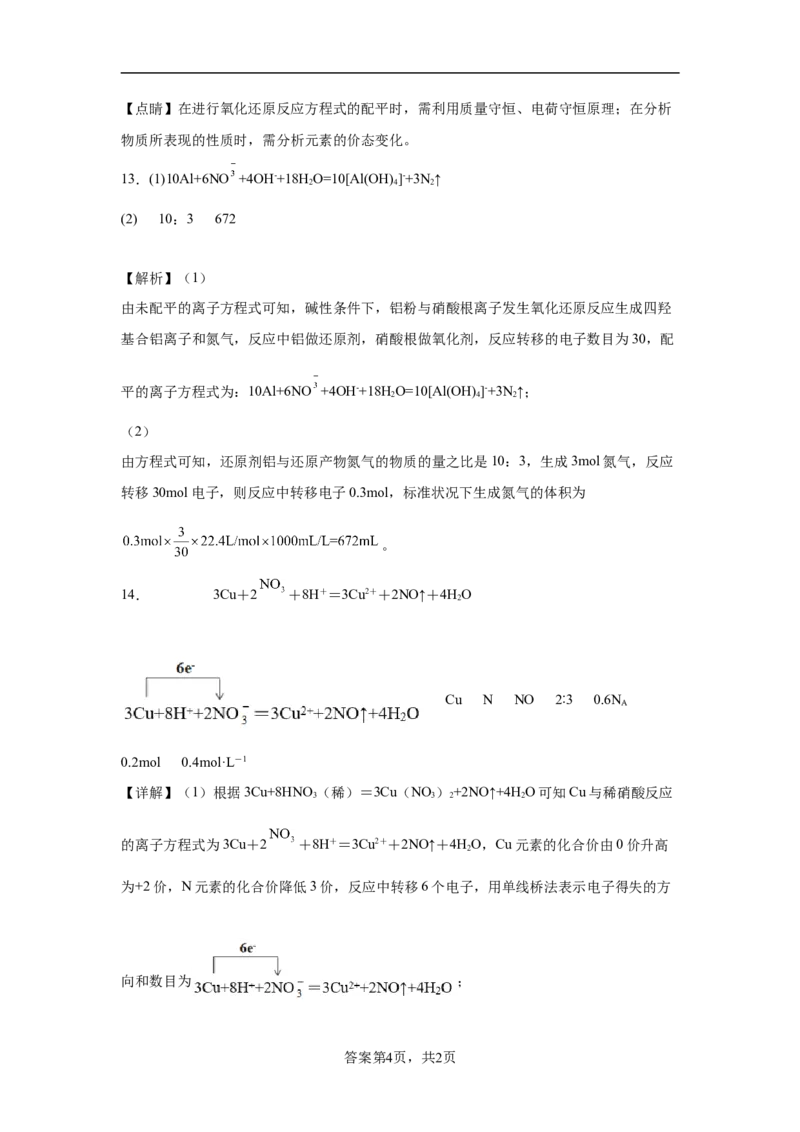
14. 3Cu+2 +8H+=3Cu2++2NO↑+4HO
2
Cu N NO 2∶3 0.6N
A
0.2mol 0.4mol·L-1
【详解】(1)根据3Cu+8HNO (稀)=3Cu(NO )+2NO↑+4HO可知Cu与稀硝酸反应
3 3 2 2
的离子方程式为3Cu+2 +8H+=3Cu2++2NO↑+4HO,Cu元素的化合价由0价升高
2
为+2价,N元素的化合价降低3价,反应中转移6个电子,用单线桥法表示电子得失的方
向和数目为 ;
答案第4页,共2页(2)铜失去电子,被氧化,还原剂是Cu,氮元素化合价降低,被还原的元素是N,还原
产物是NO,根据(1)中分析可知氧化剂与还原剂的物质的量比为2∶3。
(3)19.2g的Cu的物质的量是19.2g÷64g/mol=0.3mol,500mL2mol·L-1稀硝酸中硝酸的物
质的量是1mol,根据方程式可知硝酸过量,铜完全反应,转移的电子的物质的量是
0.3mol×2=0.6mol,其数目为0.6N ,根据电子得失守恒可知被还原的HNO 为0.6mol÷3=
A 3
0.2mol,消耗硝酸的物质的量是0.8mol,剩余硝酸是1mol-0.8mol=0.2mol,则反应后溶
液中c(H+)=0.2mol÷0.5L=0.4mol·L-1。
15.(1) (球形)冷凝管 平衡气体压强,使溶液顺利流出
(2) 防止过氧化氢发生分解 增大溶液中钠离子的浓度,有利于过碳酸钠的析出
(3)使于保存和运输
(4) 当滴入最后一滴(或半滴) 溶液时,溶液蓝色褪去,且半分钟内不恢复原
色 14% 是
【分析】在三颈瓶中加入 固体,再由B向三颈瓶中加入 ,充分反应。向反应
后的混合物中加入 固体,搅拌、静置、过滤、洗涤、烘干,得到过碳酸钠晶体。
(1)
根据装置图,仪器A的名称为球形冷凝管;仪器B的侧面导管连通了三口烧瓶和恒压滴液
漏斗,其作用是平衡气体压强,使溶液顺利流出。
(2)
温度升高,HO 分解速率加快,为防止过氧化氢发生分解,反应温度不能太高;加入NaCl
2 2
固体,钠离子浓度增大,有利于过碳酸钠的析出,所以向反应后的混合物中加入NaCl固体
可以形成过碳酸钠晶体。
(3)
过碳酸钠较稳定,将过氧化氢制成过碳酸钠,便于保存和运输。
(4)
①滴定终点时,碘单质完全被NaSO 消耗,所以滴定终点的现象为当滴入最后一滴(或半
2 2 3
滴)Na SO 溶液时,溶液蓝色褪去,且半分钟内不恢复原色;
2 2 3
② 和 ,可得 ,则可得 ,则可得
>13%,则该过碳酸钠是优
等品。
16. CO + Ca2++2OH-=CaCO ↓+H O H++ SO +Ba2+ +OH-= BaSO↓+H O
2 3 2 4 2
NaHSO = Na+ + HSO
4
2KMnO +5H O+3H SO =KSO +2MnSO +5O ↑+8H O
4 2 2 2 4 2 4 4 2 2
【详解】(1)①少量二氧化碳通入澄清石灰水中生成碳酸钙沉淀和水,离子方程式为
CO + Ca2++2OH-=CaCO ↓+H O,故答案为:CO + Ca2++2OH-=CaCO ↓+H O;
2 3 2 2 3 2
②硫酸氢钠与过量氢氧化钡溶液混合生成硫酸钡、氢氧化钠和水,离子方程式为H++ SO
+Ba2+ +OH-= BaSO↓+H O,故答案为:H++ SO +Ba2+ +OH-= BaSO↓+H O;
4 2 4 2
③熔融状态下NaHSO 电离方程式为NaHSO = Na+ + HSO ,故答案为:NaHSO = Na+ +
4 4 4
HSO ;
(2)①Mn元素的化合价从+7价降低到+2价,得到5个电子,高锰酸钾是氧化剂。氯元素
的化合价从-1价升高到0价,失去1个电子,氯化氢是还原剂,根据电子得失守恒可知电
答案第6页,共2页子转移可以表示为 ,故
答案为: ;
②Mn元素的化合价从+7价降低到+2价,得到5个电子,高锰酸钾是氧化剂。双氧水中
氧元素的化合价从-1价升高到0价,失去1个电子,双氧水是还原剂,根据电子得失守恒
可知配平后的方程式为2KMnO +5H O+3H SO =KSO +2MnSO +5O ↑+8H O,故答案为:
4 2 2 2 4 2 4 4 2 2
2KMnO +5H O+3H SO =KSO +2MnSO +5O ↑+8H O。
4 2 2 2 4 2 4 4 2 2答案第8页,共2页